无机及分析化学课后练习辅导资料Word文档格式.docx
《无机及分析化学课后练习辅导资料Word文档格式.docx》由会员分享,可在线阅读,更多相关《无机及分析化学课后练习辅导资料Word文档格式.docx(16页珍藏版)》请在冰豆网上搜索。
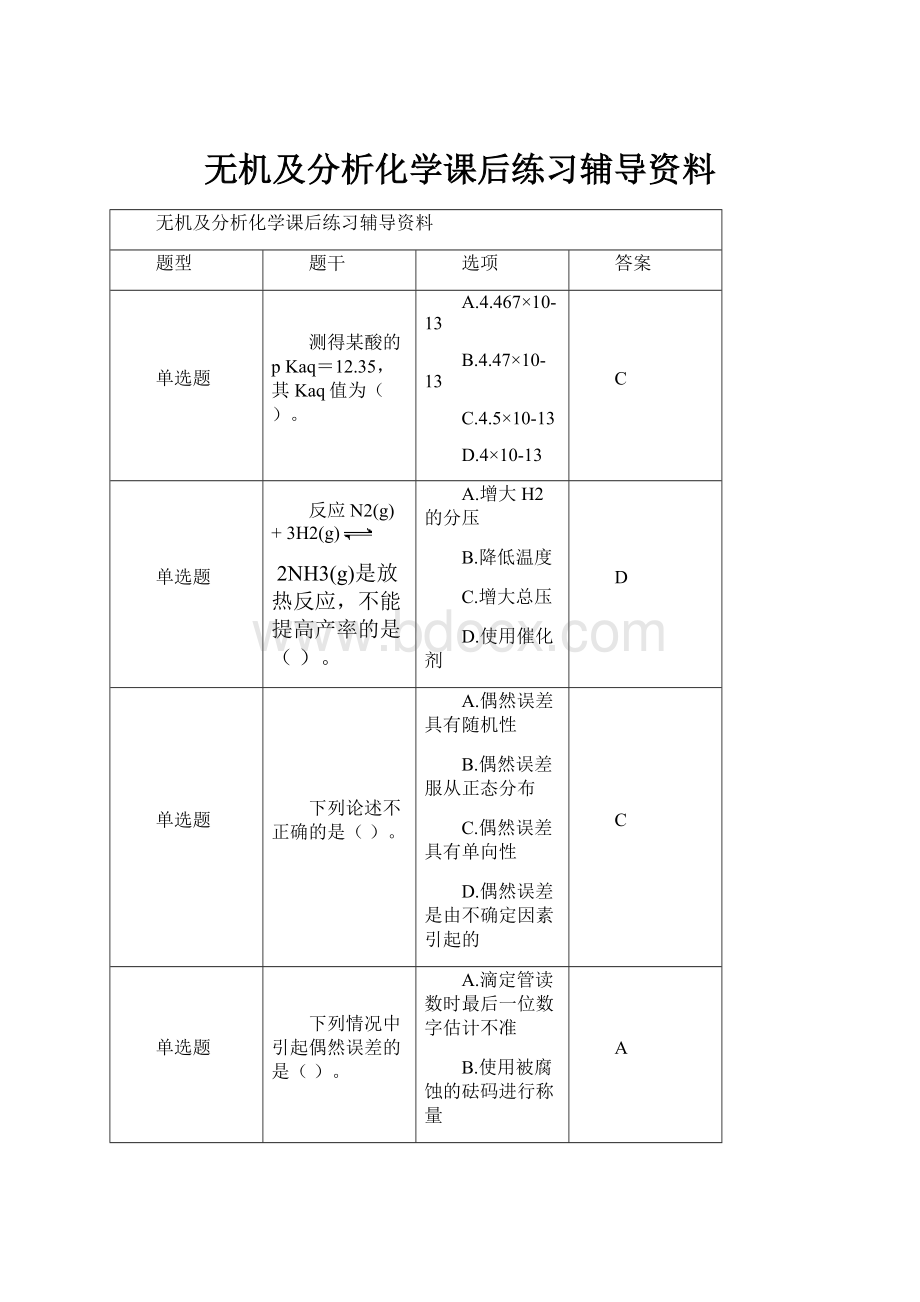
D.移液管和容量瓶不配套
A
在1L0.1mol·
L-1HAc溶液中加入少量NaAc晶体并使之溶解,会发生的情况是()。
A.HAc的解离常数增大
B.HAc的解离常数减小
C.溶液的pH增大
D.溶液的pH减小
0.1mol·
L-1NH3水溶液稀释10倍后,下列结果正确的是()。
A.pH值不变
B.解离常数变大
C.解离度变大
D.pH值变大
在下列化合物中,其相同浓度的水溶液的pH最高的是()。
A.NaCl
B.Na2CO3
C.NH4Cl
D.NaHCO3
B
向饱和AgCl溶液中加水,下列叙述正确的是()。
A.AgCl的溶解度增大
B.AgCl的溶解度、Kθsp均不变
C.AgCl的Kθsp增大
D.AgCl的溶解度、Kθsp增大
在半电池Cu2+|Cu溶液中,加入氨水后,可使该电对的电极电势值()。
A.增大
B.减小
C.不变
D.等于零
已知某元素+3价离子的核外电子排布式为1s22s22p63s23p63d5,该元素在周期表中属于()。
A.ⅤB族
B.ⅢB族
C.Ⅷ族
D.ⅤA族
下列各组数字都是分别指原子的次外层、最外层电子数和元素的常见氧化态,哪一组最符合于硫的情况?
()
A.2,6,-2
B.8,6,-2
C.18,6,+4
D.2,6,+6
H2S分子以不等性sp3杂化轨道成键,所以它的键角是:
()。
A.109.5°
B.小于109.5°
C.大于109.5°
D.无法预知
下列分子中,哪一个分子中有π键?
A.NH3
B.CS2
C.CuCl2
下列物质分子间氢健最强的是()。
B.HF
C.H2O
D.H3BO3
下列物质:
CaO、MgO、BaCl2晶体熔点的高低顺序是()。
A.BaCl2>CaO>MgO
B.MgO>BaCl2>CaO
C.BaCl2>MgO>CaO
D.MgO>CaO>BaCl2
下列说法正确的是()。
A.色散力仅存在于非极性分子之间
B.非极性分子内的化学键总是非极性键
C.取向力仅存在于极性分子之间
D.有氢原子的物质分子间一定存在氢键
判断
偏差是指测定值与真实值之间的差,偏差的大小说明分析结果精密度的高低。
F
在一定温度下,改变溶液的pH,水的离子积常数不变。
T
对缓冲溶液进行适当稀释时,溶液本身的pH保持不变。
在某溶液中加入甲基橙指示剂后,溶液显黄色,则溶液一定呈碱性。
由于同离子效应的存在,电解质溶液的pH一定会因此而增大。
电对的电极电势值不一定随pH的改变而改变。
钴原子(原子序数=27)的价电子构型是4s2。
HF的氢键属于分子内氢键,H3BO3属于分子间氢键。
在配离子[Co(C2O4)2(en)]-中,中心离子的配位数为4。
含氧酸盐的氧化性随介质的酸性增强而增强。
难电离的HgCl2在水中的溶解度(mol·
L-1)与其饱和溶液中下列物质的浓度最接近的是()。
A.Hg2+离子
B.Cl-离子
C.HgCl+离子
D.HgCl2分子
BaSO4的相对分子质量为233,Kθsp=1×
10-10,把1mmolBaSO4置于10L水中,有多少克BaSO4尚未溶解?
()
A.2.1g
B.0.21g
C.0.021g
D.0.0021g
下列化合物中,碳原子的氧化数为-3的是()。
A.CHCl3
B.C2H2
C.C2H4
D.C2H6
下列说法中不正确的是()。
A.H2O2分子结构为直线型
B.H2O2既有氧化性又有还原性
C.H2O2与K2Cr2O7的酸性溶液反应生成CrO(O2)2
D.H2O2是弱酸
欲使Mg2+沉淀为Mg(OH)2,用氨水为沉淀剂的效果比用强碱NaOH的效果好得多。
除H、He外,p区元素的原子,最外层电子都是p电子。
共价键类型有σ键和π键,其中键能较大的是π键。
一定温度下,反应N2(g)+3H2(g)
2NH3(g)达平衡后,增大N2的分压,平衡移动的结果是()。
B.减小N2的分压
C.增大NH3的分压
D.减小平衡常数
下列论述中,正确的是()。
A.精密度高,准确度一定好
B.准确度好,一定要有高的精密度
C.精密度高,系统误差一定小
D.测量时,过失误差不可避免
对可逆反应2NO(g)
N2(g)+O2(g)+Q,下列几种说法中正确的是()。
A.Kθ与温度有关
B.增加NO的浓度,Kθ值增大
C.温度升高时,平衡右移
D.使用催化剂,Kθ值增大
下列物质可用直接法配制其标准溶液的有()。
A.H2SO4
B.KOH
C.Na2S2O3
D.邻苯二甲酸氢钾
质子理论认为,下列物质中可以作为质子酸的是()。
A.H2S,C2O42-,HCO3
B.H2CO3,NH4+,H2O
C.Cl-,BF3,OH
D.H2S,CO32-,H2O
下列溶液中,pH最大的是()。
A.0.10mol·
L-1NH4NO3
B.0.10mol·
L-1Na3PO4
C.0.10mol·
L-1NH4Ac
D.0.10mol·
L-1NaCl
某酸碱指示剂的pKHInθ=5,其理论变色范围的pH为()。
A.2~8
B.3~7
C.4~6
D.5~7
已知Kθsp(Ag2SO4)=1.20×
10-5,Kθsp(AgCl)=1.77×
10-10,Kθsp(BaSO4)=1.08×
10-10,将等体积的0.0020mol·
L-1的Ag2SO4与2.0×
10-6mol·
L-1的BaCl2溶液混合,将会出现()。
A.BaSO4沉淀
B.AgCl沉淀
C.BaSO4与AgCl共沉淀
D.无沉淀
1LAg2C2O4饱和溶液中所含Ag2C2O4质量为0.06257g,Ag2C2O4的相对分子质量为303.8,若不考虑离子强度、水解等因素,Ag2C2O4的Kθsp是()。
A.4.24×
10-8
B.3.50×
10-11
C.2.36×
10-10
D.8.74×
10-12
下列化合物中,碳原子的氧化数为-2的是()。
在溴原子中,有3s、3p、3d、4s、4p各轨道,其能量高低的顺序是()。
A.3s<3p<4s<3d<4p
B.3s<3p<4s<4p<3d
C.3s<3p<3d<4s<4p
D.3s<3p<4p<3d<4s
分别在含有下列离子的水溶液中加入过量的氨水,最终生成有色沉淀的是()。
A.Fe3+
B.Cu2+
C.Co2+
D.Ag+
属于sp3不等性杂化的分子是()。
A.CH4
B.NH3
C.BF3
D.CH3—CH3
下列物质分子中有sp杂化轨道的是()。
A.H2O
C.CO2
D.CH4
下列分子中偶极矩不为零的是()。
A.BeCl2
B.H2O
下列各分子中,中心原子在成键时以不等性杂化的是()。
B.H2S
C.CCl4
D.BF3
误差是指测定值与真实值之间的差,误差的大小说明分析结果精密度的高低。
外加少量的酸或碱溶液时,缓冲溶液本身的pH保持不变。
在共轭酸碱对H3PO4-H2PO4-中,H3PO4为质子碱。
用强碱溶液滴定弱酸时,弱酸强度越大滴定突跃越大。
二元弱酸,其酸根离子的浓度近似等于该酸的一级解离常数。
对于给定的难溶电解质来说,温度不同,其溶度积也不同。
已知难溶电解质的Kθsp(AgCl)>Kθsp(Ag2CrO4),则在水中AgCl的溶解度较Ag2CrO4大。
共价键的极性可以用电负性差值来衡量;
而分子的极性可以用分子的偶极距来衡量。
在配离子[Co(C2O4)2(en)]-中,中心离子的配位数为3。
氧化还原电对的电极电势越大,则其还原型作为还原剂的还原能力就越弱。
标准氢电极的电极电势为零,是实际测定的结果。
质子理论认为,下列物质中全部是两性物质的是()。
A.Ac-,CO32-,PO43-,H2O
B.CO32-,CN-,Ac-,NO3-
C.HS-,NH3,H2PO4-,H2O
D.H2S,Ac,NH4,H2O
难溶电解质AB2的饱和溶液中,c(A+)=xmol·
L-1,c(B-)=ymol·
L-1,则Kθsp值为()。
A.xy2/2
B.xy
C.xy2
D.4xy2
在含有Mg(OH)2沉淀的饱和溶液中加入固体NH4Cl后,则Mg(OH)2沉淀()。
A.溶解
B.增多
D.无法判断
下列电极的电极电势与介质酸度无关的为()。
A.O2/H2O
B.MnO4-/Mn2+
C.H+/H2
D.AgCl/Ag
由反应Fe(s)+2Ag+(aq)
Fe2+(aq)+2Ag(s)组成的原电池,若将Ag+浓度减小到原来浓度的1/10,则电池电动势的变化为()。
A.0.0592V
B.-0.0592V
C.-118V
D.0.118V
在已经产生了AgCl沉淀的溶液中,能使沉淀溶解的方法是()。
A.加入盐酸
B.加入AgNO3溶液
C.加入氨水
D.加入NaCl溶液
通常情况下,使难溶的电解质溶解的方法有生成弱电解质(弱酸弱碱)、生成配位化合物、发生氧化还原反应等。
在多电子原子中,(n-1)d能级的能量总是大于ns能级的。
某电池反应A+B2+
A2++B的平衡常数为104,则该电池在298K时的标准电动势是()。
A.+0.060V
B.-0.119V
C.-0.060V
D.+0.119V
下列物质分子之间只存在色散力的是()。
A.CO2
C.NH3
D.HBr
在下列各种含氢的化合物中含有氢键的是()。
A.HCl
B.H3BO3
C.CH3F
BaCl2、MgF2、MgCl2晶体熔点的高低顺序是()。
A.BaCl2>MgF2>MgCl2
B.MgF2>MgCl2>BaCl2
C.MgCl2>BaCl2>MgF2
D.BaCl2>MgCl2>MgF2
在任何给定的溶液中,若Q<Kθsp,则表示该溶液为过饱和溶液,沉淀从溶液中析出。
NH3和CCl4的中心原子杂化轨道类型分别属于不等性sp3杂化和等性杂化sp3。
在N2中有两个σ键一个π键。
在0.1mol·
L-1NaF溶液中,下列关系正确的为()。
A.[H+]≈[HF]
B.[HF]≈[OH]
C.[H]≈[OH]
D.[OH]≈[HF]
加热分解可以得到金属单质的是()。
A.Hg(NO3)2
B.Cu(NO3)2
C.KNO3
D.Mg(NO3)2
σ键是原子轨道以肩并肩方式重叠;
而π键是原子轨道以头碰头方式重叠。