电解池习题.docx
《电解池习题.docx》由会员分享,可在线阅读,更多相关《电解池习题.docx(5页珍藏版)》请在冰豆网上搜索。
电解池
1.下列关于电解池形成的闭合回路的叙述中,不正确的是( )
A.电解池中的闭合回路是由电子的定向运动形成的
B.金属导线中,电子从电源的负极流向电解池的阴极,从电解池的阳极流向电源的正极
C.在电解质溶液中,阴离子向阳极移动,阳离子向阴极移动
D.相同时间内,阳离子在阴极上得到的电子与阴离子在阳极上失去的电子数相等
2.以下能用电解原理说明的是( )
①电解是把电能转化成化学能 ②电解是把化学能转化成电能 ③电解质溶液导电是化学变化,金属导电是物理变化 ④不能自发进行的氧化还原反应,通过电解的原理可以实现 ⑤任何溶液被电解时,必然导致氧化还原反应的发生
A.①②③④B.②③⑤C.③④D.①③④⑤
3.用惰性电极Pt电解下列物质的溶液,阴极上有金属析出的是( )
A.Na2SO4B.NaClC.AgNO3D.KOH
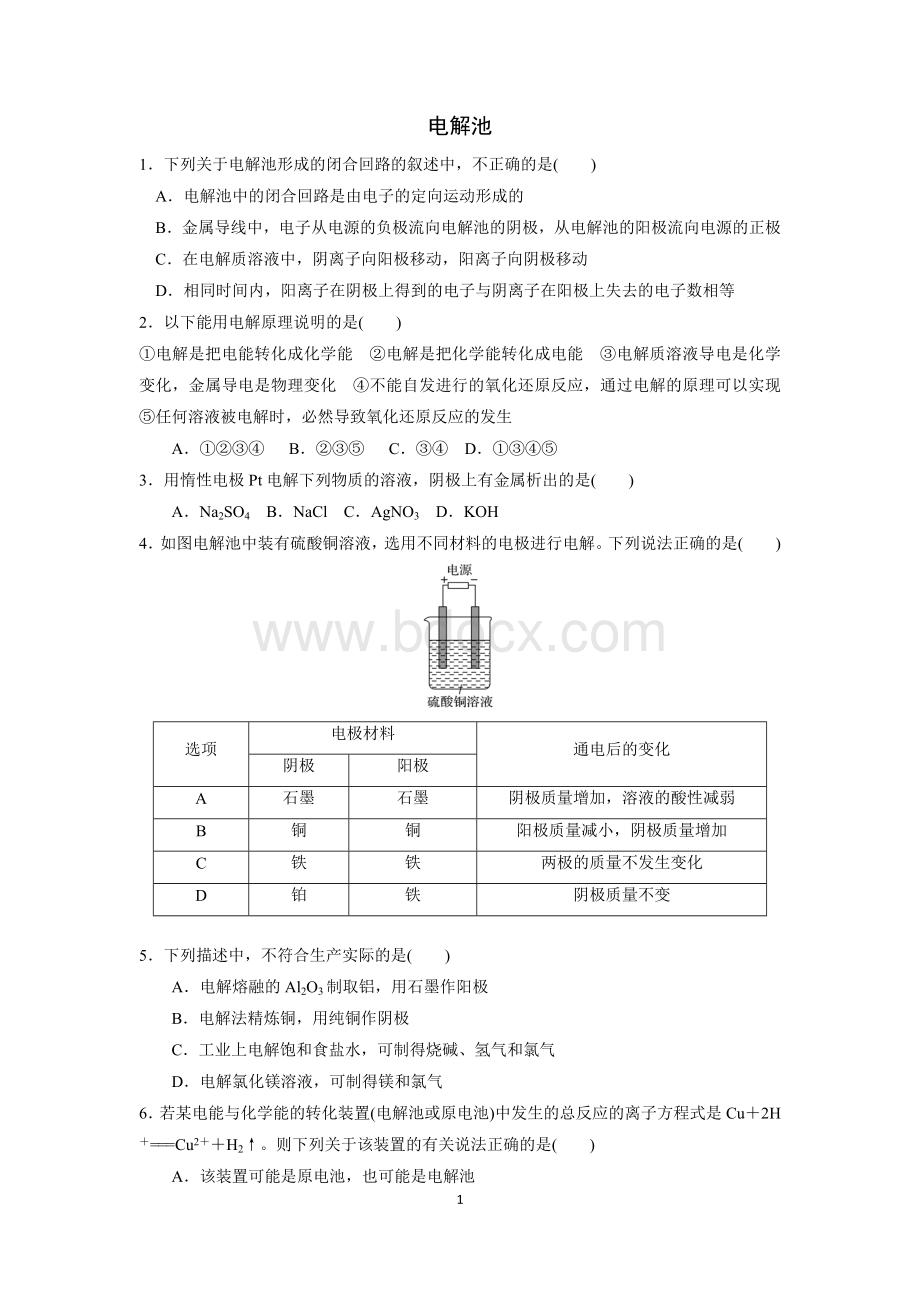
4.如图电解池中装有硫酸铜溶液,选用不同材料的电极进行电解。
下列说法正确的是( )
选项
电极材料
通电后的变化
阴极
阳极
A
石墨
石墨
阴极质量增加,溶液的酸性减弱
B
铜
铜
阳极质量减小,阴极质量增加
C
铁
铁
两极的质量不发生变化
D
铂
铁
阴极质量不变
5.下列描述中,不符合生产实际的是( )
A.电解熔融的Al2O3制取铝,用石墨作阳极
B.电解法精炼铜,用纯铜作阴极
C.工业上电解饱和食盐水,可制得烧碱、氢气和氯气
D.电解氯化镁溶液,可制得镁和氯气
6.若某电能与化学能的转化装置(电解池或原电池)中发生的总反应的离子方程式是Cu+2H+===Cu2++H2↑。
则下列关于该装置的有关说法正确的是( )
A.该装置可能是原电池,也可能是电解池
B.该装置只能是原电池,且电解质溶液为硝酸
C.该装置只能是电解池,且金属铜为该电解池的阳极
D.该装置只能是原电池,电解质溶液不可能是盐酸
7.以CuSO4溶液为电解质溶液进行粗铜(含Al、Zn、Ag、Pt、Au等杂质)的电解精炼,下列说法正确的是( )
A.电能全部转化为化学能B.粗铜接电源正极,发生还原反应
C.溶液中Cu2+向阳极移动D.利用阳极泥可回收Ag、Pt、Au等金属
8.下列各组溶液电解一段时间后,再加入相关物质,溶液能恢复原状况的是( )
选项
电解质溶液
阳极
阴极
加入的物质
A
NaCl溶液
碳
铁
盐酸
B
NaOH溶液
碳
碳
水
C
硫酸铜溶液
碳
碳
硫酸铜
D
硫酸
铁
碳
H2O
9.用Pt作电极电解下列某种溶液,当阳极生成112mL气体时,阴极上析出0.64g金属。
则该电解池中溶质可能是( )
A.CuSO4B.MgSO4C.Al2(SO4)3D.Na2SO4
10.Cu2O是一种半导体材料,基于绿色化学理念,设计制取Cu2O的电解池示意图如下,电解总反应:
2Cu+H2OCu2O+H2↑。
下列说法正确的是( )
A.石墨电极上产生氢气
B.铜电极发生还原反应
C.铜电极接直流电源的负极
D.当有0.1mol电子转移时,有0.1molCu2O生成
11.根据如图所示电化学实验装置图,回答下列问题。
(1)若只闭合S1,该装置属于________,能量转化形式为________,锌极作________极。
(2)若只闭合S2,该装置属于________,能量转化形式为________,锌极上所发生反应的电极方程式为________________________________________________________
________________________________________________________________________。
(3)若只闭合S3,该装置属于________,铜极作________极,锌极上所发生反应的电极方程式为____________,总反应的化学方程式为____________________。
12.如图是电解CuCl2溶液的装置,其中c、d为石墨电极。
(1)正极为________(填“a”或“b”),阳极为________(填“c”或“d”)。
(2)阳极反应式为_____________________________________________
________________________________________________________________________,
检验该阳极产物的方法是________。
(3)电解一段时间后发现阴极增重6.4g,则外电路中通过的电子的物质的量是________mol,若该电解反应所需的电子全部由氢氧燃料电池提供,则至少需要消耗________L氢气(标准状况下)才能满足需要。
13.电解原理在化学工业中有广泛应用。
如图表示一个电解池,装有电解液a;X、Y是两块电极板,通过导线与直流电源相连。
请回答以下问题:
(1)若X、Y都是惰性电极,a是饱和NaCl溶液,实验开始时,同时在两边各滴入几滴酚酞溶液,则:
①电解池中X极上的电极反应式为__________________________________________。
在X极附近观察到的实验现象是_________________________________________
________________________________________________________________________。
②Y电极上的电极反应式为_______________________________________________。
(2)如要用电解方法精炼粗铜,电解液a选用CuSO4溶液,则
①X电极的材料是__________________,电极反应式为
________________________________________________________________________。
②Y电极的材料是________,电极反应式为_______________________________________
______________________。
(说明:
杂质发生的电极反应不必写出)
14.某兴趣小组的同学用下图所示装置研究有关电化学的问题。
当闭合该装置的电键时,观察到电流计的指针发生了偏转。
请回答下列问题:
(1)甲装置的名称是________(填“原电池”或“电解池”),Zn为________极,Pt为________极。
(2)写出电极反应式:
Pt极_______________________________________________,
Cu极______________________________。
当甲中产生0.1mol气体时,乙中析出铜的质量应为________________________________________________________________________。
(3)若乙中溶液不变,将其电极都换成铜电极,电键闭合一段时间后,乙中溶液的颜色________(填“变深”、“变浅”或“不变”)。
答案
1A2D3C4B5D6C7D8B9A10A
11答案
(1)原电池 化学能转化为电能 负
(2)电解池 电能转化为化学能 Zn-2e-===Zn2+
(3)电解池 阳 2H++2e-===H2↑ Cu+H2SO4CuSO4+H2↑
解析
(1)若只闭合S1,没有外接电源,则Zn、Cu、稀硫酸构成原电池,该装置将化学能转化为电能,较活泼的锌作负极。
(2)若只闭合S2,装置中有外接电源,该装置为电解池,将电能转化为化学能,与电源正极相连的锌极作阳极,锌被氧化。
(3)若只闭合S3,该装置为电解池,与电源正极相连的铜极作阳极,铜被氧化,溶液中的H+在阴极(锌极)上被还原为H2。
12答案
(1)a c
(2)2Cl--2e-===Cl2↑ 用湿润的淀粉碘化钾试纸放在该电极附近,试纸变蓝 (3)0.2 2.24
13答案
(1)①2H++2e-===H2↑ 放出气体,溶液变红
②2Cl--2e-===Cl2↑
(2)①纯铜 Cu2++2e-===Cu
②粗铜 Cu-2e-===Cu2+
解析
(1)用惰性电极电解饱和食盐水时阳极反应为2Cl--2e-===Cl2↑;阴极反应为2H++2e-===H2↑。
X极反应产物为H2和NaOH,H2逸出,NaOH使溶液呈现碱性,加入酚酞变红,Y极产生氯气,能使湿润的淀粉碘化钾试纸变蓝色。
14答案
(1)原电池 负 阳
(2)2Cl--2e-===Cl2↑2H++2e-===H2↑ 6.4g (3)不变
解析
(1)由图中的铜、锌两种电极和电解质稀硫酸构成闭合电路知:
该装置为原电池,Zn活泼,则Zn作负极;乙为电解池,Pt作阳极。
(2)甲装置为原电池,乙装置为电解池,石墨和铂都为惰性电极,连接电源正极的铂电极为电解池的阳极,发生氧化反应:
2Cl--2e-===Cl2↑,Cu为原电池的正极,发生还原反应:
2H++2e-===H2↑。
连接电源负极的碳电极为电解池的阴极,发生:
Cu2++2e-===Cu,根据电子守恒,当甲中产生0.1mol气体时,铜正极上发生2H++2e-===H2↑,转移0.2mol电子,根据Cu2++2e-===Cu,乙中析出铜0.1mol,即6.4g。
(3)若乙中溶液不变,将其电极都换成铜电极,电键闭合一段时间后,为电镀池,阳极铜溶解Cu-2e-===Cu2+,阴极铜上铜离子得电子析出金属铜Cu2++2e-===Cu,溶液中铜离子颜色为蓝色,溶液中c(Cu2+)不变,所以颜色不变
5