北京高三二模化学实验汇编.doc
《北京高三二模化学实验汇编.doc》由会员分享,可在线阅读,更多相关《北京高三二模化学实验汇编.doc(10页珍藏版)》请在冰豆网上搜索。
实验
海淀13年2模
27.(14分)硫化氢(H2S)是一种具有臭鸡蛋气味的无色气体,有剧毒;存在于多种生产过程以及自然界中。
在人体的很多生理过程中也起着重要作用。
资料:
①H2S可溶于水(约1:
2),其水溶液为二元弱酸。
②H2S可与许多金属离子反应生成沉淀。
③H2S在空气中燃烧,火焰呈淡蓝色。
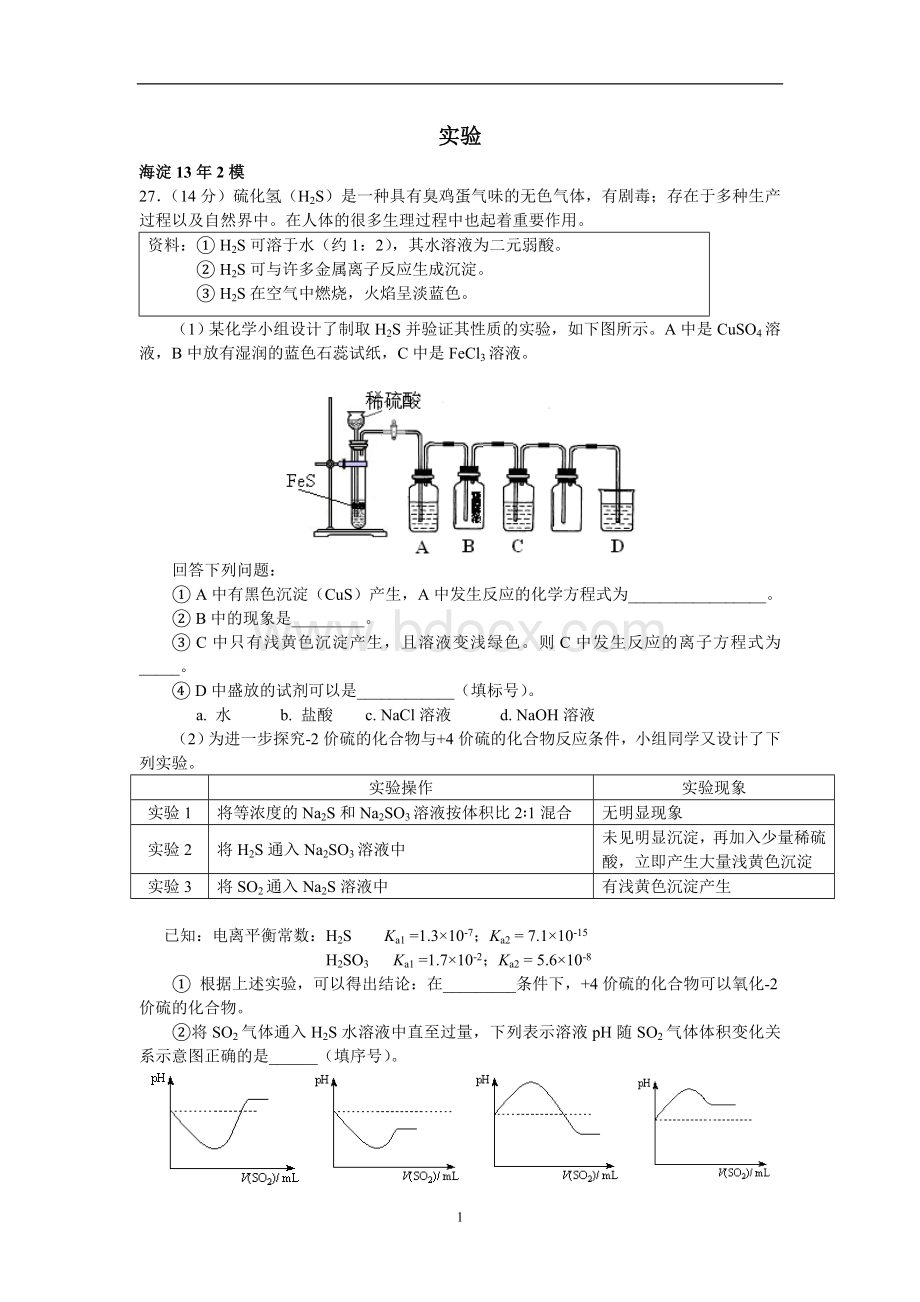
(1)某化学小组设计了制取H2S并验证其性质的实验,如下图所示。
A中是CuSO4溶液,B中放有湿润的蓝色石蕊试纸,C中是FeCl3溶液。
回答下列问题:
①A中有黑色沉淀(CuS)产生,A中发生反应的化学方程式为_________________。
②B中的现象是_________。
③C中只有浅黄色沉淀产生,且溶液变浅绿色。
则C中发生反应的离子方程式为_____。
④D中盛放的试剂可以是____________(填标号)。
a.水b.盐酸c.NaCl溶液d.NaOH溶液
(2)为进一步探究-2价硫的化合物与+4价硫的化合物反应条件,小组同学又设计了下列实验。
实验操作
实验现象
实验1
将等浓度的Na2S和Na2SO3溶液按体积比2∶1混合
无明显现象
实验2
将H2S通入Na2SO3溶液中
未见明显沉淀,再加入少量稀硫酸,立即产生大量浅黄色沉淀
实验3
将SO2通入Na2S溶液中
有浅黄色沉淀产生
已知:
电离平衡常数:
H2SKa1=1.3×10-7;Ka2=7.1×10-15
H2SO3Ka1=1.7×10-2;Ka2=5.6×10-8
①根据上述实验,可以得出结论:
在_________条件下,+4价硫的化合物可以氧化-2价硫的化合物。
②将SO2气体通入H2S水溶液中直至过量,下列表示溶液pH随SO2气体体积变化关系示意图正确的是______(填序号)。
A
B
C
D
(3)文献记载,常温下H2S可与Ag发生置换反应生成H2。
现将H2S气体通过装有银粉的玻璃管,请设计简单实验,通过检验反应产物证明H2S与Ag发生了置换反应_______。
西城13年2模
27.(16分)某小组同学为探究H2O2、H2SO3、Br2氧化性强弱,设计如下实验(夹持仪器已略去,装置的气密性已检验)。
实验记录如下:
实验操作
实验现象
I
打开活塞a,滴加氯水,关闭活塞a
A中溶液变为红棕色。
II
吹入热空气
A中红棕色明显变浅;B中有气泡,产生大量白色沉淀,混合液颜色无明显变化。
III
停止吹入空气,打开活塞b,逐滴加入H2O2溶液
开始时颜色无明显变化;继续滴加H2O2溶液,一段时间后,混合液逐渐变成红棕色。
请回答下列问题:
(1)A中反应的离子方程式是。
(2)实验操作II吹入热空气的目的是。
(3)装置C的作用是,C中盛放的药品是。
(4)实验操作III,混合液逐渐变成红棕色,其对应的离子方程式。
(5)由上述实验得出的结论是。
(6)实验反思:
①有同学认为实验操作II吹入的热空气,会干扰(5)中结论的得出,你认为是否干扰,理由是。
②实验操作III,开始时颜色无明显变化的原因是(写出一条即可):
。
东城13年2模
27.(14分)某兴趣小组用Ⅰ装置制取漂白液(气密性已检验,试剂已添加),并研究其相关性质。
实验操作和现象:
打开分液漏斗的活塞,缓缓滴加一定量浓盐酸,点燃酒精灯;一段时间后,关闭分液漏斗的活塞,熄灭酒精灯。
(1)烧瓶中反应的化学方程式是。
(2)饱和食盐水的作用是。
(3)若用图Ⅱ装置收集多余的氯气,请在虚线框内画出该装置简图。
(4)该小组同学用上述装置制得的漂白液中NaClO的浓度偏低。
查阅资料:
在溶液中发生反应:
(a)Cl2(g)+2NaOH(aq)═NaCl(aq)+NaClO(aq)+H2O(l)DH1=-101.1kJ/mol
(b)3NaClO(aq)═2NaCl(aq)+NaClO3(aq)DH2=-112.2kJ/mol
反应(a)的反应速率很快,反应(b)在室温下较慢
根据资料,请对图Ⅰ装置提出改进建议:
。
(5)修改方案后,该小组同学制得了较高浓度的NaClO溶液。
他们把漂白液和滴有酚酞的红色Na2SO3溶液混合后,得到无色溶液。
提出猜想:
ⅰ.NaClO把Na2SO3氧化了ⅱ.NaClO把酚酞氧化了
ⅲ.NaClO把Na2SO3和酚酞均氧化了
①下列实验方案中可以证明NaClO氧化了Na2SO3的是。
a.向混合后的溶液中加入过量盐酸
b.向混合后的溶液中加入过量盐酸,再加入氯化钡溶液
c.向混合后的溶液中加入过量硝酸,再加入硝酸银溶液
d.向混合后的溶液中加入氢氧化钡溶液,再加入过量盐酸
②为证明NaClO氧化了酚酞,可进行的实验是。
朝阳13年2模27.(16分)某实验小组把CO2通入饱和Na2CO3溶液制取NaHCO3,装置如图所示(气密性已检验,部分夹持装置略):
(1)D中产生NaHCO3的化学方程式是。
(2)请结合化学平衡移动原理解释B中溶液的作用。
(3)当D中有大量白色固体析出时,停止实验,将固体过滤、洗涤、干燥备用。
为确定固体的成分,实验小组设计方案如下(称取一定质量的固体,配成1000mL溶液作为样液,其余固体备用):
①方案1:
取样液与澄清的Ca(OH)2溶液混合,出现白色沉淀。
实验小组对现象产生的原理进行分析,认为该方案不合理,理由是。
②方案2:
取样液与BaCl2溶液混合,出现白色沉淀并有气体产生。
实验小组认为固体中存在NaHCO3,其离子方程式是。
该小组认为不能确定是否存在Na2CO3,你认为该结论是否合理?
_____。
③方案3:
实验小组中甲、乙同学利用NaHCO3的不稳定性进行如下实验:
甲同学:
取样液400mL,用pH计测溶液pH,再水浴加热蒸发至200mL,接下来的操作是,结果表明白色固体中存在NaHCO3。
为进一步证明白色固体是否为纯净的NaHCO3,结合甲同学实验,还应补充的实验是。
乙同学:
利用仪器测定了固体残留率随温度变化的曲线,如下图所示。
a.根据A点坐标得到的结论是。
b.根据B点坐标,计算残留固体中
n(NaHCO3:
n(Na2CO3))=。
通过上述实验,该小组认为,可以向饱和Na2CO3溶液中通入过量CO2制备NaHCO3。
13年丰台2模
27.(15分)某课外活动小组探究镁与CO2、NO2的反应
①实验发现点燃的镁条能在CO2气体中继续燃烧,产生黑、白两种固体,请用化学反应
解释该现象。
(2)该小组采用类比Mg与CO2反应的思路对Mg与NO2的反应进行预测:
写出Mg与NO2反应的化学方程式。
Mg
弹簧夹
特种不锈
钢钢板
NO2
B
A
水
(3)设计实验验证猜测(用于连接玻璃管的乳胶管均内衬锡纸)
资料信息:
2NO2+2NaOH=NaNO3+NaNO2+H2O
①装置A中的试剂是。
②干燥管和装置B的作用分别是、。
③实验开始时正确的操作步骤是。
a.通入NO2
b.打开弹簧夹
c.点燃酒精灯
d.当硬质玻璃管充满红综色气体后,关闭弹簧夹
(4)实验结束时,同学们观察到与预测相符合的现象,但当用水洗涤硬质玻璃管时,固
体遇水产生有刺激性气味的气体,该气体能使湿润的石蕊试纸变蓝。
①同学们认为硬质玻璃管中还发生了另一个反应,该反应为。
②请用化学方程式解释加水产生该气体的原因。
顺义27.(16分)亚硝酸钠是重要的防腐剂。
某化学兴趣小组以碳和浓硝酸为起始原料,设计如下装置利用一氧化氮与过氧化钠反应制备亚硝酸钠。
(夹持装置和A中加热装置已略,气密性已检验),
查阅资料:
①HNO2为弱酸,室温下存在反应3HNO2=HNO3+2NO↑+H2O;
②在酸性溶液中,NO2-可将MnO4-还原为Mn2+且无气体生成。
③NO不与碱反应,可被酸性KMnO4溶液氧化为硝酸
实验操作:
①关闭弹簧夹,打开A中分液漏斗活塞,滴加一定量浓硝酸,加热;
②一段时间后停止加热;③从C中取少量固体,检验是否是亚硝酸钠。
(1)A中反应的化学方程式是。
(2)B中观察的主要现象是, D装置的作用是。
(3)检验C中产物有亚硝酸钠的操作是。
(4)经检验C产物中亚硝酸钠含量较少。
a.甲同学认为C中产物不仅有亚硝酸钠,还有碳酸钠和氢氧化钠。
生成碳酸钠的化学方程式是________。
为排除干扰甲在B、C装置间增加装置E,E中盛放的试剂应是________(写名称)。
b.乙同学认为除上述干扰因素外,还会有空气参与反应导致产品不纯,所以在实验操作①前应增加一步操作,该操作是________。
(5)实验经改进后可制得较纯亚硝酸钠,下列关于亚硝酸钠的说法正确的是________。
a.亚硝酸钠有咸味,可代替食盐食用
b.常温下,0.1mol/L亚硝酸钠溶液pH>1
c.0.1mol/L亚硝酸钠溶液中存在:
c(Na+)+c(H+)=c(NO2—)+c(OH—)
d.0.1mol/L亚硝酸钠溶液中存在:
c(NO2—)>c(Na+)>c(OH—)>c(H+)
房山27.(15分)资料显示:
在煤中加入适量石灰石粉可使煤(含S)燃烧时产生的SO2转化成固体CaSO4,从而减少SO2排放,该方法被称为钙基固硫。
这一过程是通过以下两步反应实现的:
㈠CaCO3CaO+CO2㈡2CaO+2SO2+O2=2CaSO4
对此,某实验小组利用下列实验装置和药品对其可行性进行了模拟探究。
已知实验所用样品:
Ⅰ:
S粉与CaCO3粉末的混合物;Ⅱ:
CaSO4粉末
(1)实验一:
①取样品Ⅰ装入A中。
连续通入过量O2,加热至50