动物细胞染色体荧光原位杂交.docx
《动物细胞染色体荧光原位杂交.docx》由会员分享,可在线阅读,更多相关《动物细胞染色体荧光原位杂交.docx(10页珍藏版)》请在冰豆网上搜索。
动物细胞染色体荧光原位杂交
动物细胞染色体荧光原位杂交(fluorescenceinsituhybridization,FISH)
FISH(fluorescence in situ hybridization)技术是一种重要的非放射性原位杂交技术,其基本原理是利用被检测的染色体上的靶DNA与所用的核酸探针(probes)间的序列同源互补性,经“变性→退火→复性”,形成靶DNA与核酸探针的杂交体
关键词:
动物细胞染色体荧光原位杂交fluorescenceinsituhybridizationFISH核酸探针probes
实验目的:
使学生掌握染色体荧光原位杂交(fluorescenceinsituhybridization,FISH)分析技术,了解染色体荧光原位杂交分析技术的应用价值。
实验原理:
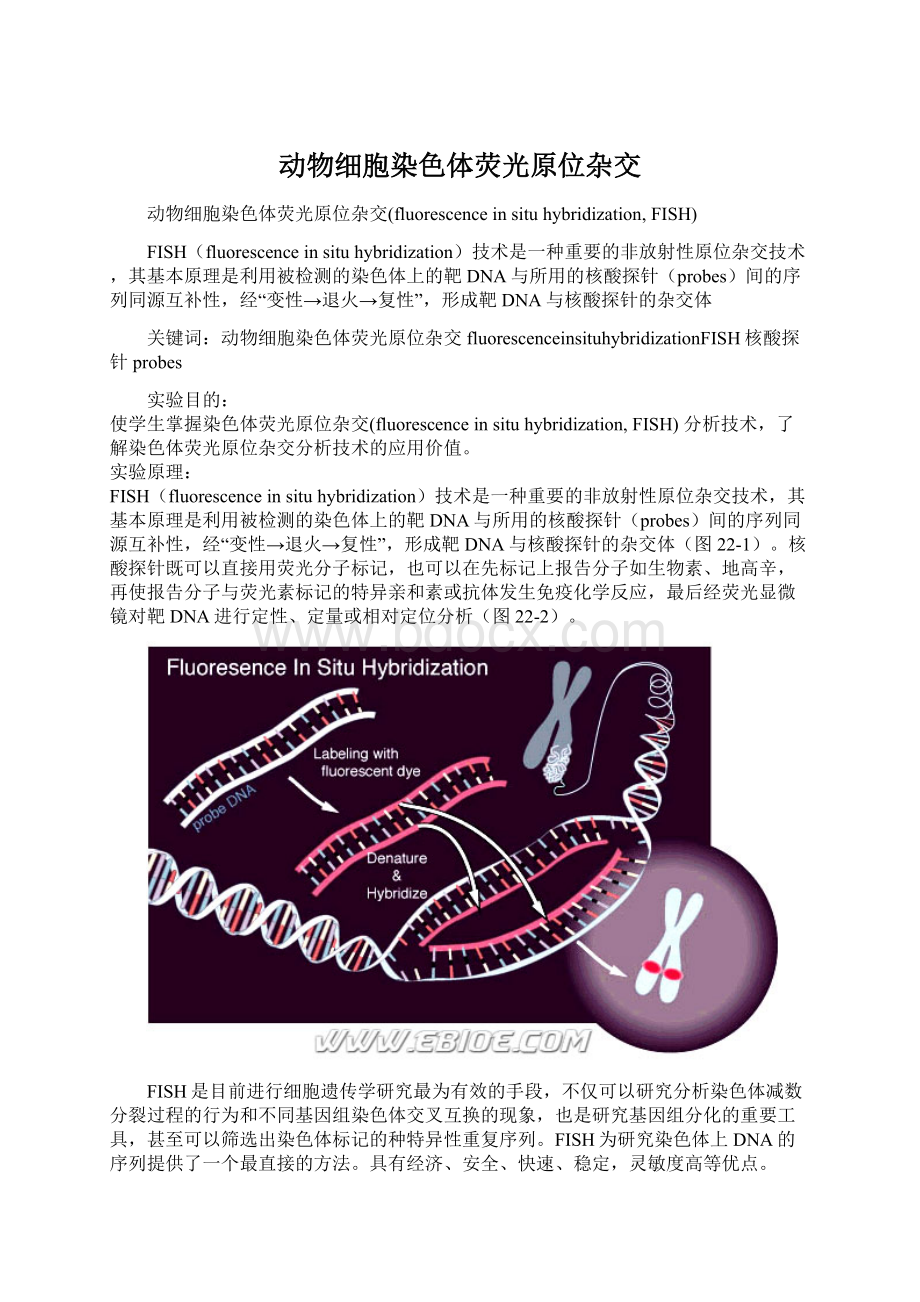
FISH(fluorescenceinsituhybridization)技术是一种重要的非放射性原位杂交技术,其基本原理是利用被检测的染色体上的靶DNA与所用的核酸探针(probes)间的序列同源互补性,经“变性→退火→复性”,形成靶DNA与核酸探针的杂交体(图22-1)。
核酸探针既可以直接用荧光分子标记,也可以在先标记上报告分子如生物素、地高辛,再使报告分子与荧光素标记的特异亲和素或抗体发生免疫化学反应,最后经荧光显微镜对靶DNA进行定性、定量或相对定位分析(图22-2)。
FISH是目前进行细胞遗传学研究最为有效的手段,不仅可以研究分析染色体减数分裂过程的行为和不同基因组染色体交叉互换的现象,也是研究基因组分化的重要工具,甚至可以筛选出染色体标记的种特异性重复序列。
FISH为研究染色体上DNA的序列提供了一个最直接的方法。
具有经济、安全、快速、稳定,灵敏度高等优点。
FISH中使用的探针有:
(1)基因组探针(genomicprobe):
人类基因组内一些高频率的重复序列,在进化上很少具有保守性。
若以基因组DNA作为探针,这些存在于探针和靶细胞DNA序列中的高度重复序列之间会首先退火结合,越过那些保守的和单一的序列,故杂交会呈现出种特异性。
基因组重复序列包括:
着丝点重复(Centromererepeats)、端粒重复(Telomererepeats)、核糖体DNA(RibosomalDNA,rDNA)、Interspersedrepetitiveelements(SINEs,LINEs)等(图22-3、4)。
(2)染色体特异性序列探针(proberecognizingchromosomespecificsequences):
目前在人几乎所有染色体中已经克隆出一些重复序列,重复一百到五千次不等,各具染色体特异性。
大多在某一染色体的着丝粒区或异染色质区产生致密的杂交带。
从而可特异性地识别某一染色体(图22-5)。
(3)染色体文库探针(chromosomelabrariesprobe):
染色体文库收集人类单条染色体的DNA作为探针,又称整体染色体探针。
单条染色体的获得一般有两种方法:
来自仅携有某一条人类染色体的体细胞杂交株,或经流式细胞分类仪从染色体悬液中分离。
(4)单一序列探针(single-copysequencesprobe):
FISH有一弱点,就是要求探针足够大,探针越小,杂交位点检出率就越低。
欲利用FISH检测存在基因组内的单一序列基因,最有效的方法是应用含大插入片段的克隆载体,如全Cosmids(载约40kb的插入片段),更大的YAC载体(载100-800kb插入片段)。
若掌握好,小到2kb的质粒探针亦可用FISH方法定位,但效率较低(图22-6)。
图22-2
24色mFISH(MulticolorFISH)核型分析技术是近年建立的一种新技术。
其原理是使用5种荧光染料按比例标记探针,杂交后形成24条染色体各自呈现特异的荧光色彩以供核型分析(图22-7,8)。
为研究人员提供了更丰富详尽的细胞遗传学信息,包括确定标记染色体的来源、检测微小的染色体易位和检测复杂的染色体易位,尤其为肿瘤细胞染色体分析提供了全新、高效的方法。
FISH的应用领域有:
(1)基因定位与基因制图(genemapping)。
FISH已经极大地加速了人类基因定位和基因制图的进程。
(2)基因诊断(genediagnosis)。
精确、直观、明了;(3)间期细胞遗传学(interphasecytogenetics);(4)FISH在肿瘤生物学中的应用:
①肿瘤细胞遗传学(onco-cytogenetics);②基因定位:
FISH可用于分离出的癌基因与抑癌基因初步定位;③病毒基因插入基因组部分的检测。
利用FISH可以检测到病毒整合到人基因组中的情况,对深入研究病毒致癌机理,以及检测、防治肿瘤均具有重要意义;④基因的扩增与缺失:
原癌基因的激活与抑癌基因的失活是目前肿瘤研究的热点。
已知原癌基因的激活方式有:
突变、基因扩增、易位、病毒序列插入。
抑癌基因的失活方式有:
点突变、基因缺失。
FISH为研究基因的扩增和缺失提供了新的方法,能将基因扩增和染色体重复分开。
图22-3TelomeresFISH
图22-4FISHwithrepetitiveprobestohumanchromosomes
(a)FISHwitha"pan-centromeric"probedelineatesallcentromeres.(b)Aprobecontainingthehighlyconservedrepetitivesequencehybridizedtoalltelomeres.(c)ArDNAprobehybridizedtoallhumanNORbearingchromosomes(chromosome13-15,21,22).(d)FISHwiththedisperserepetitiveAlumimicsaRbandingpattern.(From:
)
图22-5Humanchromosome1
图22-6特异位点定位BACFISH
图22-724色染色体mFISH核型分析
图22-8
实验试剂:
[1].γ-氨基丙基三乙氧基硅烷(APTES)
[2].细胞的培养、秋水仙素处理、低渗及固定处理试剂同实验27。
[3].端粒DNA检测探针:
5′-FITC-CCCTAACCCTAACCCTAA-3′;FITC的激发波长为494nm和发射波长518nm。
探针在合成时,同时进行5′末端的生物素(biotin)、或地高辛(DIG)、或荧光标记(如FITC、Cy3等)标记。
注意:
DNA探针标记物荧光检测的荧光分子激发和发射波长不能和复染液中DAPI染料的激发和发射波长重叠,应有较大差值,避免相互干扰。
[4].鲑鱼精DNA(SalmonSpermDNA):
超声打碎。
[5].20×SSC(pH7.0):
3MNaCl,0.3M柠檬酸钠(sodiumcitrate),NaOH调pH为7.0,高压灭菌,室温保存。
[6].甲酰胺(formamyde)(去离子,pure)
[7].50%硫酸葡萄糖(DextranSolfate)
[8].250mM磷酸钠(sodiumphosphate)(pH7.0)
[9].Hybridizationbuffer:
50%deionizedformamide,2×SSC,50mMsodiumphosphate(pH7.0),5%dextransulfate,and3ng/mlprobe.
[10].变性液A:
70%甲酰胺,2×SSC,用1MHCl调pH到7.0,加入50mM磷酸钠以维持pH。
[11].漂洗液A:
30%~50%甲酰胺,2×SSC;用1MHCl调pH到7.0。
[12].漂洗液B:
0.1~1×SSC;用1MHCl调pH到7.0。
[13].漂洗液C:
2×SSC,0.1%Tween20;用1MHCl调pH到7.0。
[14].封闭液:
5%BSA或脱脂奶粉,4×SSC
[15].复染液:
2×SSC,0.1%Tween20,200ng/mlDAPI。
也可以使用10ng/ml碘化丙锭(PI)或Hoechst33258(500ng/ml)。
DAPI,即4',6-二脒基-2-苯基吲哚(4',6-diamidino-2-phenylindole)。
DAPI是一种可以穿透细胞膜的蓝色荧光染料。
和双链DNA结合后可以产生比DAPI自身强20多倍的荧光。
和EB(ethidiumbromide)相比,对双链DNA的染色灵敏度要高很多倍。
DAPI的最大激发波长为340nm,最大发射波长为488nm;DAPI和双链DNA结合后,最大激发波长为364nm,最大发射波长为454nm。
DAPI溶液用水配制。
用于细胞核染色时,推荐的DAPI工作浓度为0.5-10μg/ml。
Hoechst33258,也称bisBenzimideH33258或HOE33258。
Hoechst33258是一种可以穿透细胞膜的蓝色荧光染料,对细胞的毒性较低。
Hoechst33258染色常用于细胞凋亡检测,染色后用荧光显微镜观察或流式细胞仪检测。
Hoechst33258也常用于普通的细胞核染色,或常规的DNA染色。
Hoechst33258的最大激发波长为346nm,最大发射波长为460nm;Hoechst33258和双链DNA结合后,最大激发波长为352nm,最大发射波长为461nm。
Hoechst33258溶于水,溶解度可达10mg/ml。
用于细胞核染色时,推荐的Hoechst33258工作浓度为0.5~10μg/ml。
[16].封片液:
2.5%DABOCO或1%邻苯胺二盐酸,200mMTris-HCl,pH8.6,90%甘油。
[17].coplinjar:
实验步骤:
[1].从体外培养的贴壁细胞准备的中期染色体标本:
A.细胞的培养、秋水仙素处理、低渗处理、固定处理同实验21。
B.载玻片用硫酸洗液浸泡过夜,清洗烘干,在5%APTES-乙醇溶液中60℃处理
3h,取出清洗,70℃干燥备用。
C.将固定后的细胞滴于APTES修饰的载玻片上,空气干燥。
D.脱水:
70%、90%和100%乙醇脱水,每次5min,空气干燥。
注意:
室温下玻片标本可保存数天到数周;若载玻片要长期保存,应在室温下过夜使组织“老化”(aged),然后放入容器中,该容器密封于含干燥剂的塑料袋内,-70℃保存。
-20℃保存的玻片可在6个月内使用;-70℃可保存一年以上;但标本一旦溶化,则不能在此冷冻。
[2].染色体标本变性及脱水:
A.载玻片静置60℃烤箱孵育预热。
B.变性液A在水浴中加热至70℃。
C.将染色体标本载玻片浸入变性液A中,70℃作用2min。
D.脱水:
立即将载玻片依次移入冰冷的70%、90%及100%乙醇中,各保持5min。
空气干燥玻片。
[3].探针杂交液的准备(10μl/片):
A.10~20ng探针DNA和1~3μg鲑鱼精DNA混合,热块干燥DNA。
B.DNA中加入6~7μl甲酰胺,悬浮DNA,保持30min。
C.DNA溶液中加入1μl20×SSC(终浓度2×SSC)、2μl硫酸葡萄糖(终浓度10%)、1μl250mM磷酸钠(终浓度25mM)。
保持30min。
D.75℃变性DNA探针5min。
[4].染色体标本的杂交:
A.将10μl含变性探针的杂交液加至载玻片的变性靶DNA上。
B.在杂交液液滴上小心地盖上18×18cm的盖玻片,避免压入气泡。
C.载玻片置于湿盒内,37℃温育过夜。
D.杂交结束前,42℃水浴预热漂洗液A,60℃水浴预热漂洗液B。
E.载玻片移入42℃预热的漂洗液A中,在42℃水浴中振荡10min直至盖玻片脱落。
F.载玻片移入另一份42℃预热的漂洗液A中,振荡5min,更换漂洗液A两次,每次振荡5min。
G.载玻片移入含60℃预热的漂洗液B中,漂洗5min,更换漂洗液两次,每次漂洗5min。
若DNA探针用荧光标记,则无需进行下列检测步骤,可直接进行显微镜荧光观察。
[5].染色体标本的检测:
A.载玻片滴加50~200μl封闭液,22×40mm盖玻片覆盖,置湿盒内,37℃温育至少30min。
取出载玻片,无菌水轻轻冲去盖玻片。
B.用封闭液配制的检测化合物溶液(1~20μg/ml)。
如荧光素偶联的链亲和素(streptavidin),或抗地高辛抗体(Anti-DIG-fluorescent-conjugate)溶液。
C.载玻片上滴加50μl含荧光标记分子的检测液,22×40mm盖玻片覆盖,置湿盒内,37℃温育30min,或室温放置1h。
D.取出载玻片,无菌水轻轻冲去盖玻片;将载玻片移入漂洗液C中,42℃振荡漂洗3次,每次5min。
[6].将载玻片置入含复染液中,室温振荡20min。
[7].将载玻片移入漂洗液C中,室温温育1~2min。
[8].载玻片上滴加10~50μl甘油封片液,22×40mm盖玻片覆盖,用洁净指甲油封闭玻片。
玻片在-20℃或-70℃暗处保存数天或数月。
注意事项:
[1].进行荧光物质的实验步骤时,采取避光措施。
[2].DAPI对人体有一定刺激性,请注意适当防护。
[3].原位杂交最好使用易透过细胞膜进入胞内或核内的寡核苷酸探针和短的PCR标记探针(80~150bp)。
[4].原位杂交中,无论应用何种标记探针,其用量均为0.5~5.0μg/ml。
[5].最适复性温度(Optimunmrenaturationtemperature,TOR):
TOR=Tm–25℃。
[6].苛刻复性温度:
Ts=Tm–(10或15℃)
[7].非苛刻复性温度:
Tns=Tm–(30或35℃)
参考文献:
Fluorescenceinsituhybridization.NatureMethods2005,2(3):
237-238
示例图片:
Insituhybridizationofa-satelliteprobestohumanchromosomes1,15and17detectedbytyramidesignalamplification.a-Satelliteprobestochromosomes1,15and17werelabeledbynicktranslationwithbiotin-11-dUTP,TexasRed-12-dUTPandOregonGreen488-5-dUTP,respectively.Followingsimul¬taneoushybrid¬izationofallthreeprobes,thebiotin¬ylatedchromosome1probewasdetectedwithHRP–streptavidinconjugateandAlexaFluor546tyramide.HRPactivityfromthisfirstTSAdetectionstepwasthenquenchedbytreatmentwith1%hydrogenperoxidefor30minutes.Lastly,theOregonGreen488dye–labeledchromosome17probewasdetectedwithanti-fluorescein/OregonGreenantibodyfollowedbyHRP-conjugatedgoatanti–mouseIgGantibodyandAlexaFluor594tyramide.HRPactivityfromthissecondTSAdetectionstepwasthenquenchedbytreatmentwith1%hydrogenperoxidefor30minutes.TheTexasReddye–labeledchromosome15probewasthendetectedwithrabbitanti–TexasRedantibodyfollowedbyHRP-conjugatedgoatanti–rabbitIgGantibodyandAlexaFluor488tyramide.AftercounterstainingwithHoechst33258,theimageswereacquiredusingfilters
appropriateforDAPI,FITC,TRITCandtheTexasReddye.