生物药物分析.docx
《生物药物分析.docx》由会员分享,可在线阅读,更多相关《生物药物分析.docx(21页珍藏版)》请在冰豆网上搜索。
生物药物分析
生物药物分析
第八章抗生素类药物的分析
一、效价的测定方法:
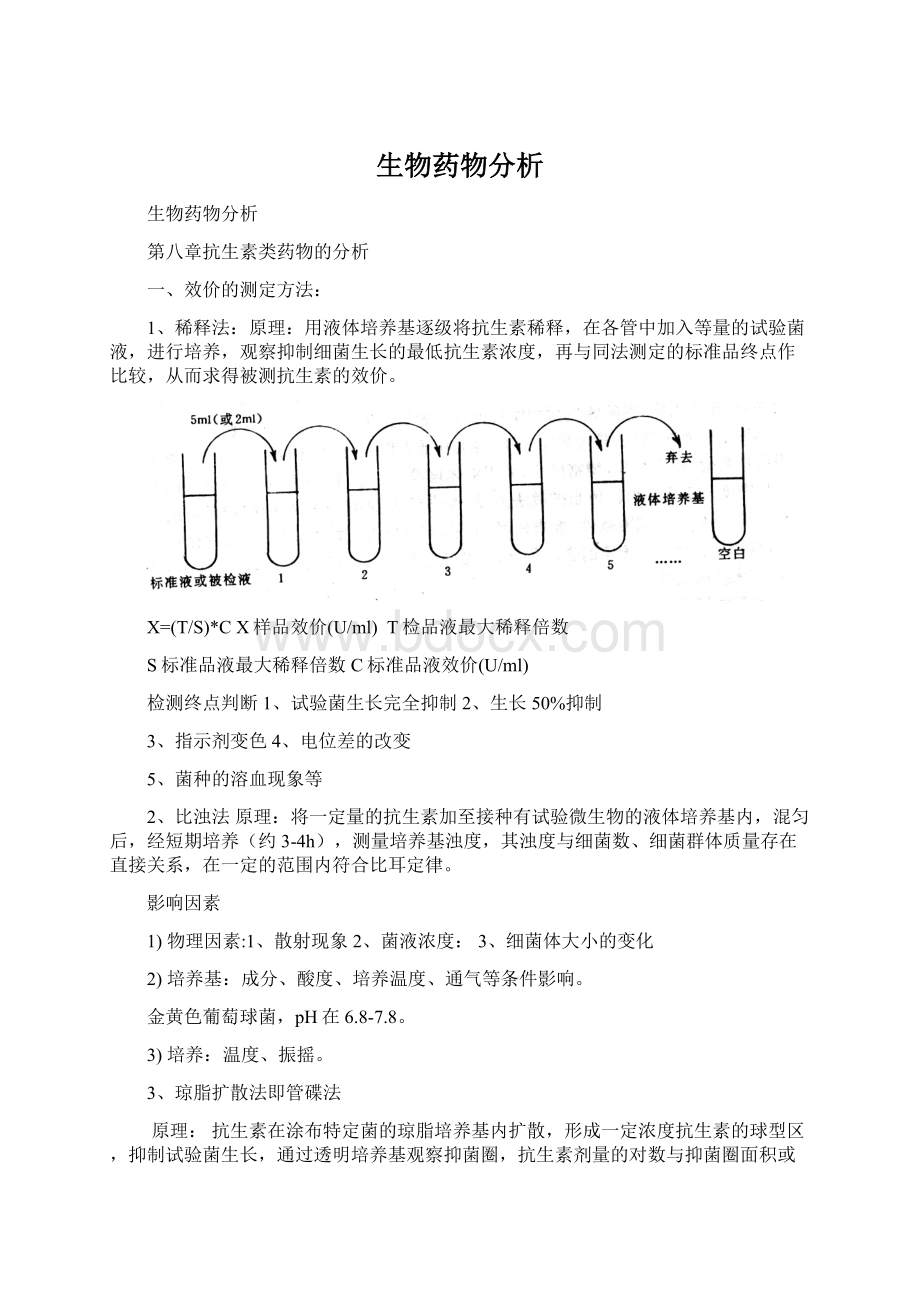
1、稀释法:
原理:
用液体培养基逐级将抗生素稀释,在各管中加入等量的试验菌液,进行培养,观察抑制细菌生长的最低抗生素浓度,再与同法测定的标准品终点作比较,从而求得被测抗生素的效价。
X=(T/S)*CX样品效价(U/ml)T检品液最大稀释倍数
S标准品液最大稀释倍数C标准品液效价(U/ml)
检测终点判断1、试验菌生长完全抑制2、生长50%抑制
3、指示剂变色4、电位差的改变
5、菌种的溶血现象等
2、比浊法原理:
将一定量的抗生素加至接种有试验微生物的液体培养基内,混匀后,经短期培养(约3-4h),测量培养基浊度,其浊度与细菌数、细菌群体质量存在直接关系,在一定的范围内符合比耳定律。
影响因素
1)物理因素:
1、散射现象2、菌液浓度:
3、细菌体大小的变化
2)培养基:
成分、酸度、培养温度、通气等条件影响。
金黄色葡萄球菌,pH在6.8-7.8。
3)培养:
温度、振摇。
3、琼脂扩散法即管碟法
原理:
抗生素在涂布特定菌的琼脂培养基内扩散,形成一定浓度抗生素的球型区,抑制试验菌生长,通过透明培养基观察抑菌圈,抗生素剂量的对数与抑菌圈面积或直径成正比。
在同样条件下将已知效价的标准品溶液与未知效价的供试品溶液的剂量反应(抑菌圈)进行比较;
当标准品和供试品是属于同一性质的抗生素时,标准品溶液和供试品溶液.对一定试验菌所得的剂量反应曲线,在一定剂量范围内应互相平行。
根据以上原理,可设计为一剂量法、二剂量法及三剂量法。
从而可以较为准确地测定供试品的效价
公式里各字母意义要记下。
影响抑菌圈半径的因素:
(1)D的影响因素:
抗生素本身结构、分子量等
杂质:
琼脂含量:
菌种对抗生素的吸附作用:
pH影响分子的形式、
温度影响扩散
D增大,r也增大
(2)T的影响:
一般T增加,r增大。
(3)M的影响:
在一定的范围内,小管内M越大,抑菌圈直径越大。
(4)C的影响:
C越小,抑菌圈直径越大
(5)H的影响:
培养基增厚,则抑菌圈减小。
操作步骤:
1、试验菌的纯化与悬液的制备
2、缓冲液、灭菌水与培养基的制备
3、标准品、供试品的称量、溶解与稀释
4、双碟的制备及放管
5、滴加药液
6、恒温培养
7、测量抑菌圈直径或面积
8、计算
二、可靠性测验:
通过统计各组均数间的方差,以试品间、回归、剂间(列)、碟间(行)……的方差与误差项(S2)的比值(称F值),来确定各自差异的显著性程度和实验结果的可靠性。
F值(F值=该项方差/误差项S2)可作为观察实验显著性程度的一个指标
试品间差异不显著(P>0.05)
回归项非常显著(P<0.01)
偏离平行不显著(P>0.05)
剂间差异显著(P<0.05)
碟间差异不显著(P>0.05)
三、链霉素呈色反应:
1、茚三酮反应:
蓝紫色化合物
2、坂口反应(sagaguchitest):
链霉素水解产物链霉胍特有。
链霉胍,8-羟喹啉分别与次溴酸钠反应,其各自的产物在相互作用生成橙红色化合物。
3、糖类反应:
莫利西反应(Molischtest),五碳糖或六碳糖在硫酸存在的条件下脱水成羟甲基糠醛,与蒽酮显蓝色,与α-奈酚呈红紫色。
4、埃尔松-摩根(Elson-Morgantest):
样品在强酸或强碱水解后释放出氨基己糖,在碱性条
件下与乙酰丙酮缩合,形成吡咯的衍生物,在碱性条件下与对二甲胺基苯甲醛的乙醇及盐酸溶液(Ehrlich试剂)成红色,在540nm处可定量测定。
5、麦芽酚反应(maltoltest):
链霉素在碱性溶液中水解,重排,生成麦芽酚在酸性溶液中与三价铁离子结合,形成紫红色络合物。
四、四环素类抗生素(了解)
(一)呈色反应
1、浓硫酸反应四环素深紫色;金霉素蓝色至绿色;
土霉素朱红色;强力霉素黄色;
2、三氯化铁反应:
含有酚羟基,遇三氯化铁立即呈色反应,
(二)荧光反应:
土霉素绿色荧光,四环素黄色荧光
(三)紫外光谱
(四)色谱
五、大环内酯抗生素(了解)
(一)呈色反应
1、硫酸反应:
遇硫酸均呈红棕色
2、莫利西反应:
糖类的反应
3、Seliwanaff反应:
脱水间苯二酚
糖糖醛衍生物具颜色产物
红霉素淡黄色;螺旋霉素亮紫红色;
碳霉素深青紫色;柱晶白霉素淡青色;
(二)薄层色谱
(三)光谱学鉴别
紫外光谱
红外光谱
六、利福霉素类抗生素(了解)
呈色反应:
1、浓盐酸反应:
2、三氯化铁:
向1ml利福霉素的溶液中,滴加三氯化铁乙醇溶液,有绿色,蓝绿色。
表明有酚羟基
3、硝酸盐反应:
利福平,溶液中加入硝酸钠溶液,颜色由橙色变为暗红色。
七、杂质检查
1、青霉素过敏原:
青霉噻唑多肽或青霉噻唑蛋白(青霉噻唑基团)
凝胶过滤法分离,用Penamaldate法测定
HgCl2
青霉噻唑衍生物Penamaldate衍生物(285nm)
2、链霉素
毒性杂质:
链霉胍,链胍双氢链糖;双氢链霉素;链霉素醛基化合物;
神经毒性:
二链霉胺
二链霉胺含量测定原理:
二链霉胺等不被KBH4还原,能与盐酸氨基脲反应,生成的缩氨脲在233nm有吸收峰
3、四环素
杂质:
脱水四环素、差向四环素、差向脱水四环素(HPLC测定)
4、土霉素
杂质:
脱水土霉素、差向土霉素、α-阿扑土霉素、β-阿扑土霉素等降解产物.(薄层分离,荧光测定)
第九章维生素及辅酶类药物分析
一、维生素C类的分析
1、性质
1)酸性:
烯二醇结构—酸性。
一元酸.能与NaHCO3作用生成钠盐
C3-OH,pKa=4.7(共轭效应)
C2-OH,pKa=11.57(邻位羰基)
2)还原性:
烯二醇基—还原性。
与硝酸银反应可生成金属银黑色沉淀
与2,6-二氯吲哚酚反应(2,6-二氯靛酚)
3)荧光反应:
4)糖的性质:
VC的结构很象糖结构,具有糖的性质。
可在三氯醋酸或盐酸存在下,经水解、脱羧、失水等反应,转变为糠醛,再与吡咯在50℃反应生成蓝色,用于鉴别反应
2、鉴别:
1)还原性:
维生素C分子中的二个烯醇基具有强还原性可以被氧化为二酮基
2)利用糖类的性质可在三氯醋酸或盐酸存在下,经水解、脱羧、失水等反应,转变成糠醛,再与吡咯在50℃反应生成蓝色。
3)紫外分光光度法:
根据维生素C在盐酸液(0.01mol/L)中,243nm有最大吸收
3、含量测定
1)碘量法:
维生素C由于分子中的烯二醇基具有还原性,能被I2氧化成二酮基.1mol维生素C与1molI2定量反应.终点颜色:
无色→蓝色。
反应条件:
酸性使VC在空气中氧化速度减慢。
溶剂新沸放冷的水。
减少水中溶解氧的影响
要排除亚硫酸的影响则在滴定前加入丙酮或甲醛。
2)2,6-二氯靛酚滴定法原理:
在酸性下,维生素C氧化型是红色的;还原型是无色的.酸性下直接用2,6-二氯靛酚滴定,用滴定剂自身的颜色变化指示终点,不需要另外的指示剂。
3)与1,10-菲洛啉-铁(III)试剂的比色法
基于维生素C将Fe(Ⅲ)还原生成Fe(Ⅱ),Fe(Ⅱ)与菲洛啉形成桔红色络合物,在510nm有最大吸收。
4)紫外分光光度法
二、维生素E的分析
合成型为dl-α-生育酚醋酸酯
天然型为d-α-生育酚醋酸酯
检查:
天然维生素E采用硫酸铈滴定法检查游离生育酚。
游离生育具有还原性,可被硫酸铈定量氧化
取本品0.10g,加无水乙醇5ml溶解后,加二苯胺试液1滴,用硫酸铈滴定(0.01mol/L)滴定(黄色),消耗硫酸铈滴定液(0.01mol/L)不得过1.0ml。
每1ml硫酸铈滴定液(0.01mol/L)相当于0.002154g的游离生育酚,维生素E中所含的游离生育酚的限量相当于不得过2.15%。
三、辅酶Q10的分析
1、鉴别
1)根据氧化型和还原型颜色不同来鉴别
氧化型辅酶Q10还原型辅酶Q10
(黄色)(无色)
2)氧化型辅酶Q10可将还原型亚甲蓝(无色)氧化而显蓝
3)紫外吸收光谱,275nm
第十章核苷酸类药物分析
一、嘌呤类核苷酸药物分析
1、鉴别
定糖法地衣酚orcinol反应:
核酸与浓盐酸共热时,可形成糠醛(绿色670nm)
二苯胺反应:
脱氧核糖核酸经酸水解后得脱氧核糖
(蓝色595nm)
间苯三酚反应:
其中的核糖在水溶液中加间苯三酚,水浴,显玫瑰红色
第十三章酶类药物的分析
一、酶活力测定方法
1)固定时间法
在适宜的条件下,使酶和底物共同保温一定时间,测定产物生成的量或底物消耗的量,计算出酶的含量(或活力)。
[E]表示酶浓度,[P]为反应产物浓度,t表示酶作用时间,K为常数。
2)连续监测法
在酶反应过程中,连续记录不同时间的底物消耗量或产物生成量。
(一)、需NAD+或NADP+作指示的连续监测法
还原型辅酶(NADH和NADPH)在340nm处有紫外吸收,氧化型辅酶(NAD+和NADP+)在340nm处无紫外吸收.利用340nm处每分钟吸收度升高或降低的速率与酶活性成正比的关系,推算出酶的活力单位。
包括:
直接测定法:
大多数需NADH(NADPH)参加的脱氢酶,可利用紫外分光光度法直接测定反应体系在340nm处吸收度的变化,计算酶活力单位。
丙酮酸+NADH+H+乳酸+NAD+
340nm处吸收度降低的速率与NADH的氧化速率成正比,与LDH的活力成正比。
偶联法:
此类酶催化反应不需NAD+或NADP+,但当与需NAD+或NADP+的脱氢酶反应偶联以后,能用紫外分光光度法测定.
由脱氢酶引起的反应为指示反应,脱氢酶是指示酶,指示酶活力要比测定酶活力至少大100倍。
例如:
谷草转氨酶的测定:
三联酶活测定:
引入一个辅助酶反应,将被测酶反应系统与指示酶反应系统联系起来,组成一个“三合一”酶反应系统,使底物转化率、辅助酶反应和NADH(NADPH)氧化速率之间成正比函数关系,辅助酶和指示酶的活力必须大大超过测定酶活力。
例如:
磷酸肌酸+ADP肌酸+ATP……
(1)
葡萄糖+ATPG-6-P+ADP……
(2)
G-6-P+NADP+
葡萄糖酸-6-磷酸+NADPH+H+…(3)
(1)被测反应,
(2)辅助反应,HK(己糖激酶)辅助酶,(3)指示反应,G-6-PDH(6—磷酸葡萄糖脱氢酶)指示酶。
(二)、不需NAD+或NADP+作指示的连续监测法
3)固定浓度法
根据酶催化反应,使反应产物达到额定的浓度时其反应时间与酶浓度成反比的原理进行设计的.[P]=K[E]t
以所需时间的倒数(1/t)对酶浓度作图即可制备标准曲线。
优点:
1、记录时间。
2、准确
二、酶活性测定方法的设计
一、正交设计——多因素选择
正交试验设计(Orthogonalexperimentaldesign)是一种高效的利用正交表来安排多因素多水平设计试验的方法。
通过巧妙的安排和分组,用较少的试验次数,就能分析各因素的作用大小,找出最佳的试验条件。
利用各因素所对应指标的极差R及平均极差D作出判断。
正交试验优选中性蛋白酶活力测定条件:
中性蛋白酶是一种蛋白水解酶,活力测定以酪蛋白为底物,水解产物与福林试剂在碱性情况下反应生成有色物质,于680nm处测定吸收值。
中性蛋白酶作用受缓冲液的pH值、底物浓度、反应时间及酶浓度等因素的影响。
供试品:
0.01%的中性蛋白酶溶液