专题3金属及其化合物高三总复习Word文档格式.docx
《专题3金属及其化合物高三总复习Word文档格式.docx》由会员分享,可在线阅读,更多相关《专题3金属及其化合物高三总复习Word文档格式.docx(16页珍藏版)》请在冰豆网上搜索。
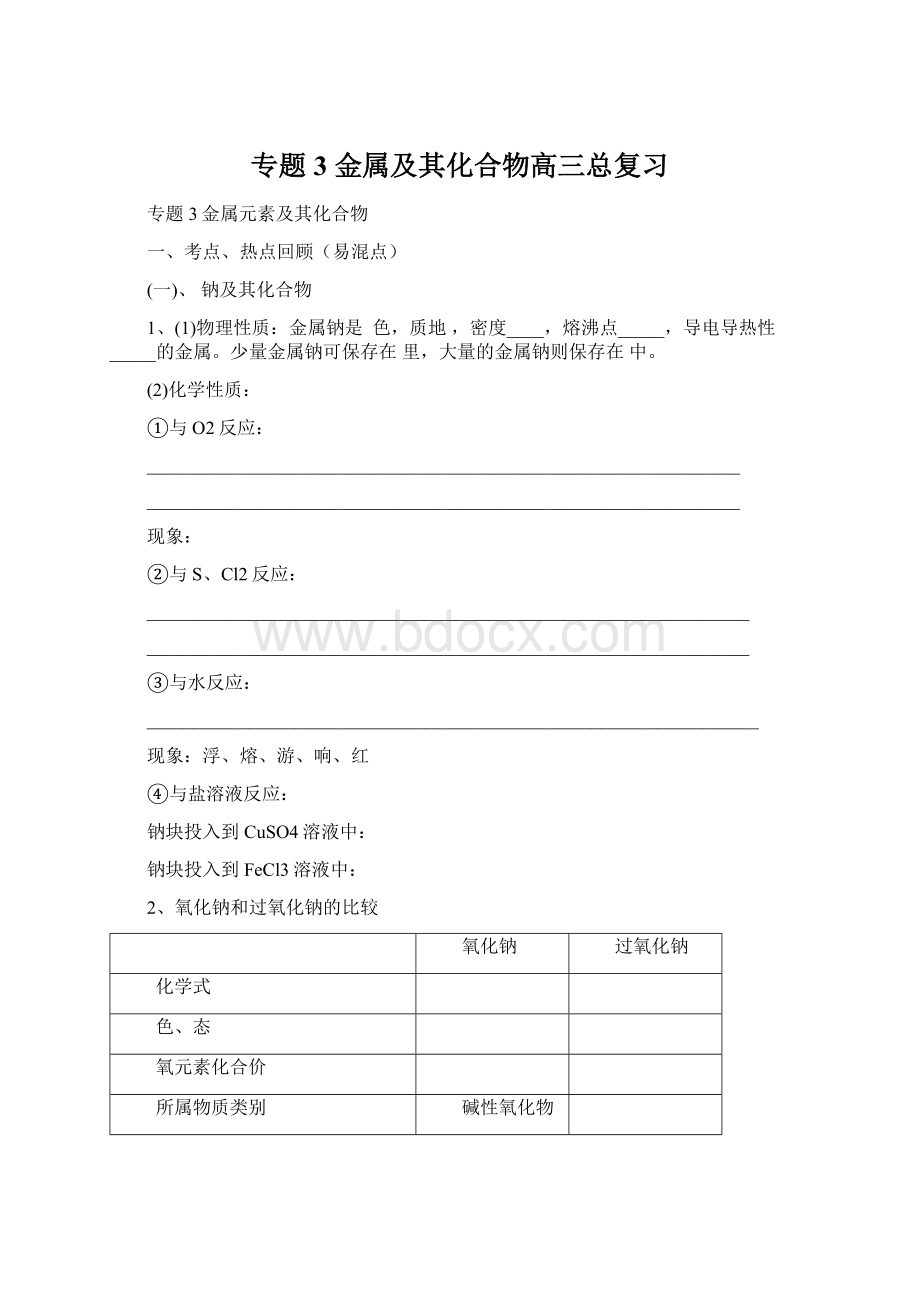
稳定性
>
用途
制碱
氧化剂、供氧剂
氧化性与漂白性
考点剖析:
1、下列灭火剂能用于扑灭金属钠着火的是()
A.干冰灭火剂 B.黄砂C.干粉(含NaHCO3)灭火剂D.泡沫灭火剂
2、向紫色石蕊试液中加过量的Na2O2粉末,振荡,正确的叙述是()
A.溶液仍为紫色B.最后溶液变为蓝色
C.最后溶液褪色D.反应中有气泡产生
3、下列四组反应中既有沉淀产生又有气体放出的是()
A.金属钠投入到MgSO4溶液中B.BaCl2和NaHSO4溶液反应
C.小苏打溶液和澄清石灰水反应D.Na2O2和CuSO4溶液反应
4、将等质量的Na、Na2O、Na2O2、NaOH,分别投入等质量的足量水中,所得溶液质量分数最大的是()
A.NaB.Na2OC.Na2O2D.NaOH
5、将ag水煤气(成分为CO和H2)充分燃烧,将燃烧生成的气体(150℃)通过盛有过量的Na2O2的干燥管(反应气体无损失),充分反应后干燥管增重bg,则a和b的关系为()
A.a>bB.a=bC.a<bD.无法比较
6、(双选)将金属钠分别投入下列物质的溶液中,有气体放出,且溶液质量减轻的是()
A.HClB.K2SO4 C.CuCl2D.饱和NaOH溶液
7、有一块表面被氧化成氧化钠的金属钠,质量为10.8g,投入到100g水中完全反应后,收集到0.2g氢气,试计算:
(1)未被氧化的金属钠的质量是多少克?
(2)钠元素的质量分数是多少?
(3)反应后所得溶液的溶质的质量分数?
(二)、镁及其化合物
1、
(1)镁是色的金属,是的良导体,质地,硬度较,熔点较,镁的密度较_____,镁可形成许多合金,硬度和强度都很____,氧化镁的熔点可以达到2800℃,是很好的______材料。
_______________________________________________________
②与Cl2反应:
______________________________________________________
③与N2反应:
④与CO2反应:
______________________________________________________(MgO+C)
⑤与HCl反应:
_____________________________________________________
加
1、海水提镁的步骤:
石灰乳
煅烧
贝壳(CaCO3)
Mg
MgCl2·
6H2O
MgCl2
沉淀
、
相关的化学反应方程式为:
①
②③
④⑤
2、质量相同,浓度相同的稀硫酸分别与足量的下列物质反应,所得硫酸镁溶液的质量分数最小的是()
A.MgB.MgOC.Mg(OH)2D.MgCO3
(三)、铝及其化合物
1、铝是较活泼的金属元素,在自然界中以态存在,在地壳中的含量占金属中的第位,铝元素在地壳中主要存在的物质是。
2、
(1)铝是色,硬度、质地较,具有良好的性、性和性。
常温下,铝在空气中生成,因此常温下铝制品具有抗腐蚀的性能。
(2)铝的化学性质:
___________________________________________________
②与S反应:
③与Cl2反应:
④与Fe2O3反应:
_________________________________________________
__________________________________________________
⑥与NaOH反应:
3、
(1)氧化铝是色,溶于水,熔点。
属于氧化物。
(2)氧化铝的化学性质:
与HCl反应(离子方程式)
与H2SO4反应(化学方程式)
与强碱反应(离子方程式)
4、
(1)氢氧化铝是(白色胶状物),溶于水,有较强的(吸附性),可用作。
属于氢氧化物。
(2)氢氧化铝的化学性质:
完成反应方程式:
与氢氧化钠反应(离子方程式)
实验室常用和反应制取氢氧化铝:
(离子方程式)
5、铝三角
典例剖析:
1、两个烧杯加入同体积的浓度为2mol/L的H2SO4,置于天平两端,调平天平后分别加入10.8g的A1和Mg,则反应完毕后,天平()
A.向加Mg一端下倾B.向加Al一端下倾
C.仍保持天平平衡D.无法判断
2、用铝箔包装0.1mol金属钠,用针扎出一些小孔,放入水中,完全反应后,用排水集气法收集产生的气体,则收集到的气体为(标准状况)()
A.O2和H2的混合气体B.1.12LH2
C.大于1.12LH2D.小于1.12L气体
3、等量镁铝合金粉末分别与下列4种过量的溶液充分反应,放出氢气最多的是()
A.2mol·
L-1H2SO4溶液B.18mol·
L-1H2SO4溶液
C.6mol·
L-1KOH溶液D.3mol·
L-1HNO3溶液
4、下列各金属的混合物2.5g和足量的盐酸反应,放出的H2在标准状况下体积为2.24L,其中可能的是()
A.Zn和FeB.Mg和ZnC.Al和MgD.Cu和Fe
5、Na、Mg、Al三种金属各0.2mol,分别与100mL1mol/L的HCl溶液反应,放出H2的量是()
A.Mg最多B.Al最多C.Na最多D.一样多
6、有10.2gMg、Al混合物,溶于0.5L4mol/L盐酸中。
若加入2mol/LNaOH溶液,使得沉淀量最大,应加NaOH溶液的体积是()
A.0.1LB.0.5LC.1LD.1.5L
7、有一根粗铝含铁和硅两种杂质,取等质量的粗铝分别投入足量稀HCl和足量的NaOH溶液中,放出等量的H2,则该粗铝中,铁和硅的关系为()。
a.物质的量之比为2∶1b.物质的量之比为3∶1
c.质量之比为2∶1d.质量之比为4∶1
A.bdB.bcC.adD.只有d
8、等体积、等物质的量浓度的硫酸、氢氧化钠溶液分别放在甲、乙两烧杯中,各加等质量的铝,生成氢气的体积比为5:
6,则甲、乙两烧杯中的反应情况可能分别是()
A.甲、乙中都是铝过量B.甲中铝过量、乙中碱过量
C.甲中酸过量、乙中铝过量D.甲中酸过量、乙中碱过量
9、氢氧化铝沉淀量图象大致可以分为如图六类。
[图中横坐标为加入试剂的体积]
(1)图为向AlCl3溶液中滴人NaOH溶液
反应离子方程式:
A~B段:
B~C段:
(3)图为向盐酸酸化了的AlCl3溶液中滴入NaOH溶液
C~D段:
(5)图为向NaAlO2溶液中加入盐酸
(四)、铁及其化合物
1、在地壳中含量第一的元素是,铁是含量第的元素,铁是含量第的金属元素。
铁元素在自然界中的存在形式是态。
2、
(1)纯净的铁是色金属,有较好的、、性能,
还能被吸引。
(2)铁的化学性质:
____________________________________________________
与O2点燃:
与I2反应:
_____________________________________________________(生成二价铁)
③与S反应:
④与H2O反应:
________________________________________________________(Fe3O4+H2)
⑤与HNO3反应:
Fe+HNO3(过量)==
离子方程式为:
Fe(过量)+HNO3==
Fe+HNO3(浓)
铁与浓HNO3、浓H2SO4在常温下会发生现象,所以可用铁制容器贮存和运输浓HNO3和浓H2SO4。
⑤Fe+Cu2+====Fe+Fe3+====
3、铁的氢氧化物
Fe(OH)2
Fe(OH)3
色态
制法(方程式)
二者的关系
空气中,Fe(OH)2能迅速被氧气氧化成Fe(OH)3,
现象是______色迅速变成________色,最后变成_______色,
反应方程式为_____________________________________________
由此可知Fe(OH)3比Fe(OH)2稳定
4、Fe、Fe2+、Fe3+之间的相互转化关系(铁三角)
Fe单质具有还原性、Fe3+具有氧化性、Fe2+既具有氧化性又具有还原性
特别提醒:
注意转化过程所选氧化剂或还原剂的强弱
(1)常见Fe2+转化成Fe3+的离子方程式
2Fe2++Cl2(Br2)===2Fe3++2Cl-(Br-)
3Fe2++4H++NO3-===3Fe3++NO↑+2H2O
2Fe2++H2O2+2H+===2Fe3++2H2O
(2)常见Fe3+转化成Fe2+的离子方程式
2Fe3++Cu===2Fe2++Cu2+
2Fe3++Fe===3Fe2+
2Fe3++2I-===2Fe2++I2
2Fe3++S2-===2Fe2++S↓或2Fe3++H2S===2Fe2++S↓+2H+
2Fe3++SO2+2H2O===2Fe2++SO42-+4H+
(3)Fe2+、Fe3+转化成单质铁一般是高温时利用还原剂(H2、C、CO、Al)进行还原生成。
5、Fe2+、Fe3+的检验
(1)Fe2+:
①加强碱溶液,得到白色沉淀迅速转化为灰绿色,最后转化为红褐色。
②加KSCN溶液无明显现象,通入氯气后溶液变红。
(2)Fe3+:
①加强碱溶液,得到红褐色沉淀。
②加入KSCN溶液,溶液变为红。
③加入苯酚溶液,溶液变为紫色。
1、铁与下列物质反应后中铁元素的化合价只有+3的是()
A.氧气(燃烧)B.稀硫酸C.氯化铁D.氯化铜E氯气F硫单质
2、下列物质发生反应时其离子方程式正确的是()
A、铁与三氯化铁溶液反应:
Fe+Fe3+=2Fe2+
B、足量的氯气通入溴化亚铁溶液中:
2Fe2++4Br-+3Cl2=2Fe3++2Br2+6Cl-
C、Fe(OH)3跟盐酸反应:
Fe(OH)3+3H+=Fe3++3H2O
D、FeS跟稀硝酸反应:
FeS+2H+=Fe2++H2S
3、1.4g铁全部溶于盐酸中,加入足量NaOH溶液,得红棕色沉淀,过滤后给红棕色沉淀加热(在空气中),最后得到红色物质的质量是()
A.1gB.1.6gC.2gD.1.8g
4、将Fe,Cu,Fe2+,Fe3+和Cu2+盛于同一容器中充分反应,如Fe有剩余,则容器中只能有()
A.Cu,Fe3+B.Fe2+,Fe3+C.Cu,Cu2+,FeD.Cu,Fe2+,Fe
5、在FeCl3和CuCl2的混合物溶液中,加入过量的Fe屑,反应停止后,称得固体与加入的铁屑质量相等。
原混合液中FeCl3和CuCl2的物质的量之比是。
6、(14分)(13全国)氧化锌为白色粉末,可用于湿疹、癣等皮肤病的治疗。
纯化工业级氧化锌(含有Fe(II)、Mn(II)、Ni(II)等杂质)的流程如下:
提示:
在本实验条件下,Ni(II)不能被氧化;
高锰酸钾的还原产物是MnO2。
回答下列问题:
(1)反应②中除掉的杂质离子是,发生反应的离子方程式为;
在加高锰酸钾溶液前,若pH较低,对除杂的影响是。
(2)反应③的反应类型为,过滤得到的滤渣中,除了过量的锌外还有。
(3)反应④形成的沉淀要用水洗,检查沉淀是否洗涤干净的方法是。
(4)反应④中产物的成分可能是ZnCO3·
xZn(OH)2。
取干燥后的滤饼11.2g,锻烧后可得到产品8.1g,则x等于。
解:
(1)根据题意,Ni(Ⅱ)不能被氧化,反应②中除掉的杂质离子是Fe2+和Mn2+,发生的离子方程式为MnO4-+3Fe2++7H2O=3Fe(OH)3↓+MnO2↓+5H+、2MnO4-+3Mn2++2H2O=5MnO2↓+4H+;
加高锰酸钾溶液前,若pH较低,铁离子和锰离子不能生成沉淀,从而无法除去铁和锰杂质;
故答案为:
Fe2+和Mn2+;
MnO4-+3Fe2++7H2O=3Fe(OH)3↓+MnO2↓+5H+、2MnO4-+3Mn2++2H2O=5MnO2↓+4H+;
铁离子和锰离子不能生成沉淀,从而无法除去铁和锰杂质;
(2)反应③为锌与镍离子的发生反应得到锌离子和镍,反应类型为置换反应;
得到的滤渣中,除了过量的锌外还有金属镍,
置换反应;
镍;
(3)取最后一次少量水洗液于试管中,滴入1~2滴稀硝酸,再滴入硝酸钡溶液,若无白色沉淀生成,则说明沉淀已经洗涤干净,故答案为:
取最后一次少量水洗夜于试管中,滴入1~2滴稀硝酸,再滴入硝酸钡溶液,若无白色沉淀生成,则说明沉淀已经洗涤干净;
(4)根据关系式ZnCO3•xZn(OH)2~(x+1)ZnO
125+99x81(x+1)
11.2g8.1g
解得:
x=1
1.
(五)、金属材料及金属矿物的开发:
I、合金及常见金属材料
1、合金
(1)概念:
两种或两种以上的金属或金属与非金属熔合而成的具有金属特性的物质。
(2)性质特点:
合金具有不同于各成分金属的物理、化学或机械性能。
①具有金属特性
②合金的硬度一般比它的各成分金属的大,
③多数合金的熔点一般比它的各成分金属的低。
2.常见金属材料
铁、铬、锰以及它们的合金
除黑色金属以外的其他金属及其合金
金属材料
(l)重要的黑色金属材料
钢、生铁、铁合金、铸铁
(2)几种有色金属材料
青铜板、紫铜带、黄铜管
II、金属矿物的开发利用
1.金属在自然界中存在的形态
除了金、铂等极少数金属外,绝大多数金属以化合物的形式存在于自然界中。
在这些金属化合物中,金属元素都显正化合价。
2.金属冶炼的实质
使金属化合物中的金属离子得电子被还原
为金属单质的过程:
Mn++ne-===M。
3.金属冶炼法
根据金属的活动性不同,金属冶炼的方法分为:
电解法、热还原法、热分解法和富集法等。
(1)、热分解法
有些不活泼金属仅用热分解法就能制得。
在金属活动性顺序表中,位于氢后面的某些金属的氧化物受热就能分解。
(2)、热还原法
多数金属的冶炼过程属于热还原法。
常用的还原剂有焦炭、一氧化碳、氢气和活泼金属等。
(3)、电解法
在金属活动性顺序中,钾、钠、钙、铝等几种金属的还原性很强,这些金属都很容易失去电子,因此不能用一般的方法和还原剂使其从化合物中还原出来,而只能用通电分解其熔融盐或氧化物的方法来冶炼。
(4)、方法选择
金属活动顺序表:
_______________________________________________________________________
(六)、金属铜及其重要化合物的主要性质及应用
1、单质铜
(1)物理性质:
紫红色、不能被磁体吸引。
(2)化学性质
①与O2反应
加热:
。
常温下在潮湿的空气中:
(棕黄色烟)。
③与酸的反应
a.与非氧化性酸:
不反应
b.与氧化性酸反应
与浓硫酸的反应:
与浓硝酸的反应:
与稀硝酸的反应:
④与盐溶液的反应(用离子方程式表示)
与硝酸银溶液的反应:
Cu+2Ag+====Cu2++2Ag
与氯化铁溶液的反应:
2Fe3++Cu====2Fe2++Cu2+
2、氢氧化铜
蓝色不溶于水的固体。
Cu(OH)2属于弱碱,能与酸反应生成盐和水。
3、CuSO4·
5H2O
CuSO4·
5H2O为蓝色晶体,俗称蓝矾、胆矾。
无水CuSO4为白色粉末,遇水变蓝色(生成CuSO4·
5H2O),可作为水的检验依据。
1、工业制硫酸铜不是直接用铜和浓硫酸反应,而是将粗铜(含少量银)浸入稀硫酸中,并不断从容器下部吹入细小的空气泡。
有关该制备方法的叙述中,不正确的是()
A.该方法应用了原电池工作原理
B.该方法不产生污染大气的二氧化硫
C.该方法提高了硫酸的利用率
D.该方法提高了铜的利用率
【解析】选D。
该方法的原理是:
2Cu+O2+2H2SO4====2CuSO4+2H2O,由于铜、银和稀硫酸能构成无数微小的原电池,加快了化学反应速率,故A项正确;
由该方法的原理知,B、C项均正确;
由于两种方法铜的利用率相同,故D项错误。
2、(12·
江苏)向27.2gCu和Cu2O的混合物中加入某浓度的稀硝酸0.5L,固体物质完全反应,生成NO和Cu(NO3)2。
在所得溶液中加入1.0mol/L的NaOH溶液1.0L,此时溶液呈中性,金属离子已完全沉淀,沉淀质量为39.2g。
下列有关说法不正确的是()
A.Cu与Cu2O的物质的量之比为2:
1B.硝酸的物质的量浓度为2.6mol/L
C.产生的NO在标准状况下的体积为4.48LD.Cu、Cu2O与硝酸反应后剩余HNO3为0.2mol
【解析】选B。
根据题意得到的金属离子的沉淀为氢氧化铜0.4mol,根据元素守恒可以确定原混合物中有铜0.2mol有氧化亚铜0.1mol,将溶液变成中性时消耗硝酸1mol,沉淀铜离子只消耗了0.8mol,因此反应过程中硝酸过量0.2mol,由于固体混合物与硝酸的反应为氧化还原反应,该反应过程中铜元素的化合价均升高为+2价,化合价升高了0.4+0.2=0.6mol,硝酸中氮原子的化合价由+5价降低为+2价,因此生成的一氧化氮的物质的量为0.2mol,根据氮元素守恒可以判断原溶液中硝酸的物质的量为1.2mol浓度为2.4mol.L-1。
3.(11·
山东)Al、Fe、Cu都是重要的金属元素。
下列说法正确的是()
A.三者对应的氧化物均为碱性氧化物
B.三者的单质放置在空气中只生成氧化物
C.制备AlCl3、Fe
Cl3、CuCl2均不能采用将溶液直接蒸干的方法
D.电解AlCl3、FeCl3、CuCl2的混合溶液时阴极上依次析出Cu、Fe、Al.
【解析】选C,正确地运用所学的水解原理、电解原理分析C项和D项,同时对三者的化学性质要相当熟悉,尤其是对铜的性质的拓展。
A项,铝的氧化物Al2O3属于两性氧化物,A错误;
B项,Al与Fe一般都生成对应的氧化物,而Cu除了生成氧化物,还易与空气中的CO2、H2O反应生成铜绿[Cu2(OH)2CO3],B错误;
C项,因AlCl3、Fe
Cl3、CuCl2都属于强酸弱碱盐,弱碱阳离子都能发生水解,生成对应的碱和盐酸,由于盐酸属于挥发性酸,故蒸干后得到的为对应的碱,而不是原溶质,C正确;
D项,因氧化性:
Cu2+>H+,故析出铜;
但电解AlCl3和FeCl3时,不能析出铝和铁,因氧化性:
H+>Al3+、Fe3++e-=Fe2+,应产生氢气和Fe2+,故D错误,
4.(11·
全国)0.80gCuSO4·
5H2O样品受热脱水过程的热重曲线(样品质量随温度变化的曲线)如图所示。
请回答下列问题:
(1)试确定200℃时固体物质的化学式______________(要求写出推断过程);
(2)取270℃所得样品,于570℃灼烧得到的主要产物是黑色粉末和一种氧化性气体,该反应的化学方程式为______________。
把该黑色粉末溶解于稀硫酸中,经浓缩、冷却,有晶体析出,该晶体的化学式为_________,其存在的最高温度是_____________;
(3)上述氧化性气体与水反应生成一种化合物,该化合物的浓溶液与Cu在加热时发生反应的化学方程式为________________;
(4)在0.10mol·
L-1硫酸铜溶液中加入氢氧化钠稀溶液充分搅拌有浅蓝色氢氧化铜沉淀生成,当溶液的pH=8时,c(Cu2+)=________________mol·
L-1(Ksp[Cu(OH)2]=2.2×
10-20)。
在0.1mol·
L-1硫酸铜溶液中通入过量H2S气体,使Cu2+完全沉淀为CuS,此时溶液中的H+浓度是_______________mol·
L-1。
【解析】解答本题时应首先根据图像推断各温度时存在的物质。
根据Ksp[Cu(OH)2]=c(Cu2+)×
c2(OH-),可以计算c(Cu2+)。
(1)CuSO4·
CuS