元素周期律知识点总结(精华版).doc
《元素周期律知识点总结(精华版).doc》由会员分享,可在线阅读,更多相关《元素周期律知识点总结(精华版).doc(1页珍藏版)》请在冰豆网上搜索。
湖南省长郡中学远程管理学校资料
§—9元素周期律&元素周期表(俄门捷列夫)
★元素周期律:
元素的性质随着原子序数的递增而呈周期性的变化。
★元素周期律的本质:
随着原子序数的递增,元素原子最外层电子排布呈周期性的变化。
周期数=电子层数数
第一周期2
第二周期8
第三周期8
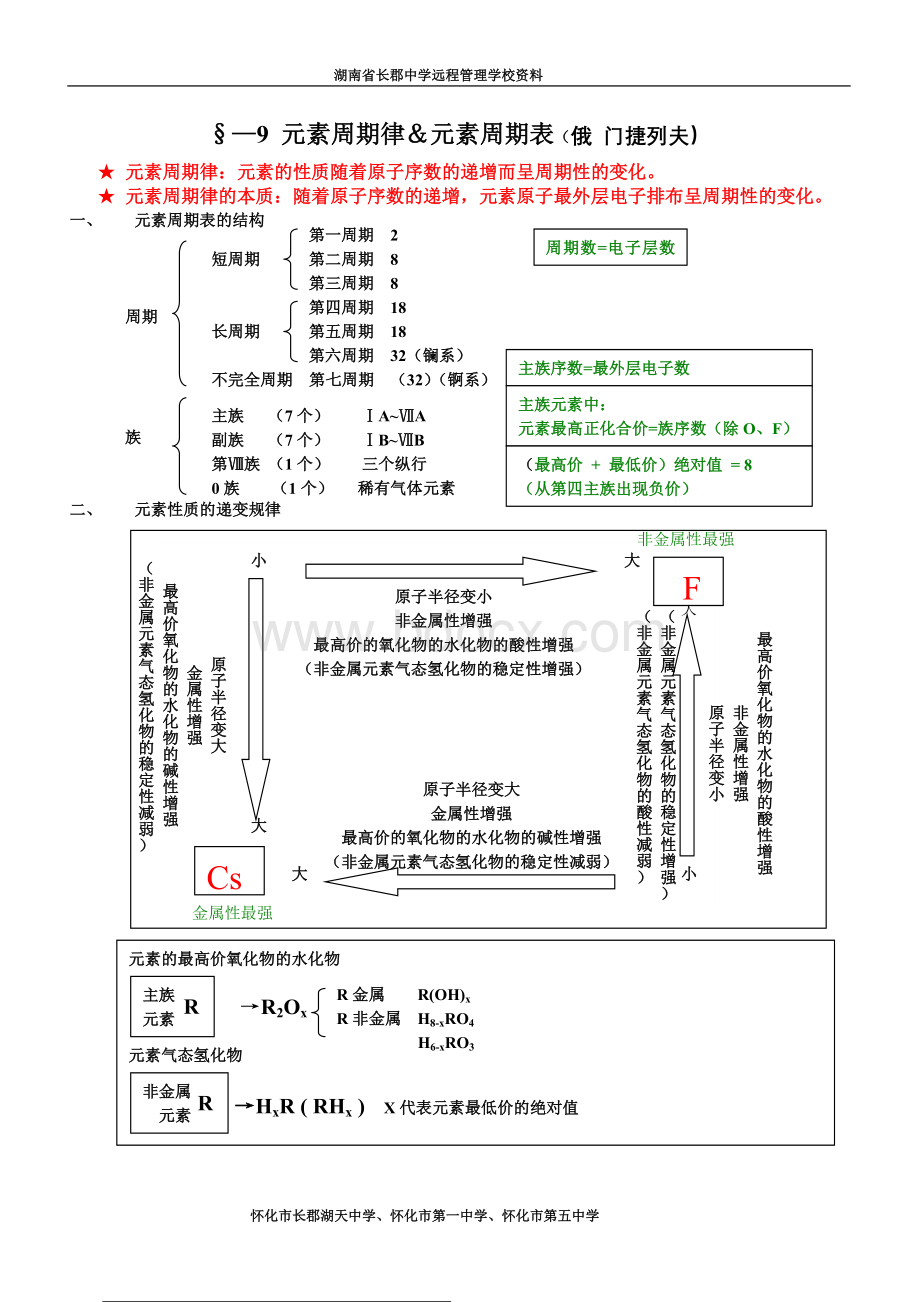
一、元素周期表的结构
短周期
长周期
不完全周期第七周期(32)(锕系)
第四周期18
第五周期18
第六周期32(镧系)
周期
主族序数=最外层电子数
主族元素中:
元素最高正化合价=族序数(除O、F)
主族(7个)ⅠA~ⅦA
副族(7个)ⅠB~ⅦB
第Ⅷ族(1个)三个纵行
0族(1个)稀有气体元素
(最高价+最低价)绝对值=8
(从第四主族出现负价)
族
二、元素性质的递变规律
非金属性最强
小大
大
大
大小
F
金属性最强
Cs
元素的最高价氧化物的水化物
元素气态氢化物
→HxR(RHx)X代表元素最低价的绝对值
5
R
非金属
元素
R
主族
元素
→R2Ox
R金属R(OH)x
R非金属H8-xRO4
H6-xRO3
原子半径变大
金属性增强
最高价氧化物的水化物的碱性增强
(非金属元素气态氢化物的稳定性减弱)
原子半径变大
金属性增强
最高价的氧化物的水化物的碱性增强
(非金属元素气态氢化物的稳定性减弱)
原子半径变小
非金属性增强
最高价的氧化物的水化物的酸性增强
(非金属元素气态氢化物的稳定性增强)
最高价氧化物的水化物的酸性增强
非金属性增强
原子半径变小
(非金属元素气态氢化物的稳定性增强)
(非金属元素气态氢化物的酸性减弱)
怀化市长郡湖天中学、怀化市第一中学、怀化市第五中学