定量分析简明教程课后练习题答案第三章Word文件下载.docx
《定量分析简明教程课后练习题答案第三章Word文件下载.docx》由会员分享,可在线阅读,更多相关《定量分析简明教程课后练习题答案第三章Word文件下载.docx(11页珍藏版)》请在冰豆网上搜索。
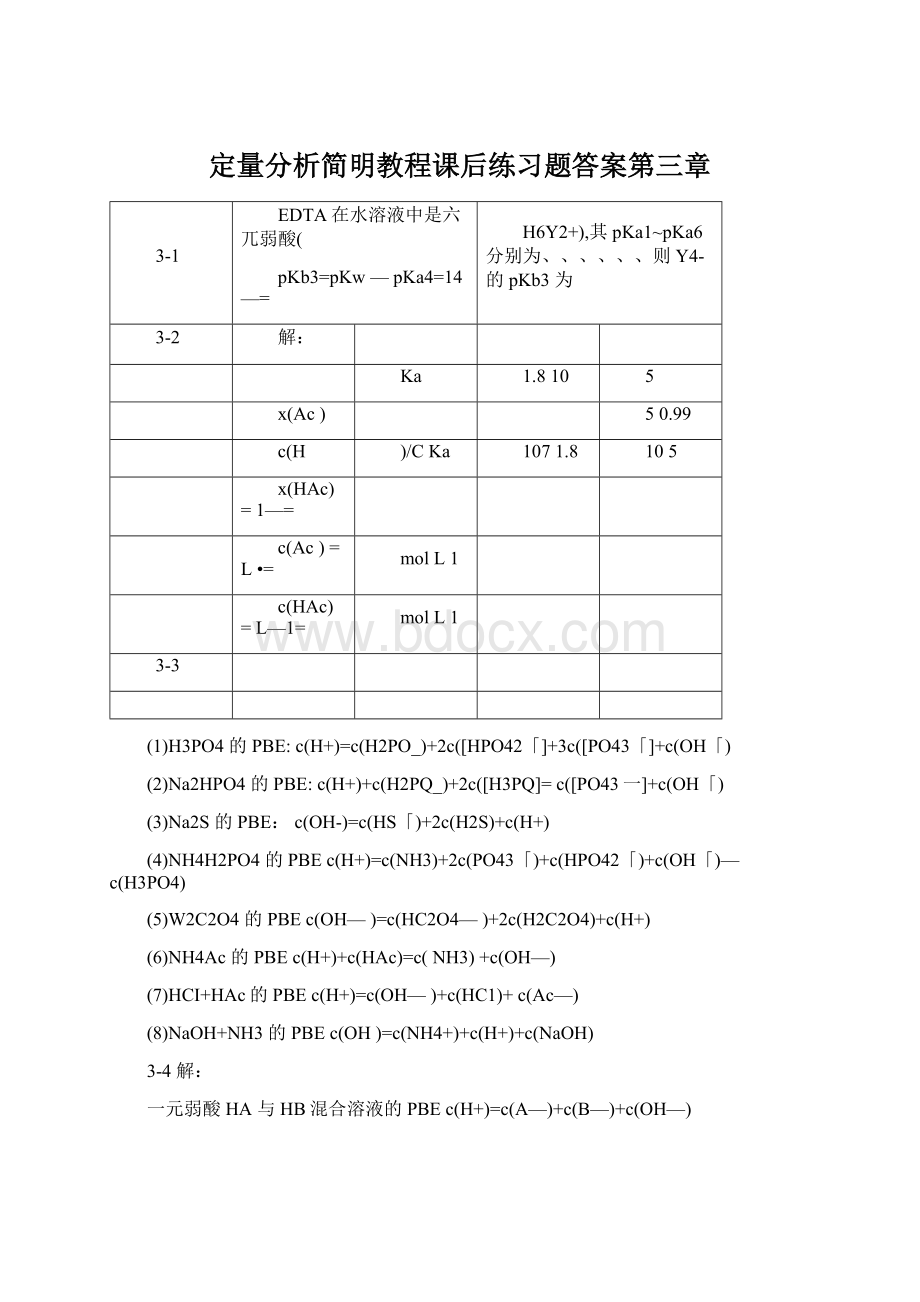
(3)Na2S的PBE:
c(OH-)=c(HS「)+2c(H2S)+c(H+)
(4)NH4H2PO4的PBEc(H+)=c(NH3)+2c(PO43「)+c(HPO42「)+c(OH「)—c(H3PO4)
(5)W2C2O4的PBEc(OH—)=c(HC2O4—)+2c(H2C2O4)+c(H+)
(6)NH4Ac的PBEc(H+)+c(HAc)=c(NH3)+c(OH—)
(7)HCI+HAc的PBEc(H+)=c(OH—)+c(HC1)+c(Ac—)
(8)NaOH+NH3的PBEc(OH)=c(NH4+)+c(H+)+c(NaOH)
3-4解:
一元弱酸HA与HB混合溶液的PBEc(H+)=c(A—)+c(B—)+c(OH—)
(1)
将有关平衡关系式代入质子等衡式中得到计算
c(H+)的精确式:
)/c
K(HA)c(HA)/c
K(HB)
c(HB)/c
Kw
c(H)/c
K(HA)c(HA)/c
⑴由PBEc(H+)=c(A—)+c(B—)+c(OH—),若忽略c(OH—),则:
c(H+)=c(A—)+c(B—),计算c(H+)的近似公式为:
c(H)K(HA)c(HA)/cK(HB)c(HB)/c
(2)再若{c(HA)/c}/KHa,{c(HB)/c}/Khb均较大,则ceq(HA)C0(HA),ceq(HB)C0(HB),计算[H+]的近似公式为:
c(H).K(HA)—c0(HA)—K(HB)—q(HB)
3-5计算下列溶液的pH值:
(1),c(H3PO4)=L—1
因为Ka1/Ka2>
10,(C/C)/Ka2>
只考虑H3PQ的第一步解离
又因为(C/C)Ka1>
("
C)/Ka1=29<
,用近似式计算:
Ka1駅0—4Ka1C/c6.9103v(6.9103)246.91030.2
c(H)/c--—0.034pH=
22
(3)c(Na3PO4)=L—1
Na3PO4Kb1=10—2,Kb2=10—7,Kb3=10—12
因为Kb1/Kb2>
10,(c/c)/Kb2>
只考虑Na3PO4的第一步解离又因为(c/c)Kb1>
10—,(c/c)/Kb1<
用近似式计算:
pOH=,pH=
(4)c(NH4CN)=L-1
NH4CN为两性物质,其酸常数pKa(NH4+)=,其共轭酸的酸常数pKa(HCN)=用最简式计算:
pH=
3-6答:
若用弱酸弱碱作标准溶液,则滴定反应的反应完全程度小,pH突跃范围小,滴定的终点误差大。
标准溶液的浓度大约为L-1左右,若浓度太稀,则pH突跃范围小,滴定的终点误差大。
3-7下列说法哪些正确:
(1)用同一NaOH滴定相同浓度和体积的不同的弱一元酸,贝UKa较大的弱一元酸:
b.突跃范围大;
c.计量点pH较低。
(2)酸碱滴定中选择指示剂时可不考虑的因素是:
f.指示剂的结构
(3)用同一NaOH滴定同浓度的HA和H2A(至第一计量点),若Ka(HA)=Ka1(H2A),则:
b.HA突跃较大
3-8解:
(1)Kb(NaCN)=Kw/Ka(HCN)=105
因为(c/c)Kb>
10-8
能用HCI标准溶液准确滴定NaCN
滴定反应:
HCI+NaCN=HCN+NaCI
化学计量点时c(HCN)=L1
选择甲基红指示剂
(2))Kb(NaAc)=Kw/Ka(HAc)=10「10因为(c/c)Kb<
不能用HCI标准溶液直接滴定NaAc。
也不能用返滴定法测定。
(3)Ka(HCOOH)=104
因为(c/C)Ka>
10「8
能用NaOH标准溶液直接滴定HCOOH
化学计量点时c(HCOONa)=L1
pOH=pH=
选酚酞指示剂
3-9解
(1)用NaOH标准溶液滴定c(HCl)=L1,c(NH4Cl)=L1的混合溶液,因Ka(NH4+)10-9,达第一化学计量点有突跃,可测强酸的分量。
此时溶液中c(NH4Cl)=molL-1/2=L-1
(2)
因为Ka(NH4+)<
10-7
不能用NaOH滴定,即不能测总酸量。
(3)
故不能测强
用NaOH标准溶液滴定c(HCI)=匕1,c(HAc)=L1的混合溶液至第一化学计量点无突跃,酸的分量。
因为Ka(HAc)>
10-7,滴定至第二化学计量点有突跃,即可测总酸量。
此时溶液中c(NaAc)=molL-1/3=L-1
c(H)/c.Ka(HCN)c/c、4.91010:
4.010
pH(计)=
可选酚酞作指示剂
(4)Na3PO4为三元碱
因为Kb1>
10-7,心1/心2>
105;
Kb2>
10-7,Kb2/Kb3>
105
可分别滴定至第一,第二终点
因为(c/c)Kb3<
不能滴定至第三终点
滴定至第一终点时生成Na2HPO4
若用最简式计算pH(计):
pH=(1/2)(pKa2+pKa3)=(1/2)+=
滴定至第二终点时生成NaH2PO4
pH=(1/2)(pKai+pKa2)=(1/2)+=
可选甲基红作指示剂
(5)焦磷酸H4F2O7
因为Ka1>
10-7,Kai/Ka2<
不能分步滴定至第一终点
因为Ka2>
10-7,Ka2/Ka3>
104
能分步滴定至第二终点
因为Ka3>
10-7,Ka3/Ka4<
不能分步滴定至第三终点
因为cKa4<
不能滴定至第四终点
滴定达第二终点时生成H2F2O72-
pH(计)=(1/2)(pKa2+pKa3)=(1/2)+=
可选甲基红或甲基橙作指示剂
3-11答:
(1)用将NaHCQ加热至270—300C的方法制备NazCOs基准物时,若温度超过300C,部分NazCO分解为Na2O,用其标定HCI时,标定结果将偏低。
(2)用Na2C2Q作基准物标定HCI时,是将准确称取的Na2C2O4灼烧为Na2CC3后,再HCI滴定至甲基橙终点。
若灼烧时部分Na2CQ分解为Na2O,对标定结果无影响。
(3)以H2C2O42H2O为基准物标定NaOH时,若所用基准物已部分风化,标定结果将偏低。
(4)c(NaOH)=L-1的氢氧化钠标准溶液,因保存不当,吸收了CQ,当用它测定HCI浓度,滴定至甲基
橙变色时,则对测定结果无大影响。
用它测定HAc浓度时,应选酚酞作指示剂,则会使测定结果
偏咼。
3-12解:
Na2CO3+2HCI=2NaCI+HO+CQ
3-13解:
2NaOH+CQ=Na2CQ+H2O
所以,吸收CQ后,NaOH的实际浓度和N&
CQ的浓度分别为:
0.3000moI/L0.1000L-20.0020moI
0.1000L
c(Na2CO3)0.0200moI/L
若以酚酞为指示剂,用HCI标准溶液滴定此溶液,发生的反应为:
HCI+NaOH=NaCI+HO
HCI+Na2CO3=NaHCO3+NaCI
过程中消耗HCI的物质的量=L+L)=
故据此计算得NaOH的浓度c'
(NaOH)=/=L3-14答:
4NH4++6HCHO=(CH)6N4H++3H++6H2O
(CH2)6N4H++3H++4OH-=(CH2)6N4+4H2O
w(N)
c((NaOH)V(NaOH)M(N)
ms
c((NaOH)V(NaOH)M(NH3)w(NH3)
1c((NaOH)V(NaOH)M{(NH4)2SO4}
W(NH4)2SO4]-
3-15解:
c(HCl)
c(NaOH)V(NaOH)
V(NaOH)
0.07891molL115.83mL
25.00mL
0.04997molL
/K1X[c(HCl)V(HCl)c(NaOH)V(NaOH)]M(N)w(N)
-111
(0.04997molL0.05000L0.07891molL0.01312L)14.01gmol
0.4750g
H3PO4+NaOH=NaH2PC4+H2O
3-16解:
W(H3PO4)
4.31%
c(NaOH)V(NaOH)M(H3PO4)
ms稀释倍数
0.09460molL10.02130L97.99gmol
98.72%
wROs)
M(P2O5)
2M(H3PO4)
w(HsPO4)
1
黑粘98.72%71.48%
或:
w(P2O5)
-c(NaOH)V(NaOH)M(P2O5)
2
3-17解:
(1)样品为Na2CO
gCOs)
c(HCI)V(HCI)M(Na2CO3)
V
0.2500molL10.02432L106.0gmol1
0.02500L
25.78gL
⑵样品为Na2CQ和NaHCO
0.2500moIL10.01520L106.0gmoI11
16.11gL0.02500L
(NaHCO3)
c(HCI)[V2(HCI)V1(HCI)]M(NaHCO3)
Vs
0.2500moIL1(0.03319L0.01520L)84.01gmoI1
15.11gL
(Na2CO3)
c(HCI)Vi(HCI)M(Na2CO3)
(3)样品为NaOH和Na2CO
(NaOH)
c(HCI)M(HCI)V2(HCI)]M(NaOH)
VS
0.2500molL1(0.03521L0.01885L)40.00gmol1
6.544gL1
c(HCI)V2(HCI)M(Na2CO3)
(NazCOs)
0.2500moIL10.01885L106.0gmoI
19.98gL
3-18解:
1,NaOH+HCI=NaCI+HO
Na2CO3+2HCI=2NaCI+HO+CQ
2,Na2CO3+BaC2=BaCC3+2NaCI
NaOH+HCI=NaCI+HO
20.4852g
381.4gmol10.02437L
w(NaOH)
0.1044molL0.02374L40.00gmol
2.546g
25.00
250.0
38.94%
-c(HCl)[V1(HCl)V2(HCl)]M(Na2CO3)
w(Na2CO3)
mS稀释倍数
2.43%
0.1044molL1(0.02486L0.02374L)106.0gmol
2.546g-