水吸收 低浓度二氧化硫 填料吸收塔 设计Word文档格式.docx
《水吸收 低浓度二氧化硫 填料吸收塔 设计Word文档格式.docx》由会员分享,可在线阅读,更多相关《水吸收 低浓度二氧化硫 填料吸收塔 设计Word文档格式.docx(30页珍藏版)》请在冰豆网上搜索。
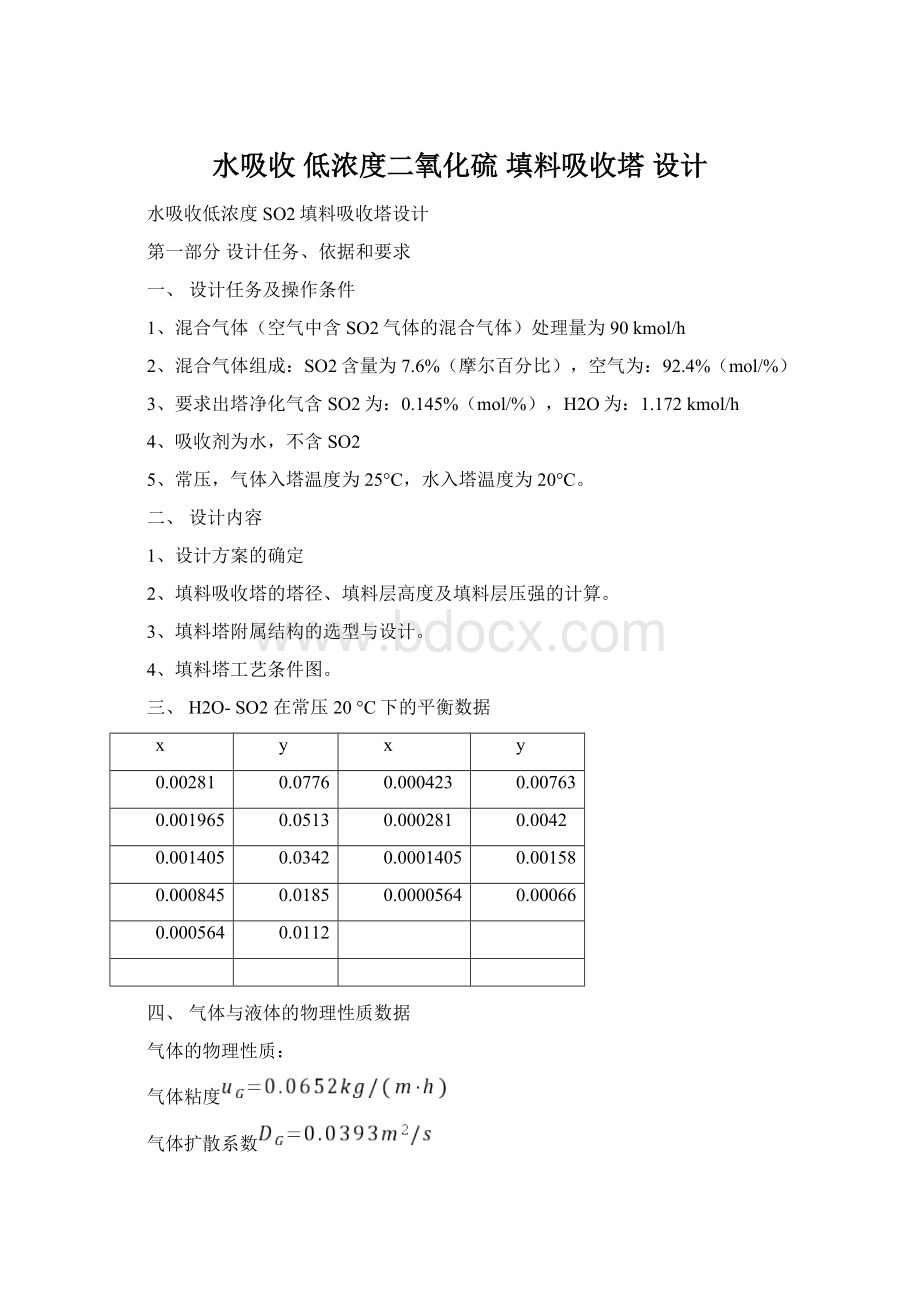
三、H2O-SO2在常压20°
C下的平衡数据
x
y
0.00281
0.0776
0.000423
0.00763
0.001965
0.0513
0.000281
0.0042
0.001405
0.0342
0.0001405
0.00158
0.000845
0.0185
0.0000564
0.00066
0.000564
0.0112
四、气体与液体的物理性质数据
气体的物理性质:
气体粘度
气体扩散系数
气体密度
液体的物理性质:
液体粘度
液体扩散系数
液体密度
液体表面张力
五、设计要求
1、设计计算说明书一份
2、填料塔图(2号图)一张
第二部分SO2净化技术和设备
一、SO2的来源、性质及其危害:
1、二氧化硫的来源
二氧化硫的来源很广泛,几乎所有企业都要产生二氧化硫,最主要途径是含硫化石燃料的燃烧。
大约一吨煤中含有5-50kg硫,一吨石油中含有5-30kg硫。
这些燃料经燃烧都产生并排放出二氧化硫,占所有排放总量的96%.
二氧化硫的来源包括微生物活动,火山活动,森林火灾以及海水飞沫。
主要有自然来源和人为来源两大类:
自然来源主要是火山活动,喷出的火山气体中含有大量的二氧化硫气体,地质深处的天然硫元素在火山喷发过程中燃烧氧化为二氧化硫,随火山灰一起喷射到大气中。
地球上57%的二氧化硫来自自然界,沼泽、洼地、大陆架等处所排放的硫化氢,进入大气,被空气中的氧氧化为二氧化硫。
自然排放大约占大气中全部二氧化硫的一半,通过自然循环过程,自然排放的硫基本上是平衡的。
人为来源则指在人类进行生产、生活活动中,使用含硫及其化合物的矿石进行燃烧,以及硫矿石的冶炼和硫酸、磷肥纸浆的生产等产生的工业废气,从而使其中一部分或全部的硫以二氧化硫的形式排放到大气中,形成二氧化硫污染。
这部分二氧化硫占地球上二氧化硫来源的43%。
随着化石燃料消费量的不断增加,全世界认为排放的二氧化硫在不断在增加,其中北半球排放的二氧化硫占人为排放总量的90%。
我国的能源主要依靠煤炭和石油,而我国的煤炭、石油一般含硫量较高,因此,火力发电厂、钢铁厂、冶炼厂、化工厂和炼油厂排放出的大量二氧化硫和二氧化碳是造成我国大气污染的主要原因。
由于我国部分地区燃用高硫煤,燃煤设备未能采取脱硫措施,致使二氧化硫排放量不断增加,造成严重的环境污染。
2、二氧化硫的性质
(1)物理性质:
二氧化硫又名亚硫酸酐,英文名称:
sulfurdioxide。
无色气体,有强烈刺激性气味。
分子量64.07密度为1.4337kg/m3(标准状况下),密度比空气大。
溶解度:
9.4g/mL(25℃)熔点-76.1℃(200.75K)沸点-10℃(263K)蒸汽压338.32kPa(2538mmHg,21.11℃)易溶于水,在338.32kPa水中溶解度为8.5%(25℃);
易容于甲醇和乙醇;
容于硫酸、乙酸、氯仿和乙醚等。
易液化(mp:
-10℃)。
(2)化学性质:
二氧化硫是一种酸性氧化物,它极易溶于水,其水溶液呈酸性,为亚硫酸水溶液。
实际上,二氧化硫水溶液中成分为SO2·
7H2O,仅含有微量的亚硫酸,但是亚硫酸盐含有亚硫酸根离子。
所谓的亚硫酸水溶液能被空气逐渐氧化成硫酸,其浓度越低氧化越快,而且一经加热就会有自行氧化。
二氧化硫在完全燃烧干燥时几乎不与氧气发生反应,当在有初生态氧的燃烧环境下,或者对二氧化硫与氧气的混合物进行放电,则有氧化反应发生。
氧化性:
SO2+2H2S=3S+2H2O;
还原性:
能被Cl2、Br2、I2、Fe3+、KMnO4、HNO3等强氧化剂氧化成高价态硫元素。
SO2+X2+2H2O=H2SO4+2HX
3、二氧化硫的危害
二氧化硫对人体及动物健康的危害:
主要是对眼角膜和上呼吸道粘膜的强烈刺激作用。
其浓度与反应关系如下:
0.4毫克/立方米时无不良反应;
0.7毫克/立方米时,普遍感到上呼吸道及眼睛的刺激;
2.6毫克/立方米时,短时间作用即可反射性的引起器官、支气管平滑肌收缩,使呼吸道阻力增加。
一般认为空气中二氧化硫浓度达1.5毫克/立方米,对人体健康即为有危害,长期接触主要引起鼻、咽、支气管,嗅觉障碍和尿中硫酸盐增加。
吸入高浓度二氧化硫,可引起支气管炎、肺炎,严重时可发生肺水肿及呼吸中枢麻痹。
二氧化硫进入呼吸道后,因其易溶于水,故大部分被阻滞在上呼吸道,在湿润的粘膜上生成具有腐蚀性的亚硫酸、硫酸和硫酸盐,使刺激作用增强。
上呼吸道的平滑肌因有末梢神经感受器,遇刺激就会产生窄缩反应,使气管和支气管的管腔缩小,气道阻力增加。
上呼吸道对二氧化硫的这种阻留作用,在一定程度上可减轻二氧化硫对肺部的刺激。
但进入血液的二氧化硫仍可通过血液循环抵达肺部产生刺激作用。
二氧化硫进入血液可引起全身性毒作用,破坏酶的活性,影响糖及蛋白质的代谢;
对肝脏有一定损害。
液态二氧化硫可使角膜蛋白质变性引起视力障碍。
二氧化硫与烟尘同时污染大气时,两者有协同作用。
因烟尘中含有多种重金属及其氧化物,能催化二氧化硫形成毒性更强的硫酸雾。
因加剧其毒性作用。
动物试验证明,二氧化硫慢性中毒后,机体的免疫受到明显抑制。
大量吸入可引起肺水肿、喉水肿、声带痉挛而致窒息。
急性中毒:
轻度中毒时,发生流泪、畏光、咳嗽,咽、喉灼痛等;
严重中毒可在数小时内发生肺水肿;
极高浓度吸入可引起反射性声门痉挛而致窒息。
皮肤或眼接触发生炎症或灼伤。
慢性影响:
长期低浓度接触,可有头痛、头昏、乏力等全身症状以及慢性鼻炎、咽喉炎、支气管炎、嗅觉及味觉减退等。
少数工人有牙齿酸蚀症。
二氧化硫浓度为10~15ppm时,呼吸道纤毛运动和粘膜的分泌功能均能受到抑制。
浓度达20ppm时,引起咳嗽并刺激眼睛。
若每天吸入浓度为100ppm8小时,支气管和肺部出现明显的刺激症状,使肺组织受损。
浓度达400ppm时可使人产生呼吸困难。
二氧化硫与飘尘一起被吸入,飘尘气溶胶微粒可把二氧化硫带到肺部使毒性增加3~4倍。
若飘尘表面吸附金属微粒,在其催化作用下,使二氧化硫氧化为硫酸雾,其刺激作用比二氧化硫增强约1倍。
长期生活在大气污染的环境中,由于二氧化硫和飘尘的联合作用,可促使肺泡纤维增生。
如果增生范围波及广泛,形成纤维性病变,发展下去可使纤维断裂形成肺气肿。
二氧化硫可以加强致癌物苯并(α)芘的致癌作用。
据动物试验,在二氧化硫和苯并(α)芘的联合作用下,动物肺癌的发病率高于单个因子的发病率,在短期内即可诱发肺部扁平细胞癌。
二氧化硫对植物的危害:
大气中含二氧化硫过高,对叶子的危害首先是对叶肉的海绵状软组织部分,其次是对栅栏细胞部分。
侵蚀开始时,叶子出现水浸透现象,特别是介于叶边和叶脉之间的部分损害尤为严重。
干燥后,受影响的叶面部分呈白色或乳白色。
如果二氧化硫的浓度为(0.3-0.5)×
,并持续几天后,就会对敏感性植物产生慢性损害。
二氧化硫直接进入气孔,叶肉中的植物细胞使其转化为亚硫酸盐,再转化成硫酸盐。
当过量的二氧化硫存在时,植物细胞就不能尽快地把亚硫酸盐转化成硫酸盐,并开始破坏细胞结构。
菠菜,莴苣和其他叶状蔬菜对二氧化硫最为敏感。
棉花和苜蓿也都很敏感。
松针也受其影响,不论叶尖或是整片针叶都会变成褐色,并且很脆弱。
二氧化硫对建筑物及其它的危害:
大气中的二氧化硫及其生成的酸雾、酸滴等,能使金属表面产生严重的腐蚀,使纺织品、纸品、皮革制品等腐蚀破损,使金属涂料变质,降低其保护效果。
造成金属腐蚀最为有害的污染物一般是二氧化硫,已观察到城市大气中金属的腐蚀率约是农村环境中腐蚀率的1.5-5倍。
温度尤其是相对湿度皆显著影响着腐蚀速度。
含硫物质或硫酸会侵蚀多种建筑材料,如石灰石、大理石、花岗岩、水泥砂浆等,这些建筑材料先形成较易溶解的硫酸盐,然后被雨水冲刷掉。
尼龙织物,尤其是尼龙管道等,其老化显然是由二氧化硫或硫酸气溶胶造成的。
长期的酸雨作用还将对土壤和水质产生不可估量的损失,对生态环境会产生严重的影响。
二、SO2的净化技术:
二氧化硫不仅在大气中形成酸雨,造成空气污染,而且严重腐蚀锅炉尾部设备,影响生产和安全运行。
电站锅炉是我国二氧化硫的主要排放源,它的特点是烟气量大,SO2浓度低,综合利用难度大。
在电站烟气脱硫的运行费中,脱硫剂的费用占有很高比例。
我国发电用煤的平均含硫量高达1.15%,因此,电站烟气脱硫对我国来说更为重要。
控制SO2排放的工艺按其在燃烧过程中所处位置可分为燃烧前、燃烧中和燃烧后脱硫三种。
燃烧前脱硫主要是洗煤、煤的气化和液化。
洗煤可用作脱硫的辅助手段,经济适用的煤气化和液化技术在进一步开发之中。
就燃烧中脱硫的型煤和循环流化床燃烧来说,燃用型煤比直接燃用原煤节煤又干净,较多用于中小锅炉上。
当前应用的脱硫方法,大致可分为两类,即干法脱硫和湿法脱硫。
干法脱硫:
该法是用粉状、粒状吸收剂,吸附剂或催化剂去除废气中的二氧化硫。
干法的最大优点是治理中无废水、废酸排出,减少了二次污染;
缺点是脱硫效率低,设备庞大,操作要求高。
湿法脱硫:
该法是采用液体吸收剂如水或碱溶液洗涤含二氧化硫的烟气,通过吸收去除其中的二氧化硫,湿法脱硫所用设备较简单,操作容易,脱硫效率较高。
但脱硫后烟气温度降低,于烟囱排烟扩散不利。
由于使用不同的吸收剂可获得不同的副产物而加以利用,因此湿法是全国研究最多的方法。
湿法脱硫效率较高,而且设备简单,操作运行方便,运行成本低,产生的副产物如硫酸盐和压硫酸盐,可回收利用,作为工业原料。
所以在本设计中选取湿法脱硫。
三、吸收设备:
板式塔与填料塔的比较
一般为了强化吸收过程,降低设备的投资和运行费用,要求吸收设备应满足以下基本要求:
1.气液之间应有较大的接触面积和一定接触时间;
2.分离效率高;
操作稳定,弹性大;
3.对气体的阻力小;
4.结构简单,制作维修方便,造价低廉;
5.相应的抗腐蚀能力和防堵塞能力。
常用的吸收设备有喷淋塔、填料塔、板式塔、湍流塔、鼓泡塔等。
这里我们主要比较板式塔和填料塔各自的特点:
板式塔内沿塔高装有若干层塔板(或称塔盘),液体靠重力作用由顶部逐板流向塔底,并在各块板面上形成流动的液层;
气体则靠压强差推动,由塔底向上依次穿过各塔板上的液层而流向塔顶。
气、液两相在塔内进行逐级接触,两相的组成沿塔高呈阶梯式变化。
填料塔内装有各种形式的固体填充物,即填料。
液相由塔顶喷淋装置分布于填料层上,靠重力作用沿填料表面流下;
气相则在压强差推动下穿过填料的间隙,由塔的一端流向另一端。
气、液在填料的润湿表面上进行接触,其组成沿塔高连续地变化。
目前在工业生产中,当处理量大时多采用板式塔,而当处理量较小时多采用填料塔。
蒸馏操作的规模往往较大,所需塔径常达一米以上,故采用板式塔较多;
吸收操作的规模一般较小,故采用填料塔较多。
项目
塔型
备注
板式塔
填料塔
造价
Ф600以下,安装较困难
普通填料塔Ф800以下造价一般较板式塔便宜,直径大则昂贵
由于填料塔造价随体积几乎正比的增大,单位体积造价降低
分离效率
每块塔板的效率较稳定,大塔效率比小塔效率有所提高
工业塔等板高度