碳和碳的化合物 总结.docx
《碳和碳的化合物 总结.docx》由会员分享,可在线阅读,更多相关《碳和碳的化合物 总结.docx(16页珍藏版)》请在冰豆网上搜索。
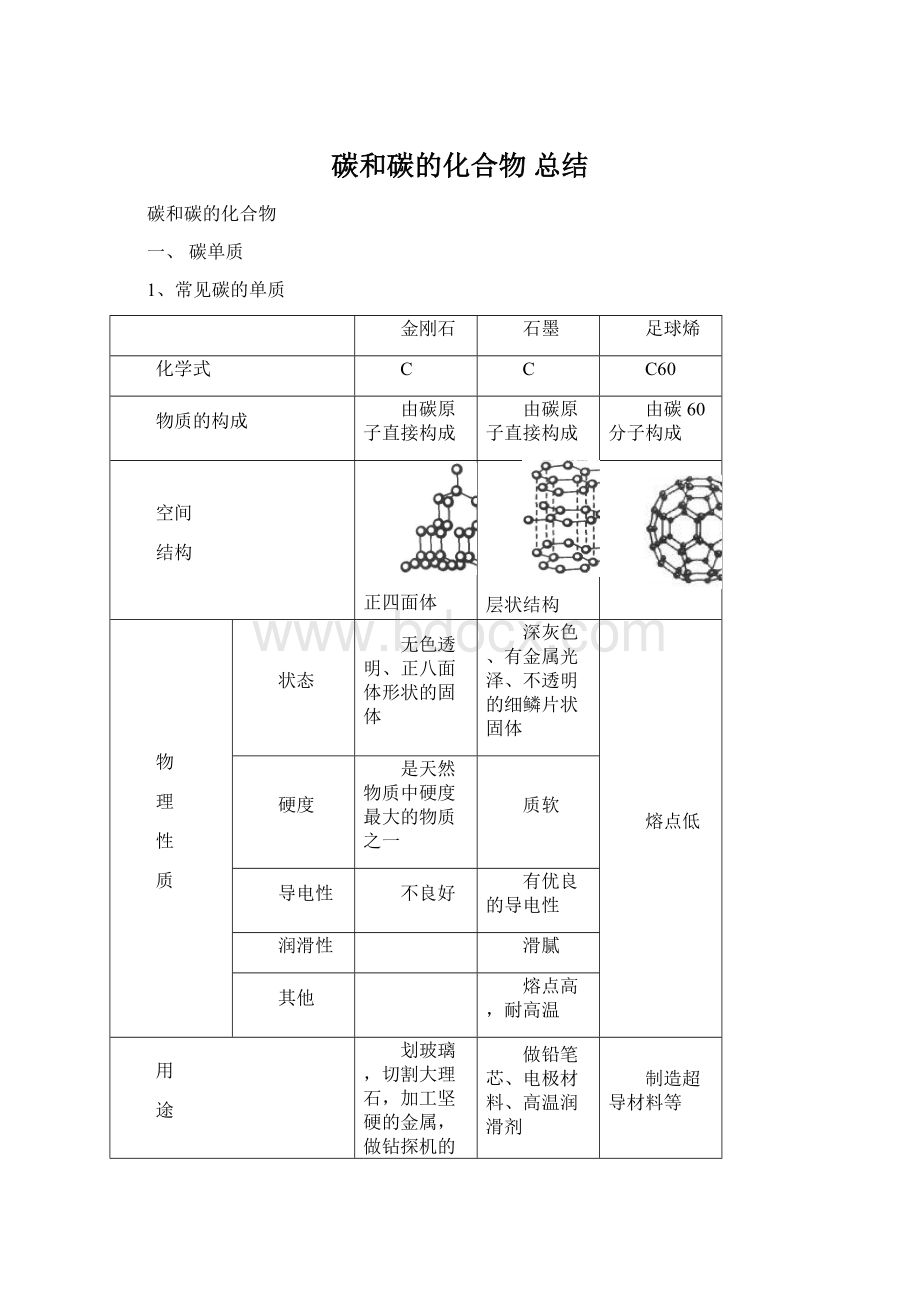
碳和碳的化合物总结
碳和碳的化合物
一、碳单质
1、常见碳的单质
金刚石
石墨
足球烯
化学式
C
C
C60
物质的构成
由碳原子直接构成
由碳原子直接构成
由碳60分子构成
空间
结构
正四面体
层状结构
物
理
性
质
状态
无色透明、正八面体形状的固体
深灰色、有金属光泽、不透明的细鳞片状固体
熔点低
硬度
是天然物质中硬度最大的物质之一
质软
导电性
不良好
有优良的导电性
润滑性
滑腻
其他
熔点高,耐高温
用
途
划玻璃,切割大理石,加工坚硬的金属,做钻探机的钻头,做装饰品
做铅笔芯、电极材料、高温润滑剂
制造超导材料等
2、炭黑、木炭、焦炭、活性炭
均是无定形碳,主要是石墨的微小晶体和少量杂质构成的。
(为混合物)
结构特点:
疏松多孔性质特点:
吸附性良好用途:
冰箱的除臭剂等
木炭经水蒸气高温处理可以得到更大表面积的活性炭,吸附能力更强。
【例】(10湖北)防毒面具的滤毒罐中用来吸附毒气的物质是:
A、炭黑B、活性炭C、木炭D、石墨
3、化学性质
(1)碳的稳定性:
常温下,碳的化学性质不活泼。
例:
我国古代用墨绘制的字画能够保持多年而不褪色,这是因为:
;
埋木质电线杆之前,常要把埋入土里的一端微微烧焦,这是因为;
黑墨水写的字不易褪色,蓝墨水写的字容易褪色,这是因为,可是铅笔
写的字确同样容易褪去,这是因为。
(2)碳的可燃性:
氧气不足条件下:
2C+O2点燃2CO
(还原性)氧气充足条件下:
C+O2点燃CO2
机理:
第一步:
2C+O2点燃2CO
第二步:
2CO+O2点燃2CO2
应用:
1、有关碳与氧气反应的相关计算
结论:
碳与氧气反应随着氧气与碳的质量的不同,产物可能会出现三种不同的情况。
A、只有CO:
m(O2)/m(C)≤4/3
B、既有CO又有CO2:
4/3≤m(O2)/m(C)≤8/3
C、只有CO2:
m(O2)/m(C)≥8/3
例:
在密闭容器中盛有6g碳和12g氧气,加热使它们充分反应后,最后容器里的气体应该是()
A.CO2B.CO2和COC.COD.CO2和O2
【答案】B
2、氧化反应,还原反应;氧化性,还原性
氧化反应:
物质得到“氧”的反应(氧元素质量分数增大)
还原反应:
物质失去“氧”的反应(氧元素质量分数减小)
氧化剂:
失去“氧”的反应物
还原剂:
得到“氧”的反应物
氧化性:
物质失去“氧”的性质
还原性:
物质得到“氧”的性质
(3)碳的还原性:
在加热或高温条件下,碳能夺取氧化物中的氧,表现出还原性。
如:
2CuO+C高温2Cu+CO2↑。
2Fe2O3+3C高温4Fe+3CO2↑。
4、经典例题
【例2】铜粉和碳粉的混合物在空气中充分灼烧后,最终得到的黑色物质与原来的混合物质
量相等,则碳粉在原混合物中所占的质量百分比是()
A.20%B.80%C.15.8%D.84.2%
二、碳的氧化物
1、一氧化碳
A、物理性质
无色无味的气体,难溶于水,密度比空气略小
气体的收集装置:
B、化学性质
a、可燃性:
2CO+O2 点燃 2CO2(火焰颜色:
蓝色)
(还原性)
点燃时火焰颜色为蓝色的有:
固体:
硫粉
气体:
CO,H2,CH4
应用:
气体的检验:
①、CO,H2,CH4
②H2O、CO2
③O2
【例1】一纯净气体可能是H2、CO、CH4中的一种,现将它点燃后的生成物依次通过右图所示装置。
A装置中盛放的是浓硫酸(浓硫酸有吸水性,作为干燥剂),B装置中盛放的是氢氧化钠溶液,则:
(1)如果A装置质量增加,B装置质量不变,则原气体是,
(2)如果A装置质量不变,B装置质量增加,则原气体是,
(3)如果A装置、B装置质量都增加,则原气体是。
(4)能否将A装置和B装置的位置对调?
为什么?
【例2】有CH4、CO、H2三种纯净的气体,分别燃烧后,将生成的气体先通过无水硫酸铜固体(A装置),再通过澄清的石灰水(B装置),则:
(1)如果A装置变蓝,B装置无现象,则原气体是,
(2)如果A装置不变蓝,B装置变浑浊,则原气体是,
(3)如果A装置变蓝,B装置变浑浊,则原气体是。
(4)能否将A装置和B装置的位置对调?
为什么?
【例3】某无色混合气体可能含有CO2、CO、H2O、H2中的两种或几种,依次进行如下处理(假设每次处理反应都很完全)。
①通过碱石灰(生石灰和氢氧化钠固体的混合物,可以吸收水和二氧化碳),气体体积变小;②通过灼热的氧化铜,固体变红色;③通过白色硫酸铜粉末,粉末变蓝色;(白色硫酸铜粉末遇水变成蓝色)④通过澄清石灰水,溶液变浑浊。
由此可知()
A.一定含有CO2、H2O,至少含有H2、CO中的一种
B.一定含有H2O、CO,至少含有CO2、H2中的一种
C.一定含有CO、CO2,至少含有H2O、H2中的一种
D.一定含有CO、H2,至少含有H2O、CO2中的一种
【小结】气体的检验装置:
A、检验药品为固体
B、检验药品为液体
C、注意事项
b、还原性:
CuO+CO △Cu+CO2;
Fe2O3+3CO 高温 2Fe+3CO2
应用:
还原性气体还原金属氧化物的实验(五大实验之一)
实验装置:
注意事项:
还原性气体“早出晚归”酒精灯“迟到早退”
【例1】(06北京)根据下图回答问题:
(1)写出标有序号的仪器名称:
a,b。
(2)CO和Fe2O3均属于(填序号)。
①单质②氧化物③酸④碱⑤盐
(3)澄清石灰水中可观察到的现象是。
(4)点燃b的目的是。
(5)高温条件下此反应的化学方程式为
【例2】(07北京)某课外小组的同学们收集了含一氧化碳和
二氧化碳的废气,为了确认这种废气的组成,他们在实验室按如下
装置进行了实验。
(l)B装置中盛放足量浓氢氧化钠溶液,其作用是_________。
(2)C装置中发生反应的化学方程式是___________________。
(3)A装置和D装置完全相同,其作用的不同之处是_______。
(4)该小组同学认为废气中的一氧化碳可以利用,于是设计如下
装置除去废气中的二氧化碳,并收集一瓶一氧化碳,准备进行后
续地探究。
其中最合理的装置是_________(填序号,瓶内为氢氧
化钠溶液)。
【例3】用含杂质二氧化碳和水蒸气的某种还原性气体,测定一种铁的氧化物(FexOy)的组成,实验装置如下图所示,试根据图示回答:
(1)甲装置的作用是:
,反应的化学方程式是。
(2)若将甲、乙两装置位置对换,对实验结果有无影响?
为什么?
。
(3)在实验过程中,丁装置没有明显变化,而戊装置中出现了白色沉淀,则该还原性气体是。
(4)当丙装置中的FexOy全部被充分还原,冷却后称量剩余固体的质量是22.4克,同时测得戊装置的质量增加了26.4克,则FexOy中铁元素和氧元素的质量比是(7:
3),该氧化物的化学式为(Fe2O3)
(5)上述实验中,如果没有甲装置,将使测定结果中铁元素与氧元素的质量比(填“偏大”、“偏小”或“无影响”)。
如果没有已装置,可能产生的后果是。
【例4】如图所示,A是CO还原CuO的演示实验,B是一种改进实验装置,C装置是某同学对方案B的进一步改进。
另据报道:
多孔陶瓷已广泛用于汽车尾气的净化;氯化钯水溶液与CO气体迅速发生化学反应:
PdCl2+CO+H2O
Pd↓+CO2+2HCl
(1)装置A与B对CO的处理原理有何不同?
(2)该同学设计的C装置有哪些优缺点?
(3)用题中所给的信息,再设计一种改进装置
【小结】:
气体的除杂装置:
A、除杂药品为固体
B、除杂药品为液体
C、注意事项
尾气处理装置
1.收集式:
2.点燃式:
3.吸收式:
注意:
防倒吸:
c、毒性:
CO与血红蛋白结合,阻碍氧气与血红蛋白结合,使人体缺氧而窒息死亡。
2、二氧化碳
A、物理性质
无色无味的气体,能溶于水,密度比空气大。
B、化学性质
1、)不燃烧、不支持燃烧、不支持呼吸
2、)与水反应:
CO2+H2OH2CO3;
3、)与氢氧化钙的反应:
CO2+Ca(OH)2CaCO3↓+H2O。
CaCO3+CO2+H2O=Ca(HCO3)2
4、)氧化性:
C+CO2 高温 2CO
应用:
三大气体的性质实验(CO2)
【例1】下列有关二氧化碳的实验中,只能证明二氧化碳物理性质的是()
【例2】如图所示,将四个大小完全一样的装置,同时放在阳光下,
(1)过一段时间后我们观察到:
,
原因是:
。
(2)由上述模拟实验,你认识到空气中CO2含量升高,对环境的主要影响是;为了保证空气中CO2含量的相对稳定,可采用的主要措施有
【例3】(09北京)32小刚和小丽两位同学用下图所示装置进行实验,验证二氧化碳与氢氧化钠、氢氧化钙都能发生反应。
(1)小刚关闭K,通入二氧化碳,A、B中均无明显变化。
B中盛放_____溶液。
(2)小刚打开K,继续通入二氧化碳。
B中反应的化学方程式为_____。
此步实验目的是_____。
小丽认为:
通常状况下,1体积的水约能溶解1体积二氧化碳,因此上述实验不足以证
明二氧化碳和氢氧化钠发生了反应。
(3)小丽用洗涤干净的上述装置重新实验,分别量取50mL上述溶液放入A、B中,关闭K,通入约500mL二氧化碳,A、B中均无明显变化。
此实验可以说明二氧化碳和氢氧化钠发生了反应,其理由是_____。
C、二氧化碳的制备
1、)反应原理:
药品:
用稀盐酸与块状大理石或石灰石(主要成分是碳酸钙)
原理:
CaCO3+2HClCaCl2+H2O+CO2↑
2、)实验装置
A、发生装置的选择依据:
一看反应物状态;二看反应条。
B、收集装置的选择依据:
排水法:
所收集气体不易溶于水、且不与水发生反应。
排空气法:
所收集气体的密度和空气密度的大小不同、且不与空气中任何成分发生反应。
C、二氧化碳的实验室制取:
1、)装置:
2、)收集方法:
向上排空气法
3、)步骤:
①检查反应装置的气密性
②装入块状大理石,塞紧塞子,出气导管刚好伸入锥形瓶内
③把反应装置固定好
④从长颈漏斗加入稀盐酸至浸没漏斗导管末端
⑤收集气体
⑥检验是否集满
4、)检验:
验证:
将被检验的气体通入澄清石灰水中,若澄清石灰水变浑浊,证明是CO2,否则不是。
验满:
用燃着的木条靠近集气瓶口,若木条熄灭,证明已集满,否则未满。
5、)注意事项:
①一般不用稀硫酸来代替稀盐酸,是因为反应生成的硫酸钙是微溶物,这种沉淀会附着在块状大理石或石灰石的表面,阻碍反应的继续进行。
②一般不用浓盐酸代替稀盐酸,是因为浓盐酸易挥发,挥发出来的氯化氢气体易混入产生的二氧化碳气体中,会给实验带来误差。
③实验室也不用碳酸钠,粉末状石灰石来代替块状石灰石或大理石,原因是反应速度太快,不便于控制。
D、工业制法:
高温煅烧石灰石:
CaCO3高温CaO+CO2↑
【思考1】如何除去二氧化碳中混有少量的一氧化碳?
【思考2】用盐酸作原料制取二氧化碳时,制得的气体中常混有什么杂质?
应用:
三大气体的制备实验
【例1】下列对a,b,c,d四套装置中,在注入酸起反应后对气球的变化情况分析正确的是()
(已知:
Ca(OH)2+2HCl==CaCl2+2H2O)
A.气球①不胀大,②③④都能迅速胀大
B.气球②逐渐胀大,气球③不变化,气球④迅速胀大
C.气球②逐渐胀大,气球③缓缓膨胀后停止,气球④迅速胀大
D.以上都不正确。
【例2】根据下图所示装置和信息回答有关问题
(1)写出图中编号为①②的仪器名称:
①;②
(2)实验室制取二氧化碳的发生装置是,当用G装置收集二氧化碳时,导气管下端的位置应在(填e或f)处,欲得到干燥的二氧化碳还需用到的装置是,装置内的浓硫酸具有吸水性,是常见的干燥剂。
(3)已知甲烷的密度比空气小,难溶于水。
实验室可用加热无水醋酸钠和碱石灰固体混合物来制取甲烷。
试问,实验室制取甲烷的发生装置应选,收集装置应选。
【例3】(09北京)31.实验室制取气体所需装置如下图所示。
ABCDE
请回答以下问题:
(1)装置中标“a”的仪器名称是_____。
(2)用高锰酸钾制取氧气时,所选用的发生装置是_____(填字母序号,下同),收集装置是C或_____。
(3)用大理石和稀盐酸制取二氧化碳时,所选用的发生装置是_____,其反应的化学方程式为_____。
该装置还可用于制氧气,其反应的化学方程式为_____。
3、经典例题
【例1】(10江西)“吸烟有害于健康”。
我国政府规定:
从2010年5月1日起,公共
室内禁止吸烟。
烟草燃烧释放的有害物质中,能与血红蛋白结合引起中毒的是()
A.尼古丁B.一氧化碳C.焦油D.甲醛
【例2】(10徐州)用右图装置可以探究二氧化碳的制取和性质。
下列关于该实验的叙述
正确的是()
A浸有紫色石蕊试液的棉花会变蓝
B粗铜丝能控制反应的发生和停止
C产生的二氧化碳可用生石灰干燥
D能验证二氧化碳的密度比空气大
【例3】按图所示装置持续通入X气体,并在导管口P处点燃(温度足够),实验结果是
澄清的石灰水变浑浊。
则X、Y可能是()
A.CO2和CuOB.CO和CuO
C.CO和Fe2O3D.CO2和碳单质
【例4】超氧化钾(KO2)是一种黄色固体,它能与二氧化碳反应生成氧气,在潜水艇中
用它作制氧剂,供给人们呼吸之用。
它与二氧化碳反应的化学方程式为:
4KO2+2CO22K2CO3+3O2。
某学生为了验证这一实验,以大理石,足够的盐酸和超
氧化钾为原料制取O2,设计出如图的实验装置:
(1)A是制取二氧化碳的装置,应从右图中选择的装置是。
(填数字序号)B装
置的作用是吸收A装置中产生的盐酸酸雾,C装置中可能出现的现象是。
为
了检验E中收集到的气体,可以在取出集气瓶后用。
(2)若E中的石灰水出现少量的白色沉淀,这是因为。
(3)表明D中的超氧化钾样品接近反应完毕时的现象是。
三、燃烧与燃料
1.燃烧和灭火
燃烧灭火
可燃物清除可燃物或使可燃物与其它物品隔离
氧气(或空气)隔绝氧气或空气
温度达到着火点使温度降到着火点以下
2.燃料和热量
三大化石燃料:
煤、石油、天然气
新型燃料:
乙醇——C2H5OH,俗称酒精
它是非常重要的燃料;C2H5OH+3O2点燃2CO2+3H2O
其它新能源:
氢能源、太阳能、核能、风能、地热能、潮汐能
氢气是最理想的燃料:
(1)优点:
资源丰富,放热量多,无污染。
(2)需解决问题:
如何大量廉价的制取氢气?
如何安全地运输、贮存氢气?
化学反应中的能量变化
(1)放热反应:
如所有的燃烧、金属与酸反应、中和反应
(2)吸热反应:
如一般条件为“高温”的反应、分解
【例1】小刚和小强用图甲和图乙所示实验来探究可燃物燃烧的条件。
经查阅资料知:
白磷着火点为40℃,红磷着火点为240℃,它们在空气中燃烧都生成有毒的白烟——五氧化二磷,五氧化二磷易溶于水。
(1)小刚用图甲所示装置进行实验,观察到的现象是
(2)小强用图乙所示装置进行实验,得到以下实验事实:
①不通空气时,冷水中的白磷不燃烧;②通空气时,冷水中的白磷不燃烧;③不通空气时,
热水中的白磷不燃烧;④通空气时,热水中的白磷燃烧。
该实验中,能证明可燃物通常需
要接触空气才能燃烧的实验事实是(填序号,下同);能证明可燃物必须达到一
定温度(着火点)才能燃烧的实验事实是。
【例2】(10湖北)2008年以来国际油价的持续“高烧”,引发人们对未来能源供需及价格的深切关注,并且促使人们寻求石油的替代品。
下列说法错误的是()
A.我们应珍惜化石燃料,因为它们既是燃料,又是重要的化工原料,且不可再生
B.在合理使用化石燃料的同时,我们应努力寻求开发新能源
C.国家决定推广乙醇汽油的应用,乙醇汽油是一种新型化合物
D.汽车使用乙醇汽油能减少有害气体的排放
【例3】(10苏州)为了避免火灾,加油站采取的下列措施中不合理的是
A.严禁烟火B.禁止使用手机C.架高顶棚加强通风D.降低燃料着火点
【例4】(10宁夏)某学校化学学习小组设计出右图所示装置,并进行白磷
燃烧实验。
(1)当烧杯内的水受热,温度计显示30℃时,打开活塞,在盛有水的试管中有气泡均匀逸出,白磷未燃烧,关闭活塞。
锥形瓶内反应的化学方程式是:
___________________。
白磷未燃烧的原因是。
(2)随着水温升高,温度计显示45℃时,再次打开活塞,白磷在水里燃烧。
常言道,水火不相容。
水能灭火的原因是。
而本实验中白磷在水里还能够燃烧的原因是。
(3)本实验装置的A部分还可以用于制取的气体是,收集方法是。