学习资料收货验收.docx
《学习资料收货验收.docx》由会员分享,可在线阅读,更多相关《学习资料收货验收.docx(16页珍藏版)》请在冰豆网上搜索。
学习资料收货验收
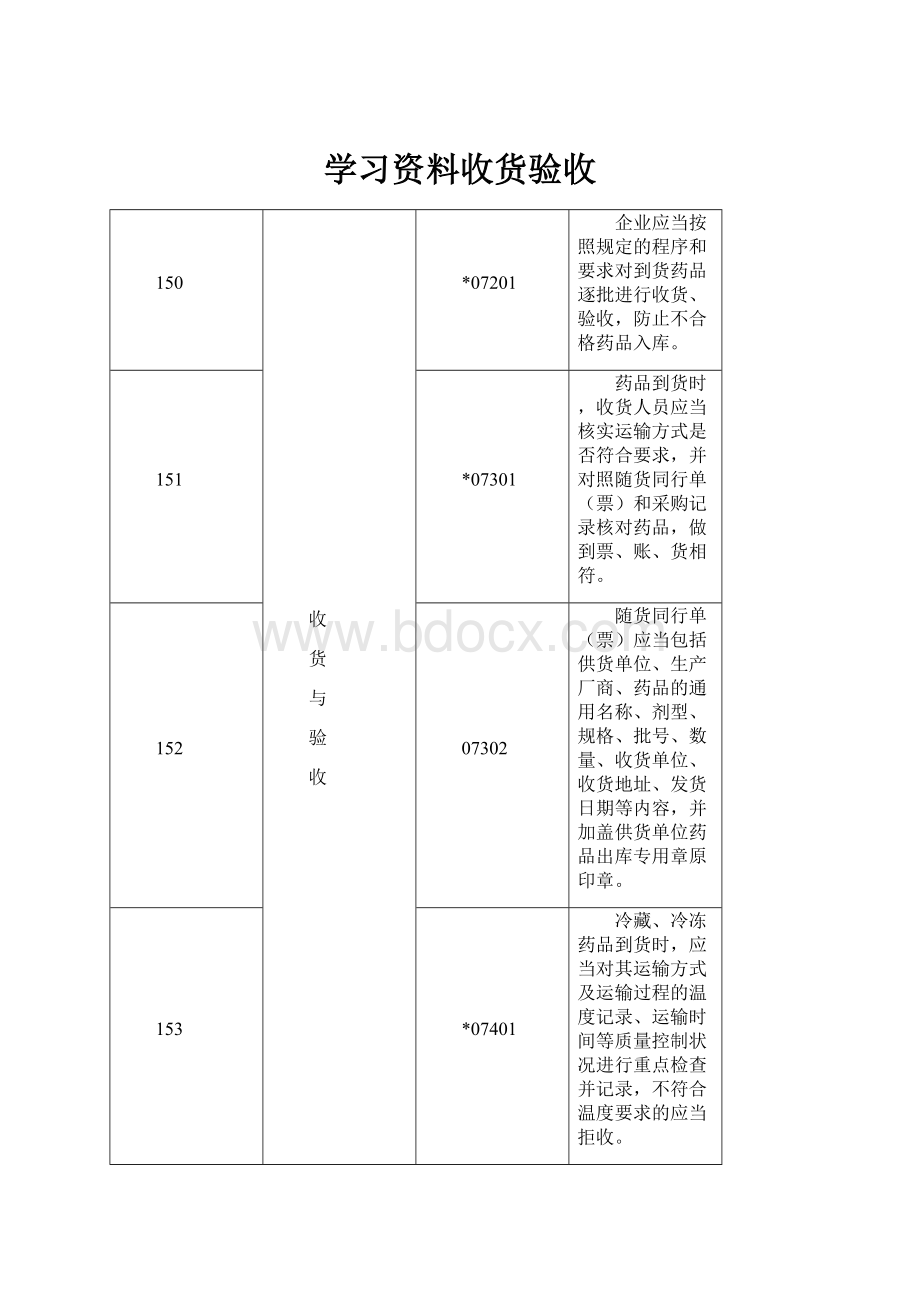
150
收
货
与
验
收
*07201
企业应当按照规定的程序和要求对到货药品逐批进行收货、验收,防止不合格药品入库。
151
*07301
药品到货时,收货人员应当核实运输方式是否符合要求,并对照随货同行单(票)和采购记录核对药品,做到票、账、货相符。
152
07302
随货同行单(票)应当包括供货单位、生产厂商、药品的通用名称、剂型、规格、批号、数量、收货单位、收货地址、发货日期等内容,并加盖供货单位药品出库专用章原印章。
153
*07401
冷藏、冷冻药品到货时,应当对其运输方式及运输过程的温度记录、运输时间等质量控制状况进行重点检查并记录,不符合温度要求的应当拒收。
154
07501
收货人员对符合收货要求的药品,应当按品种特性要求放于相应待验区域,或者设置状态标志,通知验收。
155
*07502
冷藏、冷冻药品应当在冷库内待验。
156
07601
验收药品应当按照药品批号查验同批号的检验报告书。
157
07602
供货单位为批发企业的,检验报告书应当加盖其质量管理专用章原印章。
检验报告书的传递和保存可以采用电子数据形式,但应当保证其合法性和有效性。
158
*07701
企业应当按照验收规定,对每次到货药品进行逐批抽样验收。
159
07702
抽取的样品应当具有代表性。
160
07703
同一批号的药品至少检查一个最小包装,但生产企业有特殊质量控制要求或者打开最小包装可能影响药品质量的,可不打开最小包装。
161
07704
破损、污染、渗液、封条损坏等包装异常以及零货、拼箱的,应当开箱检查至最小包装。
162
07705
外包装及封签完整的原料药、实施批签发管理的生物制品,可不开箱检查。
163
07801
验收人员应当对抽样药品的外观、包装、标签、说明书以及相关的证明文件等逐一进行检查、核对。
164
07802
验收结束后,应当将抽取的完好样品放回原包装箱,加封并标示。
165
*07901
特殊管理的药品应当按照相关规定在专库或者专区内验收。
166
08001
验收药品应当做好验收记录,包括药品的通用名称、剂型、规格、批准文号、批号、生产日期、有效期、生产厂商、供货单位、到货数量、到货日期、验收合格数量、验收结果等内容。
167
08002
中药材验收记录应当包括品名、产地、供货单位、到货数量、验收合格数量等内容。
168
08003
中药饮片验收记录应当包括品名、规格、批号、产地、生产日期、生产厂商、供货单位、到货数量、验收合格数量等内容,实施批准文号管理的中药饮片还应当记录批准文号。
169
08004
验收不合格的应当注明不合格事项及处置措施。
170
08005
验收人员应当在验收记录上签署姓名和验收日期。
171
*08101
对实施电子监管的药品,应当按规定进行药品电子监管码扫码,并及时将数据上传至中国药品电子监管网系统平台。
172
08201
对未按规定加印或者加贴中国药品电子监管码,或者监管码的印刷不符合规定要求的,应当拒收。
173
08202
监管码信息与药品包装信息不符的,应当及时向供货单位查询,未得到确认之前不得入库,必要时向当地药品监督管理部门报告。
174
08301
企业应当建立库存记录,验收合格的药品应当及时入库登记;验收不合格的,不得入库,并由质量管理部门处理。
175
08401
企业按《规范》规定进行药品直调的,可委托购货单位进行药品验收。
176
08402
购货单位应当严格按照《规范》的要求验收药品和进行药品电子监管码的扫码与数据上传。
177
08403
应当建立专门的直调药品验收记录。
178
08404
验收当日应当将验收记录相关信息传递给直调企业。
(四)药品收货与验收
条款号
检查项目
所对应附录检查内容
*03701
质量管理、验收岗位职责。
验收人员应当负责对中药材样品的更新与养护,防止样品出现质量变异。
收集的样品放入中药样品室(柜)前,应当由质量管理人员确认。
04708
库房应当有验收的专用场所。
1.药品待验区域有明显标识,并与其他区域有效隔离。
2.待验区域符合待验药品的储存温度要求。
3.验收设施设备清洁,不得污染药品。
4.待验区按规定配备药品电子监管码扫码与数据上传设备。
*07201
企业应当按照规定的程序和要求对到货药品逐批进行收货、验收,防止不合格药品入库。
1.企业应当按照国家有关法律法规及《规范》要求,制定药品收货与验收标准。
2.对药品收货与验收过程中出现的不符合质量标准或疑似假、劣药的情况,应当交由质量管理部门按照有关规定进行处理,必要时上报药品监督管理部门。
3.企业应当根据不同类别和特性的药品,明确待验药品的验收时限,待验药品要在规定时限内验收。
4.验收中发现的问题应当尽快处理,防止对药品质量造成影响。
*07301
药品到货时,收货人员应当核实运输方式是否符合要求,并对照随货同行单(票)和采购记录核对药品,做到票、账、货相符。
药品到货时,收货人员:
1.应当检查运输工具是否密闭,如发现运输工具内有雨淋、腐蚀、污染等可能影响药品质量的现象,应当通知采购部门并报质量管理部门处理。
2.根据运输单据所载明的启运日期,检查是否符合协议约定的在途时限,对不符合约定时限的,应当报质量管理部门处理。
3.供货方委托运输药品的,企业采购部门应当提前向供货单位索要委托的承运方式、承运单位、启运时间等信息,并将上述情况提前告知收货人员。
4.要逐一核对承运方式、承运单位、启运时间等信息,不一致的应当通知采购部门并报质量管理部门处理。
5.应当查验随货同行单(票)以及相关的药品采购记录。
6.无随货同行单(票)或无采购记录的应当拒收。
7.随货同行单(票)记载的供货单位、生产厂商、药品的通用名称、剂型、规格、批号、数量、收货单位、收货地址、发货日期等内容与采购记录以及本企业实际情况不符的,应当拒收,并通知采购部门处理。
8.应当依据随货同行单(票)核对药品实物。
随货同行单(票)中药品的通用名称、剂型、规格、批号、数量、生产厂商等内容与药品实物不符的,应当拒收,并通知采购部门进行处理。
收货过程中,收货人员:
1.对于随货同行单(票)内容中除数量以外的其他内容与采购记录、药品实物不符的,经采购部门向供货单位核实确认后,由供货单位提供正确的随货同行单(票)后,方可收货。
2.对于随货同行单(票)与采购记录、药品实物数量不符的,经供货单位确认后,应当按照采购制度由采购部门确定并调整采购数量后,方可收货。
3.供货单位对随货同行单(票)与采购记录、药品实物不相符的内容不予确认的,到货药品应当拒收,存在异常情况的,报质量管理部门处理。
4.应当拆除药品的运输防护包装,检查药品外包装是否完好,对出现破损、污染、标识不清等情况的药品,应当拒收。
*07401
冷藏、冷冻药品到货时,应当对其运输方式及运输过程的温度记录、运输时间等质量控制状况进行重点检查并记录,不符合温度要求的应当拒收。
1.冷藏、冷冻药品到货时,应当查验冷藏车、车载冷藏箱或保温箱的温度状况,核查并留存运输过程和到货时的温度记录。
2.收货人员根据运输单据所载明的启运日期,检查是否符合协议约定的在途时限,对不符合约定时限的,应当报质量管理部门处理。
3.供货方委托运输药品的,企业采购部门应当提前向供货单位索要委托的承运方式、承运单位、启运时间等信息,并将上述情况提前告知收货人员。
4.收货人员在药品到货后,要逐一核对承运方式、承运单位、启运时间等信息,不一致的应当通知采购部门并报质量管理部门处理。
5.对未采用规定的冷藏设施运输的或者温度不符合要求的应当拒收,做好记录并报质量管理部门处理。
07501
收货人员对符合收货要求的药品,应当按品种特性要求放于相应待验区域,或者设置状态标志,通知验收。
收货人员应当将核对无误的药品放置于相应的待验区域内,并在随货同行单(票)上签字后移交验收人员。
07702
抽取的样品应当具有代表性。
1.验收抽取的样品应当具有代表性。
2.对到货的同一批号的整件药品按照堆码情况随机抽样检查。
3.整件数量在2件及以下的应当全部抽样检查;整件数量在2件以上至50件以下的至少抽样检查3件;整件数量在50件以上的每增加50件,至少增加抽样检查1件,不足50件的按50件计。
4.对抽取的整件药品应当开箱抽样检查。
5.应当从每整件的上、中、下不同位置随机抽取3个最小包装进行检查,对存在封口不牢、标签污损、有明显重量差异或外观异常等情况的,至少再加一倍抽样数量进行检查。
6.到货的非整件药品应当逐箱检查,对同一批号的药品,至少随机抽取一个最小包装进行检查。
07801
验收人员应当对抽样药品的外观、包装、标签、说明书以及相关的证明文件等逐一进行检查、核对。
1.验收人员应当对抽样药品的外观、包装、标签、说明书等逐一进行检查、核对,出现问题的,报质量管理部门处理。
2.检查运输储存包装的封条有无损坏,包装上是否清晰注明药品通用名称、规格、生产厂商、生产批号、生产日期、有效期、批准文号、贮藏、包装规格及储运图示标志,以及特殊管理的药品、外用药品、非处方药的标识等标记。
3.检查最小包装的封口是否严密、牢固,有无破损、污染或渗液,包装及标签印字是否清晰,标签粘贴是否牢固。
4.检查每一最小包装的标签是否有药品通用名称、成份、性状、适应症或者功能主治、规格、用法用量、不良反应、禁忌、注意事项、贮藏、生产日期、产品批号、有效期、批准文号、生产企业等内容。
4.1对注射剂瓶、滴眼剂瓶等因标签尺寸限制无法全部注明上述内容的,至少标明药品通用名称、规格、产品批号、有效期等内容。
4.2中药蜜丸蜡壳至少注明药品通用名称。
5.化学药品与生物制品说明书列有以下内容:
药品名称(通用名称、商品名称、英文名称、汉语拼音)、成分[活性成分的化学名称、分子式、分子量、化学结构式(复方制剂可列出其组分名称)]、性状、适应症、规格、用法用量、不良反应、禁忌、注意事项、孕妇及哺乳期妇女用药、儿童用药、老年用药、药物相互作用、药物过量、临床试验、药理毒理、药代动力学、贮藏、包装、有效期、执行标准、批准文号、生产企业(企业名称、生产地址、邮政编码、电话和传真)。
6.中药说明书列有以下内容:
药品名称(通用名称、汉语拼音)、成分、性状、功能主治、规格、用法用量、不良反应、禁忌、注意事项、药物相互作用、贮藏、包装、有效期、执行标准、批准文号、说明书修订日期、生产企业(企业名称、生产地址、邮政编码、电话和传真)。
7.特殊管理的药品、外用药品的包装、标签及说明书上均有规定的标识和警示说明;处方药和非处方药的标签和说明书上有相应的警示语或忠告语,非处方药的包装有国家规定的专有标识;蛋白同化制剂和肽类激素及含兴奋剂类成分的药品有“运动员慎用”警示标识。
8.进口药品的包装、标签以中文注明药品通用名称、主要成分以及注册证号,并有中文说明书。
9.中药饮片的包装或容器与药品性质相适应及符合药品质量要求。
中药饮片的标签需注明品名、包装规格、产地、生产企业、产品批号、生产日期;整件包装上有品名、产地、生产日期、生产企业等,并附有质量合格的标志。
实施批准文号管理的中药饮片,还需注明批准文号。
10.中药材有包装,并标明品名、规格、产地、供货单位、收购日期、发货日期等;实施批准文号管理的中药材,还需注明批准文号。
验收地产中药材时,如果对到货中药材存在质量疑问,应当将实物与企业中药样品室(柜)中收集的相应样品进行比对,确认后方可收货。
11.验收实施批签发管理的生物制品时,应当有加盖供货单位药品检验专用章或质量管理专用章原印章的《生物制品批签发合格证》复印件。
12.验收进口药品应当有加盖供货单位质量管理专用章原印章的相关证明文件:
《进口药品注册证》或《医药产品注册证》;进口麻醉药品、精神药品以及蛋白同化制剂、肽类激素应当有《进口准许证》;进口药材应当有《进口药材批件》;《进口药品检验报告书》或注明“已抽样”字样的《进口药品通关单》;进口国家规定的实行批签发管理的生物制品,必须有批签发证明文件和《进口药品检验报告书》。
07802
验收结束后,应当将抽取的完好样品放回原包装箱,加封并标示。
检查验收结束后,应当将检查后的完好样品放回原包装,并在抽样的整件包装上标明抽验标志,对已经检查验收的药品,应当及时调整药品质量状态标识或移入相应区域。
*07901
特殊管理的药品应当按照相关规定在专库或者专区内验收。
1.设置特殊管理的药品专用待验区域,并符合安全控制要求。
2.验收特殊管理的药品应当符合国家相关规定。
08301
企业应当建立库存记录,验收合格的药品应当及时入库登记;验收不合格的,不得入库,并由质量管理部门处理。
1.验收合格的药品,应当及时入库。
2.对验收合格的药品,应当由验收人员与仓储部门办理入库手续,由仓储部门建立库存记录。
3.对于不符合验收标准的,不得入库,并报质量管理部门处理。
4.对于相关证明文件不全或内容与到货药品不符的,不得入库,并交质量管理部门处理。
*11601
企业应当加强对退货的管理,保证退货环节药品的质量和安全,防止混入假冒药品。
1.企业应当加强对退货药品的收货、验收管理,保证退货环节药品的质量和安全,防止混入假冒药品。
2.收货人员要依据销售部门确认的退货凭证或通知对销后退回药品进行核对,确认为本企业销售的药品后,方可收货并放置于符合药品储存条件的专用待验场所。
3.对销后退回的冷藏、冷冻药品,根据退货方提供的温度控制说明文件和售出期间温度控制的相关数据,确认符合规定条件的,方可收货;对于不能提供文件、数据,或温度控制不符合规定的,给予拒收,做好记录并报质量管理部门处理。
4.验收人员对销后退回的药品进行逐批检查验收,并开箱抽样检查。
5.整件包装完好的,数量在2件及以下的应当全部抽样检查;数量在2件以上至50件以下的至少抽样检查6件;整件数量在50件以上的每增加50件,至少增加抽样检查2件,不足50件的按50件计。
6.抽样检查应当从每整件的上、中、下不同位置随机抽取6个最小包装进行检查,对存在封口不牢、标签污损、有明显重量差异或外观异常等情况的,至少再加一倍抽样数量进行检查。
7.无完好外包装的,每件须抽样检查至最小包装,必要时送药品检验机构检验。
8.销后退回药品经验收合格后,方可入库销售,不合格药品按《规范》有关规定处理。