版《单元滚动检测卷》高考化学人教全国精练检测一从实验学化学文档格式.docx
《版《单元滚动检测卷》高考化学人教全国精练检测一从实验学化学文档格式.docx》由会员分享,可在线阅读,更多相关《版《单元滚动检测卷》高考化学人教全国精练检测一从实验学化学文档格式.docx(18页珍藏版)》请在冰豆网上搜索。
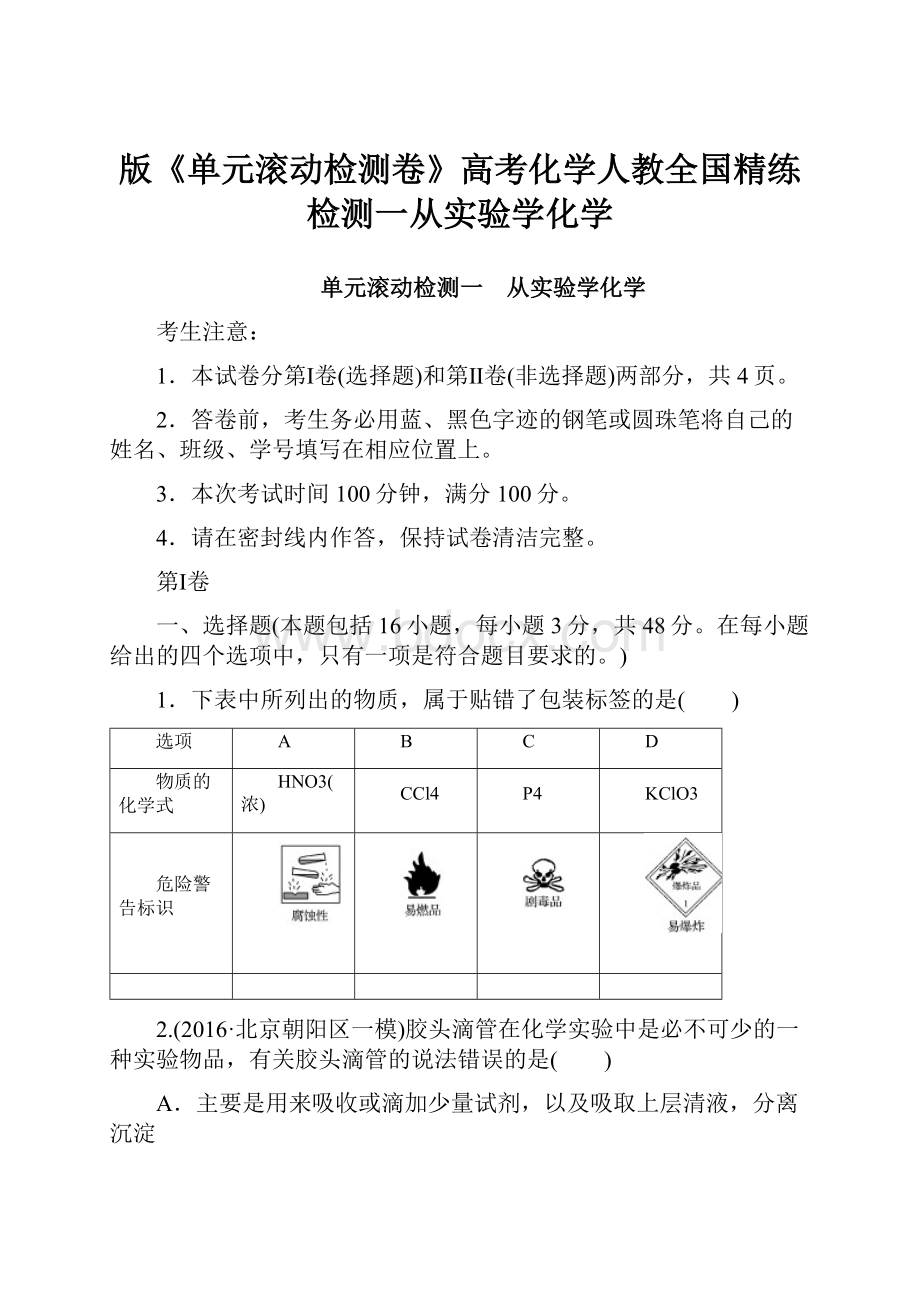
D.测定中和反应的反应热时,将碱缓慢倒入酸中,所测温度值偏小
4.正确的实验操作是实验成功的重要因素,下列实验操作正确的是( )
A.①②B.②③
C.①④D.③④
5.(2016·
惠州模拟)设NA为阿伏加德罗常数的值,下列说法正确的是( )
A.分子数为NA的CO和C2H4混合气体的体积约为22.4L
B.标准状况下,4.48L重水(D2O)中含有的中子数为2NA
C.用MnO2与浓盐酸制取Cl2时,每生成0.5molCl2则转移电子数为NA
D.0.1L3.0mol·
L-1的NH4NO3溶液中含有NH
的数目为0.3NA
6.三聚氰胺事件,使中国乳业多年走在阴影之中,现已步入复苏。
三聚氰胺又名蛋白精[分子式为C3N3(NH2)3,相对分子质量:
126]是一种低毒性化工产品,婴幼儿大量摄入可引起泌尿系统疾患。
有关三聚氰胺说法正确的是( )
A.2.52g三聚氰胺含氮原子数目为0.12NA
B.标准状况下,1mol三聚氰胺的体积为22.4L
C.三聚氰胺含氮量约为10%
D.三聚氰胺的摩尔质量为126g
7.使用容量瓶配制溶液时,由于操作不当,会引起误差。
下列情况会使所配溶液浓度偏低的是( )
①用天平(使用游码)称量时,被称量物与砝码的位置放颠倒
②溶液转移到容量瓶后,烧杯及玻璃棒未用蒸馏水洗涤
③转移溶液前容量瓶内有少量蒸馏水
④定容时,俯视容量瓶的刻度线
⑤定容后摇匀,发现液面降低,又补加少量水,重新达到刻度线
A.①②⑤B.①③⑤C.③④⑤D.②③⑤
8.(2017·
保定调研)欲配制250mL0.5mol·
L-1的NaOH溶液,在下列仪器中,需要用到的仪器按先后顺序排列正确的是( )
①量筒 ②250mL容量瓶 ③托盘天平和砝码 ④500mL容量瓶 ⑤烧杯 ⑥玻璃棒 ⑦漏斗 ⑧药匙 ⑨胶头滴管 ⑩250mL烧瓶
A.⑧⑤③⑥②⑨B.②③⑦⑤⑥
C.②⑤⑦⑥①D.④③⑦⑤⑥
9.下列各图表示某些同学从溴水中萃取溴并分液的实验环节(夹持仪器已省略),其中正确的是( )
10.(2016·
西安模拟)在海水浓缩过程中,析出盐的种类和质量见下表(单位g·
L-1)。
海水密度(g·
mL-1)
CaSO4
NaCl
MgCl2
MgSO4
NaBr
1.20
0.91
1.21
0.05
3.26
0.004
0.008
1.22
0.015
9.65
0.01
0.04
1.26
2.64
0.02
1.31
1.40
0.54
0.03
0.06
当海水密度达到1.21~1.22g·
mL-1时,析出的盐中,质量分数最大的是( )
A.CaSO4B.MgSO4
C.NaClD.MgCl2
11.(2016·
江西六校联考)若NA表示阿伏加德罗常数的值。
下列说法正确的是( )
A.标准状况下,22.4LNO与11.2LO2混合后气体的体积约为22.4L
B.1L0.2mol·
L-1Al2(SO4)3溶液中的离子总数为NA
C.标准状况下,22.4LH2O所含原子个数大于3NA
D.含4molHCl的浓盐酸跟足量MnO2加热反应,可制得Cl2的分子数为NA
12.设NA表示阿伏加德罗常数的值,下列说法错误的是( )
A.若1mol·
L-1HF溶液中H+数目为NA,则等体积的2mol·
L-1HF溶液中H+数目为2NA
B.44gCO2、N2O组成的混合气体中所含有的原子数为3NA
C.36g3H2中含有的中子数目为24NA
D.2.24L(标准状况)O2与钠反应时,转移电子数目可能为0.3NA
13.(2016·
安徽模拟)NA为阿伏加德罗常数的值,下列说法正确的是( )
A.过氧化钠与水反应时,生成0.1molO2转移的电子数为0.2NA
B.4.48L氨气分子中含0.6NA个N—H键
C.100mL0.2mol·
L-1的FeCl3溶液中,含Fe3+数为0.02NA
D.密闭容器中2molNO与1molO2充分反应,产物的分子数为2NA
14.(2016·
合肥一模)若NA表示阿伏加德罗常数的值,下列说法正确的是( )
A.0.1molNa2CO3·
10H2O晶体中,阴离子总数大于0.1NA
B.常温常压下,18mL水中所含氢离子数约为10-7NA
C.标准状况下,22.4L氦气中含有的原子数约为NA
D.23g组成为C2H6O的有机物,C—H键数目为3NA
15.如图表示1gO2与1gX气体在相同容积的密闭容器中压强(p)与温度(T)的关系,则X气体可能是( )
A.C2H4B.CH4
C.CO2D.NO
16.为了避免NO、NO2、N2O4对大气的污染,常采用氢氧化钠溶液进行吸收处理(化学方程式:
2NO2+2NaOH===NaNO3+NaNO2+H2O,NO2+NO+2NaOH===2NaNO2+H2O)。
现有由amolNO、bmolNO2、cmolN2O4组成的混合气体恰好被VL氢氧化钠溶液吸收(无气体剩余),则此氢氧化钠溶液的物质的量浓度为( )
A.
mol·
L-1B.
L-1
C.
L-1D.
第Ⅱ卷
二、非选择题(本题包括4小题,共52分)
17.(13分)计算后填空:
(1)在标准状况下,448mL某气体的质量为0.64g,这种气体的相对分子质量为________。
(2)某氯化铁与氯化钠的混合液,已知c(Fe3+)=0.2mol·
L-1,c(Cl-)=1mol·
L-1。
则c(Na+)为_____________。
(3)19g某二价金属的氯化物RCl2中含有0.4mol的Cl-,则R的相对原子质量为__________。
(4)VLFe2(SO4)3溶液中含Fe3+mg,则溶液中SO
的物质的量浓度为___________mol·
(5)在无土栽培中,配制1L含5molNH4Cl、1.6molKCl、2.4molK2SO4的某营养液,若用KCl、NH4Cl、(NH4)2SO4配制,则需KCl、NH4Cl的物质的量分别为________、________。
(6)如图所示,
分别向密闭容器内可移动活塞的两边充入空气(已知空气体积占整个容器容积的1/4)、H2和O2的混合气体,在标准状况下,若将H2、O2的混合气体点燃引爆,活塞先左弹,恢复原温度后,活塞右滑停留于容器的中央。
则原来H2、O2的体积之比可能为___________________________________________________________。
18.(13分)(2016·
郑州联考)某研究所对含硫酸亚铁和硫酸铜的工业废料进行相关的研究。
实验过程如下:
回答下列问题:
(1)滤渣的成分为_______________,操作②的名称为____________。
(2)上图溶液B中所发生反应的离子方程式为
________________________________________________________________________
________________________________________________________________________。
(3)实验要求先向溶液B中通入过量的空气,证明通入空气过量的方法是
(4)操作③第一步需要的仪器除了酒精灯、铁架台外,还需要____________________。
(5)某同学利用下面装置制备氢气并利用氢气还原某金属氧化物,根据要求回答问题。
①请设计一个实验方案验证H2的还原性并检验其氧化产物,其装置连接顺序是A→________→________→________→D(除D装置外,其他装置不能重复使用),最后D装置中所加药品为________________________________________________________________,
其作用是______________________________________________________________________。
②点燃B处酒精灯之前必须进行的操作是___________________________________________
_______________________________________________________________________________。
19.(12分)氯化亚铜(CuCl)是白色粉末,不溶于水、乙醇及稀硫酸,在空气中迅速被氧化成绿色,常用作有机合成工业中的催化剂。
实验室拟以下列方法制取CuCl:
在CuSO4溶液中加入一定量的Na2SO3和NaCl溶液,加热,生成CuCl。
试回答以下问题:
(1)CuCl制备过程中需配制物质的量浓度为2.0mol·
L-1的CuSO4溶液。
①配制950mL2.0mol·
L-1的CuSO4溶液应称取胆矾的质量为________g。
②某学生实际配制CuSO4溶液的浓度为1.8mol·
L-1,原因可能是________。
A.托盘天平的砝码生锈
B.容量瓶中原来存有少量蒸馏水
C.溶解后的烧杯未经多次洗涤
D.胶头滴管加水定容时仰视刻度
(2)写出用上述方法制备CuCl的离子方程式__________________________________
(3)在上述制取过程中,经过滤得到CuCl沉淀,用无水乙醇洗涤沉淀,在真空干燥机内于70℃干燥2小时,冷却,密封包装即得产品。
其中“于70℃真空干燥”的目的是____________;
_____________________________________________________________________(回答两点)。
(4)据世界卫生组织统计,最常用的避孕环含金属铜,避孕过程中生成了CuCl。
其原因是铜与人体分泌物中的盐酸以及子宫内的空气反应:
Cu+HCl+O2===CuCl+HO2,HO2(超氧酸)不仅是一种弱酸而且也是一种自由基,具有极高的活性。
下列说法或表示正确的是
A.氧化产物是HO2
B.HO2在碱中能稳定存在
C.HO2的电离方程式是HO2
H++O
D.1molCu参加反应有2mol电子发生转移
20.(14分)CO2是重要的化工原料,也是应用广泛的化工产品。
CO2与过氧化钠或超氧化钾反应可产生氧气。
完成下列计算:
(1)CO2通入氨水生成NH4HCO3,NH4HCO3很容易分解。
2.00molNH4HCO3完全分解,分解产物经干燥后的体积为________________L(标准状况)。
(2)某H2中含有2.40molCO2,该混合气体通入2.00LNaOH溶液中,CO2被完全吸收。
如果NaOH完全反应,该NaOH溶液的浓度为__________________________________________。
(3)CO2和KO2有下列反应:
4KO2+2CO2===2K2CO3+3O2
4KO2+4CO2+2H2O===4KHCO3+3O2
若9molCO2在密封舱内和KO2反应后生成9molO2,则反应前密封舱内H2O的量应该是多少?
列式计算。
(4)甲烷和水蒸气反应的产物是合成甲醇的原料:
CH4+H2O
CO+3H2
已知:
CO+2H2
CH3OH CO2+3H2
CH3OH+H2O
300molCH4完全反应后的产物中,加入100molCO2后合成甲醇。
若获得甲醇350mol,残留氢气120mol,计算CO2的转化率。
答案精析
1.B 2.C
3.C [A项,滴定前滴定管内无气泡,终点读数时有气泡,气体占据液体应占有的体积;
B项,用润湿的pH试纸测稀碱溶液,会对碱溶液的浓度造成稀释;
C项,定容时俯视刻度线,会导致溶液体积偏小;
D项,测定中和反应的反应热时,将碱缓慢倒入酸中,导致热量损失过大。
]
4.C [①闻气体的气味时,不能直接用鼻子闻,一些气体有毒或有刺激性;
②装置中气体应从长管进短管出,否则气体没有通过干燥剂;
③稀释浓硫酸是将浓硫酸沿着容器壁慢慢注入水中,并用玻璃棒不断搅拌,如果将水倒入浓硫酸中,水会浮在上面,浓硫酸溶于水放出的热量足可以使水沸腾,会溅出伤人,所以图中操作错误;
④添加酒精时一定要用小漏斗,以免将酒精洒出,所以图中操作正确。
5.C [A项,气体所处的状态不明确,无法计算;
B项,标况下重水为液态,故不能根据气体摩尔体积来计算;
C项,根据氯元素的价态由-1价变为0价,故生成0.5mol氯气转移1mol电子即NA个电子,正确;
D项,铵根离子为弱碱阳离子,在溶液中能水解,故溶液中的铵根离子的数目小于0.3NA,错误。
6.A [三聚氰胺为固体,摩尔质量为126g·
mol-1,1分子三聚氰胺中含有6个氮原子。
7.A
8.A [先用药匙取NaOH固体,放在小烧杯中用天平称量,加入适量水,然后用玻璃棒搅拌,溶解后将溶液转移到250mL的容量瓶中并洗涤烧杯,将洗涤液倒入容量瓶中,最后用胶头滴管定容。
9.D [酒精与水互溶,不能作为溴的萃取剂,A项错误;
苯的密度比水小,在分液时应从分液漏斗上口倒出,B项错误;
分液漏斗颈没有紧贴烧杯内壁,C项错误;
溴易挥发且有毒,可倒入盛有NaOH溶液的废液缸中使之转化为无毒物质,D项正确。
10.C [根据表中数据判断,当海水密度达到1.21~1.22g·
mL-1时,析出盐的质量越大,则该盐质量分数越大,由表中数据可知析出的NaCl的质量最大,所以析出的盐中,质量分数最大的是NaCl。
11.C [A项,由于2NO2
N2O4的存在,反应后体积小于22.4L;
B项,由于Al3+水解,还有水电离的H+和OH-,因而离子总数大于NA;
C项,标准状况下水是液体,22.4LH2O的物质的量大于1mol,故原子数大于3NA;
D项,由于HCl挥发及溶液浓度变稀不可能完全反应,因而Cl2的分子数小于NA。
12.A [A项,HF为弱酸,浓度越大,则电离程度越小,故若1mol·
L-1HF溶液中H+数目小于2NA,错误;
B项,CO2、N2O的摩尔质量均为44g·
mol-1,故44g混合物的物质的量为1mol,且两者均为三原子分子,故1mol混合物中含3NA个原子,正确;
C项,3H2的摩尔质量为6g·
mol-1,36g3H2的物质的量为
=6mol,而1mol3H2中含4mol中子,故6mol3H2中含24NA个中子,正确;
D项,标况下2.24L氧气的物质的量为0.1mol,而氧气反应后的价态可能为-1价,也可能为-2价,故当0.1mol氧气全部变为-1价时转移0.2NA个电子,当全部变为-2价时转移0.4NA个电子,由于产物中氧元素的价态不明确,故转移的电子数介于0.2NA到0.4NA之间,即可能为0.3NA个,正确。
13.A [A项,过氧化钠和水反应时,氧元素由-1价变为0价,故当生成0.1mol氧气时转移0.2NA个电子;
B项,氨气所处的状态不明确,故其物质的量无法计算;
C项,铁离子为弱碱阳离子,在溶液中会水解,故溶液中的铁离子的个数小于0.02NA;
D项,NO和氧气反应后生成的NO2中存在平衡:
2NO2N2O4,导致分子个数减少,故产物分子个数小于2NA。
14.C [Na2CO3·
10H2O晶体中CO
不发生水解,0.1mol该晶体中阴离子数目为0.1NA,A项错误;
常温常压下,18mL水中所含H+数约为10-7×
0.018×
NA,B项错误;
氦气为单原子分子,标准状况下22.4L氦气为1mol,所含原子数约为NA,C项正确;
组成为C2H6O的有机物可能为CH3CH2OH、CH3OCH3或二者的混合物,23gC2H6O为0.5mol,若为CH3CH2OH,则C—H键数目为2.5NA,若为CH3OCH3,则C—H键数目为3NA,若为二者的混合物,则C—H键数目为2.5NA~3NA,D项错误。
15.C [由图像可知,相同温度下同质量的O2比X气体的压强大,即氧气的物质的量较大,因而X的摩尔质量大,四种气体中只有CO2的相对分子质量比O2大,故C项正确。
16.B [依据方程式信息,NO、NO2、N2O4全部转化为NaNO3和NaNO2,根据氮原子守恒知n(NaOH)=n(N)。
17.
(1)32
(2)0.4mol·
L-1 (3)24 (4)
(5)6.4mol 0.2mol (6)7∶2或4∶5
解析 (6)令空气的物质的量为1mol,反应前,左右两室的体积之比为1∶3,反应前右室的物质的量为3mol,反应后,活塞处于中央,两室体积相等,则两室中气体的物质的量相等,反应后右室气体物质的量为1mol,发生反应2H2+O2
2H2O,设H2、O2的物质的量分别为xmol、ymol,
若氢气过量,则:
x-2y=1,x+y=3,解得x∶y=7∶2,
若氧气过量,则:
y-0.5x=1,x+y=3,解得x∶y=4∶5。
18.
(1)Fe、Cu 过滤
(2)4Fe2++O2+8NH3+10H2O===8NH
+4Fe(OH)3↓
(3)取上层清液少许于试管中,加入酸性高锰酸钾溶液,酸性高锰酸钾溶液的紫色不变(无变化)(或取上层清液少许于试管中,加入K3[Fe(CN)6]溶液不产生蓝色沉淀)
(4)蒸发皿、玻璃棒
(5)①C B D 碱石灰 防止空气中水蒸气进入前面装置中 ②检验氢气的纯度
19.
(1)①500 ②CD
(2)2Cu2++SO
+2Cl-+H2O
2CuCl↓+SO
+2H+
(3)加快乙醇和水的蒸发 防止CuCl在空气中被氧化
(4)C
解析
(1)①实验室没有950mL的容量瓶,应用1000mL容量瓶,因此需要胆矾的质量为m(CuSO4·
5H2O)=1000×
10-3×
2×
250g=500g;
②浓度偏小,根据c=
。
A项,砝码生锈,砝码质量增加,因此所配浓度偏大,错误;
B项,含有少量水,对溶液浓度无影响,错误;
C项,未洗涤烧杯和玻璃棒,造成溶质的质量减少,浓度偏小,正确;
D项,定容时仰视刻度,所配溶液体积偏大,浓度偏小,正确。
(2)根据题目中信息,离子反应方程式为2Cu2++SO
2CuCl↓+2H++SO
(3)乙醇易挥发,水易蒸发,70℃有利于乙醇和水的蒸发,根据信息CuCl在空气中迅速被氧化,真空的目的是防止CuCl被氧化。
(4)A项,HO2由O2生成,O2是氧化剂,则HO2属于还原产物,错误;
B项,HO2是超氧酸,和碱发生中和反应,错误;
C项,HO2是弱酸,应是部分电离,HO2H+O
,正确;
D项,Cu由0价→+1价,因此1molCu参加反应转移1mole-,错误。
20.
(1)89.6
(2)2.4mol·
L-1≥c(NaOH)≥1.2mol·
(3)8KO2+6CO2+2H2O===2K2CO3+4KHCO3+6O2
n(CO2)∶n(H2O)=6∶2 n(H2O)=(9mol÷
6)×
2=3mol
(4)300molCH4完全反应产生H2900mol
设CO2转化率为α,CO转化率为β
300βmol+100αmol=350mol
600βmol+300αmol=900mol-120mol
α=80%
或设CO2转化率为α
900mol-350mol×
2mol-100αmol=120mol
α=80/100=80%
解析
(1)碳酸氢铵分解的化学方程式为NH4HCO3
H2O+NH3↑+CO2↑,从反应的化学方程式可以看出,分解产物经干燥后,所得气体为NH3和CO2,且n(NH3)+n(CO2)=2n(NH4HCO3)=2×
2.00mol=4.00mol,则V(混合气体)=4.00mol×
22.4L·
mol-1=89.6L,即分解产物经干燥后的体积为89.6L。
(2)根据题意要求,2.40molCO2被完全吸收,NaOH也完全反应,则反应的产物可能是Na2CO3(此时NaOH溶液的浓度最大)或NaHCO3(此时NaOH溶液的浓度最小)或Na2CO3和NaHCO3的混合物。
用极值思想分析两个特殊情况:
①CO2+NaOH===NaHCO3,n(NaOH)=n(CO2)=2.40mol,
则c(NaOH)=
=1.20mol·
L-1;
②CO2+2NaOH===Na2CO3+H2O,n(NaOH)=2n(CO2)=4.80mol,则c(NaOH)=
=2.40mol·
综合①、②可知,NaOH溶液的浓度应该为1.20mol·
L-1≤c(NaOH)≤2.40mol·
(3)方法一:
依题意,9molCO2在密封舱内和KO2反应后生成9molO2,即n(C