化学选考30题专练--2108年浙江化学选考复习专题复习.doc
《化学选考30题专练--2108年浙江化学选考复习专题复习.doc》由会员分享,可在线阅读,更多相关《化学选考30题专练--2108年浙江化学选考复习专题复习.doc(6页珍藏版)》请在冰豆网上搜索。
化学选考30题专练
1.【浙江2017年11月30题】Ⅰ.十氢萘是具有高储氢密度的氢能载体,经历“十氢萘(C10H18)→四氢萘(C10H12)→萘(C10H8)”的脱氢过程释放氢气。
已知:
C10H18(l)C10H12(l)+3H2(g)△H1
C10H12(l)C10H8(l)+2H2(g)△H2
△H1>△H2>0;C10H18→C10H12的活化能为Ea1,C10H12→C10H8的活化能为Ea2,十氢萘的常压沸点为192℃;在192℃,液态十氢萘的脱氢反应的平衡转化率约为9%。
请回答:
(1)有利于提高上述反应平衡转化率的条件是_________。
A.高温高压B.低温低压C.高温低压D.低温高压
(2)研究表明,将适量的十氢萘置于恒容密闭反应器中,升高温度带来高压,该条件下也可显著释氢,理由是______________________________________________________。
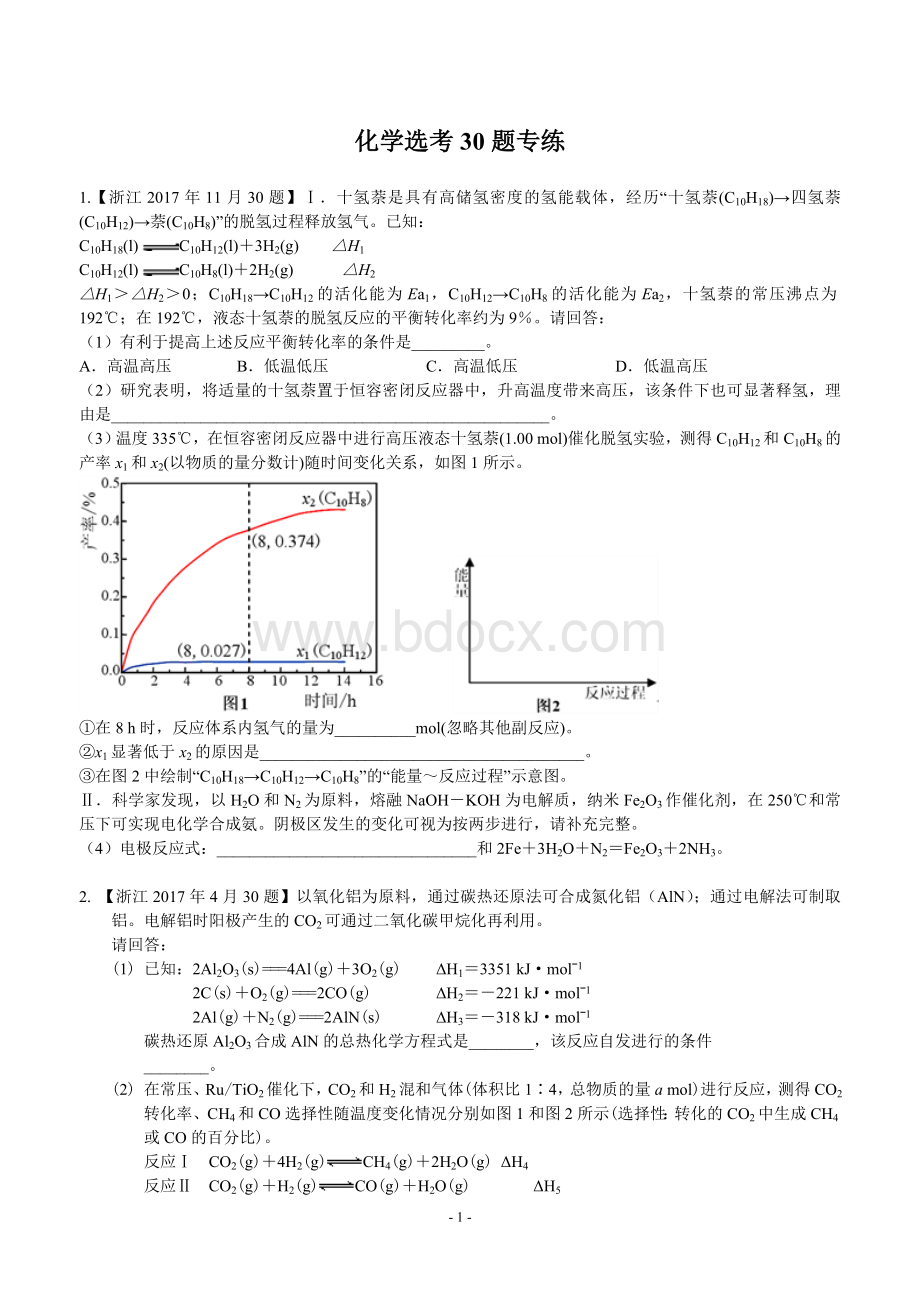
(3)温度335℃,在恒容密闭反应器中进行高压液态十氢萘(1.00mol)催化脱氢实验,测得C10H12和C10H8的产率x1和x2(以物质的量分数计)随时间变化关系,如图1所示。
①在8h时,反应体系内氢气的量为__________mol(忽略其他副反应)。
②x1显著低于x2的原因是________________________________________。
③在图2中绘制“C10H18→C10H12→C10H8”的“能量~反应过程”示意图。
Ⅱ.科学家发现,以H2O和N2为原料,熔融NaOH-KOH为电解质,纳米Fe2O3作催化剂,在250℃和常压下可实现电化学合成氨。
阴极区发生的变化可视为按两步进行,请补充完整。
(4)电极反应式:
________________________________和2Fe+3H2O+N2=Fe2O3+2NH3。
2.【浙江2017年4月30题】以氧化铝为原料,通过碳热还原法可合成氮化铝(AlN);通过电解法可制取铝。
电解铝时阳极产生的CO2可通过二氧化碳甲烷化再利用。
请回答:
(1)已知:
2Al2O3(s)===4Al(g)+3O2(g) ΔH1=3351kJ·molˉ1
2C(s)+O2(g)===2CO(g) ΔH2=-221kJ·molˉ1
2Al(g)+N2(g)===2AlN(s) ΔH3=-318kJ·molˉ1
碳热还原Al2O3合成AlN的总热化学方程式是________,该反应自发进行的条件
________。
(2)在常压、Ru/TiO2催化下,CO2和H2混和气体(体积比1∶4,总物质的量amol)进行反应,测得CO2转化率、CH4和CO选择性随温度变化情况分别如图1和图2所示(选择性:
转化的CO2中生成CH4或CO的百分比)。
反应Ⅰ CO2(g)+4H2(g)CH4(g)+2H2O(g) ΔH4
反应Ⅱ CO2(g)+H2(g)CO(g)+H2O(g) ΔH5
①下列说法不正确的是________
A.ΔH4小于零
B.温度可影响产物的选择性
C.CO2平衡转化率随温度升高先增大后减少
D.其他条件不变,将CO2和H2的初始体积比改变为1∶3,可提高CO2平衡转化率
②350℃时,反应Ⅰ在t1时刻达到平衡,平衡时容器体积为VL,该温度下反应Ⅰ的平衡常数为________(用a、V表示)
③350℃下CH4物质的量随时间的变化曲线如图3所示。
画出400℃下0~t1时刻CH4物质的量随时间的变化曲线。
(3)据文献报道,CO2可以在碱性水溶液中电解生成甲烷,生成甲烷的电极反应式是________。
3.I.
(1)氰化钠是剧毒化学品。
氰化钠泄漏到水体中,可用ClO2处理,生成两种无色无味无毒的气体。
写出用ClO2处理氰化钠废水的离子方程式____________。
(2)中国在甲醇燃料电池技术上获得突破,其装置原理如图甲。
乙池是铝制品表面“钝化”装置,两极分别为铝制品和石墨。
M电极的反应式为:
______________。
II.工业上利用合成气(主要成分为CO、CO2和H2)在催化剂的作用下合成甲醇。
已知298K和101KPa条件下:
2H2(g)+O2(g)=2H2O
(1)△H1=-571.6kJ/mol
CO(g)+l/2O2(g)=CO2(g)△H2=-283.0kJ/mol
CH3OH(l)+3/2O2(g)=CO2(g)+2H2O
(1)△H3=-726.5kJ/mol
(3)则CO(g)+2H2(g)CH3OH
(1)△H=_____kJ/mol
(4)已知:
CH3OH
(1)=CH3OH(g)△H=+35.2kJ/mol;CO(g)+2H2(g)CH3OH(g)平衡常数K随温度变化关系的曲线为30题图2中的_______(填曲线标记字母I或II)。
(5)维持反应温度为510K,以n(H2)/n(CO)=2:
1充入一定量的原料气于1L容器中,在上述条件下充分反应,tl时刻达到平衡,测得容器中c(CH3OH)=2mol/L,则平衡时CO转化率=______;若维持反应温度为520K,其它条件不变,请在30题图3中画出c(CO)在0~tl时刻变化曲线:
_____________。
(6)20世纪90年代,化学家研制出新型催化剂:
碱金属的醇盐及溶剂用于合成甲醇。
30题图4是在该新型催化剂作用下,研究温度、压强对合成甲醇的影响。
由图可知适宜的反应温度、压强为____。
温度A.90~150℃B.200~260℃C.300~360℃D.400~460℃
压强E.0.1~1MPaF.3~5MPaG.8~10MPaH.15~20MPa
4.煤的气化得CO和H2,在催化剂存在条件下进一步合成甲醇(反应I),并同时发生反应II.
I.CO(g)+2H2(g)CH3OH(g)△H1=-81kJ•mol-1
II.CO(g)+H2(g)C(s)+H2O(g)△H2
已知:
①2C(s)+O2(g)=2CO(g)△H3=-221kJ•mol-1
②H2O(g)=H2O
(1)△H4=-44.0kJ•mol-1
③H2的标准燃烧热为285.8kJ•mol-1
④反应过程中催化剂对选择性会产生影响,甲醇选择性是指转化的CO中生成甲醇的百分比。
请回答:
(1)反应II中△H2=______kJ•mol-1
(2)为减弱副反应II的发生,下列采取的措施合理的是_________。
A.反应前加入少量的水蒸气B.增压
C.降低反应温度D.使用合适催化剂,平衡前提高甲醇的选择性
(3)在常压下,CO和H2的起始加入量为10mol、14mol,容器体积为10L.选用Cu/NiO催化剂,升高温度在450℃时测得甲醇的选择性为80%,CO的转化率与温度的关系如图所示,则此温度下反应I的平衡常数K=_______,并说明CO的转化率随温度升高先增大后减小的原因:
____________。
(4)350℃时甲醇的选择性为90%,其他条件不变,画出350℃时甲醇的物质的量随时间的变化曲线。
_________________
(5)甲醇燃料电池由甲醇电极、氧电极和质子交换膜构成,写出负极的电极反应式:
_________。
实验证明CO在酸性介质中可电解产生甲醇,写出阴极的电极反应式:
__________。
5.氯化铵、甲醇、氧化铝都是重要化合物。
(1)已知:
INH4Cl(s)=NH3(g)+HCl(g)△H=+l63.9kJ·mol-1
IIHCl(g)+CH3OH(g)CH3Cl(g)+H2O(g)△H=-31.9kJ·mol-1
IIINH4Cl(s)+CH3OH(g)NH3(g)+CH3Cl(g)+H2O(g)
①反应III在_________条件下能自发反应(填“较高温度”、“较低温度”或“任何温度”),理由是_______________。
[学科@#~网%&]
②图1是反应III使用三种不同催化剂时得到的CH3Cl产率与温度关系的变化图。
己知:
催化剂用量、催化剂粒数、n(甲醇):
n(氯化铵)的值、甲醇进料速度、反应时间等测试条件都相同。
图1中a曲线CH3Cl产率先增大后减小的原因是___________。
请在图2中画出其它条件都相同时,在370℃下使用三种不同催化剂至反应平衡时,CH3Cl的产率与时间关系的变化曲线,并用a、b、c标出对应的曲线。
_______________
(2)25℃时,在某浓度的NH4Cl溶液中滴加一定量的氨水至中性,此时测得溶液中c(Cl-)=0.36mol·L-1,则混合溶液中c(NH3·H2O)=_______mol·L-1。
(25℃时,NH3·H2O的Kb=1.8×10-5)
(3)多孔Al2O3薄膜可作为催化剂载体、模板合成纳米材料等用途。
现以高纯铝片作为阳极,不锈钢作为阴极,一定溶度的磷酸溶液作为电解质进行电解,即可初步制取多孔Al2O3膜。
请写出该制取过程的阳极电极反应:
__________________。
答案:
1.
(1)C;
(2)反应吸热,温度升高,平衡正向移动。
与此同时,温度升高导致十氢萘气化,浓度增大,平衡正向移动,生成氢气量显著增加。
(3)①1.951;②反应2的活化能比反应1小,相同温度下反应2更快,所以相同时间内,生成的四氢萘大部分都转化为萘,故x1显著低于x2.
(4);(5)Fe2O3+6e-+3H2O=2Fe+6OH-。
2.
(1)
Al2O3(s)+3C(s)+N2(g)===2AlN(s)+3CO(g) ΔH=1026kJ·molˉ1
高温
(2)
①CD
②
③
(3)
CO2+6H2O+8eˉ===6CH4+8OHˉ
3.2ClO2+2CN-=2Cl-+N2+2CO22Al-6e-+6HCO3-=Al2O3+6CO2↑+3H2O△H=-128.1kJ/molI97.56%(或97.6%或98%)A、F
4.-131.3AD3.2在150℃至350℃时,测量时,反应I、II未达到平衡,随温度升高,CO转化率增大,350℃后测量时,反应I、II已达到平衡,两反应均放热,平衡逆向移动,CO转化率减小(说明:
平衡时,n=6.3)CH3OH+H2O-6e-=CO2+6H+CO+4H++4e-=CH3OH
5.
(1).较高温度
(2).因为反应Ⅲ的△S>0,△H>0(3).410℃之前,还未达到平衡,温度越高反应速率越快,因此随着温度升高,CH3Cl产率逐渐增大,
410℃之后,随着温度升高,催化剂活性降低,反应速率减小,因此CH3Cl产率逐渐减小。
(4).如图:
(5).2×10-3(6).2Al+3H2O-6e-=Al2O3+6H+
-6-