湖南省长郡中学届高三月考试题附答案二化学试题附答案808919Word文件下载.docx
《湖南省长郡中学届高三月考试题附答案二化学试题附答案808919Word文件下载.docx》由会员分享,可在线阅读,更多相关《湖南省长郡中学届高三月考试题附答案二化学试题附答案808919Word文件下载.docx(12页珍藏版)》请在冰豆网上搜索。
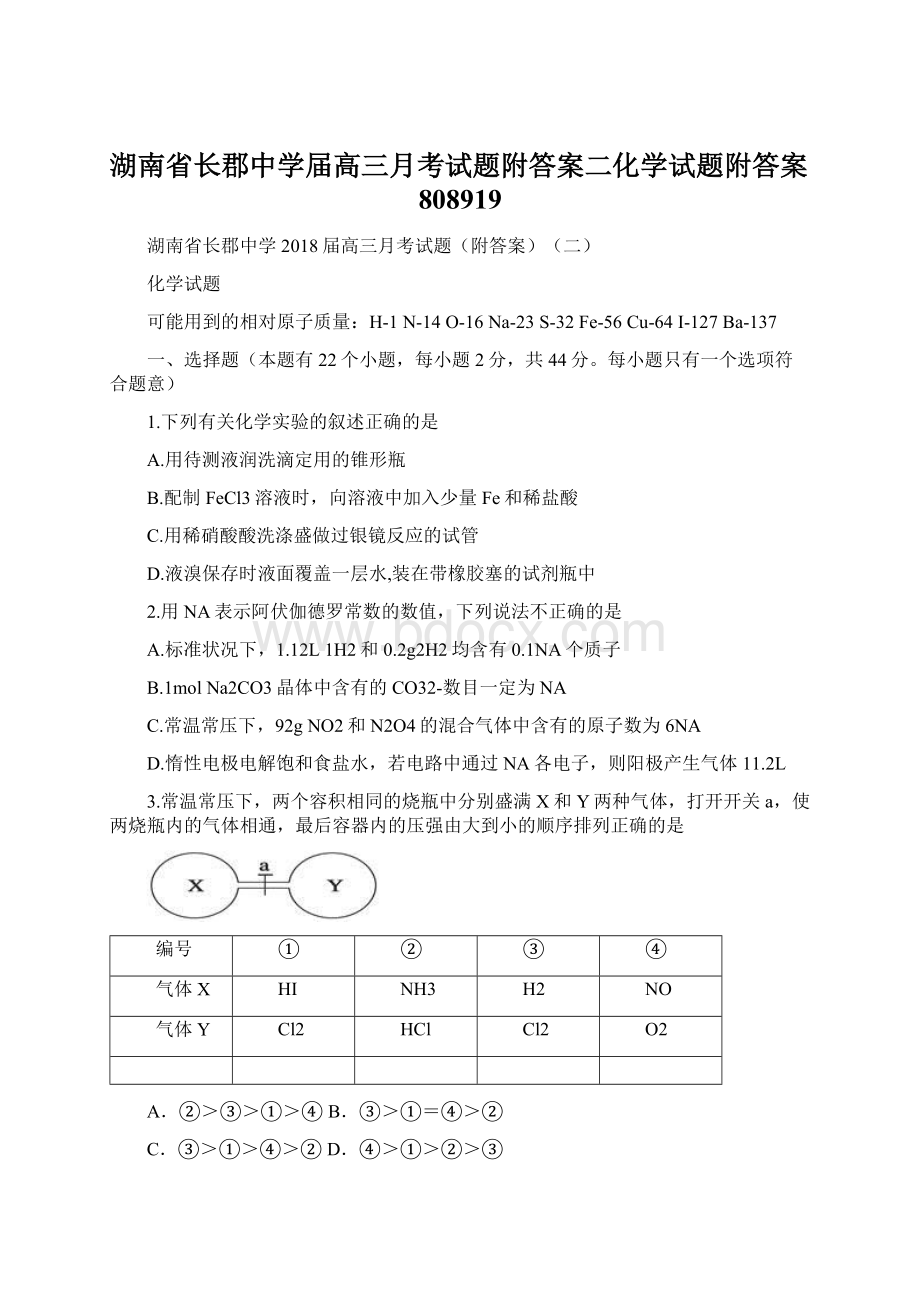
Cl2
HCl
O2
A.②>③>①>④B.③>①=④>②
C.③>①>④>②D.④>①>②>③
4.下列反应的离子方程式正确的是
A.次氯酸钙中通入过量二氧化碳:
Ca2++2C1O-+H2O+CO2=CaCO3↓+2HClO
B.硫酸亚铁溶液中加入过氧化氢溶液:
Fe2++2H2O2+4H+=Fe3+
+4H2O
C.用氨水吸收少量二氧化硫:
NH3·
H2O+SO2=NH4++HSO3-
D.硝酸铁溶液中加过量氨水:
Fe3++3NH3·
H2O=Fe(OH)3↓+3NH4+
5.下列各组离子在指定条件下,一定大量共存的是
A.在c(H+)/c(OH-)=1×
1012的溶液中:
I-、Cl-、HCO3-、Na+
B.pH=1的溶液中:
Cu2+、Al3+、SO42-、NO3-
C.能使碘化钾淀粉试纸变蓝的溶液中:
Na+、NH4+、S2-、Br-
D.水电离出的c(H+)=1×
10-12mol/L的溶液中:
Na+、Mg2+、Cl-、S2-
6.某溶液中只可能含有下列离子中的几种(不考虑溶液中含量较少的H+和OH-):
Na+、NH4+、SO42-、CO32-、NO3-.取200mL该溶液,分为等体积的二份分别做下列实验.实验1:
第一份加入足量的烧碱并加热,产生的气体在标准状况下为224mL.实验2:
第二份先加入足量的盐酸,无现象,再加足量的BaCl2溶液,得固体2.33克.下列说法正确的是
A.该溶液中可能含有Na+
B.该溶液中肯定含有NH4+、SO42-、CO32-、NO3-
C.该溶液中一定不含NO3-
D.该溶液中一定含Na+,且c(Na+)≧0.1mol/L
7.用质量分数为98%的浓硫酸(ρ=1.84g/cm3)配制240mL1.84mol/L稀硫酸,下列操作正确的是
A.将蒸馏水缓慢注入盛有一定量浓硫酸的烧杯中,并不断搅拌至冷却
B.必需的定量仪器有100mL量筒、250mL容量瓶和托盘天平
C.量取浓硫酸的体积为25.0mL
D.先在容量瓶中加入适量水,将量好的浓硫酸注入容量瓶,加水定容
8.具备基本的化学实验技能使进行科学探究的基础和保证。
下列有关实验操作正确的是
9.下列图示实验正确的是
A.除去粗盐溶液中的不溶物B.碳酸氢钠受热分解
C.除去CO气体中的CO2气体D.乙酸乙酯的制备
10.下列实验操作、现象和结论均正确的是
选项
实验操作
实验现象
实验结论
A
向苏打和小苏打溶液中分别加入盐酸
均冒气泡
两者均能与盐酸反应
B
向过量氨水中慢慢滴加少量AgNO3溶液
溶液中无明显现象
Ag+与NH3H2O能大量共存
C
将高度可调的铜丝伸入到稀HNO3中
溶液变蓝
Cu与稀HNO3发生置换反应
D
将KI和FeCl3溶液在试管中混合后,加入CCl4,震荡,静置
下层溶液显紫红色
氧化性:
Fe3+>
I2
11.有关下列各装置图的叙述,不正确的是
A.装置①可用于吸收实验中多余的Cl2
B.装置②可用于收集H2、NH3、Cl2、HCl、NO2等
C.装置③中X为苯,可用于吸收氨气或氯化氢
D.装置④可用于收集氨气,并吸收多余的氨气
12.利用下列表格中的实验器材和试剂能够完成相应实验的一组是
实验器材和试剂
相应实验
洗气甁(两只)、饱和Na2CO3溶液、浓硫酸、导管、橡皮管
出去CO2中的HCl和水蒸汽
滴定台(附滴定夹)、滴定管(酸式、碱式)、烧杯、胶头滴管、已知浓度的盐酸、未知浓度的NaOH溶液
中和滴定实验
烧杯、酒精灯、火柴、胶头滴管、蒸馏水、FeCl3饱和溶液、三脚架
制备Fe(OH)3胶体
铂丝或铁丝,蓝色钴玻璃、酒精灯、火柴、盐酸、待测液
焰色反应实验
13.为提纯下列物质(括号内的物质是杂质),所选用的除杂试剂盒分离方法都正确的是
被提纯的物质
除杂试剂
分离方法
溴化钠溶液(NaI)
溴水
蒸馏
氯化铵溶液(FeCl3)
氢氧化钠溶液
过滤
乙酸乙酯(CH3COOH)
乙醇、浓硫酸
加热蒸馏
二氧化碳(CO)
氧化铜粉末
通过灼热的CuO粉末
14.可用如图所示装置制取、净化、收集的气体是
A.铜与稀硝酸反应制一氧化氮B.亚硫酸钠固体与硫酸反应制二氧化硫
C.锌和稀硫酸反应制氢气D.浓氨水和生石灰制取氨气
15.已知CuS和Cu2S都能溶于硝酸且它们在高温下灼烧的产物相同,为区别这两种黑色粉末,某同学设计了如下几种实验方案,其中合理的是
A.将两种样品分别溶于硝酸,根据所产生的气体差异进行区别
B.将两种样品分别溶于硝酸,根据所溶液的颜色差异进行区别
C.取两种同质量的样品分别在高温灼烧,区别残留固体的质量
D.取两种同质量的样品分别在高温灼烧,区别残留固体的颜色
16.某溶液中可能含有H+、NH4+、Mg2+、Al3+、Fe3+、CO32-、SO42-、NO3-中的几种.①若加入锌粒,产生无色无味的气体;
②若加入NaOH溶液,产生白色沉淀,且产生的沉淀量与加入NaOH的物质的量之间的关系如图所示.则下列说法正确的是
A.溶液中的阳离子只有H+、Mg2+、Al3+
B.溶液中一定不含CO32-,可能含有SO42-和NO3-
C.溶液中n(NH4+)=0.2mol
D.三种离子的物质的量之比为n(H+):
n(Al3+):
n(Mg2+)=1:
1:
1
17.某稀硫酸和稀硝酸的混合溶液200mL,平均分成两份。
向其中一份中逐渐加入铜粉,最多能溶解9.6g。
向另一份中逐渐加入铁粉,产生气体的量随铁粉质量增加的变化如图所示(已知硝酸只被还原为NO气体)。
下列分析或结果错误的是
A.原混合酸中NO3-物质的量为0.1
mol
B.OA段产生的是NO,AB段的反应为Fe+2Fe3+=3Fe2+,BC段产生氢气
C.第二份溶液中最终溶质为FeSO4
D.H2SO4浓度为2.5
mol·
L-1
18.某溶液这含有下列六种离子:
①HCO3-;
②SO32-;
③Na+;
④CO32-;
⑤NH4+;
⑥NO3-。
向其中加入一定量Na2O2后,溶液中离子浓度基本保持不变的是
A.①②④⑤B.④⑥C.③④⑥D.只有⑥
19.下列各组物质相互混合反应后,最终有白色沉淀生成的是
①金属钠投入到FeCl3溶液中②过量NaOH溶液和明矾溶液混合③少量Ca(OH)2投入过量NaHCO3溶液中④向NaAlO2溶液中滴入NaHCO3溶液⑤向饱和Na2CO3溶液中通入足量CO2⑥氯化钙溶液中通入少量的CO2
A.①③④⑤B.只有①④C.只有②③⑥D.只有③④⑤
20.海水中主要含有Na+、K+、Mg2+、Ca2+、Cl-、Br-、SO42-、HCO3-、CO32-等离子,火力发电时排放的烟气可用海水脱硫,其工艺流程如下图所示:
下列说法错误的是
A.海水pH约为8的原因主要是天然海水含HCO3-、CO32-
B.吸收塔中发生的反应有SO2+H2O
H2SO3
C.氧化主要是氧气将HSO3-、SO32-、H2SO3氧化为SO42-
D.经稀释“排放”出的废水中,浓度与海水相同
21.有某硫酸和硝酸的混合溶液20mL,其中含有硫酸的浓度为2mol·
L-1,含硝酸的浓度为1mol·
L-1,现向其中加入0.96g铜粉,充分反应后(假设只生成NO气体),最多可收集到标准状况下的气体的体积为
A.89.6mL
B.112mL
C.168mL
D.224mL
22.如图,利用培养皿探究SO2的性质,实验时向Na2SO3固体上滴几滴浓硫酸,立即用另一表面扣在上面。
表中对实验现象的描述或解释不正确的是
解释
BaCl2溶液变浑浊
SO2与BaCl2溶液反应产生了BaSO3沉淀
Na2S溶液变浑浊
SO2与Na2S溶液反应产生了S单质
酸性KMnO4溶液褪色
SO2具有还原性
品红溶液褪色
SO2具有漂白性
二、非选择题(本题包括4个小题,共56分)
23.(12分)下图中A-J分别代表相关反应的一种物质。
已知A分解得到等物质的量的B、C、D,图中有部分生成物未标出。
请填写以下空白:
(1)A的化学式为,B的电子式为。
(2)写出下列反应②的化学方程式:
。
(3)写出反应③的离子方程式:
(4)写出J与F反应的化学方程式:
(5)在反应④中,当生成标准状况下2.24LG时,转移电子的物质的量为mol。
24.(16分)某研究所对含硫酸亚铁和硫酸铜的工业废料进行相关的研究。
实验过程如下:
回答下列问题:
(1)滤渣的成分为
,操作①的名称为
。
(2)上图溶液B中所发生反应的离子方程式为
(3)实验要求向溶液B中通入过量的空气,证明通入空气过量的方法是
(4)操作③第一步需要的仪器除了酒精灯、铁架台外,还需要
(5)某同学利用下面装置制备氢气并利用氢气还原某金属氧化物,根据要求回答问题。
①请设计一个实验方案验证H2的还原性并检验其氧化产物,其装置连接顺序是A→_____→_____→_____→D(除D装置外,其它装置不能重复使用),最后D装置中所加药品为____________,其作用是。
②点燃B处酒精灯之前必须进行的操作是____________________。
25.(13分)某课外小组的同学拟用下图所示的装置从含碘废液(除H2O外,还有I2、I-等)中回收碘。
回答下列问题:
(1)装置A中发生反应的离子方程式为。
(2)仪器X的名称为;
装置D的作用是。
(3)装置C中球形冷凝管冷却水从(填“a”或“b”)进入,反应控制在较低温度下且保持溶液pH=2进行,其主要原因是。
(4)三口烧瓶中液体经过滤得粗碘,粗碘可经(填操作名称)得到纯碘。
(5)为测定某含碘废水中I2的含量,取样l00mL,调节溶液pH后,滴加2滴淀粉溶液,然后用0.02500mol/LNa2S2O3标准溶液滴定,消耗标准液18.15mL。
则滴定终点时的现象为,含碘废水中I2的含量=mg/mL(结果保留小数点后三位,已知:
I2+2S2O32-=2I-+S4O62-)。
26.(15分)芳香族化合物A是一种基本化工原料,可以从煤和石油中得到。
OPA是一种重要的有机化工中间体。
A、B、C、D、E、F和OPA的转化关系如下所示:
(1)A的化学名称是
;
(2)由A生成B
的反应类型是
在该反应的副产物中,与B互为同分异构体的化合物的结构简式为
(3)写出C所有可能的结构简式
(4)D(邻苯二甲酸二乙酯)是一种增塑剂。
请用A、不超过两个碳的有机物及合适的无机试剂为原料,经两步反应合成D。
用化学方程式表示合成路线
(5)OPA的化学名称是
,OPA经中间体E可合成一种聚酯类高分子化合物F,由E合成F的反应类型为
,该反应的化学方程式为
(提示
)
(6)芳香化合物G是E的同分异构体,G分子中含有醛基、酯基和醚基三种含氧官能团,写出G所有可能的结构简式
参考答案
1-5CDCDB6-10DCCDA11-15CDDBC16-20CADDD21-22DA
二、非选择题(本题包括4镉小题,共56分)
23.(每空2分,共12分)
(1)NH4HCO3
(2)4NH3+5O2
4NO+6H2O
(3)NH4++HCO3-+2OH-
NH3↑+CO32-+2H2O
(4)C+HNO3(浓)
CO2↑+4NO2↑+2H2O
(5)0.2
24.(16分)
(1)Fe、Cu;
(2分)过滤(1分)
(2)4Fe2++O2+8NH3+10H2O=8NH4++4Fe(OH)3↓(2分)
(3)取上层清液少许于试管中,加入酸性高锰酸钾溶液,酸性高锰酸钾溶液的紫色不变(无变化)(或取上层清液少许试管中,加入K3[Fe(CN)6]溶液不产生蓝色沉淀(2分)
(4)蒸发皿、玻璃棒
(2分)
(5)①C—B—D;
(共2分)碱石灰;
(1分)防止空气中水蒸气进入前面装置中(2分)②检验氢气的纯度(2分)
25.(13分)
(1)MnO2+4H++2Cl-
Mn2++Cl2↑+2H2O(2分)
(2)圆底烧瓶(1分)
吸收来反应的Cl2,防止污染空气
(2分)
(3)a
(1分)
使氯气在溶液这有较大的溶解度或减少I2的挥发
(4)升华
(1分)
(5)当最后一滴Na2S2O3标准溶液滴入时,溶液由蓝色褪为无色,且半分钟内不变色。
(2分)0.576(2分)
26.(15分)
(1)邻二甲苯(1分)
(2)取代反应(1分)
(1分)
(3)
(4)
(其它合理答案也可)(2分)
(5)邻苯二甲醛(1分)
缩聚反应(1分)
(6)
(4分)