高中化学专题1微观结构与物质的多样性第一单元原子核外电子排布与元素周期律第2课时元素周期律学案苏教Word格式.docx
《高中化学专题1微观结构与物质的多样性第一单元原子核外电子排布与元素周期律第2课时元素周期律学案苏教Word格式.docx》由会员分享,可在线阅读,更多相关《高中化学专题1微观结构与物质的多样性第一单元原子核外电子排布与元素周期律第2课时元素周期律学案苏教Word格式.docx(16页珍藏版)》请在冰豆网上搜索。
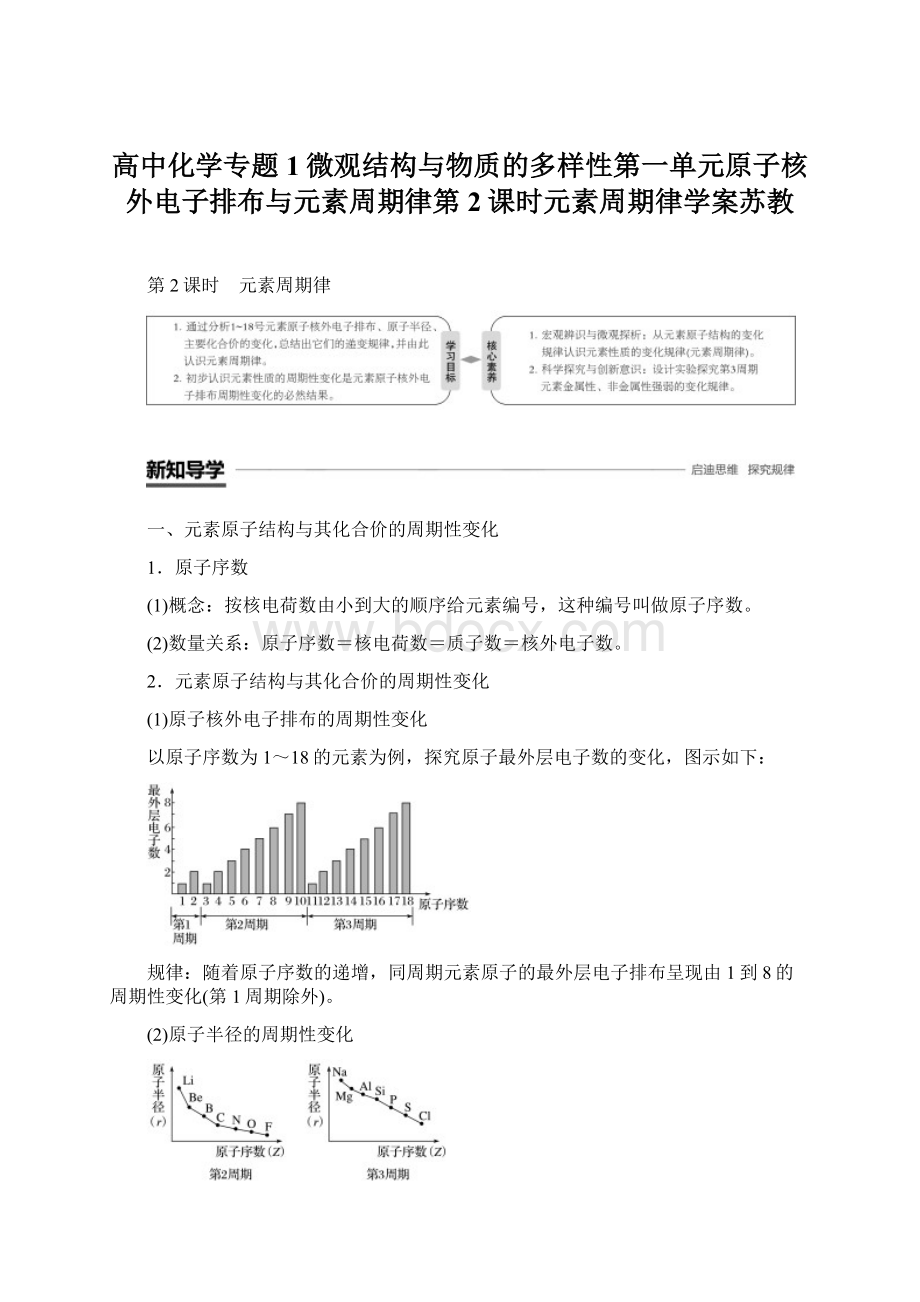
K+<
Cl-,C正确;
离子电子层越多,离子半径越大,则离子半径大小为Ba2+>
Ca2+>
Mg2+,D错误。
思维启迪
具有相同电子层结构的离子应注意:
(1)所对应的元素在元素周期表中的位置关系是:
阴上阳下,如A+、B2+、C-、D2-,在周期表中的相对位置是:
。
(2)离子半径关系是:
序小径大,如:
上面四离子半径:
D2->
C->
A+>
B2+。
二、元素金属性、非金属性的变化规律
1.钠、镁、铝金属性强弱比较
(1)实验①中,钠熔成小球,浮于水面,四处游动,有“嘶嘶”的响声,反应后溶液加酚酞变红。
该实验说明钠与冷水反应剧烈,反应的化学方程式为
2Na+2H2O===2NaOH+H2↑。
(2)实验②中,加热前,镁条表面附着了少量无色气泡,加热至沸腾后,有较多的无色气泡冒出,滴加酚酞溶液变为粉红色。
该实验说明镁与冷水几乎不反应,能与热水反应,反应的化学方程式为
Mg+2H2O
Mg(OH)2+H2↑。
(3)实验③和④中的两支试管内都有无色气泡产生,但实验③中试管放出气体的速率较快。
反应的化学方程式为
Mg+2HCl===MgCl2+H2↑;
2Al+6HCl===2AlCl3+3H2↑。
(4)结论:
钠、镁、铝置换出水(或酸)中的氢时,由易到难的顺序为Na>
Mg>
Al。
钠、镁、铝的最高价氧化物对应的水化物的碱性由强到弱的顺序为NaOH>
Mg(OH)2>
Al(OH)3。
钠、镁、铝的金属性由强到弱的顺序为Na>
2.Si、P、S、Cl的非金属性的递变规律
Si
P
S
Cl
判断依据
与氢气反应
高温
磷蒸气与氢气能反应
加热
光照或点燃
由难到易的顺序为Si、P、S、Cl
最高价氧化物对应的水化物的酸性
H2SiO3:
弱酸
H3PO4:
中强酸
H2SO4:
强酸
HClO4:
酸性:
HClO4>
H2SO4>
H3PO4>
H2SiO3
结论
Si、P、S、Cl的非金属性逐渐增强
3.11~17号元素性质递变规律
从左到右,元素的金属性逐渐减弱,非金属性逐渐增强。
(1)同周期元素性质的变化与原子结构的关系
核外电子层数相同,随着原子序数(核电荷数)的递增,原子核对核外电子的引力逐渐增强,原子半径逐渐减小,元素原子的得电子能力逐渐增强,失电子能力逐渐减弱,最终导致元素的非金属性逐渐增强,金属性逐渐减弱。
(2)元素周期律
①元素周期律是指元素的性质随着原子序数的递增而呈现周期性的变化。
②元素的性质包括:
原子半径、主要化合价、金属性、非金属性等。
③元素周期律实质是元素原子核外电子排布发生周期性变化的必然结果。
例3
下列关于元素周期律的叙述中不正确的是( )
A.Na、Mg、Al最外层电子数依次增多,其单核离子的氧化性依次增强
B.P、S、Cl最高正化合价依次升高,对应简单气态氢化物的稳定性依次增强
C.电子层数相同的元素的原子半径以第ⅦA族的为最大
D.Na、Mg、Al的氢氧化物的碱性依次减弱
考点 元素金属性与非金属性的周期性变化
题点 11~17号元素性质的变化规律
解析 Na、Mg、Al原子的最外层电子数依次为1、2、3,其原子的还原性依次减弱,但离子的氧化性依次增强;
P、S、Cl的最高正化合价分别为+5、+6、+7,由于P、S、Cl的非金属性依次增强,其所对应的气态氢化物的稳定性也依次增强;
除稀有气体元素外,同周期元素从左到右其原子半径逐渐减小;
因Na、Mg、Al的金属性依次减弱,则它们的氢氧化物的碱性也依次减弱。
例4
下列有关性质的比较,不能用元素周期律解释的是( )
A.酸性:
H3PO4
B.非金属性:
Cl>
Br
C.碱性:
NaOH>
Mg(OH)2
D.热稳定性:
Na2CO3>
NaHCO3
题点 元素金属性、非金属性强弱的综合
答案 D
解析 在元素周期表中S与P属于同周期元素,S在P的右边,非金属性强于P,所以最高价氧化物对应的水化物的酸性H2SO4强于H3PO4,A项不合题意;
在元素周期表中Cl与Br属于同主族元素,Cl在Br的上方,非金属性Cl强于Br,B项不合题意;
在元素周期表中,Na与Mg属同周期元素,Na在Mg的左边,所以金属性Na强于Mg,最高价氧化物对应的水化物碱性NaOH强于Mg(OH)2,C项不合题意;
D项考查碳酸盐与碳酸酸式盐热稳定性的问题,不涉及元素周期律的相关知识。
1.下图表示1~18号元素原子结构或性质随核电荷数递增的变化。
该图中纵坐标表示( )
A.电子层数B.最外层电子数
C.最高化合价D.原子半径
2.下列各组元素的性质递变规律错误的是( )
A.N、O、F原子最外层电子数依次增加
B.N、O、F原子半径依次增大
C.Na、Mg、Al元素最高正化合价依次升高
D.Li、Na、K的金属性依次增强
考点 元素金属性、非金属性的周期性变化
题点 元素金属性、非金属性变化规律的判断
解析 N、O、F原子最外层电子数依次为5、6、7,逐渐增多,A项正确;
N、O、F是同周期元素,同周期元素从左到右原子半径依次减小,B项错误;
Na、Mg、Al元素最高正化合价依次为+1、+2、+3,依次升高,C项正确;
Li、Na、K是同主族元素,同主族从上到下元素的金属性依次增强,D项正确。
3.下列结论正确的是( )
①粒子半径:
K+>
Al3+>
S2->
Cl- ②氢化物的稳定性:
HF>
HCl>
H2S>
PH3>
SiH4 ③离子的还原性:
Cl->
Br->
I- ④氧化性:
Cl2>
S>
Se>
Te ⑤酸性:
H2CO3>
HClO ⑥非金属性:
N>
P>
Si ⑦金属性:
Be<
Mg<
Ca<
K
A.②⑤⑦B.②⑥⑦
C.②④⑤⑥⑦D.②④⑥
题点 元素金属性、非金属性的变化规律比较
解析 ①粒子半径:
Al3+;
③还原性:
I->
Cl-。
4.(2018·
苏州月考)原子序数小于20的X元素能形成H2X和XO2两种化合物,该元素的原子序数是( )
A.13B.14C.15D.16
解析 X元素在H2X中呈-2价,在XO2中呈+4价,一般在氢化物中呈现最低负价,故最高正价为+6价,只有原子序数为16时符合要求。
5.(2018·
商丘一中下学期段考)把与下列元素有关性质相符的曲线标号填入相应空格中:
(1)第ⅡA族元素的价电子数________。
(2)第3周期元素的最高化合价________。
(3)碱金属单质熔点________。
(4)第3周期离子Na+、Mg2+、Al3+、P3-、S2-、Cl-的离子半径________。
(5)第2、3周期元素随原子序数递增原子半径的变化________。
题点 元素性质的相关综合
答案
(1)B
(2)C (3)A (4)E (5)G
解析
(1)同一主族元素价电子数相等,与原子序数无关,第ⅡA族元素价电子数都是2,图像B符合。
(2)第3周期元素的最高正化合价随着原子序数增大而增大,稀有气体除外,所以化合价从+1价升高到+7,稀有气体为0价,图像C符合。
(3)第ⅠA族金属元素单质的熔点与其原子半径成反比,所以碱金属单质的熔点随着原子序数增大而减小,图像A符合。
(4)电子层数越多,离子半径越大,电子层结构相同的离子其离子半径随着原子序数增大而减小,则Na+、Mg2+、Al3+的离子半径依次减小,P3-、S2-、Cl-的离子半径依次减小,阴离子半径大于阳离子半径,图像E符合。
(5)第2、3周期元素,电子层数越大其原子半径越大,同一周期元素,原子半径随着原子序数增大而减小,图像G符合。
[对点训练]
题组一 元素原子结构的周期性变化
1.下列说法中正确的是( )
A.元素性质的周期性变化是指原子半径、元素的主要化合价及金属性和非金属性的周期性变化
B.元素的最高正化合价等于元素原子核外电子数
C.从Li→F,Na→Cl,元素的最高化合价均呈现从+1价→+7价的变化
D.电子层数相同的原子核外电子排布,其最外层电子数均从1个到8个呈现周期性变化
答案 A
解析 O无最高正价,F无正价,B、C错误;
H、He的最外层电子数从1到2,D错误。
2.已知下列原子的半径:
原子
N
O
半径r/10-10m
0.75
1.02
0.74
1.17
根据以上数据,P原子的半径可能是( )
A.1.10×
10-10mB.0.80×
10-10m
C.1.20×
10-10mD.0.70×
题点 原子半径的大小判断
解析 根据元素周期律可知,磷原子的半径应在Si和S原子之间,故答案为选项A。
题组二 元素金属性、非金属性的周期性变化
3.对于随原子序数依次增大的11~17号元素,下列说法中不正确的是( )
A.原子半径逐渐减小
B.电子层数逐渐增多
C.最高正化合价逐渐增大
D.元素的非金属性逐渐增强
解析 在元素周期表中同一周期的元素从左到右原子半径依次减小,故A不符合题意;
在元素周期表中同一周期的元素电子层数相同,故B符合题意;
在元素周期表中同一周期的元素从左到右,元素的非金属性逐渐增强,故D不符合题意。
4.A、B两元素原子电子层数相同,如果A原子半径比B的大,则下列判断正确的是( )
A.两元素形成的最高价氧化物对应的水化物的酸性应是A强于B
B.A的气态氢化物比B的气态氢化物稳定
C.A的金属性比B的金属性强
D.A的阴离子比B的阴离子还原性弱
题点 元素金属性、非金属性变化规律判断
解析 A、B两元素位于同周期,A的原子半径比B的大,则A位于B的左边,A元素的金属性比B的强。
5.下列递变规律不正确的是( )
A.HClO4、H2SO4、H3PO4的酸性依次增强
B.钠、镁、铝的还原性依次减弱
C.HCl、H2S、PH3的稳定性依次减弱
D.P、S、Cl三种元素的最高正化合价依次升高
题点 同周期元素金属性、非金属性变化规律比较
解析 非金属性:
P,元素的非金属性越强,最高价氧化物对应的水化物的酸性越强,则HClO4、H2SO4、H3PO4的酸性依次减弱,故A项错误;
金属性:
Na>
Al,元素的金属性越强,对应的单质的还原性越强,则钠、镁、铝的还原性依次减弱,故B项正确;
非金属性:
P,元素的非金属性越强,对应的氢化物越稳定,故C项正确;
P、S、Cl三种元素原子的最外层电子数分别为5、6、7,最高正化合价分别为+5、+6、+7,故D项正确。
题组三 元素周期律
6.元素的以下性质,随着原子序数递增不呈现周期性变化的是( )
A.化合价
B.原子半径
C.元素的金属性和非金属性
D.相对原子质量
题点 元素周期律的内容和实质
解析 由元素周期律的内容知,元素的化合价、原子半径及金属性和非金属性都随着原子序数的递增呈现周期性变化,而相对原子质量随原子序数的递增呈现增大的变化趋势,绝不会出现周期性的变化。
7.(2018·
抚州市临川区3月月考)下列关于物质性质变化的比较,不正确的是( )
A.离子半径大小:
O2->
Na+
B.气态氢化物稳定性:
HBr<
HCl<
HF
C.碱性强弱:
KOH>
LiOH
D.还原性强弱:
F->
I-
题点 元素性质的比较
解析 核外电子排布相同的离子,核电荷数越大,离子半径越小,所以O2->
Na+,电子层数多的离子,半径越大,因此离子半径大小为S2->
Na+,A正确;
F>
Br,气态氢化物的稳定性为HBr<
HF,B正确;
K>
Li,对应最高价氧化物的水化物的碱性为KOH>
LiOH,C正确;
Br>
I,对应离子的还原性为F-<
Cl-<
Br-<
I-,D错误。
8.(2017·
淄博高一检测)下列微粒半径大小比较正确的是( )
A.Na+<
Mg2+<
Al3+<
O2-
B.Na+>
Cl-
C.Na<
Al<
D.Na<
K<
Rb<
Cs
题点 微粒半径的大小比较
解析 4种离子核外电子数相同,随着核电荷数增多,离子半径依次减小,即Al3+<
Na+<
O2-,A项错误;
因S2-、Cl-比Na+、Al3+多一个电子层,则S2-、Cl-半径比Na+、Al3+大,而S2-、Cl-和Na+、Al3+也分别适用“序小径大”的原则,则S2->
Na+>
Al3+,B项错误;
Na、Mg、Al、S的原子半径依次减小,C项错误;
Na、K、Rb、Cs最外层电子数相同,电子层数依次增多,半径依次增大,D项正确。
9.已知原子序数均小于18的四种元素的离子aA2+、bB+、cC2-、dD-都具有相同的电子层结构,则下列叙述正确的是( )
A.原子半径:
A>
B>
D>
C
B.原子的最外层电子数目:
C.原子序数:
d>
c>
b>
a
D.离子半径:
C2->
D->
B+>
A2+
题点 具有相同电子层结构的微粒的判断与比较
解析 A、B、C、D在元素周期表中的位置为
所以原子序数:
a>
c;
原子半径:
C>
D;
离子半径:
A2+<
B+<
D-<
C2-;
原子的最外层电子数目:
B。
10.X、Y、Z、M、Q、R皆为前20号元素,其原子半径与化合价的关系如图所示。
下列说法错误的是( )
A.Q的原子结构示意图为
B.X、Y、Z三种元素组成的化合物可能是盐或碱
C.简单离子半径:
M->
Q+>
R2+
D.Z与M的最高价氧化物对应水化物均为强酸
题点 根据原子半径、化合价推断元素
解析 由图推断Y为氧元素;
X的原子半径小且只有+1价,X为氢元素;
M的最高正价是+7价,最低负价是-1价,为氯元素;
Z的原子半径比氯元素小,最低负价是-3价,最高正价是+5价,则为氮元素;
Q只有+1价,原子半径大于氯原子,但小于只有+2价的R,故Q代表钠元素、R代表钙元素。
X、Y、Z三种元素分别代表H、O、N,可以形成硝酸、硝酸铵及NH3·
H2O,B项正确;
Na+,C项错误;
HClO4、HNO3都是强酸,D项正确。
11.某元素X最高价含氧酸的化学式为HnXO2n-2,则在其气态氢化物中X元素的化合价为( )
A.5n-2B.3n-12
C.3n-6D.n-10
题点 化学式与元素化合价的关系
12.原子序数11~17的X、Y、Z三种元素,已知其最高价氧化物对应的水化物的酸性强弱顺序是:
HXO4>
H2YO4>
H3ZO4,则下列判断中正确的是( )
X>
Y>
Z
B.单质的非金属性:
C.气态氢化物稳定性:
X<
Y<
D.原子序数:
题点 运用元素周期律进行相关推断
[综合强化]
13.在11~17号元素中,除稀有气体元素外:
(1)原子半径最小的元素是________(填元素符号)。
(2)金属性最强的元素是________(填元素符号)。
(3)最高价氧化物对应水化物酸性最强的是________(用化学式回答,下同)。
(4)最不稳定的气态氢化物是________。
(5)最高价氧化物对应水化物碱性最强的是________。
(6)氧化物中具有两性的是________。
答案
(1)Cl
(2)Na (3)HClO4 (4)SiH4(5)NaOH (6)Al2O3
解析
(1)第3周期元素从左到右原子半径逐渐减小,原子半径最小的是Cl。
(2)金属性最强的元素在最左边,应为Na。
(3)非金属性最强的元素,其最高价氧化物对应水化物的酸性最强,氯的非金属性最强,其对应的酸是HClO4。
(4)非金属性最弱的元素Si的气态氢化物最不稳定。
(5)金属性最强的Na对应的NaOH的碱性最强。
(6)铝的氧化物Al2O3具有两性。
14.某学生为比较镁、铝的金属性强弱,设计了如下实验:
(1)向两支试管中分别加入3mL同浓度的稀盐酸,再将两块大小相同且纯净的镁片和铝片分别加入试管中,反应过程中观察到如图所示的现象,则试管b内加入的金属为______________________(写化学式)。
(2)若加入的两块金属的物质的量相等,且试管中稀盐酸足量,充分反应后,气球状态也如上图所示,则试管b中反应的离子方程式为________________________________。
(3)分析判断,实验________[填“
(1)”或“
(2)”]能证明镁的金属性强于铝。
题点 元素金属性和非金属性周期性变化的实验探究
答案
(1)Al
(2)Mg+2H+===Mg2++H2↑ (3)
(1)
解析 (3)大小相同的镁片、铝片分别与相同浓度的盐酸反应时,二者反应的剧烈程度不同,可说明镁、铝金属性的强弱不同,但产生气体的多少不能说明镁、铝金属性的强弱,如实验
(2)。
15.有A、B、C、D、E五种元素,它们的原子序数按E、C、D、A、B依次增大,E原子最外层有4个电子;
A-与B+的核外电子排布相同;
D的气态氢化物的化学式为H2D,最高价氧化物中D的质量分数为40%,且D原子核内质子数和中子数相等;
C的原子序数比D少9,比B少12。
(1)写出五种元素的符号:
A__________,B__________,
C__________,D__________,E__________。
(2)画出A-、B+的结构示意图:
______________________________________________、
________________________。
(3)A、D最高价氧化物对应的水化物化学式分别为________、________。
(4)写出E的最高价氧化物与过量B的最高价氧化物对应的水化物反应的离子方程式:
________________________________________________________________________
________________________________________________________________________。
(5)写出B、C最高价氧化物对应的水化物之间相互反应的化学方程式:
题点 元素推断的相关综合
答案
(1)Cl K N S C
(2)
(3)HClO4 H2SO4 (4)CO2+2OH-===CO
+H2O
(5)KOH+HNO3===KNO3+H2O
解析 D的最高价氧化物分子式为DO3,D的质量分数为40%,可推出D的相对原子质量为32,从而推出D为S元素;
C原子序数比D少9,比B少12,则C为N元素,B为K元素;
A-与B+核外电子排布相同,则A为Cl元素;
E原子最外层有4个电子,且原子序数按E、C、D、A、B依次增大,则E为C元素。
予少家汉东,汉东僻陋无学者,吾家又贫无藏书。
州南有大姓李氏者,其于尧辅颇好学。
予为儿童时,多游其家,见有弊筐贮故书在壁间,发而视之,得唐《昌黎先生文集》六卷,脱落颠倒无次序,因乞李氏以归。
读之,见其言深厚而雄博,然予犹少,未能悉究其义.徒见其浩然无涯,若可爱。
是时天下学者杨、刘之作,号为时文,能者取科第,擅名声,以夸荣当世,未尝有道韩文者。
予亦方举进士,以礼部诗赋为事。
年十有七试于州,为有司所黜。
因取所藏韩氏之文复阅之,则喟然叹曰:
学者当至于是而止尔!
因怪时人之不道,而顾己亦未暇学,徒时时独念于予心,以谓方从进士干禄以养亲,苟得禄矣,当尽力于斯文,以偿其素志。