高考化学一轮复习讲义第九章有机化合物 第31讲Word文档格式.docx
《高考化学一轮复习讲义第九章有机化合物 第31讲Word文档格式.docx》由会员分享,可在线阅读,更多相关《高考化学一轮复习讲义第九章有机化合物 第31讲Word文档格式.docx(22页珍藏版)》请在冰豆网上搜索。
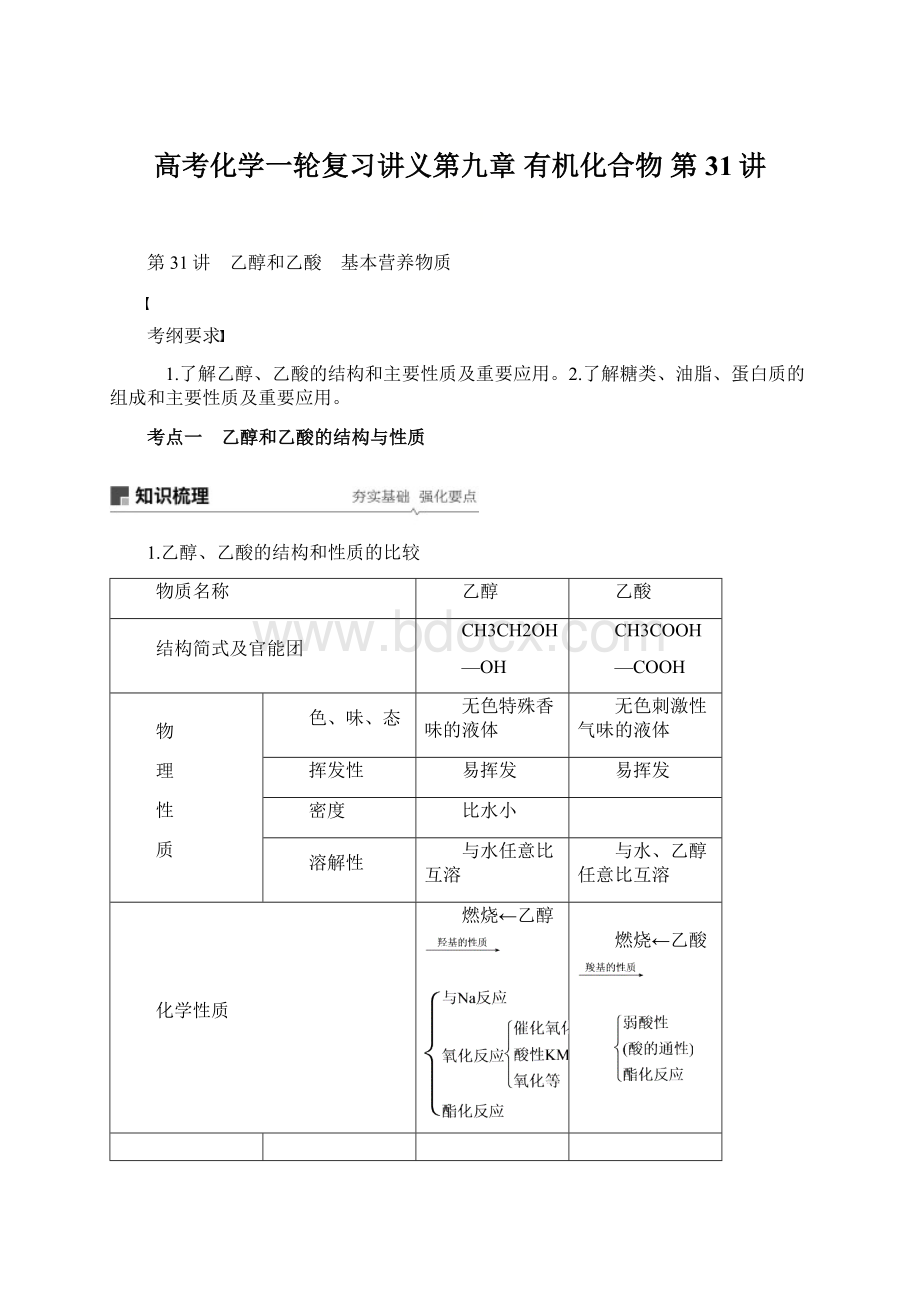
无色刺激性气味的液体
挥发性
易挥发
密度
比水小
溶解性
与水任意比互溶
与水、乙醇任意比互溶
化学性质
燃烧←乙醇
燃烧←乙酸
2.乙酸乙酯的制取
(1)实验原理
+H2O。
(2)实验装置
(3)反应特点
(4)反应条件及其意义
①加热,主要目的是提高反应速率,其次是使生成的乙酸乙酯挥发而收集,使平衡向正反应方向移动,提高乙醇、乙酸的转化率。
②浓硫酸的作用:
作催化剂,提高反应速率;
作吸水剂,提高乙醇、乙酸的转化率。
③可适当增加乙醇的量,提高乙酸的转化率。
④有冷凝回流装置,可提高产率。
(5)饱和Na2CO3溶液的作用:
降低乙酸乙酯的溶解度、中和乙酸、溶解乙醇。
(6)实验现象:
在饱和Na2CO3溶液上方有透明的、具有香味的油状液体。
3.乙酸乙酯的水解反应
在酸性或碱性条件下均可发生水解反应。
CH3COOC2H5+H2O
CH3COOH+C2H5OH(可逆)
CH3COOC2H5+NaOH―→CH3COONa+C2H5OH(完全)
(1)乙醇与乙酸中均含有—OH,所以均能与Na反应生成氢气(√)
(2)医用酒精的浓度通常为95%(×
)
(3)乙醇、乙酸与Na2CO3溶液反应均产生CO2(×
(4)制备乙酸乙酯时可用热的NaOH溶液收集产物以除去其中的乙酸(×
(5)可以用分液漏斗分离乙酸乙酯和乙醇(×
(6)乙酸和乙酸乙酯可用饱和Na2CO3溶液加以区别(√)
(7)乙酸分子中含有羧基,可与NaHCO3溶液反应生成CO2(√)
(8)乙酸乙酯、油脂与NaOH溶液反应均有醇生成(√)
(1)能否用Na检验酒精中是否含有水?
应如何检验酒精中的少量水?
(2)CH3COOH分别与NaOH、CH3CH2OH发生反应,CH3COOH分子中的断键部位相同吗?
答案
(1)不能。
因为Na与乙醇也发生反应生成H2。
向酒精中加入适量无水CuSO4,若无水CuSO4的颜色由白色变为蓝色,则酒精中含有水。
(2)不同。
与NaOH反应的断键部位是氢氧键,与乙醇反应的断键部位是碳氧键。
完成下列各步转化的化学方程式,并指出反应类型。
①________________________________________________________________________;
________________。
②________________________________________________________________________;
③________________________________________________________________________;
④________________________________________________________________________;
⑤________________________________________________________________________;
⑥________________________________________________________________________;
答案 ①CH2==CH2+H2O
CH3CH2OH 加成反应
②2CH3CH2OH+O2
2CH3CHO+2H2O 氧化反应
③2CH3CHO+O2
2CH3COOH 氧化反应
④2CH3COOH+CaCO3―→(CH3COO)2Ca+CO2↑+H2O 复分解反应
⑤CH3COOH+C2H5OH
CH3COOC2H5+H2O 酯化反应(或取代反应)
⑥CH3COOC2H5+H2O
CH3COOH+C2H5OH 取代反应(或水解反应)
题组一 乙醇、乙酸的性质及应用
1.下列关于乙醇和乙酸的说法错误的是( )
A.乙醇和乙酸都是常用调味品的主要成分
B.相同条件下,与金属钠反应的速率,乙醇比乙酸慢
C.乙醇可由乙烯与水发生加成反应制得,乙酸可由乙醇氧化制得
D.乙醇和乙酸之间能发生酯化反应,酯化反应的逆反应为皂化反应
答案 D
解析 乙醇和乙酸都是常用调味品的主要成分,A项正确;
相同条件下,与金属钠反应时,—COOH易电离出氢离子,则乙醇比乙酸反应慢,B项正确;
乙烯与水发生加成反应生成乙醇,乙醇被强氧化剂氧化制得乙酸,C项正确;
乙醇和乙酸之间能发生酯化反应,酯化反应为可逆反应,油脂在碱性溶液中的水解反应为皂化反应,D项错误。
2.下列物质中不能用来区分乙酸、乙醇、苯的是( )
A.金属钠B.溴水
C.碳酸钠溶液D.紫色石蕊溶液
答案 B
解析 乙酸和金属钠反应剧烈,乙醇和金属钠反应缓慢,苯和金属钠不反应,可以区分;
乙酸、乙醇均溶于溴水,且不分层,苯可以把溴水中的溴萃取出来,出现分层,不能区分;
乙酸和碳酸钠反应放出气泡,乙醇和碳酸钠互溶不分层,苯不溶于碳酸钠,出现分层,可以区分;
乙酸显酸性,能使紫色石蕊溶液变红色,乙醇溶于石蕊溶液不分层,苯与石蕊溶液混合,出现分层,可以区分。
3.(2019·
徐州模拟)山西老陈醋素有“天下第一醋”的盛誉。
食醋中含有乙酸,下列关于乙酸的说法中错误的是( )
A.乙酸分子中含有4个氢原子,但乙酸是一元酸
B.往食醋溶液中滴入紫色石蕊溶液,溶液将变红
C.往热水瓶内胆中加入适量的食醋,可去除水垢
D.制取乙酸乙酯时,乙酸分子中的氢原子被乙基(—C2H5)取代
解析 乙酸发生酯化反应时,乙酸中的—OH被乙氧基(C2H5O—)取代。
1.羟基氢的活动性顺序
>
>H—OH>C2H5—OH
2.乙醇的化学性质与羟基的关系
(1)与Na反应时,只断裂a处键。
(2)乙醇催化氧化时,断裂a和c两处键,形成碳氧双键。
(3)乙醇和乙酸发生酯化反应时只断裂a处键。
题组二 乙酸乙酯的制取与拓展
4.(2018·
德州校级期末)下列关于酯化反应的说法正确的是( )
A.用CH3CH218OH与CH3COOH发生酯化反应,生成H218O
B.反应液混合时,顺序为先倒乙醇再倒浓硫酸最后倒乙酸
C.乙酸乙酯不会和水生成乙酸和乙醇
D.用蒸馏的方法从饱和Na2CO3溶液中分离出乙酸乙酯
解析 A项,CH3CH218OH与CH3COOH发生酯化反应,生成CH3CO18OCH2CH3和H2O,错误;
B项,浓硫酸密度比乙醇大,溶于乙醇放出大量的热,为防止酸液飞溅,加入药品时应先在试管中加入一定量的乙醇,然后边搅拌边振荡试管将浓硫酸慢慢加入试管,最后再加入乙酸,正确;
C项,乙酸乙酯在酸性条件下水解可生成乙酸和乙醇,错误;
D项,乙酸乙酯与饱和Na2CO3溶液分层,因此应采取分液操作实现二者的分离,错误。
5.(2019·
贵阳高三调研)某课外兴趣小组欲在实验室里制备少量乙酸乙酯,该小组的同学设计了以下四个制取乙酸乙酯的装置,其中正确的是( )
答案 A
解析 B和D中的导管插到试管b内液面以下,会引起倒吸,C和D中,试管b中的试剂NaOH溶液会与生成的乙酸乙酯反应,B、C、D错误。
6.1丁醇和乙酸在浓硫酸作用下,通过酯化反应制得乙酸丁酯,反应温度为115~125℃,反应装置如下图,下列对该实验的描述错误的是( )
A.不能用水浴加热
B.长玻璃管起冷凝回流作用
C.提纯乙酸丁酯需要经过水、氢氧化钠溶液洗涤
D.加入过量乙酸可以提高1丁醇的转化率
答案 C
解析 该酯化反应需要的温度为115~125℃,水浴的最高温度为100℃,A项正确;
长导管可以起到冷凝回流酸和醇的作用,B项正确;
乙酸丁酯在氢氧化钠溶液中容易发生水解,C项错误;
在可逆反应中,增加一种反应物的用量可以提高另一种反应物的转化率,D项正确。
题组三 乙醇的催化氢化实验
7.如图所示进行乙醇的催化氧化实验,试管A中盛有无水乙醇,B中装有CuO(用石棉绒作载体)。
请回答下列问题:
(1)向试管A中鼓入空气的目的是__________________________________________________。
(2)试管A上部放置铜丝网的作用是________________________________________________。
(3)玻璃管B中可观察到的现象是_________;
相关化学方程式是________________________。
答案
(1)使空气通过乙醇,形成乙醇和空气的混合气体
(2)防止乙醇和空气的混合气体爆炸
(3)黑色固体变红 CuO+C2H5OH
CH3CHO+H2O+Cu,2C2H5OH+O2
2CH3CHO+2H2O
考点二 基本营养物质——糖类、油脂、蛋白质
1.糖类、油脂、蛋白质的化学组成
有机物
元素组成
代表物
代表物分子
水溶性
糖
类
单糖
C、H、O
葡萄糖、果糖
C6H12O6
易溶
二糖
麦芽糖、蔗糖
C12H22O11
多糖
淀粉、纤维素
(C6H10O5)n
油
脂
植物油
不饱和高级脂肪酸甘油酯
不溶
脂肪
动物脂肪
饱和高级脂肪酸甘油酯
蛋白质
C、H、O、N、S、P等
酶、肌肉、毛发等
氨基酸连接成的高分子
2.糖类、油脂、蛋白质的性质
特征反应
水解反应
葡萄糖
有银镜产生
蔗糖
产物为葡萄糖与果糖
淀粉
遇碘单质(I2)变蓝色
产物为葡萄糖
油脂
酸性条件下:
产物为甘油、高级脂肪酸;
碱性条件下(皂化反应):
产物为甘油、高级脂肪酸盐
①遇浓硝酸变黄色
②灼烧有烧焦羽毛气味
生成氨基酸
3.糖类、油脂、蛋白质的用途
(1)糖类物质是绿色植物光合作用的产物,是动植物所需能量的重要来源;
葡萄糖是重要的工业原料,主要用于食品加工、医疗输液、合成药物等;
纤维素可用于造纸,制造纤维素硝酸酯、纤维素乙酸酯、黏胶纤维等。
(2)油脂提供人体所需要的能量,等质量的糖类、油脂、蛋白质完全氧化时,油脂放出的热量最多。
油脂用于生产高级脂肪酸和甘油。
(3)蛋白质是人体必需的营养物质,在工业上有很多用途,动物的毛、皮、蚕丝可制作服装,大多数酶是一类特殊的蛋白质,是生物体内重要的催化剂。
(1)糖类、油脂、蛋白质在一定条件下都能发生水解反应(×
(2)蔗糖、淀粉、油脂及其水解产物中均既有电解质也有非电解质(×
(3)油脂在酸性或碱性条件下,均可发生水解反应,且产物相同(×
(4)淀粉和纤维素在酸催化下完全水解后的产物都是葡萄糖(√)
(5)纤维素在人体内可水解为葡萄糖,故可用作人体的营养物质(×
(6)淀粉、纤维素和油脂