高考浙江版高考化学 专题十 从海水中获得的化学物质Word格式文档下载.docx
《高考浙江版高考化学 专题十 从海水中获得的化学物质Word格式文档下载.docx》由会员分享,可在线阅读,更多相关《高考浙江版高考化学 专题十 从海水中获得的化学物质Word格式文档下载.docx(21页珍藏版)》请在冰豆网上搜索。
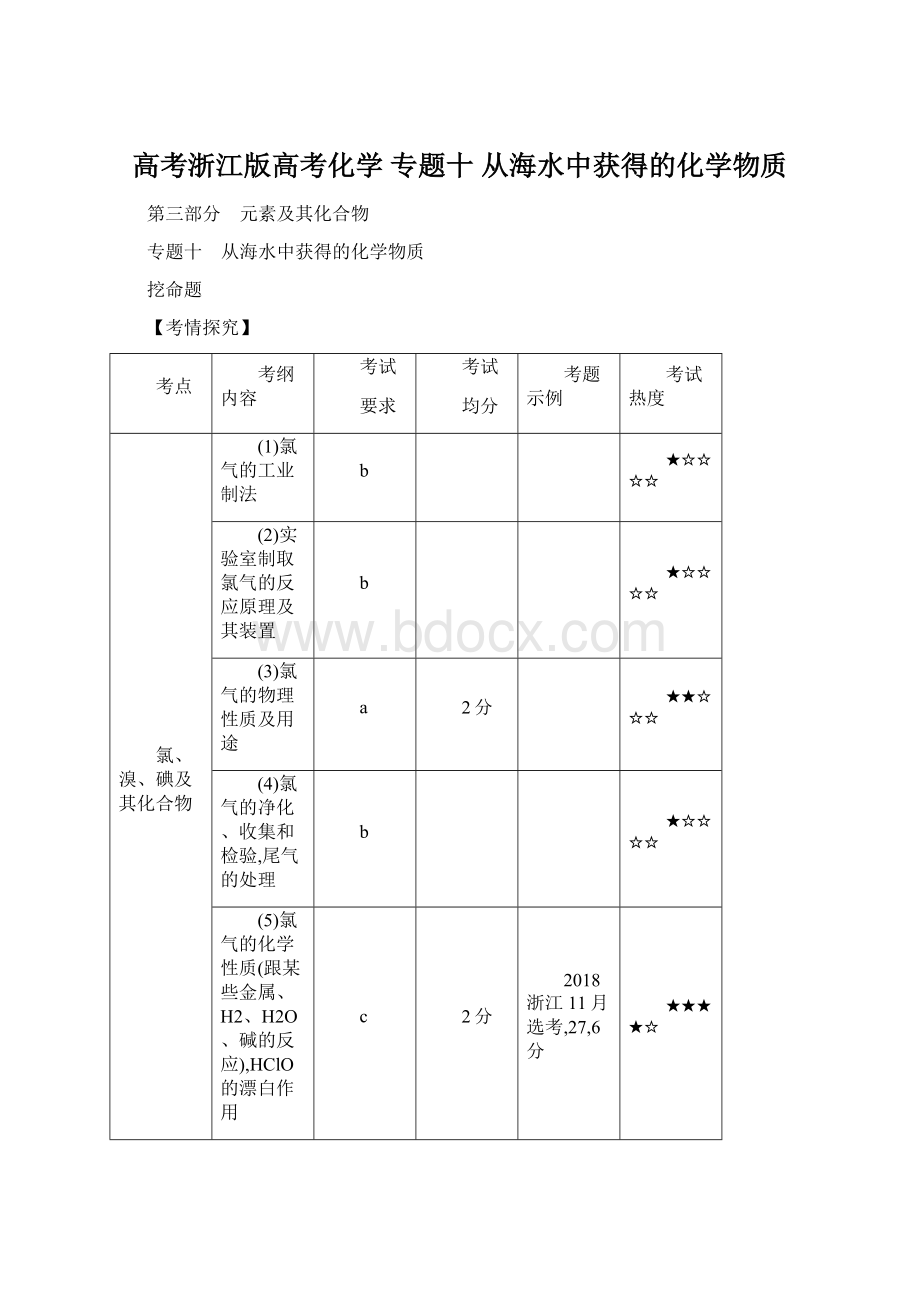
2分
★★☆☆☆
(4)氯气的净化、收集和检验,尾气的处理
(5)氯气的化学性质(跟某些金属、H2、H2O、碱的反应),HClO的漂白作用
c
2018浙江11月选考,27,6分
★★★★☆
(6)溴、碘单质的物理性质
(7)氯、溴、碘单质间的置换反应
★★★☆☆
(8)海水中提取溴、碘
☆☆☆☆☆
(9)检验Br-、I-的常用方法
钠、镁及其化合物
(1)钠、镁的物理性质及用途
(2)钠、镁的化学性质(跟非金属、酸、某些氧化物的反应)
(3)钠、镁的生产原理
2016浙江4月选考,8,2分
(4)碳酸钠、碳酸氢钠的性质及检验方法
2018浙江11月选考,5,2分
(5)碳酸钠、碳酸氢钠的用途
2017浙江11月选考,6,2分
(6)过氧化钠的主要性质
分析解读 本专题选择题重点考查点有二:
一是氯气的性质及用途;
二是钠、碳酸钠和碳酸氢钠的性质及用途,试题难度不大。
主观题部分单独命题的可能性不大,通常以元素化合物知识为载体,融离子反应、氧化还原反应、反应速率与化学平衡、电化学及盐类的水解与电离等知识于一体进行考查。
预计今后高考对本专题内容的考查方式基本不变。
【真题典例】
破考点
【考点集训】
考点一 氯、溴、碘及其化合物
1.(2019届浙江宁波镇海中学高一单元测试,6)下列离子方程式正确的是( )
①氯气与水反应:
Cl2+H2O2H++Cl-+ClO-;
②氯气与氢氧化钠溶液反应:
Cl2+2OH-Cl-+ClO-+H2O;
③浓盐酸与二氧化锰共热:
MnO2+4HCl(浓)Mn2++2Cl-+Cl2↑+2H2O;
④漂白粉溶液中通入少量的二氧化碳气体:
Ca2++2ClO-+H2O+CO2CaCO3↓+2HClO。
A.①③B.②④C.②③D.①④
答案 B
2.(2019届浙江温州瑞安中学单元检测,3)下列与含氯化合物有关的说法正确的是( )
A.HClO是弱酸,所以NaClO是弱电解质
B.向沸水中逐滴加入少量饱和FeCl3溶液,可制得Fe(OH)3胶体
C.HCl溶液和NaCl溶液均通过离子导电,所以HCl和NaCl均是离子化合物
D.电解NaCl溶液得到22.4LH2(标准状况),理论上需要转移NA个电子(NA表示阿伏加德罗常数)
3.(2018浙江武义一中高一期末,12)已知常温下氯酸钾与浓盐酸反应放出氯气,现按下图所示装置进行氯、溴、碘的性质实验。
玻璃管内装着分别滴有不同溶液的白色棉球,反应一段时间后,对图中指定部位颜色描述正确的是( )
A.①黄绿色 ②橙色 ③蓝色 ④白色
B.①无色②橙色③紫色④白色
C.①黄绿色②橙色③蓝色④无色
D.①黄绿色②无色③紫色④白色
答案 A
4.(2019届浙江宁波效实中学高一单元检测,25)如图是实验室制备氯气并进行一系列相关实验的装置(夹持装置已略)。
(1)制备氯气选用的药品为漂白粉固体和浓盐酸,则相关反应的化学方程式为 。
(2)装置B中饱和食盐水的作用是 ;
同时装置B也是安全瓶,监测实验进行时装置C是否发生堵塞,请写出发生堵塞时装置B中的现象:
。
(3)装置C的实验目的是验证氯气是否具有漂白性,为此装置C中Ⅰ、Ⅱ、Ⅲ处依次放入 (填字母)。
d
Ⅰ
干燥的有色布条
湿润的有色布条
Ⅱ
碱石灰
硅胶
浓硫酸
无水氯化钙
Ⅲ
(4)设计装置D、E的目的是比较氯、溴、碘的非金属性。
当向D装置中缓缓通入一定量氯气时,可以看到无色溶液逐渐变为 色,说明氯的非金属性强于溴。
(5)打开活塞,将装置D中少量溶液加入装置E中,振荡后静置。
观察到的现象是
。
答案
(1)Ca(ClO)2+4HCl(浓)CaCl2+2Cl2↑+2H2O
(2)除去Cl2中的HCl 长颈漏斗中液面上升,形成水柱 (3)d (4)棕黄 (5)装置E中溶液分为两层,上层(苯层)为紫红色
考点二 钠、镁及其化合物
1.(2018浙江6月学考,4,2分)下列物质中,不能与金属钠反应的是( )
A.氯气 B.水 C.乙醇 D.煤油
答案 D
2.(2019届浙江温州瑞安中学单元检测,3)下列有关金属镁的说法不正确的是( )
A.Mg在CO2中燃烧生成MgO和C,是放热反应
B.工业上通过电解MgCl2溶液制取金属镁
C.Mg和稀硫酸反应时,滴加少量硫酸铜溶液,能加快反应速率
D.Mg可以用来制造信号弹和焰火,MgO可以作耐高温材料
3.(2019届浙江宁波镇海中学高一单元测试,10)鉴别两瓶失去标签的同浓度的Na2CO3和NaHCO3无色溶液,下列方法中不合理的是( )
①用干燥的pH试纸检验,pH大的是Na2CO3溶液
②取等量的溶液于两支试管中,各滴入等量的酚酞溶液,红色较深的是Na2CO3溶液
③取等量的溶液于两支试管中,加热,有气泡产生的是NaHCO3溶液
④取等量的溶液于两支试管中,逐滴加入稀盐酸,开始就有气体放出的是NaHCO3溶液
⑤取等量的溶液于两支试管中,滴加BaCl2溶液,生成白色沉淀的是Na2CO3溶液
⑥取等量的溶液于两支试管中,滴加Ba(OH)2溶液,生成白色沉淀的是Na2CO3溶液
A.①② B.③⑥ C.④⑤ D.②⑤
4.(2018浙江宁波鄞州中学单元检测,8)过氧化钠具有强氧化性,遇木炭、铝粉等还原性物质时可燃烧。
下列有关说法不正确的是( )
A.Na2O2与CO2反应时,Na2O2是氧化剂,CO2是还原剂
B.熔融过氧化钠时不可使用石英坩埚
C.过氧化钠与木炭、铝粉反应时,均表现出强氧化性
D.过氧化钠与SO2反应可生成硫酸钠
炼技法
【方法集训】
方法 对氯水性质多样性的分析
1.(2019届浙江宁波镇海中学高一单元测试,4)某同学在一pH试纸上滴几滴新制的氯水,现象如图所示,下列有关该实验的说法中正确的是( )
A.该实验说明Cl2分子具有漂白性
B.该实验说明H+扩散速度比HClO分子快
C.将实验后的pH试纸在酒精灯上微热,试纸又恢复为原来的颜色
D.若用久置的氯水进行实验,现象相同
2.(2017浙江金华汤溪高中月考)下列实验现象与新制氯水中的某些成分(括号内物质)没有关系的是( )
A.将NaHCO3固体加入新制氯水,有无色气泡冒出(H+)
B.新制氯水使红色布条褪色(HClO)
C.滴加AgNO3溶液生成白色沉淀(Cl-)
D.向FeCl2溶液中滴加氯水后,再滴加KSCN溶液,溶液呈血红色(HCl)
3.饱和氯水与石灰石的反应是制取较浓的HClO溶液的方法之一。
某同学运用这一方法,尝试制取HClO溶液并进行了如下定性实验:
①在试管中加入过量的块状碳酸钙,再加入约20mL饱和氯水,充分反应,有少量气泡产生,溶液的黄绿色褪去;
②过滤,将滤液滴在有色布条上,发现其漂白性更强;
③为了确定反应产物,将滤液分为三份,分别进行以下实验:
第一份与石灰水混合,立即产生大量白色沉淀;
第二份与稀盐酸混合,立刻产生大量气泡;
第三份加热,看到溶液变浑浊且有大量无色气体产生。
经检测,上述实验中产生的无色气体均为CO2气体。
(1)试解释可以在饱和氯水中加入石灰石制备HClO的原因:
。
(2)写出步骤③中第一份及第二份滤液发生反应的离子方程式。
第一份:
。
第二份:
。
(3)试根据所学知识推测,在②的滤液中含有的溶质,除了溶解的极少量氯气外,还含有的其他溶质为(写化学式)
。
答案
(1)由于饱和氯水中存在:
Cl2+H2OH++Cl-+HClO,加入CaCO3后,CaCO3与HCl反应使平衡右移,HClO的浓度增大
(2)Ca2++HC+OH-CaCO3↓+H2O HC+H+CO2↑+H2O
(3)CaCl2、Ca(HCO3)2、HClO
过专题
【五年高考】
A组 自主命题·
浙江卷题组
1.(2017浙江11月选考,6,2分)下列说法不正确的是( )
A.干冰可用于人工降雨
B.碘酸钾可用作加碘食盐的添加剂
C.碳酸钠是发酵粉的主要成分
D.次氯酸钙是漂白粉的有效成分
答案 C
2.(2015浙江1月学考,13,2分)下列说法中,正确的是( )
A.向KI溶液中通入适量Cl2后,溶液颜色变深
B.向KCl溶液中滴加几滴酚酞试液,溶液颜色变红
C.溴水与NaCl溶液混合时,会发生置换反应
D.NaCl溶液在空气中会被氧化,故需要密封保存
3.(2018浙江4月选考,27,6分)某同学用含结晶水的正盐X(四种短周期元素组成的纯净物)进行了如下实验:
实验中观测到:
混合气甲呈无色并被蒸馏水全部吸收;
固体乙为纯净物;
在步骤③中,取溶液丙,恰好中和需消耗0.00200molNaOH;
另取一定量溶液丙,加入少量K2FeO4固体,产生黄绿色气体。
请回答:
(1)X的化学式是 ,步骤①的化学方程式是 。
(2)溶液丙与K2FeO4固体反应的化学方程式是 。
答案 (6分)
(1)MgCl2·
6H2O(2分) MgCl2·
6H2OMgO+2HCl↑+5H2O↑(2分)
(2)2K2FeO4+16HCl4KCl+2FeCl3+3Cl2↑+8H2O(2分)
4.(2018浙江6月学考,5,2分)下列金属元素的单质或化合物在火焰上灼烧时,焰色为紫色的是( )
A.钠B.钾C.镁D.铁
5.(2018浙江11月选考,5,2分)可用于治疗胃酸过多的物质是( )
A.碳酸氢钠B.氯化钠C.氯化钾D.氢氧化钠
6.(2015浙江10月选考,3,2分)常温下能与水反应的金属单质是( )
A.SiO2B.Br2C.Na2OD.Na
7.(2018浙江4月选考,6,2分)下列说法不正确的是( )
A.纯碱可用于去除物品表面的油污
B.二氧化碳可用作镁燃烧的灭火剂
C.植物秸秆可用于制造酒精
D.氢氧化铁胶体可用作净水剂
8.(2017浙江4月选考,6,2分)下列说法不正确的是( )
A.二氧化碳是酸雨的主要成分