高二化学化学反应速率辅导教案文档格式.docx
《高二化学化学反应速率辅导教案文档格式.docx》由会员分享,可在线阅读,更多相关《高二化学化学反应速率辅导教案文档格式.docx(20页珍藏版)》请在冰豆网上搜索。
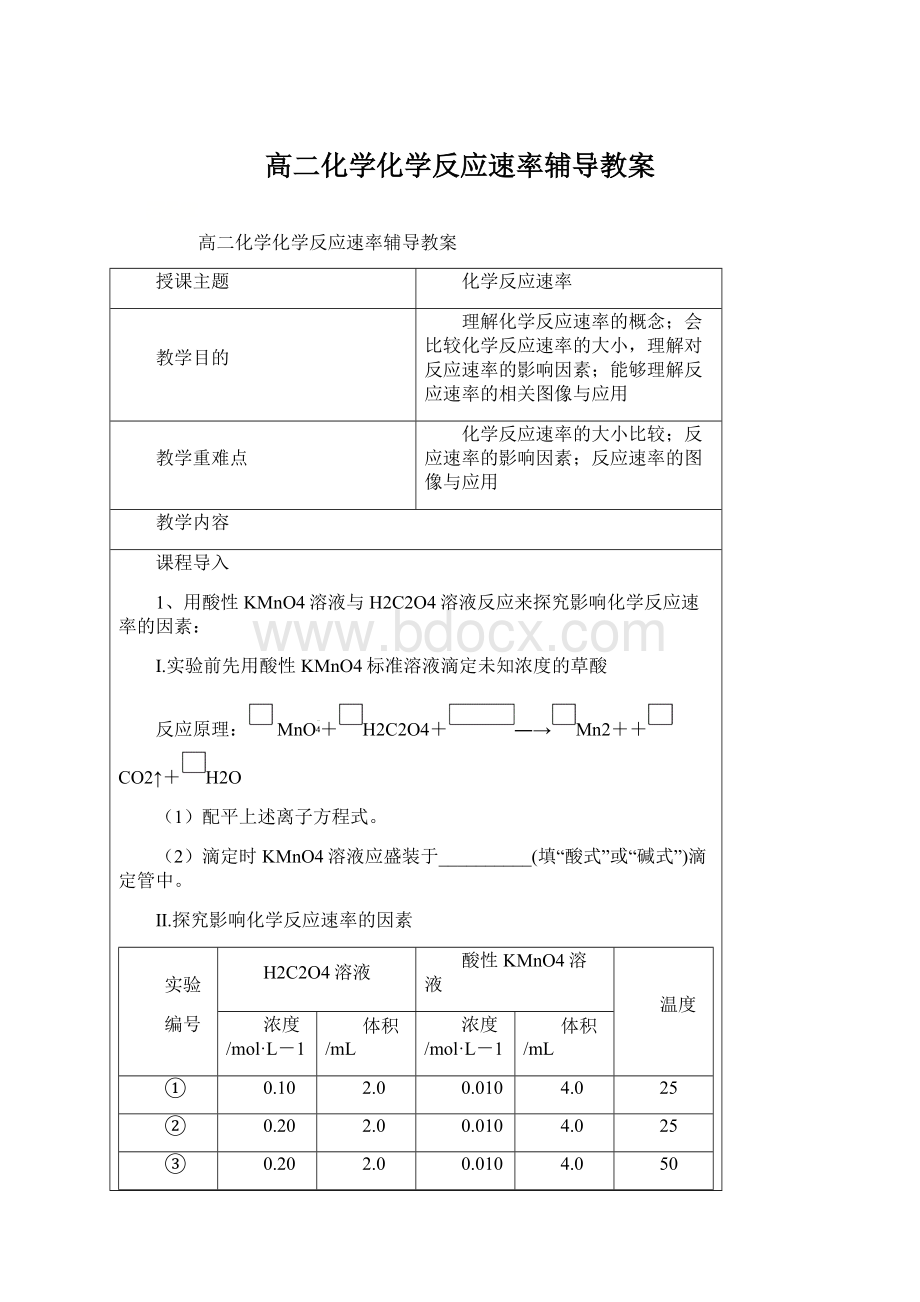
温度
浓度/mol·
L-1
体积/mL
①
0.10
2.0
0.010
4.0
25
②
0.20
③
50
(1)探究温度对化学反应速率影响的实验编号是________(填编号,下同)。
(2)探究反应物浓度对化学反应速率影响的实验编号是________。
学#科@网
Ⅲ.测得某次实验(恒温)时溶液中Mn2+物质的量与时间关系如图所示,请解释“n(Mn2+)在反应起始时变化不大,一段时间后快速增大”的原因:
___________________________________________。
本节知识点讲解
一、化学反应速率
1.定义
化学反应速率是用来衡量化学反应进行快慢的物理量。
2.表示方法
通常用单位时间内反应物浓度的减少量或生成物浓度的增加量来表示。
数学表达式为v=,单位为mol/(L·
min)、mol/(L·
s)或mol/(L·
h)。
3.化学反应速率与化学计量数的关系:
对于已知反应mA(g)+nB(g)pC(g)+qD(g),其化学反应速率可用不同的物质来表示,当单位相同时,化学反应速率的数值之比等于方程式中各物质的化学计量数之比,即v(A)∶v(B)∶v(C)∶v(D)=m∶n∶p∶q。
例如:
在一个2L的容器中发生反应:
3A(g)+B(g)2C(g),加入2molA,1s后剩余1.4mol,则v(A)=0.3mol·
L−1·
s−1,v(B)=0.1mol·
s−1,v(C)=0.2mol·
s−1。
过关秘籍
(1)在同一化学反应中,无论选用反应物还是生成物表示化学反应速率,其值均为正值。
(2)化学反应速率通常是指在某一段时间内的平均反应速率,而不是某一时刻的瞬时反应速率。
(3)同一化学反应中,在相同的反应时间内,不同的物质表示的反应速率的数值可能不同。
但表示的意义相同。
因此表示化学反应速率时,必须指明是用反应体系中的哪种物质作依据。
(4)固体或纯液体的浓度恒为常数,不能用固体或纯液体的浓度表示化学反应速率。
但是化学反应速率与固体和纯液体参与反应的表面积有关,因此,通常增大固体或纯液体参与反应的表面积(如将固体粉碎,将液体变成雾状,加速搅拌等)可加快化学反应速率。
(5)同一化学反应中,各物质表示的化学反应速率之比=化学方程式中各物质的化学计量数之比=各物质的浓度变化量之比。
二、化学反应速率的计算与大小比较方法
1.根据定义求化学反应速率
v=
2.根据反应速率与化学方程式中各物质化学计量数的关系计算
同一个化学反应,同一段时间内,用不同物质的浓度变化表示的反应速率,数值可能不同,但意义相同,其数值之比等于化学方程式中各物质的化学计量数之比。
对于化学反应mA(g)+nB(g)pC(g),即v(A)∶v(B)∶v(C)=m∶n∶p,或。
3.由于同一反应的化学反应速率用不同的物质表示时数值可能不同,所以比较反应的快慢不能只看数值的大小,而要进行一定的转化。
(1)单位是否统一,若不统一,换算成相同的单位。
(2)换算成同一物质表示的反应速率,再比较数值的大小。
(3)比较反应速率与化学计量数的比值,即对于一般的化学反应aA(g)+bB(g)cC(g)+dD(g),比较与,若>,则用A表示的反应速率比B的大。
三、影响化学反应速率的因素
1.内因(主要因素)反应物的结构、性质。
2.外因(其他条件不变,只改变一个条件)
条件变化
活化能
单位体积内
活化分子
百分数
单位时间内有效碰撞的次数
分子
总数
活化
分子数
浓度
增大
不变
增多
减小
减少
压强
加压(减小容器体积)
减压(增大容器体积)
升高
降低
使用催化剂
3.理论解释——有效碰撞理论
(1)活化分子、活化能、有效碰撞
①活化分子:
能够发生有效碰撞的分子。
②活化能:
如右图
图中E1为正反应的活化能,E3为使用催化剂时的活化能,E2为逆反应的活化能,反应热为E1−E2。
③有效碰撞:
活化分子之间能够引发化学反应的碰撞。
(2)活化分子、有效碰撞与反应速率的关系
(1)催化剂有正催化剂和负催化剂之分,正催化剂即通常所说的催化剂,负催化剂又称为抑制剂。
催化剂只有在适宜的温度下催化活性才最高,反应速率才达到最大。
(2)固体或纯液体的浓度可视为常数,其物质的量的变化不会引起反应速率的变化,但固体颗粒的大小会影响接触面积的大小,从而影响反应速率的大小。
(3)改变压强,对反应速率产生影响的根本原因是引起浓度的改变。
对于有气体参加的反应体系,有以下几种情况:
①恒温时:
增大压强→体积缩小→浓度增大→反应速率增大。
②恒温恒容时:
a.充入气体反应物→反应物浓度增大→反应速率增大。
b.充入稀有气体(或非反应气体)→总压强增大,但各物质的浓度不变,反应速率不变。
③恒温恒压时:
充入稀有气体(或非反应气体)→体积增大→各物质浓度减小→反应速率减小。
(4)增加反应物的浓度,v正急剧增大(突变),v逆逐渐增大(渐变)。
(5)催化剂能同时同等程度地改变正逆反应速率。
四、化学反应速率图象及其应用
(一)全程速率—时间图象
Zn与足量盐酸的反应,反应速率随时间的变化出现如图情况。
原因解释:
AB段(v渐大),因反应为放热反应,随反应的进行,温度逐渐升高,导致反应速率逐渐增大;
BC段(v渐小),则主要因为随反应的进行,溶液中c(H+)减小,导致反应速率减小。
(二)物质的量(或浓度)—时间图象
某温度时,在定容(VL)容器中,X、Y、Z三种物质的物质的量随时间的变化曲线如图所示。
1.由图象得出的信息是
(1)X、Y是反应物,Z是生成物;
(2)t3时反应达平衡,X、Y没有全部反应。
2.根据图象可进行如下计算:
(1)求某物质的平均速率、转化率,如
v(X)=mol/(L·
s);
Y的转化率=×
100%。
(2)确定化学方程式中的化学计量数之比,如X、Y、Z三种物质的化学计量数之比为(n1-n3)∶(n2-n3)∶n2。
(三)速率—外界条件图象及反应
以N2(g)+3H2(g)2NH3(g) ΔH=-92.4kJ/mol为例。
1.速率—浓度(c)图象
速率变化
速率变化曲线
增大反应物的浓度
v正、v逆均增大,且v′正>
v′逆
减小反应物的浓度
v正、v逆均减小,且v′逆>
v′正
增大生成物的浓度
v正、v逆均增大,且v′逆>
减小生成物的浓度
v正、v逆均减小,且v′正>
2.速率—温度(T)的图象
升高温度
降低温度
3.速率—压强(p)图象
增大压强
减小压强
4.速率—催化剂图象
使用催化剂,v正、v逆同等倍数增大,图象为
说明:
(1)条件增强,曲线在原图象的上方;
条件减弱,曲线在原图象的下方。
(2)浓度改变时,图象曲线一条连续,一条不连续;
其他条件改变,图象曲线不连续。
(3)对于反应前后气体的体积不变的反应,改变压强时,v正、v逆同等倍数增大或减小。
例题解析
考向一化学反应速率的计算
典例1一定温度下,10mL0.40mol/LH2O2溶液发生催化分解。
不同时刻测得生成O2的体积(已折算为标准状况)如下表。
t/min
2
4
6
8
10
V(O2)/mL
0.0
9.9
17.2
22.4
26.5
29.9
下列叙述不正确的是(溶液体积变化忽略不计)
A.0~6min的平均反应速率:
v(H2O2)≈3.3×
10−2mol/(L·
min)
B.6~10min的平均反应速率:
v(H2O2)<
3.3×
C.反应至6min时,c(H2O2)=0.30mol/L
D.反应至6min时,H2O2分解了50%
化学反应速率计算的三个方法
(1)定义式法:
v(B)==。
(2)比例关系法:
化学反应速率之比等于化学计量数之比,如mA(g)+nB(g)pC(g)中,v(A)∶v(B)∶v(C)=m∶n∶p。
(3)三段式法:
列起始量、转化量、最终量,再根据定义式或比例关系计算。
反应 mA(g)+nB(g)pC(g)
起始浓度(mol·
L−1)abc
转化浓度(mol·
L−1)x
某时刻浓度(mol·
L−1)a−xb−c+
巩固练习
1.把0.6molX气体和0.4molY气体混合于2L容器中,使它们发生如下反应:
3X(g)+Y(g)nZ(g)+2W(g),在5min时已经生成0.2molW,若测知以Z的浓度变化表示平均反应速率为0.01mol·
min−1,则上述反应中Z气体的化学计量数n的值是
A.1B.2C.3D.4
考向二化学反应速率的比较
典例1对于可逆反应A(g)+3B(s)2C(g)+2D(g),在不同条件下的化学反应速率如下,其中表示的反应速率最快的是
A.v(A)=0.5mol·
min−1B.v(B)=1.2mol·
s−1
C.v(D)=0.4mol·
min−1D.v(C)=0.1mol·
化学反应速率大小的比较方法
(1)归一法:
将同一反应中的不同物质的反应速率转化成同一单位、同一种物质的反应速率,再进行速率的大小比较。
(2)比值法:
将各物质表示的反应速率转化成同一单位后,再除以对应各物质的化学计量数,然后对求出的数值进行大小排序,数值大的反应速率快。
如反应mA(g)+nB(g)pC(g)+qD(g),若>
,则反应速率A>
B。
2.反应A+3B2C+2D在四种不同情况下的反应速率分别为
①v(A)=0.15mol·
s−1②v(B)=0.6mol·
③v(C)