从海水中获得的化学物质.docx
《从海水中获得的化学物质.docx》由会员分享,可在线阅读,更多相关《从海水中获得的化学物质.docx(23页珍藏版)》请在冰豆网上搜索。
从海水中获得的化学物质
专题2从海水中获得的化学物质
《第一单元氯、溴、碘及其化合物》导学
【学海导航】
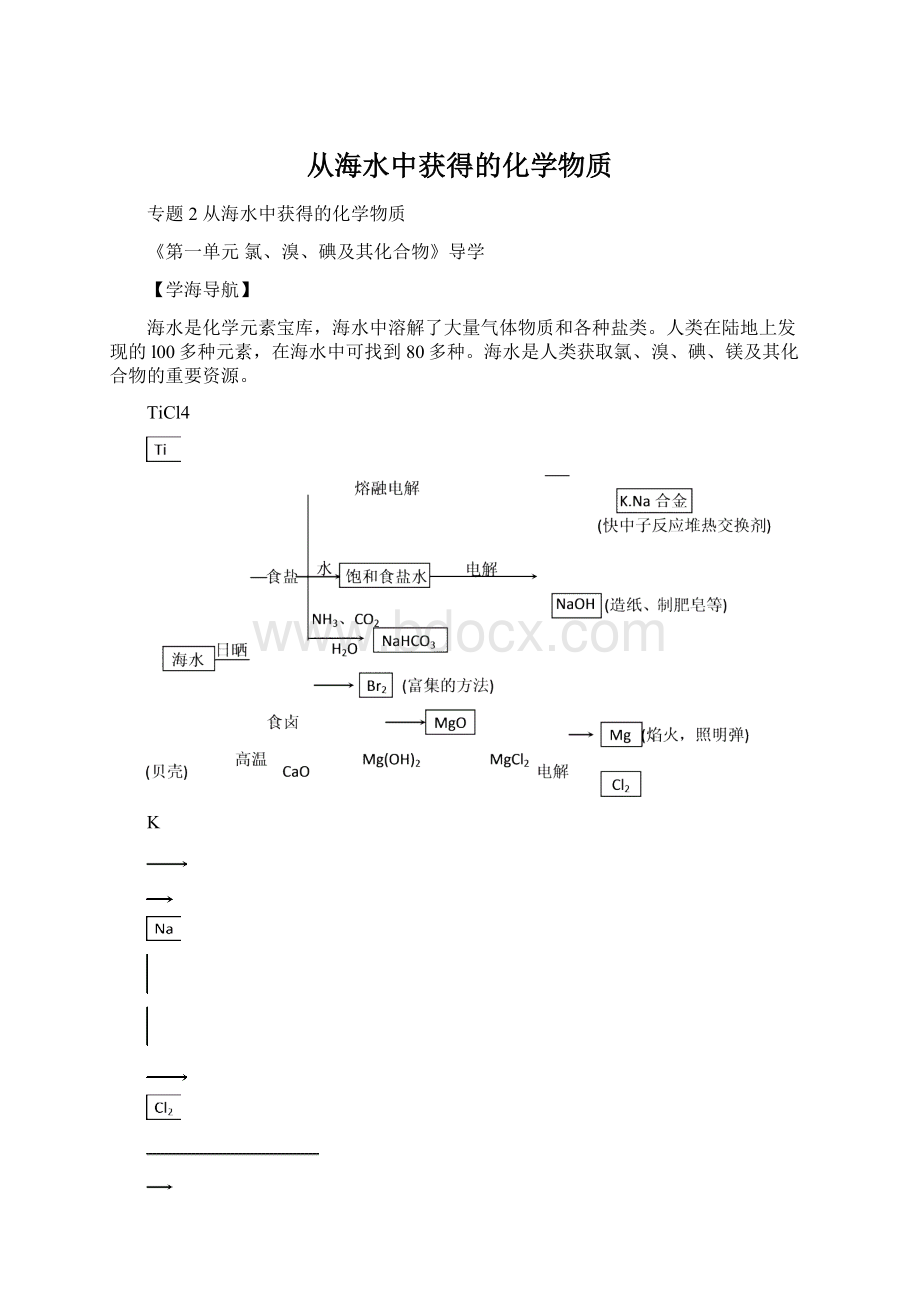
海水是化学元素宝库,海水中溶解了大量气体物质和各种盐类。
人类在陆地上发现的l00多种元素,在海水中可找到80多种。
海水是人类获取氯、溴、碘、镁及其化合物的重要资源。
TiCl4
K
H2
△
△
(耐火材料)
熔融
过滤
CaCO3
一、氯、溴、碘的提取
(一)氯碱工业——电解食盐水生产氯气和烧碱的化学工业
1、
通电
我国主要以海盐为原料。
海盐中含硫酸钙、硫酸镁、氯化镁等杂质,要净化后制成饱和食盐水再电解。
2NaCl+2H2O==2NaOH+H2↑+Cl2↑
氯碱工业面临问题:
①产品对设备腐蚀严重、环境污染显著。
②电能消耗量大。
(二)从海水中提取溴的常见工艺
①浓缩并酸化海水后,通入适量的氯气,使溴离子转化为溴单质:
2NaBr+Cl2=Br2+2NaCl
②向含溴单质的水溶液中通空气和水蒸汽,将溴单质吹入盛二氧化硫溶液的吸收塔内以达到富集的目的:
Br2+SO2+2H2O==2HBr+H2SO4(也可用NaOH或Na2CO3溶液吸收)
③向吸收塔内的溶液中通入适量的氯气:
2HBr+Cl2==2HCl+Br2
④用四氯化碳(或苯)萃取吸收塔内的溶液中的溴单质。
(三)从海洋植物中提取碘的主要工艺
①用水浸泡海带或海藻灼烧后的灰烬
②向水中通入适量的氯气,使碘离子转化为碘单质:
2NaI+Cl2==I2+2NaCl
③过滤,用有机溶剂萃取碘单质。
二、氯、溴、碘的性质和用途
(一)氯气(chlorinegas)的性质和用途
氯自1774年被舍勒发现,到1810年被戴维确认为一种元素,经历了36年。
实验室制备:
①原理:
MnO2+4HCl(浓)△MnCl2+Cl2↑+2H2O②装置:
固液加热型③收集:
向上排空气法④验满:
湿润的淀粉-碘化钾试纸等⑤尾气吸收:
NaOH溶液。
1、物理性质:
通常是黄绿色、密度比空气大、有刺激性气味气体。
能溶于水,有毒。
2、化学性质:
氯原子易得电子,氯是活泼的非金属元素。
氯气与金属、非金属等发生氧化还原反应,一般作氧化剂。
与水、碱溶液则发生自身氧化还原反应,既作氧化剂又作还原剂。
3、氯气的用途:
重要的化工原料,能杀菌消毒、制盐酸、漂白粉及制氯仿等有机溶剂和农药。
拓展1:
氯水(chlorinewater)
氯水为黄绿色,所含Cl2有少量与水反应(Cl2+H2O
HCl+HClO),大部分仍以分子形式存在,氯水的主要溶质是Cl2。
新制氯水含Cl2、H2O、HClO、H+、Cl-、ClO-、OH-等微粒。
拓展2:
次氯酸(hypochlorousacid)
次氯酸(HClO)是比H2CO3还弱的酸,溶液中主要以HClO分子形式存在。
性质:
①易分解(2HClO==2HCl+O2↑),光照时会加速。
②是强氧化剂:
能杀菌;能使某些有机色素褪色。
拓展3:
漂白粉
次氯酸盐比次氯酸稳定,容易保存,工业上以Cl2和石灰乳为原料制成漂白粉;漂白粉的有效成分【Ca(ClO)2】,须和酸(或空气中CO2)作用产生次氯酸,才能发挥漂白作用。
(二)溴、碘的性质和用途
溴
碘
物理性质
深红棕色,密度比水大的液体,强烈刺激性气味,易挥发,强腐蚀性。
紫黑色固体,易升华。
气态碘在空气中显深紫红色,有刺激气味。
在水中溶解度很小,易溶于酒精、四氯化碳等有机溶剂
化学性质
能与氯气反应的金属、非金属一般也能与溴、碘反应,只是反应活性不如氯气。
氯、溴、碘单质间能够发生置换反应:
氯能把溴和碘从它们的卤化物中置换出来,溴能把碘从它的卤化物中置换出来,即氯、溴、碘的氧化性强弱为:
Cl2>Br2>I2
用途
染料、防爆剂、胶卷感光材料、杀虫剂、红药水、镇静剂,催泪性毒剂等。
重要的化工原料。
配碘酒和碘化物,食用盐中加KIO3,碘化银制造相底片和人工降雨。
三、氧化还原反应(oxidation-reductionreaction)
1、氧化还原反应的有关概念
氧化还原反应的实质:
发生电子转移(电子的得失或电子对的偏移)。
化合价降低+ne-被还原
氧化剂+还原剂=还原产物+氧化产物
化合价升高-ne-被氧化
2、氧化还原反应的一般规律
同一反应中:
①氧化反应与还原反应同时发生,相互依存。
②氧化剂得电子总数与还原剂失电子总数相等。
即氧化剂化合价降低总数与还原剂化合价升高总数相等。
2、氧化还原反应中电子转移的表示方法(双线桥法)书写要求:
①箭头是由反应物中的某一元素指向对应的生成物中的同一元素。
②一定要标出得、失电子的总数,并且数值相等。
练习
1、氧化还原反应的实质是( )
A、元素化合价发生变化B、反应中有氧原子的得失
C、反应中有电子得失或电子对的偏移D、反应后生成新物质
2、下列反应一定是氧化还原反应的是( )
A、化合反应 B、分解反应 C、复分解反应D、置换反应
3、下列反应中,不属于氧化还原反应的是( )
A、3Cl2+6KOH==5KCl+KClO3+3H2OB、2FeBr2+3Cl2==2FeCl3+2Br2
C、SnCl4+2H2O==SnO2+4HClD、Ca(OH)2+CO2==CaCO3↓+H2O
4、下列反应中,水作还原剂的是( )
A、2Na+2H2O==2NaOH+H2↑B、Cl2+H2O
HCl+HClO
C、2F2+2H2O==4HF+O2D、SO2+H2O
H2SO3
5、从海水中可以提取溴,主要反应为:
2Br-+Cl2=2Cl-+Br2,下列说法正确的是()
A、溴离子具有氧化性B、氯气是还原剂
C、该反应属于复分解反应D、氯气是氧化剂
6、在Cl2+2NaOH=NaCl+NaClO+H2O反应中,氧化剂与还原剂物质的量之比为()
A、1︰2B、1︰1C、2︰1D、3︰2
7、在下列各反应中,盐酸既表现出酸性又表现出氧化性的是
A、HCI+NaOH=NaCl+H2O B、Zn+2HCl=ZnCl2+H2↑
C、HCl+AgNO3=AgCl↓+HNO3 D、MnO2+4HCI(浓)=MnCl2+C12↑+2H2O
8、下列物质的用途,利用氧化还原反应的是()
A、用氯气消毒自来水
B、用稀盐酸除去热水瓶胆壁上的水垢(主要成分是CaCO3)
C、用食盐腌渍食物D、用小苏打治疗胃酸过多
10、鲜榨苹果汁是人们喜爱的饮料。
由于此饮料中含Fe2+,现榨的苹果汁在空气中会由淡绿色变为棕黄色(Fe3+)。
这个变色的过程中的Fe2+被(填“氧化”或“还原”)。
若榨汁时加入适量的维生素C,可有效防止这种现象的发生。
这说明维生素C具有性。
11、为防止碘缺乏病,通常在食盐中添加少量碘酸钾(KIO3),碘酸钾和碘化钾在酸性溶液中能发生下列反应。
请标出方程式中电子转移的方向与数目,并指出氧化剂和还原剂。
5KI+KIO3+3H2SO4=3I2+3K2SO4+3H2O
此反应中,氧化剂是,还原剂是。
氧化剂和还原剂的物质的量之比是。
12、某工厂在山坡坑道的仓库里贮有氯气钢瓶。
某天,有一只贮有氯气的钢瓶损坏,造成氯气泄漏,在场工人采取以下措施,请选择填充并简述理由。
⑴处理钢瓶的方法正确的是,简述理由
A、钢瓶推到坡下的小河里B、把钢瓶丢到深坑里,用石灰填埋C、把钢瓶扔到农田中
⑵钢瓶处理后,工人应立即,简述理由
A、转移到坡下B、转移到坡上
⑶若在场工人没有防毒面具,可以用浸有某种物质的一定浓度的水溶液的毛巾捂住鼻子。
最适宜采用的物质是。
(A、NaOHB、NaClC、Ca(OH)2D、Na2CO3)
13、新制氯水中含有多种组分:
,氯水应存放在瓶中保存。
将紫色石蕊试液滴入氯水中,溶液显红色,起作用的成分是 ;过一会儿,溶液的颜色逐渐褪去,起作用的成分是 ;往氯水中滴入硝酸银溶液,产生白色沉淀,起作用的成分是 ;氯水能使淀粉碘化钾试纸变蓝,起作用的成分是 。
14、下图是一个实验室制取氯气并以氯气为原料进行特定反应的装置:
⑴实验开始时,先点燃A处的酒精灯,打开旋塞K,让Cl2充满整个装置,再点燃D处酒精灯,连接上E装置。
Cl2通过C瓶后再进入D。
D装置的硬质玻管内盛有炭粉,发生化学反应,其产物为CO2和HCl。
试写出D中化学方程式:
,
⑵在E处,紫色石蕊试液的颜色由紫色变为红色,再变为无色,为什么?
。
⑶D处反应完毕后,关闭旋塞K,移去酒精灯,但由于余热的作用,A处仍有Cl2产生,此时B中的现象是,B的作用是。
《第二单元钠、镁及其化合物》导学
【学海导航】
一、钠的原子结构及性质
结构
钠原子最外层只有一个电子,化学反应中易失去电子而表现出强还原性。
物理性质
质软、银白色,有金属光泽的金属,具有良好的导电导热性,密度比水小,比煤油大,熔点较低。
化学
性质
与非金
属单质
钠在常温下切开后表面变暗:
4Na+O2=2Na2O(灰白色)
点燃
钠在氯气中燃烧,黄色火焰,白烟:
2Na+Cl2====2NaCl
与
化合物
与水反应,现象:
浮、游、球、鸣、红2Na+2H2O=2NaOH+H2↑
与酸反应,现象与水反应相似,更剧烈,钠先与酸反应,再与水反应。
与盐溶液反应:
钠先与水反应,生成NaOH,H2,再考虑NaOH与溶液中的盐反应。
如:
钠投入CuSO4溶液中,有气体放出和蓝色沉淀。
2Na+2H2O+CuSO4===Cu(OH)2↓+Na2SO4+H2↑
700~800oC
与某些熔融盐:
4Na+TiCl4========4NaCl+Ti
存在
自然界中只能以化合态存在
保存
煤油或石蜡中,使之隔绝空气和水
制取
通电
2NaCl(熔融)====2Na+Cl2↑
用途
1、钠的化合物2、钠钾合金常温为液体,用于快中子反应堆热交换剂
3、作强还原剂4、作电光源
二、碳酸钠与碳酸氢钠的性质比较
碳酸钠(Na2CO3)
碳酸氢钠(NaHCO3)
俗名
纯碱、苏打
小苏打
溶解性
易溶(同温下,溶解度大于碳酸氢钠)
易溶
热稳定性
稳定
2NaHCO3△Na2CO3+CO2↑+H2O
碱性
碱性(相同浓度时,碳酸钠水溶液的PH比碳酸氢钠的大)
碱性
与
酸
盐酸
Na2CO3+2HCl=2NaCl+H2O+CO2↑
NaHCO3+HCl=NaCl+H2O+CO2↑
碳酸
Na2CO3+H2O+CO2=2NaHCO3
不能反应
与
碱
NaOH
不能反应
NaHCO3+NaOH=Na2CO3+H2O
Ca(OH)2
Na2CO3+Ca(OH)2=CaCO3+2NaOH
产物与反应物的量有关
三、镁的性质
物理性质
银白色金属,密度小,熔沸点较低,硬度较小,良好的导电导热性
化学性质
与O2
点燃
2Mg+O2====2MgO
与其他
非金属
点燃
点燃
Mg+Cl2====MgCl2,3Mg+N2====Mg3N2
与氧化物
点燃
2Mg+CO2====2MgO+C
与酸
Mg+2HCl=MgCl2+H2↑
制取
MgCl2+Ca(OH)2=Mg(OH)2↓+CaCl2Mg(OH)2+2HCl=MgCl2+2H2O
通电
HCl
MgCl2•6H2O====MgCl2+6H2O↑MgCl2(熔融)=====Mg+Cl2↑
四、侯氏制碱法
向饱和食盐水中通入足量氨气至饱和,然后在加压下通入CO2,利用NaHCO3溶解度较小,析出NaHCO3,将析出的NaHCO3晶体煅烧,即得Na2CO3。
五、电解质和非电解质
电解质
非电解质
定义
溶于水或熔化状态下能导电的化合物
溶于水和熔化状态下都不能导电的化合物
物质种类
大多数酸、碱、盐,部分氧化物
大多数有机化合物,CO2、SO2、NH3等
能否电离
能
不能
实例
H2SO4、NaOH、NaCl、HCl等
酒精,蔗糖,CO2,SO3等
六、离子方程式的书写方法:
写——写出反应的化学方程式;
拆——把易溶于水,易电离的物质拆成离子形式
删——将不参加反应的离子从方程式两端删去。
查——检查方程式两端各元素的原子个数和电荷数是否相等。
练习
1、在pH=1的溶液中,可以大量共存的离子是()
A、K+、Na+、SO42—、SO32—B、NH4+、Mg2+、SO42—、Cl—
C、Na+、K+、HCO3—、Cl—D、K+、Na+、OH—、NO3—
2、能用离子方程式H++OH-=H2O表示的反应是()
A、稀醋酸和稀氨水反应B、稀硫酸和烧碱溶液反应
C、稀盐酸和氢氧化铜反应D、稀硫酸和氢氧化钡溶液反应
3、下列离子在溶液中因发生氧化还原反应而不能大量共存的是()
A、H+、I-、Br2、Na+B、Ag+、NO3-、Cl-、K+
C、K+、Ba2+、OH-、SO42-D、Cu2+、NH4+、Br-、OH-
4、下列反应的离子方程式错误的是()
A、向碳酸氢钙溶液中加过量氢氧化钠
Ca2++2HCO3-+2OH-=CaCO3↓+2H2O+CO32-
B、等体积等物质的量浓度的氢氧化钡溶液与碳酸氢铵溶液混合
Ba2++2OH-+NH4++HCO3-=BaCO3↓+NH3·H2O+H2O
C、氢氧化铝与足量盐酸反应Al(OH)3+3H+=Al3++3H2O
D、过量CO2通入氢氧化钠溶液中CO2+2OH-=CO32-+H2O
5、下列离子方程式正确的是()
A、碳酸氢钠溶液与少量石灰水反应
HCO3-+Ca2++OH-=CaCO3↓+H2O
B、氯化铵与氢氧化钠两种浓溶液混合加热OH-+NH4+△H2O+NH3↑
C、氢氧化镁与稀硫酸反应H++OH-=H2O
D、碳酸钠溶液与盐酸反应Na2CO3+2H+==2Na++H2O+CO2↑
6、能正确表示下列化学反应的离子方程式的是()
A、氢氧化钡溶液与盐酸的反应OH-+H+=H2O
B、澄清的石灰水与稀盐酸反应Ca(OH)2+2H+=Ca2++2H2O
C、铜片插入硝酸银溶液中Cu+Ag+=Cu2++Ag
D、碳酸钙溶于稀盐酸中CaCO3+2H+=Ca2++H2O+CO2
7、在溶液中能大量共存,若加入OH-就有沉淀析出,若加入H+就能放出气体的是()
A、Mg2+、Na+、Cl-、CO32-B、Ba2+、K+、OH-、NO3-
C、H+、Al3+、NH4+、SO42-D、Na+、Ca2+、Cl-、HCO3-
8、只能表示一个化学反应的离子方程式为()
A、BaCO3+2CH3COOH==Ba2++CO2↑+H2O+2CH3COO-
B、Ba2++2OH-+2H++SO42-==2H2O+BaSO4↓
C、CH3COOH+OH-==CH3COO-+H2O
D、Fe3++3NH3•H2O==Fe(OH)3↓+3NH4+
9、离子方程式BaCO3+2H+==CO2↑+H2O+Ba2+中的H+不能代表的物质是()
①HCl②H2SO4③HNO3④NaHSO4⑤CH3COOH
A、①③B、①④⑤C、②④⑤D、①⑤
10、下列反应属于离子反应的是()
A、H2和O2反应生成水B、锌片投入稀硫酸中
C、KClO3和MnO2混合共热制O2D、CuSO4溶液中加入NaOH溶液
11、在强酸性溶液中可发生如下反应:
2Mn2++5R2O8x-+8H2O==16H++10RO42-+2MnO4-,这个反应可定性地检验Mn2+的存在。
在反应中充当氧化剂的R2O8x-中,x的值是()
A、0B、1C、2D、3
12、写出下列反应的离子方程式:
(1)石灰石溶于稀硝酸
(2)电解氯化钠的水溶液
(3)氧化铜溶于氢溴酸
(4)氯气通入水中
(5)氯气通入氢氧化钠溶液中
13、在反应2MnO4-+5H2S+6H+==2Mn2++5S↓+8H2O中,电子转移的总数为,还原剂为,还原产物为,当反应中有80gS析出时,有molMnO4-被,同时有gH2S被。
14、某溶液中可能含有NH4+,Ba2+,Mg2+,Ag+,OH-,SO42-,CO32-中的某几种,现用该溶液做以下实验:
①取此溶液少许,加入足量盐酸无明显现象;②另取少许加入足量浓氢氧化钠溶液,有白色沉淀生成;③将②中沉淀过滤,取滤液微热,有无色刺激性气味气体放出,该气体能使湿润的红色石蕊试纸变蓝。
⑴由此推断,该溶液中肯定有离子,肯定无离子。
⑵写出有关反应的离子方程式
15、在含有35.8gNa2CO3和NaHCO3溶液内,加入1mol/L的盐酸700ml,反应完全后可以生成8.96LCO2(标准状况)。
问:
⑴其中______过剩;溶液中Na2CO3有______g;
⑵若在上述溶液中加1mol/L的盐酸450ml,反应完全后,可生成标准状况下CO2L。
三、实验题
16、据图提供的仪器装置,完成提纯并测定Na2CO3样品的纯度(其中含NaHCO3杂质)请回答下列问题:
实验一:
测定Na2CO3样品中NaHCO3的分解放出的CO2的体积(不考虑溶于水)。
(1)装置的正确顺序是。
(2)完成实验一尚缺少的仪器是。
(3)产生的气体从装置④的端进入,从装置⑤中端进入。
实验二:
测定经实验一后的残留固体物质与盐酸反应放出的CO2的体积。
(4)应将实验一的装置作哪些调整?
(5)实验一不再产生气体时,通过量筒内的水位读数折算成标准状况下产生aLCO2,实验二中加盐酸无气体产生时,通过量筒内水位读数折算成标准状况下产生bLCO2,则样品中Na2CO3纯度的实验值为。
专题3从矿物到基础材料
第一单元从铝土矿到铝合金
学海导航:
化学研究和应用的一个重要目标就是开发和利用自然界中一切可能的物质资源,为人类生存和社会发展提供必要的物质基础。
本专题以自然界的一些矿物为例,介绍了如何利用化学变化实现物质间的转化,并介绍了这些产物在我们日常生活和社会发展中的重要作用。
让我们从科学、技术和社会相互影响的角度,体会化学在综合利用自然资源中的作用。
1.氧化铝(Al2O3):
典型的两性氧化物,既能溶于强酸,又能溶于强碱
Al2O3+6H+=2Al3++3H2O Al2O3+2OH-=2AlO2-+H2O
用途:
(1)耐火材料(Al2O3熔点高)
(2)冶炼金属铝
2.氢氧化铝Al(OH)3:
典型的两性氢氧化物,既能溶于强酸,又能溶于强碱
Al(OH)3+3H+=Al3++3H2O Al(OH)3+OH-=AlO2-+2H2O
Al3+、AlO2-、Al(OH)3之间的关系可用下式表示
从铝土矿中提取铝的过程中的的化学方程式
灼烧
通电
Al2O3+2NaOH=2NaAlO2+H2O
NaAlO2+CO2+2H2O=Al(OH)3+NaHCO3
2Al(OH)3=====Al2O3+3H2O
2Al2O3=====4Al+3O2↑
3.硫酸铝钾
(1)明矾:
化学式KAl(SO4)2·12H2O(十二水合硫酸铝钾),无色晶体,易溶于水。
(2)明矾净水原理:
明矾溶于水发生水解反应,生成Al(OH)3胶体,吸附水中的杂质,使水澄清。
4.铝
(1)铝在常温下能很快被氧化,形成致密的氧化膜,因而具有一定的抗腐蚀性。
(2)跟酸的反应
非氧化性酸:
2Al+6HCl=2AlCl3+3H2↑
强氧化性酸:
常温下铝遇浓硫酸或浓硝酸,会在铝表面生成致密的氧化膜而发生钝化。
(3)跟碱的反应
铝能和强碱溶液反应。
该反应可理解为铝先和强碱溶液中的水反应生成氢氧化铝,氢氧化铝再和强碱反应生成偏铝酸盐:
2Al+6H2O=2Al(OH)3+3H2↑ Al(OH)3+NaOH=NaAlO2+2H2O
简写为:
2Al+2H2O+2NaOH=2NaAlO2+3H2↑
(4)与氧化物的反应:
铝热反应:
2Al+Fe2O3====Al2O3+2Fe
高温
2Al+Cr2O3====Al2O3+2Cr
高温
特点:
放出大量热,使生成的金属呈液态。
本质:
铝从金属氧化物中夺取氧,表现出很强的还原性。
应用:
焊接钢轨和冶炼某些难熔金属(如V、Cr、Mn等)。
习题精练:
一.选择题
1.将钠、镁、铝各0.3mol分别放入100mL1mol·L-1的盐酸中,同温同压下产生的气体体积比是
A、1︰2︰3B、6︰3︰2C、3︰1︰1D、1︰1︰1
2.铝分别与足量的稀盐酸和氢氧化钠溶液反应,当两个反应放出的气体在相同状况下体积相等时,反应中消耗的HCl和NaOH物质的量之比为
A.3:
1B.2:
1C.1:
1D.1:
3
3.将表面已完全钝化的铝条,插入下列溶液中,不会发生反应的是
A.稀硝酸B.稀盐酸C.硝酸铜D.氢氧化钠
4.把Ba(OH)2溶液滴入明矾溶液中,使SO42-全部转化为BaSO4沉淀,此时铝元素的主要存在形式是
A、Al3+B、Al(OH)3C、AlO2-D、Al3+和Al(OH)3
5.铝合金因坚硬、轻巧、美观、洁净、易于加工而成为新型建筑装潢材料,主要用于制作窗框、卷帘门、防护栏等。
下列与这些用途无关的性质是
A.不易生锈B.导电性好C.密度小D.强度高
6.等体积、等物质的量浓度的硫酸、氢氧化钠溶液分别放在甲、乙两烧杯中,各加等质量的铝,生成氢气的体积比为5︰6,则甲、乙两烧杯中的反应情况可能分别是
A甲、乙中都是铝过量B甲中铝过量、乙中碱过量
C甲中酸过量、乙中铝过量D甲中酸过量、乙中碱过量
7.某些化学试剂可用于净水。
水处理中使用的一种无机高分子混凝剂的化学式可表示为[Al2(OH)nClm·yH2O]X,式中m等于
A.3-n B.6-n C.6+n D.3+n
8.铝热剂中铝的作用是
A.催化剂 B.氧化剂 C.还原剂 D.填充剂
9.将一定质量的Mg、Zn、Al混合物与足量稀H2SO4反应,生成H22.8L(标准状况),原混合物的质量可能是
A.2gB.4gC.8gD.10g
10.甲、乙两烧杯中各盛放有100mL3mol·L-1的盐酸和氢氧化钠溶液,向两烧杯中分别加入等质量的铝粉,反应结束后测得生成的气体体积比为甲∶乙=1∶2,则加入铝粉的质量为
A.5.4gB.3.6gC.2.7gD.1.8g
二.填空题
11.请写出下列反应的离子方程式
①金属铝溶于盐酸中