碱金属腐蚀分析.docx
《碱金属腐蚀分析.docx》由会员分享,可在线阅读,更多相关《碱金属腐蚀分析.docx(11页珍藏版)》请在冰豆网上搜索。
碱金属腐蚀分析
碱金属腐蚀分析
元素迁移
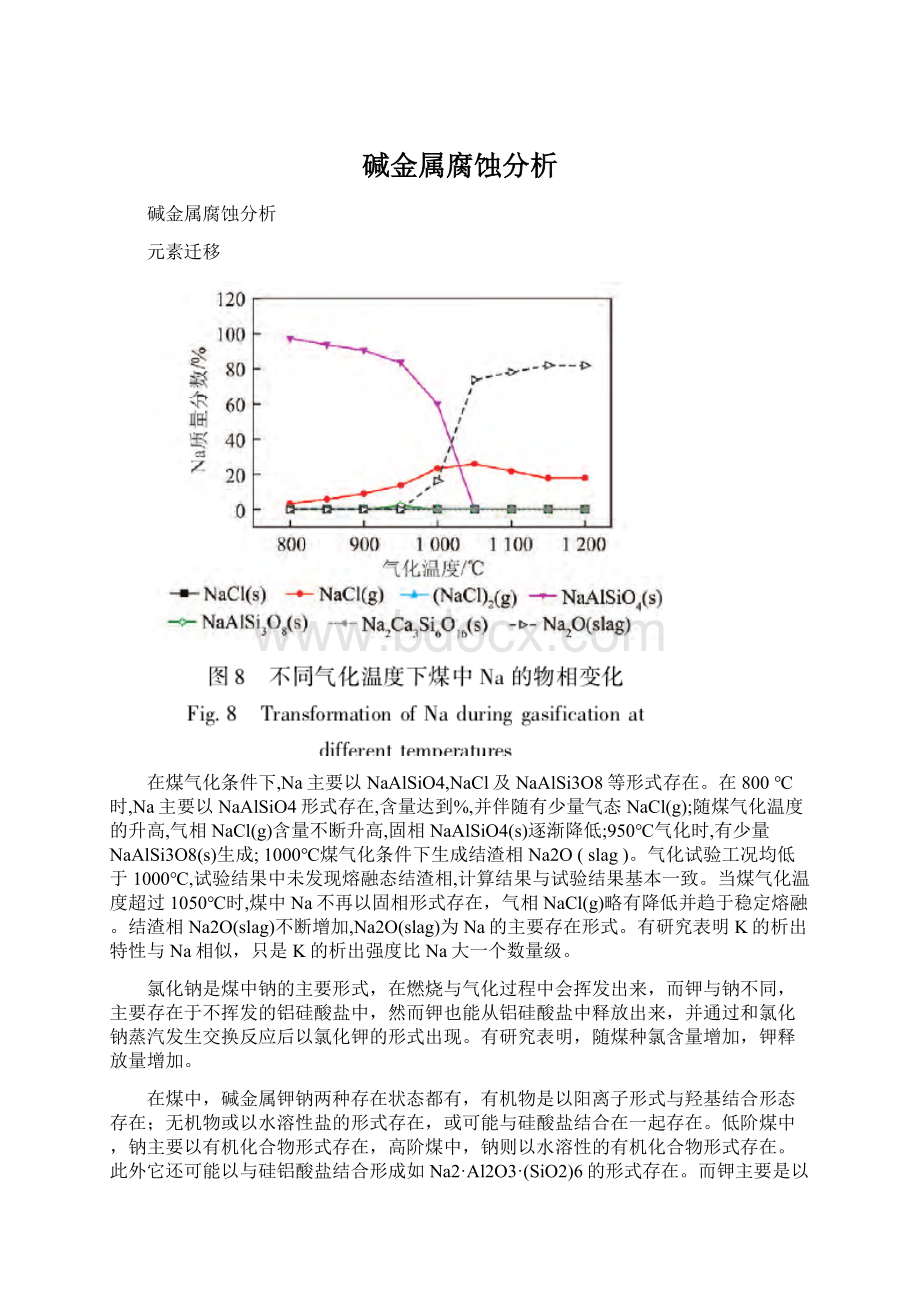
在煤气化条件下,Na主要以NaAlSiO4,NaCl及NaAlSi3O8等形式存在。
在800℃时,Na主要以NaAlSiO4形式存在,含量达到%,并伴随有少量气态NaCl(g);随煤气化温度的升高,气相NaCl(g)含量不断升高,固相NaAlSiO4(s)逐渐降低;950℃气化时,有少量NaAlSi3O8(s)生成;1000℃煤气化条件下生成结渣相Na2O(slag)。
气化试验工况均低于1000℃,试验结果中未发现熔融态结渣相,计算结果与试验结果基本一致。
当煤气化温度超过1050℃时,煤中Na不再以固相形式存在,气相NaCl(g)略有降低并趋于稳定熔融。
结渣相Na2O(slag)不断增加,Na2O(slag)为Na的主要存在形式。
有研究表明K的析出特性与Na相似,只是K的析出强度比Na大一个数量级。
氯化钠是煤中钠的主要形式,在燃烧与气化过程中会挥发出来,而钾与钠不同,主要存在于不挥发的铝硅酸盐中,然而钾也能从铝硅酸盐中释放出来,并通过和氯化钠蒸汽发生交换反应后以氯化钾的形式出现。
有研究表明,随煤种氯含量增加,钾释放量增加。
在煤中,碱金属钾钠两种存在状态都有,有机物是以阳离子形式与羟基结合形态存在;无机物或以水溶性盐的形式存在,或可能与硅酸盐结合在一起存在。
低阶煤中,钠主要以有机化合物形式存在,高阶煤中,钠则以水溶性的有机化合物形式存在。
此外它还可能以与硅铝酸盐结合形成如Na2·Al2O3·(SiO2)6的形式存在。
而钾主要是以K2O·(Al2O3)3·(SiO2)6·H2O和K2O·Al2O3·(SiO2)6的硅铝酸盐形式存在。
因此在热转化过程中,煤中的钾很难释放到气相中。
原煤中钠的含量要高于钾,并且原煤中钠的存在形态的反应性高于钾存在形态的反应性。
挥发性K是不断迁移的,部分K以气态形式释放,如KCl(g)、K2S04(g)、KOH(g)、K(g);其他以硅酸钾、硅铝酸钾和硫酸钾的形式存在于灰分中。
冷凝过程中,气态钾冷凝在飞灰颗粒上或者经过硫酸化、炭化形成气溶胶或小的飞灰颗粒,最终造成颗粒聚团、结渣。
温度高于500c时,无机钾因蒸汽压升高而挥发出来。
Na的析出特性与K相似,只是Na的析出强度比K小一个数量级。
C1主要以离子的形式存在。
在600°C以上,C1以碱金属氯化物形式挥发进入气相,这是C1进入气相的主要形式。
它可促进碱金属的气化,形成的气态碱金属氯化物是稳定的挥发物,从而对碱金属起到运输的作用,对积灰结澄的作用相当重要。
腐蚀类型及反应机理
(1)碱金属氯化物腐烛
完全燃烧过程中,由于炉内的高温以及K、Na等碱金属的高挥发性,碱金属氯化物会以气相形态进入烟气中,当烟气遇到低温管壁时会凝结下来形成积灰。
气化过程中的氯化物腐蚀
而气化条件下含有大量H2和CO,生成的FeO氧化膜多孔、松脆且极易脱落,对受热面的腐蚀严重。
(2)HCl和Cl2腐蚀
HCl的来源(准东)
HCl随温度变化对金属管壁的腐蚀强度是呈波浪状的。
露点以下腐烛严重;露点以上260c以下,腐烛强度减弱;260以上,因高温剧烈反应而腐烛加剧。
刘纪福[39]等研究了Cl2干、湿两种状态下金属的年腐烛量的情况,实验结果表明壁温相同状态下,水分的存在,促进了cl腐烛。
(3)硫及其化合物腐烛
1.还原气氛下,烟气中容易形成H2S而非S02,H2S在C、CO存在的条件下易与金属氧化层和金属基体反应,生成FeS,破坏致密氧化层的保护作用,使腐蚀性气体自由出入,加速腐烛。
2.硫元素还会以硫化钠、硫化钾、硫化亚铁的形式存在于积灰中,对氧化层造成腐烛。
3.硫酸盐的腐蚀
鲁奇炉认为硫酸盐可能是导致夹套内壁腐蚀减薄的主要原因之一。
在还原性气氛下,并同时存在CO2时,会使碱金属硫酸盐分解生成含硫化合物,这些含硫化合物在碱金属硫酸盐、铁和铁的化合物共同作用下会生成复杂的低熔点化合物,如可能生成复杂的复合式硫酸盐和焦硫酸盐。
富含碱金属硫酸盐且在SO3分压相对较高的情况下,在金属表面易形成熔盐层,使正常的保护性氧化物发生酸助熔。
也有学者提出先是通过反应生成焦硫酸钠和焦硫酸钾,而焦硫酸钠和焦硫酸钾非常容易侵蚀金属表面的氧化物保护膜,具体见反应:
上述反应发生的温度在399~482C之间,SO3的来源主要两个:
一是硫铁矿硫被氧化生成SO2,SO2被灰中的一些成分催化氧化成SO3;另一个来源是灰成分中硫酸钙,硫酸镁等受热易分解产生SO3。
四、煤质比较
五、材料分析
秸秆燃料锅炉受热面工作温度低于500℃时,选用价格最低的20G管材;锅炉受热面工作温度低于550℃,选用价格稍高一点的12Cr1MoVG管材;工作温度低于600℃时,选用价格更高的10Cr9Mo1VNb管材;当锅炉受热面工作温度高于600℃时,只能选用价格更高的1Cr19Ni11Nb管材。
五、结论分析
K\NA的不同
K对积灰结渣的作用主要表现在两个方面:
一是它的化合物的高挥发性,使其更容易进入气相,增大其化合物的蒸汽压,从而更容易的参加反应;二是它的化合物普遍具有低灰溶点的特性。
任何形态的碱金属化合物都与Si02反应生成低熔点化合物。
一、煤质分析报告:
实验室编号
.
来样编号
SampleNo
Mar
%
工业分析ProximateAnalysis
St,ad
%
St,d
%
Mad%
Aad%
Ad%
Vad%
Vd%
Vdaf%
FCd%
CRC
2017-093
塔什店矿
4
2017-094
华安矿
4
2017-095
秦华矿
7
2017-096
金川矿
3
实验室编号
.
来样编号
SampleNo
Qgr,ad
MJ/kg
Qgr,d
MJ/kg
Qnet,ar
MJ/kg
Cad
%
Cd
%
Had
%
Hd
%
Nad
%
Nd
%
Oad
%
Od
%
HGI
2017-093
塔什店矿
60
2017-094
华安矿
52
2017-095
秦华矿
47
2017-096
金川矿
73
实验室编号
.
来样编号
SampleNo
Clad
%
Cld
%
Fad
g/g
Fd
g/g
Asad
g/g
Asd
g/g
Pad
%
Pd
%
2017-093
塔什店矿
158
161
1
1
2017-094
华安矿
227
232
2
2
2017-095
秦华矿
59
60
1
1
2017-096
金川矿
253
257
1
1
实验室编号
.
来样编号
SampleNo
灰熔融性℃(弱还原)
灰成分Compositionofash%
DT
ST
HT
FT
SiO2
Al2O3
Fe2O3
TiO2
CaO
MgO
K2O
Na2O
MnO2
SO3
P2O5
2017-093
塔什店矿
1230
1270
1280
1290
2017-094
华安矿
1330
1430
1440
1460
2017-095
秦华矿
1320
1430
1440
1470
2017-096
金川矿
1440
>1500
>1500
>1500
准东煤
准东沙尔湖煤
沙尔湖煤属于高钠高氯煤,煤灰中含有较高的Na2O,煤中Na主要以水溶性Na存在,达到%,其次为醋酸铵溶态Na,占%,其余为盐酸溶态Na及不溶态Na,分别%和%。
煤中氯含量高达1.132%。
灰分比较(本案取各煤种最高值)
天业准东
Na2O:
K2O:
CL:
(ad)(ar)
KCl-ZnCl2混合盐是一种强腐蚀介质,混合后共晶点约为250℃,在650℃反应温度下已呈熔融态,因此材料的腐蚀主要在熔融的氯化物中进行,与相同材料的高温氧化相比,腐蚀速度加快,能形成非常厚的腐蚀产物。
在650℃条件下,KCl-ZnCl2混合盐已呈熔融状态,涂层表面完全置于熔盐内,由于氧在熔盐中的溶解度和扩散系数都很有限,熔盐内实际上是一个低氧势环境,氧的供应极不充分,结果增加了Cr2O3保护性氧化膜的稳定性,使材料的腐蚀速率能够随Cr含量增加而得以显著降低。
事实上,在垃圾焚烧工艺流程中如果添加适当的添加剂,由于其与氧发生反应而造成低氧势环境,往往可以据此大大减低材料的腐蚀程度,尤其是那些形成Cr2O3型保护膜的合金的耐蚀性得以显著提高。
与Fe、Cr的氧化物相比,Ni在氯化物熔盐中表现得最稳定。
由于NiCl2具有很高的熔点(约为1030℃),并且NiO极易在氯化盐熔融盐中达到饱和状态,因此NiO在氯化环境中比Fe、Cr等具有更好的耐蚀性。
由于钛与氢原子容易生成氢化物使材料韧性降低,故不选用含钦合金做为覆盖层。
锅炉燃料普遍含S,在燃烧过程中S几乎都氧化成SO2,其中约有6%~7%的SO2进一步氧化成SO3。
高温下,SO2和SO3均呈气态。
反应过程如下:
FeS2=FeS+[S]
2H2S+SO2=2H2O+3[S]
Fe+[S]=FeS
FeO+H2S=FeS+H2O
3FeS+5O2=Fe3O4+3SO2
2SO2+O2=2SO3
硫化物型腐蚀所生成的FeS,熔点是1195℃,在温度较低时一般不会发生氧化反应,当温度较高时,FeS与O2就发生缓慢氧化反应而生成黑色的磁性Fe3O4和SO2,新生成的SO2在管壁Fe3O4的催化作用下进一步被氧化成为SO3。
反应后腐蚀产物中含有FeS、Fe3O4、SO2、SO3等成分,其中FeS较疏松,不起保护作用,因而腐蚀会一直进行下去[5]。
所以当H2S的浓度越高,壁温越高,腐蚀速度越快。
硫化物型腐蚀持续发展的条件是:
1)铁矿颗粒能到达壁面;2)近壁附近是还原性气氛;3)有较高的壁面温度。
一般认为应大于350℃。