中考化学专题练习溶液.docx
《中考化学专题练习溶液.docx》由会员分享,可在线阅读,更多相关《中考化学专题练习溶液.docx(55页珍藏版)》请在冰豆网上搜索。
中考化学专题练习溶液
溶液
一、选择题
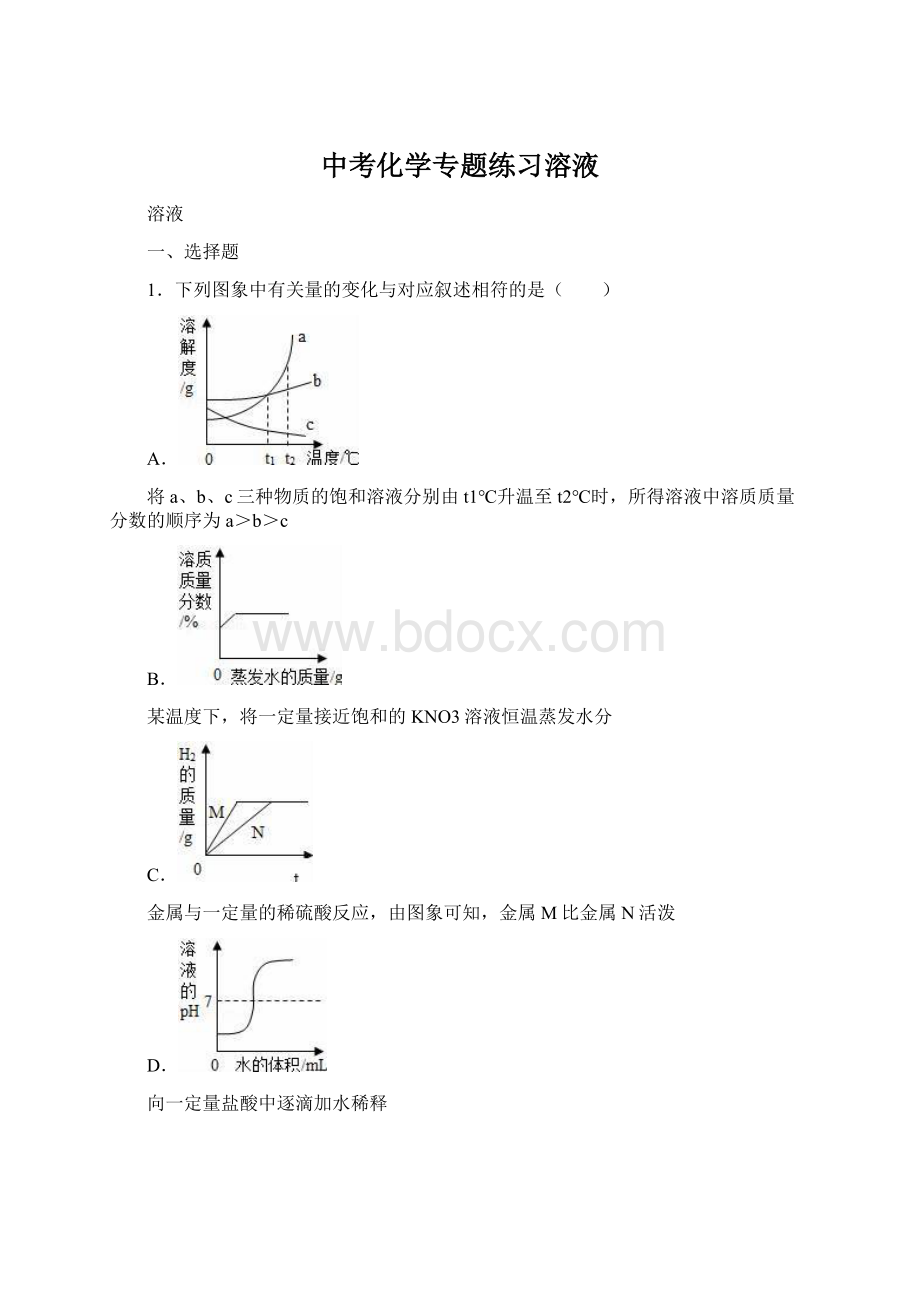
1.下列图象中有关量的变化与对应叙述相符的是( )
A.
将a、b、c三种物质的饱和溶液分别由t1℃升温至t2℃时,所得溶液中溶质质量分数的顺序为a>b>c
B.
某温度下,将一定量接近饱和的KNO3溶液恒温蒸发水分
C.
金属与一定量的稀硫酸反应,由图象可知,金属M比金属N活泼
D.
向一定量盐酸中逐滴加水稀释
2.图1是甲、乙、丙三种固体物质(不含结晶水)的溶解度曲线,图2是30℃时,取其中两种固体各1g分别放进盛有10g水的两支试管中,充分振荡后的溶解情况,下列说法正确的是( )
A.甲物质的溶解度比乙物质的溶解度大
B.加入试管1的固体是丙
C.向烧杯中加入NH4NO3固体后,试管2中一定有晶体析出
D.将30℃时甲、乙、丙三种物质的饱和溶液降温至20℃,所得溶液中溶质的质量分数的大小关系是乙>甲=丙
3.如图是a、b、c三种物质的溶解度曲线,下列说法错误的是( )
A.t2℃时a、b、c三种物质的溶解度由大到小的顺序是a>b>c
B.P点表示t1℃时,a、c两种物质的溶解度相等
C.将c的饱和溶液变为不饱和溶液,可采用降温的方法
D.t2℃时,将30ga物质加入到50g水中充分搅拌,得到80ga的饱和溶液
4.甲、乙、丙三种固体物质的溶解度曲线如图所示.下列叙述错误的是( )
A.t1℃时,将等质量的甲、乙分别配成饱和溶液,所得溶液质量:
甲>乙
B.将t1℃时甲、丙的饱和溶液升温到t2℃,两种溶液中溶质的质量分数相等
C.将t2℃时甲的饱和溶液变为t3℃时甲的饱和溶液,可以采用蒸发水的方法
D.将t3℃时三种物质的饱和溶液恒温蒸发等量水后,析出溶质的质量:
甲>乙>丙
5.氯化钾的溶解度曲线如图所示,下列说法正确的是( )
A.升高温度可使接近饱和的氯化钾溶液变为饱和溶液
B.10℃时,65.5g氯化钾的饱和溶液中加入5g氯化钾,充分溶解后将温度升高到40℃,得到70g氯化钾饱和溶液
C.50g水中加入20g氯化钾充分溶解,形成氯化钾饱和溶液
D.40℃时,氯化钾饱和溶液中溶质的质量分数为40%
6.如图是甲、乙、丙三种物质的溶解度曲线.下列说法错误的是( )
A.t1℃时,三种物质的溶解度是丙>乙>甲
B.t2℃时,甲和丙的饱和溶液溶质质量分数相等
C.三种物质的溶解度均随温度的升高而增大
D.当甲中混有少量的乙时可用冷却其热饱和溶液的方法提纯
7.甲、乙两种固体物质(不含结晶水)的溶解度曲线如图所示.下列说法正确的是( )
A.甲物质的溶解度大于乙物质的溶解度
B.t1℃时,甲、乙两种物质各50g分别加入到100g水中,充分溶解,得到的溶液质量都是140g
C.t2℃时,甲溶液的溶质质量分数一定大于乙溶液的溶质质量分数
D.t2℃时甲、乙的饱和溶液降温到t1℃时,析出晶体的质量甲一定大于乙
8.甲、乙两种物质的溶解度曲线如图所示.下列说法中正确的是( )
A.t1℃时,甲饱和溶液的溶质质量分数大于乙饱和溶液
B.t2℃时,甲、乙饱和溶液的溶质质量分数都为30%
C.t2℃时,甲、乙的饱和溶液分别降温至t1℃,甲溶液饱和,乙溶液不饱和
D.t2℃时,质量相同的甲、乙饱和溶液分别升温至t3℃,为达饱和状态,需加入甲的质量大于乙
9.如图是甲、乙两种固体物质在水中的溶解度曲线,下列说法不正确的是( )
A.10℃时,甲、乙两种物质的饱和溶液浓度相同
B.保持20℃,蒸发溶剂可使接近饱和的乙溶液变成饱和溶液
C.30℃时,将40g甲物质加入50g水中,充分溶解后溶液的质量为80g
D.10℃时,将两种饱和溶液升温至30℃,溶液中溶质的质量分数都增大
10.如图为甲、乙两种盐的溶解度曲线,下列说法正确的是( )
A.甲、乙两种物质的溶解度都不相等
B.将接近饱和的甲溶液变为饱和溶液,可采用蒸发或降温的方法
C.t1℃时,甲、乙两种物质的饱和溶液中,溶质的质量分数均为15%
D.t2℃时,将30克乙物质放入100克水中,所得溶液的质量为130克
11.甲、乙两种固体物质的溶解度曲线如图所示,下列说法正确的是( )
A.t2℃时,向100g甲中加入100g水后形成溶液的质量为200g
B.t1℃时,甲、乙两种物质的溶解度相等
C.甲的溶解度比乙大
D.将t2℃时甲、乙的饱和溶液分别降到t1℃时,两溶液的溶质质量分数相等
12.甲、乙两种不含结晶水的固体物质的溶解度曲线如图,下列说法中正确的是( )
A.甲的溶解度比乙大
B.t2℃时,甲、乙的两种溶液中溶质的质量分数相等
C.t1℃时,将50g水加入15g甲物质中,可得到65g溶液
D.要使接近饱和的乙溶液转化为饱和溶液,可采用蒸发溶剂的方法
13.甲、乙两种物质的溶解度曲线如图所示,下列说法正确的是( )
A.甲的溶解度大于乙的溶解度
B.两种物质的溶解度都随温度升高而增大
C.t1℃时,甲、乙两种物质的溶液中,溶质质量分数相等
D.t2℃时,甲的饱和溶液溶质质量分数为50%
14.如图是甲、乙、丙三种固体物质溶解度曲线,下列叙述正确的( )
A.t2℃时乙物质的饱和溶液溶质的质量分数为20%
B.t2℃时三种物质溶解度关系为:
甲>乙>丙
C.随温度的升高,甲、乙、丙三种物质溶解度都增大
D.甲物质的饱和溶液从t1℃升温到t3℃时,溶质质量分数增大
二、填空题
15.如图是甲、乙两种固体物质的溶解度曲线.
(1)由图可获得的一条信息是 .
(2)若乙中混有少量甲,提纯乙的方法是 .
(3)t2℃时,将不饱和的甲溶液,转化成该温度下的饱和溶液的一种方法是 .变化过程中,溶质的质量分数 (选填“增大”、“减小”或“不变”).
(4)将等质量的甲、乙两种物质的溶液由t2℃降温至t1℃时,析出晶体的质量 (选序号).
A.甲>乙B.甲<乙C.无法确定.
16.如图为甲、乙两种固体物质在水中的溶解度曲线,据此回答下列问题:
(1)在40℃时甲、乙两种固体物质的溶解度 (填“相同”或“不同”).
(2)两种物质中 物质的溶解度随温度的升高而降低.(填“甲”或“乙”)
(3)若要从甲的60℃的饱和溶液中得到甲(固态),应该采用 的方法.(填序号)
A.升高温度到70℃B.降低温度C.加入一定量的水.
17.如图是A、B、C三种固体物质在水中的溶解度曲线图,请回答下列问题:
(1)t1℃时A物质的溶解度是 克.
(2)当A物质中混有少量B物质吋,通常可采用 的方法提纯A物质.
(3)将t1℃时A、B、C三种物质饱和溶液的温度升高到t2℃后(升温过程中溶剂的质量不变),三种溶液中溶质的质量分数由大到小的顺序是 (填字母).
18.A、B两种固体物质的溶解度曲线如图所示,请根据曲线图回答下列问题.
(1)现有常温下B的不饱和溶液,在只要求保持其中溶剂质量不变的条件下,将其变成饱和溶液,可行的方法有 .
(2)现有一杯t1℃时含A、B两种物质且均饱和的混合溶液,若要从中分离出少量A的纯净物,其操作方法是 .
(3)下列说法正确的是 .
①t2℃时,A的溶液中溶质的质量分数一定比B的溶液中溶质的质量分数大;
②将t2℃A、B的饱和溶液分别降温至t1℃,此时两溶液中的质量分数相等;
③在t1℃时,用两份等量的水分别配制成A、B的饱和溶液,这两种溶液的质量相等;
④在t2℃时,用等量的A、B分别配制成两种饱和溶液,测得其质量依次为m1g和m2g,则m1<m2.
19.甲、乙两种固体物质的溶解度曲线如图所示.
(1)t1℃时甲物质的溶解度是 g;乙物质的溶解度随着温度的升高而 (填“增大“或“减小”);
(2)t2℃时甲物质的饱和溶液中溶质的质量分数为 ;将t2℃时甲、乙两种物质的饱和溶液分别降温至t1℃,溶液中溶质质量分数大小关系是:
甲 (填“<”、“=”或“>”)乙.
20.淮安市某盐化厂生产的碳酸钠粗产品中含有少量氯化钠.碳酸钠和氯化钠的溶解度与温度的关系如图所示,回答下列问题:
(1)t1℃时碳酸钠与氯化钠中溶解度较大的物质是 .
(2)t1℃时碳酸钠溶液升温至t2℃,所得溶液的溶质质量分数 .(填“变大”、“变小”或“不变”).
(3)除去碳酸钠中混有少量氯化钠的方法是 .
21.如图是X、Y、Z三种固体物质的溶解度曲线图,根据曲线图回答下列问题.
(1)如果要配制相同浓度的Y、Z饱和溶液,需要把温度控制在 ℃.
(2)t1℃时,将X、Y、Z的饱和溶液都升温到t3℃,溶液仍然饱和的是 的溶液.
(3)t3℃时,将X、Y、Z的饱和溶液都降温到t1℃,溶液中溶质质量分数由小到大的顺序为 .
22.根据图中a、b、c三种固体物质的溶解度曲线,回答问题:
(1)温度为 ℃时,a和c物质的溶解度相同;
(2)要使接近饱和的a物质的溶解度变为饱和溶液,可采用的一种措施是 ;
(3)在t2℃时,75克c物质的饱和溶液中溶剂的质量是 g.
23.如图是硝酸钾和氯化钠的溶解度曲线.
(1)两种物质中.溶解度受温度影响较小的是 .
(2)使接近饱和的氯化钠溶液变为饱和溶液的一种方法是 .
(3)60℃时,硝酸钾饱和溶液中溶质、溶剂的质量比是 .
(4)60℃时,硝酸钾饱和溶液中溶有少量的氯化钠.提纯硝酸钾应采用的方法是 .
24.图是甲、乙两种固体物质的溶解度曲线,回答下列问题:
(1)当温度为 ℃时,甲、乙两种物质的溶解度相等;
(2)T3℃时,在100g水中加入60g甲,形成 溶液(填“饱和”或“不饱和”).此时溶液中溶质的质量分数为 (保留一位小数)
三、解答题
25.根据图中a、b、c三种固体物质的溶解度曲线,回答下列问题:
(1)t2℃,a的物质的溶解度为 .
(2)t1℃时,将接近饱和的c物质的变成该物质的饱和溶液,可采用 .(任填一种方法即可)
(3)t2℃时.将a、b、c三种物质的饱和溶液,分别降溫至t1℃时,所得溶液中溶质质置分数的大小关系是 .
A.a>b>cB.b>a=cC.b>a>c.
26.如图是A、B、C三种物质的溶解度曲线,据图回答:
(1) ℃时,A和B两种物质的溶解度相同;
(2)t3℃时,将A、B、C三种物资的饱和溶液各100g,分别蒸发5g水,析出晶体最多的是 .
27.如图是A、B两种物质的溶解度曲线,请回答:
(1)在40℃时A、B的溶解度大小关系是 ;
(2)a点是A、B两条曲线的交点,其含义是 ;
(3)20℃时将20gA固体放入50g水中,充分溶解后,所得溶液的质量是 g;
(4)若A中含有少量的B杂质,提纯A的方法是 结晶.
28.甲、乙两种物质的溶解度曲线如图所示,根据图示回答下列问题:
(1)甲、乙两种物质中溶解度受温度影响不大的是 物质;
(2)P点的意义是 .
(3)t2℃时,50g甲物质加入到50g水中充分溶解,形成溶液的质量等于 g.
29.A、B、C三种固体物质在水中的溶解度曲线如图所示,请回答:
(1) ℃时,A、B两种物质在100g水中达到饱和状态时溶解的质量相等;
(2)若B中混有少量的A,最好采用 的方法提纯B;
(3)现有接近饱和的C物质溶液,使其变成饱和溶液的方法有:
①加入C物质;②恒温蒸发溶剂;③ ;
(4)t3℃时将20gA物质放入50g水中,充分搅拌,所得溶液中溶质的质量分数是 ;
(5)将t3℃时等质量的A、B、C三种物质的饱和溶液降温至t1℃时,所得溶液的质量由大到小的顺序是 .
30.如图是甲、乙两种固体物质的溶解度曲线.据图回答:
(1)P点的含义 .
(2)要使接近饱和的甲溶液变成饱和溶液,可采用的方法有 (写出一种),当甲中含有少量乙时,可采用 的方法提纯甲.
(3)30℃时,将40g甲物质放入盛有50g水的烧杯中,所得溶液溶质的质量分数为 .若烧杯内物质升温到50℃(不考虑蒸发),溶液中变化的是 (选填序号).
a.溶质的质量b.溶液的质量c.溶质的质量分数
(4)从图中还可获得的信息是 (答出一条).
溶液
参考答案与试题解析
一、选择题
1.下列图象中有关量的变化与对应叙述相符的是( )
A.
将a、b、c三种物质的饱和溶液分别由t1℃升温至t2℃时,所得溶液中溶质质量分数的顺序为a>b>c
B.
某温度下,将一定量接近饱和的KNO3溶液恒温蒸发水分
C.
金属与一定量的稀硫酸反应,由图象可知,金属M比金属N活泼
D.
向一定量盐酸中逐滴加水稀释
【考点】固体溶解度曲线及其作用;溶质的质量分数;溶质的质量分数、溶解性和溶解度的关系;金属的化学性质;酸碱溶液的稀释.
【专题】元素化合物知识型;溶液、浊液与溶解度.
【分析】A、根据a、b的溶解度随温度的升高而增大且在t1℃时a、b物质的溶解度相同,而c物质的溶解度随温度的升高低而减小进行解答;
B、根据一定温度下的饱和溶液比不饱和溶液溶质质量分数大,且温度不变,饱和溶液溶解度不变,溶质的质量分数不变进行解答;
C、根据活动性越强的金属,反应速率越快进行解答;
D、根据向酸中加入水,溶液的酸性降低,pH变大,但溶液仍呈酸性进行解答.
【解答】解:
A、a、b的溶解度随温度的升高而增大且在t1℃时a、b物质的溶解度相同,所以t1℃升温至t2℃时溶液中溶质、溶剂的质量不变,溶质的质量分数不变,则升温后a、b溶液的溶质质量分数相同,饱和溶液中溶质质量分数=
×100%,即溶解度越大质量分数也就越大;而c物质的溶解度随温度的升高低而减小,且t2℃c物质的溶解度小于t1℃ab物质的溶解度,故c物质的溶质质量分数小于ab,所以将a、b、c三种物质的饱和溶液分别由t1℃升温至t2℃时,所得溶液中溶质质量分数的顺序为a=b>c,故A错误;
B、某温度下,将一定量接近饱和的KNO3溶液恒温蒸发水分,随着水分的蒸发,溶液质量逐渐减小,而溶质质量不变,溶质质量分数变大,但是当溶液达到饱和溶液以后,由于溶解度不变,则溶质质量分数就会保持不变,故正确;
C、活动性越强的金属,反应速率越快,由图可知,M金属用的时间少,而N金属用的时间多,所以M的金属活动性大于N,故正确;
D、向酸中加入水,溶液的酸性降低,pH变大,但溶液仍呈酸性,所以溶液的pH不会大于7,故错误;
故选:
BC.
【点评】解答该题的关键是了解反应原理、关注实验过程,在分析实验过程的同时,掌握看图象的要领,即‘三点一趋势’:
起点、终点、转折点、走势.
2.图1是甲、乙、丙三种固体物质(不含结晶水)的溶解度曲线,图2是30℃时,取其中两种固体各1g分别放进盛有10g水的两支试管中,充分振荡后的溶解情况,下列说法正确的是( )
A.甲物质的溶解度比乙物质的溶解度大
B.加入试管1的固体是丙
C.向烧杯中加入NH4NO3固体后,试管2中一定有晶体析出
D.将30℃时甲、乙、丙三种物质的饱和溶液降温至20℃,所得溶液中溶质的质量分数的大小关系是乙>甲=丙
【考点】固体溶解度曲线及其作用;溶解时的吸热或放热现象;晶体和结晶的概念与现象;溶质的质量分数、溶解性和溶解度的关系.
【专题】溶液、浊液与溶解度.
【分析】A、比较物质的溶解度大小须确定温度;
B、据30℃时三种物质的溶解度分析解答;
C、向烧杯中加入NH4NO3固体后,温度降低,若降到20℃以下,才有晶体析出,高于此温度,无晶体析出;
D、据三种物质的溶解度随温度变化情况及饱和溶液中溶质的质量分数分析解答.
【解答】解:
A、比较物质的溶解度大小须确定温度,故选项说法错误;
B、30℃时三种物质只有丙的溶解度小于10g,即100g水中溶解溶质的质量小于10g,则10g水中溶解溶质的质量小于1g,所以30℃时,取其中两种固体各1g分别放进盛有10g水的两支试管中,充分振荡后有剩余固体的是丙,即试管1,正确;
C、向烧杯中加入NH4NO3固体后,温度降低,若降到20℃以下,才有晶体析出,高于此温度,则无晶体析出;所以向烧杯中加入NH4NO3固体后,试管2中不一定有晶体析出,故选项说法错误;
D、将30℃时甲、乙、丙三种物质的饱和溶液降温至20℃,甲乙溶解度减小,均析出晶体,溶质的质量减小,溶质的质量分数减小,丙溶解度增大,溶液中溶质、溶剂的质量不变,溶质的质量分数与降温前相等;饱和溶液中溶质质量分数=
×100%,即溶解度越大质量分数也就越大,20℃时乙的溶解度大于甲的溶解度大于30℃时丙的溶解度,故所得溶液中溶质的质量分数的大小关系是乙>甲>丙,故错误;
故选:
B.
【点评】明确溶解度的概念、溶解度曲线的意义,及饱和溶液中溶质的质量分数和溶解度的关系等知识,才能结合题意正确解答.
3.如图是a、b、c三种物质的溶解度曲线,下列说法错误的是( )
A.t2℃时a、b、c三种物质的溶解度由大到小的顺序是a>b>c
B.P点表示t1℃时,a、c两种物质的溶解度相等
C.将c的饱和溶液变为不饱和溶液,可采用降温的方法
D.t2℃时,将30ga物质加入到50g水中充分搅拌,得到80ga的饱和溶液
【考点】固体溶解度曲线及其作用;饱和溶液和不饱和溶液相互转变的方法.
【专题】溶液、浊液与溶解度.
【分析】根据已有的溶解度曲线的意义进行分析解答,交点表示在该温度下两种物质的溶解度相等,根据溶解度曲线可以看出物质的溶解度受温度的变化情况,结合饱和溶液和不饱和溶液的转化以及溶解度随温度的变化特点确定析出晶体的方法进行分析解答.
【解答】解:
A、据图可以看出,t2℃时a、b、c三种物质的溶解度由大到小的顺序是a>b>c,正确;
B、P点时ac的溶解度交于一点,表示t1℃时,a、c两种物质的溶解度相等,正确;
C、c的溶解度随温度的降低而增大,将c的饱和溶液变为不饱和溶液,可采用降温的方法,正确;
D、t2℃时,a的溶解度为50g,将30ga物质加入到50g水中充分搅拌,只能溶解25g,得到75ga的饱和溶液,错误;
故选D.
【点评】明确溶解度概念、溶解度曲线的意义、饱和溶液中溶质的质量分数计算与溶解度的关系,才能结合题意正确解答.
4.甲、乙、丙三种固体物质的溶解度曲线如图所示.下列叙述错误的是( )
A.t1℃时,将等质量的甲、乙分别配成饱和溶液,所得溶液质量:
甲>乙
B.将t1℃时甲、丙的饱和溶液升温到t2℃,两种溶液中溶质的质量分数相等
C.将t2℃时甲的饱和溶液变为t3℃时甲的饱和溶液,可以采用蒸发水的方法
D.将t3℃时三种物质的饱和溶液恒温蒸发等量水后,析出溶质的质量:
甲>乙>丙
【考点】固体溶解度曲线及其作用;饱和溶液和不饱和溶液相互转变的方法;溶质的质量分数、溶解性和溶解度的关系.
【专题】溶液、浊液与溶解度.
【分析】根据已有的溶解度曲线的意义进行分析解答,交点表示在该温度下两种物质的溶解度相等,根据溶解度曲线可以看出物质的溶解度受温度的变化情况,结合饱和溶液和不饱和溶液的转化以及溶解度随温度的变化特点确定析出晶体的方法进行分析解答.
【解答】解:
A、t1℃时,乙的溶解度大于甲,将等质量的甲、乙分别配成饱和溶液,所需要的水的质量甲的大,故所得溶液质量甲大于乙,正确;
B、将t1℃时甲、丙的饱和溶液升温到t2℃,甲的溶解度随温度的升高而增大,故溶液组成不变,而丙的溶解度随温度的升高而减小,会析出晶体,溶质质量分数会减小,但t2℃是丙的溶解度大于t1℃时甲的溶解度,故两种溶液中溶质的质量分数丙大于甲,错误;
C、甲的溶解度随温度的升高而增大,将t2℃时甲的饱和溶液变为t3℃时甲的饱和溶液,可以采用蒸发水的方法,正确;
D、t3℃时三种物质的溶解度关系为甲>乙>丙,将t3℃时三种物质的饱和溶液恒温蒸发等量水后,析出溶质的质量甲>乙>丙,正确.
故选B.
【点评】明确溶解度概念、溶解度曲线的意义、饱和溶液中溶质的质量分数计算与溶解度的关系,才能结合题意正确解答.
5.氯化钾的溶解度曲线如图所示,下列说法正确的是( )
A.升高温度可使接近饱和的氯化钾溶液变为饱和溶液
B.10℃时,65.5g氯化钾的饱和溶液中加入5g氯化钾,充分溶解后将温度升高到40℃,得到70g氯化钾饱和溶液
C.50g水中加入20g氯化钾充分溶解,形成氯化钾饱和溶液
D.40℃时,氯化钾饱和溶液中溶质的质量分数为40%
【考点】固体溶解度曲线及其作用;饱和溶液和不饱和溶液相互转变的方法;溶质的质量分数、溶解性和溶解度的关系.
【专题】溶液、浊液与溶解度.
【分析】根据已有的溶解度曲线的意义以及饱和溶液和不饱和溶液的转化以及溶质质量分数的计算解答即可.
【解答】解:
A、氯化钾的溶解度随温度的升高而增大,升高温度不能使接近饱和的氯化钾溶液变为饱和溶液,错误;
B、10℃时,氯化钾的溶解度为31g,65.5g氯化钾的饱和溶液中含有氯化钾15.5g,加入5g氯化钾,溶质质量=15.5g+5g=20.5g,充分溶解后将温度升高到40℃,此时只能溶解20g,得到70g氯化钾饱和溶液,正确;
C、50g水中加入20g氯化钾充分溶解,没有提在什么温度下,不一定形成氯化钾饱和溶液,错误;
D、40℃时,氯化钾的溶解度为40g,氯化钾饱和溶液中溶质的质量分数=
,错误;
故选B.
【点评】了解溶解度曲线意义、饱和溶液中溶质的质量分数和溶解度之间的关系,饱和溶液降低温度溶解度变化大的析出晶体多等知识,才能结合题意灵活分析解答问题.
6.如图是甲、乙、丙三种物质的溶解度曲线.下列说法错误的是( )
A.t1℃时,三种物质的溶解度是丙>乙>甲
B.t2℃时,甲和丙的饱和溶液溶质质量分数相等
C.三种物质的溶解度均随温度的升高而增大
D.当甲中混有少量的乙时可用冷却其热饱和溶液的方法提纯
【考点】固体溶解度曲线及其作用;结晶的原理、方法及其应用;溶质的质量分数、溶解性和溶解度的关系.
【专题】溶液、浊液与溶解度.
【分析】根据已有的溶解度曲线的意义进行分析解答,根据溶解度曲线可以比较在相同温度下不同物质溶解度的大小,根据溶解度随温度的变化特点确定析出晶体的方法,据此解答.
【解答】解:
A、据图可以看出t1℃时,三种物质的溶解度是丙>乙>甲,正确;
B、t2℃时,甲和丙的溶解度曲线相交于一点,溶解度相等,故甲和丙的饱和溶液溶质质量分数相等,正确;
C、丙物质的溶解度随温度的升高而减小,错误;
D、甲的溶解度受温度影响变化大,当甲中混有少量的乙时可用冷却其热饱和溶液的方法提纯甲,正确;
故选C.
【点评】本题考查的是溶解度曲线的应用,完成此题,可以依据已有的溶解度曲线的意义进行.
7.甲、乙两种固体物质(不含结晶水)的溶解度曲线如图所示.下列说法正确的是( )
A.甲物质的溶解度大于乙物质的溶解度
B.t1℃时,甲、乙两种物质各50g分别加入到100g水中,充分溶解,得到的溶液质量都是140g
C.t2℃时,甲溶液的溶质质量分数一定大于乙溶液的溶质质量分数
D.t2℃时甲、乙的饱和溶液降温到t1℃时,析出晶体的质量甲一定大于乙
【考点】固体溶解度曲线及其作用;晶体和结晶的概念与现象;溶质的质量分数、溶解性和溶解度的关系.
【专题】溶液、浊液与溶解度.
【分析】根据已