盐和化肥实验化学.docx
《盐和化肥实验化学.docx》由会员分享,可在线阅读,更多相关《盐和化肥实验化学.docx(14页珍藏版)》请在冰豆网上搜索。
盐和化肥实验化学
盐和化肥实验化学
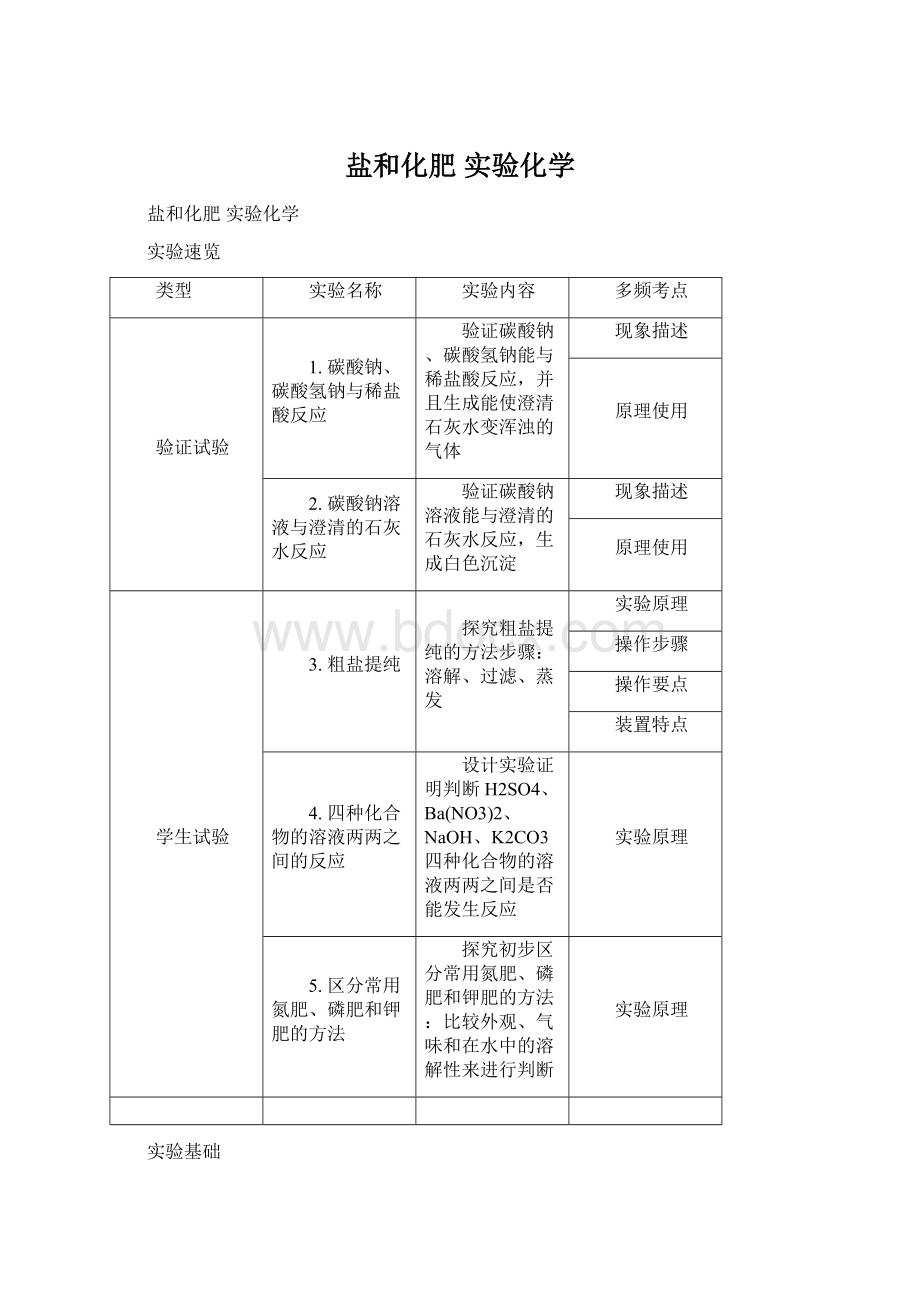
实验速览
类型
实验名称
实验内容
多频考点
验证试验
1.碳酸钠、碳酸氢钠与稀盐酸反应
验证碳酸钠、碳酸氢钠能与稀盐酸反应,并且生成能使澄清石灰水变浑浊的气体
现象描述
原理使用
2.碳酸钠溶液与澄清的石灰水反应
验证碳酸钠溶液能与澄清的石灰水反应,生成白色沉淀
现象描述
原理使用
学生试验
3.粗盐提纯
探究粗盐提纯的方法步骤:
溶解、过滤、蒸发
实验原理
操作步骤
操作要点
装置特点
4.四种化合物的溶液两两之间的反应
设计实验证明判断H2SO4、Ba(NO3)2、NaOH、K2CO3四种化合物的溶液两两之间是否能发生反应
实验原理
5.区分常用氮肥、磷肥和钾肥的方法
探究初步区分常用氮肥、磷肥和钾肥的方法:
比较外观、气味和在水中的溶解性来进行判断
实验原理
实验基础
1.氮肥的简易鉴别:
氮肥中的氨水是液态,碳酸氢铵有强烈的氨味,据此可直接将它们与其他氮肥相区别。
其他常见氮肥可按下列步骤鉴别:
第一步:
加碱。
无氨味的是尿素,有氨味的是硫酸铵、氯化铵、硝酸铵
第二步:
在硫酸铵、氯化铵、硝酸铵中加硝酸钡溶液。
有白色沉淀的是硫酸铵,无沉淀的是氯化铵、硝酸铵。
第三步:
在氯化铵、硝酸铵。
中加硝酸银溶液。
有白色沉淀的是氯化铵,无沉淀的是硝酸铵。
2.利用物理、化学性质的不同初步区分常见化肥的方法
(1)看外观:
氮肥和钾肥是白色晶体,磷肥外观呈灰白色粉状。
(2)加水:
氮肥和钾肥全部溶于水,磷肥大多不溶于水或部分溶于水。
(3)加熟石灰:
氮肥放出具有刺激性气味的氨气,钾肥没有刺激性气味的氨气放出。
实验图解
1.碳酸钠、碳酸氢钠与稀盐酸反应(验证性实验)
目的:
验证碳酸钠、碳酸氢钠能与稀盐酸反应
原理:
Na2CO3+2HCl==2NaCl+H2O+CO2↑
Na2HCO3+HCl==NaCl+H2O+CO2↑
药品:
碳酸钠、碳酸氢钠、稀盐酸、澄清石灰水
步骤:
向试管内的碳酸钠中加入稀盐酸,迅速用带导管的胶塞塞紧试管口,并将导管的一端通入盛有澄清石灰水的试管中
用碳酸氢钠代替碳酸钠重复上述实验
现象:
澄清石灰水变浑浊
结论:
碳酸盐(或碳酸氢盐)能与盐酸反应生成二氧化碳气体,这是检验碳酸根(或碳酸氢根)的方法
操作指要盐酸用2mL即可,不可用太多,否则液体喷出试管。
应试策略碳酸盐(碳酸氢盐)与盐酸反应是中考常考的内容,这是检验碳酸根(碳酸氢根)的方法,对其操作过程和实验现象要求会正确描述,并要求掌握有关计算。
例:
实验室有失去标签的两瓶白色粉末药品,分别是Na2CO3和NaHCO3。
某同学设计了下列实验进行鉴别,如右图所示。
步骤一:
往大小相同的两个锥形瓶中各倒入30mL溶质的质量分数相同的稀盐酸。
步骤二:
用相同的两只气球,分别装入足量的两瓶中的白色粉末,套在步骤一的锥形瓶口上。
步骤三:
迅速将气球中的药品倒入锥形瓶中。
请判断该同学的操作能否达到目的,并通过计算说明理由。
变题练
1.小新和小白一起动手,做一个会“喷火”的火山。
小新现在一个脸盆里放进一个小瓶子,然后,把潮湿的土堆积在瓶子周围,作成山的形状。
做这些事时,小新很小心,不让土堵住瓶口。
小白把一大勺苏打粉(碳酸氢钠)放进瓶内,然后,将一杯盛有红墨水的醋倒入瓶内。
一切工作做完了,你猜,小新和小白看到了什么?
__________________________________________________________________________________________________________________________________________
2.为了使馒头松软可口,常在揉面时加入食用碱。
为了探究食用碱的主要成分,向其中加入稀盐酸,发现产生一种能使澄清石灰水变浑浊的气体,则食用碱中可能含有()。
A.食盐B.烧碱C.纯碱D.味精
3.小金在了解了水泥的主要成分是碳酸钙后,想验证一下。
于是取水泥样品少量,向其中加入稀盐酸,发现有气泡产生,且气体能使澄清石灰水变浑浊。
他用类似的方法检验了下列生活中的物质是否也含有碳酸根,根据生活检验,下列物质中不含碳酸根的物质是()。
A.水垢B.珍珠C.鸡蛋壳D.大米
2.碳酸钠与澄清石灰水反应(验证性实验)
目的:
验证碳酸钠溶液能与澄清石灰水发生反应
原理:
Na2CO3+Ca(OH)2==CaCO3↓+2NaOH
药品:
碳酸钠溶液、澄清石灰水
步骤:
向盛有少量碳酸钠溶液的是试管里滴入澄清石灰水
现象:
有白色沉淀出现
结论:
可溶性的碳酸盐与氢氧化钙反应生成不溶性的碳酸钙
操作指要澄清石灰水逐滴滴入
应试策略碳酸钠与氢氧化钙反应生成不溶于水的碳酸钙,这是一个很有代表性的盐与碱的反应,也是常考查的一个反应。
例:
课堂上老师完成了碳酸钠溶液和澄清石灰水反应的演示实验后,对浑浊液体进行了过滤得到澄清滤液,接着师生对话如下:
老师问:
滤液里可能含有哪些溶质呢?
甲同学答:
可能是NaOH、Na2CO3。
乙同学答:
可能是NaOH、Na2CO3、Ca(OH)2。
丙同学答:
可能是NaOH。
丁同学答:
可能是_____________________。
(1)假设你是丁同学,请你提出一个与甲、乙、丙同学不同的猜想,把猜想写在上面的横线上,并对你自己的猜想设计一个简单的实验加以证明。
实验步骤
实验现象
实验结论
取样于试管中,___________________
___________________________________
自己的猜想成立
(2)你认为甲、乙、丙同学的猜想都合理吗?
如有不合理的请说明理由:
______________________________________________________________________________
(3)甲同学针对自己的猜想进行了如下实验:
实验步骤
实验现象
实验结论
取样于试管中,滴入足量稀盐酸
没有气体产生
猜想不成立
你认为甲同学的实验设计是否正确?
请说明理由:
____________________________
变题练
1.为了证明长期暴露在空气中的氢氧化钠已经部分变质,请分别选用三种不同物质类别的试剂完成三种实验方案的设计,并填写实验报告。
方案一:
步骤一是取样2mL于试管中,步骤二是___________________________________。
方案二:
步骤一是取样2mL于试管中,步骤二是___________________________________。
2.在元旦的联欢会上,晓慧同学为同学们表演了一组化学魔术。
在三支盛有液体的玻璃杯中,分别倒入用酒瓶装的一种液体,分别倒入用酒瓶装的一种液体,同学们看到下列奇特现象:
A杯中变成了“红葡萄酒”(变为红色);B杯变成了“汽水”(产生大量的气泡);C杯中变成了“牛奶”(有白色沉淀).请你来揭开魔术秘密。
(1)酒瓶中的液体可能是__________________。
(2)B杯中产生的气体是___________________。
(3)写出C杯中发生的化学方程式_______________________________________________。
3.粗盐提纯(探究性实验)
目的:
探究粗盐提纯的方法
学会过滤和蒸发的基本操作
原理:
蒸发结晶的方法从氯化钠溶液中获得晶体
药品、器材:
托盘天平、量筒、烧杯、漏斗、铁架台(带铁圈)、滤纸、玻璃棒
步骤:
溶解:
称取5.0g的粗盐放入烧杯中,倒入10mL的水,用玻璃棒搅拌,直到粗盐不再溶解为止
过滤:
做好过滤器,放在铁圈上,用玻璃棒引流,使滤液流到下面的烧杯中
③蒸发:
将滤液倒入蒸发皿中进行蒸发,边加热边搅拌
结论:
分离可溶物与不溶物时可用过滤的方法
可用蒸发的方法从溶液中得到晶体
操作指要
过滤时先让上层滤液过滤,然后再将混有大量沉淀的溶液倒入漏斗,防止过滤速度过慢。
蒸发皿里的溶液量不超过容积的2/3,倒入过多溶液,加热至沸腾时易飞溅。
③蒸发时,待有大量固体析出时,停止加热,用蒸发皿的余热将剩余的液体蒸干。
应试策略粗盐提纯是初中化学比较重要的一个实验,常考核的内容有:
加试剂除杂、实验仪器、实验装置、操作过程应注意的事项等。
例:
某化学课外活动小组展开粗盐提纯的实验。
经查阅资料知道:
粗盐中除含有NaCl外,还含有MgCl2、CaCl2、MgSO4以及泥沙等杂质;他们要除去杂质得到精盐,
Mg(OH)2是难溶物。
该活动小组的同学为除去杂质得到精盐,设计了下列实验方案(序号①~⑧表示实验操作,用于沉淀的试剂稍过量):
根据上述方案,回答下列问题:
(1)操作①中玻璃棒的作用是___________________。
(2)第⑤步操作的名称是______________,
(3)“蒸发结晶”用到的器材有:
铁架台(铁圈)、坩埚钳、石棉网、火柴、玻璃棒、_________、__________,玻璃棒的作用是______________________。
(4)实验第④步中加入“Na2CO3溶液”的目的是__________________________________。
(5)第⑥步中加入稀盐酸后发生反应的化学方程式为:
_______________________________;__________________________________________。
变题练
1.根据粗盐提纯过程,回答下列问题。
(1)粗盐中含有较多的可溶性杂质(氯化镁、氯化钙)和不溶性杂质(泥沙等),可通过____________、______________、______________等操作进行初步提纯。
这三步操作中均用到一种常见仪器是_____________,它在各步中的作用分别是_________________、_______________、___________________。
(2)小江同学在粗盐提纯的实验过程中,经过两次过滤,滤液仍然浑浊,其原因可能是___________________或仪器不干净。
(3)小李同学提纯后计算出的精盐产率比同期实验的其他同学都低得多,请你帮他分析,产生的原因可能是____________________________________________________________。
2.若按粗盐提纯的实验步骤对下列各组物质进行分离,可以达到目的的是()。
A.从空气中分离得到氧气B.将混如硝酸钾中的少量氯化钠除去
C.从草木灰中提取碳酸钾D.从氯酸钾制取氧气的残渣中回收二氧化锰和氯化钾
4.四种化合物的溶液两两之间的反应(探究性实验)
目的:
探究硫酸、硝酸镁、氢氧化钠和碳酸钾之间能否两两反应
原理:
复分解反应的条件是:
有水、气体或沉淀生成
药品:
硫酸、硝酸钡、氢氧化钠和碳酸钾溶液
步骤:
取6支试管将四种溶液两两混合,观察有什么现象
现象:
有些反应有沉淀生成,有些有气体产生,有些没有明显现象
结论:
有些反应根据现象可以判断是否发生了,有些反应必须借助指示剂才能判断
操作指要
四种溶液相互之间不要弄混,要看清试剂的标签。
四种试剂的滴管要注意区分,不要混用。
③H2SO4和NaOH反应没有现象,需借助指示剂,最好用酚酞溶液。
应试策略酸、碱、盐之间的反应是初中化学的重点内容,也是难点,判断哪些物质之间能反应,要求对溶解性表、反应条件牢记在心,并能灵活应用。
例:
现有a、b、c、d四种无色溶液,分别是碳酸钠溶液、硫酸、氯化钡溶液或盐酸中的一种。
根据下表中它们两两间相互反应的实验记录,推断按a、b、c、d顺序排列的选项是()。
a
b
c
d
b
无明显现象
有气体产生
有沉淀产生
c
有气体产生
有气体产生
有沉淀产生
A.H2SO4、Na2CO3、BaCl2、HClB.HCl、H2SO4、Na2CO3、BaCl2
C.Na2CO3、H2SO4、HCl、BaCl2D.BaCl2、HCl、Na2CO3、H2SO4
变题练
1.下列两种物质的溶液混合后能发生反应,且溶液的总质量不会发生改变的是()。
A.氢氧化钠溶液和稀盐酸B.碳酸钠溶液和稀盐酸
C.氯化钠溶液和稀硫酸D.碳酸钠溶液和氯化钙溶液
2.下列各组物质的水溶液相互混合,可发生化学反应具有气体生成的是()。
A.HCl、NaOHB.Na2CO3、H2SO4C.Ca(OH)2、Na2CO3D.KCl、H2SO4
3.下列各物质中加入稀硫酸后,有沉淀生成的是()。
A.碳酸钾溶液B.石蕊溶液C.硝酸钡溶液D.氢氧化钠溶液
5.区分常用氮肥、磷肥和钾肥的方法(探究性实验)
目的:
探究区分常用氮肥、磷肥和钾肥的方法
原理:
有些肥料有比较明显的气味,易溶于水
铵盐可以与碱性物质混合产生有刺激性气味的氨气
药品、器材:
氯化铵、碳酸氢铵、磷矿粉、过磷酸钙、硫酸钾、氯化钾、熟石灰、试管、研钵等
步骤:
观察样品的颜色和气味:
取少量样品放入试管内,加入蒸馏水,振荡,观察水溶性
取少量压碎的熟石灰放入研钵里与样品均匀研磨,闻气味
现象:
有些肥料不溶于水,外观为灰白色
有些肥料与熟石灰混合研磨有刺激性气味
结论:
磷肥为灰白色粉末,大多数不溶于水
氮肥与熟石灰混合研磨产生有刺激性气味的氨气
操作指要闻气味时,要用手轻轻扇动气体,使气体飘入鼻孔,切忌直接把鼻孔凑到容器口闻药品的气味。
应试策略考核得比较多的是铵态氮肥的检验。
它的检验还可以与氢氧化钠溶液混合加热,将湿润的红色石蕊试纸放在试管口,红色石蕊试纸变蓝色。
例:
小明暑假期间到农田施肥时,发现洒落在地上得碳酸氢铵在阳光的照射下很快消失了,同时伴有浓烈的刺激性气味。
他很好奇,返校后和同学们进行探究,请你一同参与。
【提出问题】:
温度较高时,碳酸氢铵能分解吗?
产物是什么?
【猜想假设】:
碳酸氢铵受热易分解,产物可能为水、二氧化碳、氨气。
【实验设计】:
小明设计了如图所示的装置进行实验(夹持装置省略)。
(1)根据现象:
__________________________,证明实验后生成了水和氨气。
(2)装置B中澄清石灰水_____________________,证明产物中有二氧化碳生成。
(3)小红同学认为若将装置B中澄清石灰水改为NaOH溶液,再通过实验验证B中产物,也可以证明碳酸氢铵分解后有二氧化碳生成。
请你帮她设计并完成验证B中产物的实验。
实验步骤
实验现象
反应的化学方程式
【实验结论】碳酸氢铵受热易分解,其反应的化学方程式为___________________________。
【实验评价】在上述同学们的探究活动中,你最欣赏的是_____________________________。
【实验反思】根据以上实验,你认为碳酸氢铵化肥在存放时应注意的问题是___________________________________________________。
变题练
1.下列化肥中,从外观即可与其他化肥相区别的是()。
A.硝酸钾B.碳酸铵C.氯化钾D.磷矿粉
2.请阅读下列资料,并回答下列问题:
资料一:
碳酸氢铵是一种常用的氮肥。
碳酸氢铵与碱性物质混合时,会产生一种有刺激性气味的气体——氨气,而且肥效降低。
碳酸氢铵受潮时,在常温时就能分解,温度越高,分解越快。
资料二:
草木灰是常用的农家肥,主要成分是碳酸钾,其水溶液呈碱性。
(1)储存NH4CO3时应注意:
___________________________________________________。
(2)小明的叔叔在施肥时,为了提高肥效,将钾肥草木灰与氮肥NH4HCO3混合施用了。
请你运用所学知识解释这种做法是否合理。
_____________________________________________________________________________________________________________________________________________________________。
3.化肥中的氮肥很多是铵盐,已知氨气通入水中后,其溶液呈碱性。
将硫酸铵和氢氧化钙混合后放入试管加热,用湿润的红色石蕊试纸放在试管口,这是检验铵盐的方法。
上述实验现象说明()。
A.铵盐和碱的反应属于复分解反应类型
B.氨气比空气轻
C.能使红色石蕊试纸变蓝色的就是氨气
D.铵盐能和碱反应放出氨气
4.请写出鉴别NH4Cl和K2SO4这两种化学肥料的操作方法及实验现象。
_____________________________________________________________________________________________________________________________________________________。
实验综合
物质的检验
应掌握知识:
酸、碱、盐的溶解性
复分解反应的条件
典型物质的特征及反应的现象(现象有:
沉淀、气体、颜色等)
题目类型:
不用其他试剂鉴别一组物质
用一种试剂鉴别多种物质
不限制试剂鉴别一组物质
检验中的注意事项:
排除其他物质的干扰
综合考点:
检验某种物质时,必须注意排除另一种物质的干扰。
例如:
检验氢氧化钠时必须排除碳酸钠的干扰;当氯化钠和硫酸钠同时存在时,要检验氯化钠时必须排除硫酸钠的干扰。
应试策略:
熟记酸、碱、盐的溶解性表,并熟悉酸、碱、盐间的相互反应。
【真题】做中和反应实验时,小李将稀盐酸滴入氢氧化钠溶液中,意外看到有气泡产生。
小伟提醒:
是不是拿错了药品?
小李查验后确认药品没错,只是在瓶口发现有白色粉末状物质。
小李认为是氢氧化钠溶液变质了。
(1)氢氧化钠溶液变质的原因是______________________________________________。
(2)利用与上述实验不同的原理,小李又设计了一个实验再次确认该氢氧化钠溶液已经变质。
实验步骤
实验现象
实验结论
取少量氢氧化钠溶液于试管中,滴加_______________
________________________________
________________________________
该氢氧化钠溶液已变质
(3)该氢氧化钠溶液是部分变质还是全部变质?
实验步骤
实验现象
实验结论
____________________________
_____________________________
________________________________
________________________________
该氢氧化钠溶液_______________变质
写出(3)中所涉及的一个化学方程式______________________________________________。
(4)如何用该变质的溶液来制取氢氧化钠溶液?
简述实验步骤。
变题练
1.已知在溶液中氢氧化钙和碳酸钠反应生成碳酸钙和氢氧化钠。
现实验室中有一包白色粉末,可能是碳酸钠,也可能是氧化钙或氢氧化钙。
为确定其组成,某同学设计了以下实验方案进行探究,请你按要求帮助其完成探究活动。
(1)提出假设:
假设①白色粉末是碳酸钠。
假设②白色粉末是氧化钙。
假设③白色粉末是氢氧化钙。
(2)设计实验,通过实验分析进行判断并填空:
假设
设计相关的实验操作
实验中观察到的现象
假设是否成立
1
取一定量粉末加入稀盐酸
没有气体产生
____________
2
取一定量粉末溶于水
溶液浑浊且温度升高
____________
3
取一定量粉末溶于水,静置后取上层清夜再通入二氧化碳
没有沉淀产生
____________
(3)实验后思考:
假定这包白色粉末是混有少量氧化钙的碳酸钠粉末,将混合物溶于水可观察到的现象是____________________________________。
若将反应后的混合物进行固液分离,分离的方法是____________。
再将分离后的溶液蒸干,得到的固体物质是_________(填化学式)。
达标练习实验题解题能力提高训练
基础题
1.在不使用酸碱指示剂的前提下,欲除去氯化钙溶液中德少量盐酸,得到的氯化钙溶液,最适宜选用的一种试剂是()。
A.硝酸银溶液B.澄清石灰水C.生石灰粉末D.碳酸钙粉末
2.不用其他试剂,可以鉴别石蕊、盐酸、氢氧化钙、氢氧化钠、碳酸钠五种溶液,第二个被鉴别出来的物质是()。
A.盐酸B.氢氧化钙C.氢氧化钠D.碳酸钠
3.有四种物质的溶液:
①Ba(OH)2、②Na2SO4、③HNO3、④FeCl3,不用其他试剂就可将它们逐一鉴别出来,其鉴别顺序是()。
A.④③②①B.④①②③C.①③④②D.①④③②
4.有一包固体粉末,可能含有碳酸钠、硫酸钠、硝酸钡、氯化钾和氯化铜中的一种或几种。
为确定其组成,进行如下实验:
2取该固体粉末少量,加足量水,搅拌,静置,得到白色沉淀,上层为无色溶液;
②过滤,在白色沉淀中加入足量稀硝酸,白色沉淀有一部分溶解,且有无色气体产生。
依据上述实验对原固体粉末的判断正确的是()
A.一定含有碳酸钠、硫酸钠、硝酸钡、氯化钾,可能含有氯化铜
B.一定含有碳酸钠、硫酸钠、硝酸钡,一定不含氯化铜,可能含有氯化钾
C.一定含有碳酸钠、硫酸钠、硝酸钡,可能含有氯化铜;氯化钾
D.一定含有碳酸钠、硝酸钡,一定不含硫酸钠、氯化铜,可能含有氯化钾
提高题
5.为了鉴别NaOH和Na2CO3两种无色溶液,某同学设计了以下两种实验方案:
方案1:
分别取少许两种溶液,各滴入几滴无色酚酞溶液,根据酚酞溶液是否变红色判断各是哪种溶液?
方案2:
分别取少许两种溶液,各加入少量澄清石灰水,根据是否有白色沉淀生成判断各是哪些溶液?
请回答:
(1)该同学设计的两个方案有一个是正确的,该方案是__________;另一个方案是不正确的,原因是___________________________________________________________。
(2)请你再设计一个实验,区别上述两种溶液:
实验操作
实验现象
实验结论和化学方程式
6.
右图是小华同学设计的一套验证NH4HCO3受热分解及分解产物的装置(已知
,图中固定干燥试管的部分未画出)。
实验所用药品从NH4HCO3粉末,红色石蕊试纸,澄清石灰水,水,浓硫酸等药品中选择,请按要求回答下列问题:
(1)A烧杯中盛装的药品是_______________________,作用是________________________。
(2)C烧杯中盛装的药品是______________________,实验中有何现象(用化学方程式表述)__