超值推荐 高考必考知识点巩固练习届高三高考化学专题专练化工流程.docx
《超值推荐 高考必考知识点巩固练习届高三高考化学专题专练化工流程.docx》由会员分享,可在线阅读,更多相关《超值推荐 高考必考知识点巩固练习届高三高考化学专题专练化工流程.docx(14页珍藏版)》请在冰豆网上搜索。
超值推荐高考必考知识点巩固练习届高三高考化学专题专练化工流程
化工流程
1.醋酸镍[(CH3COO)2Ni]是一种重要的化工原料。
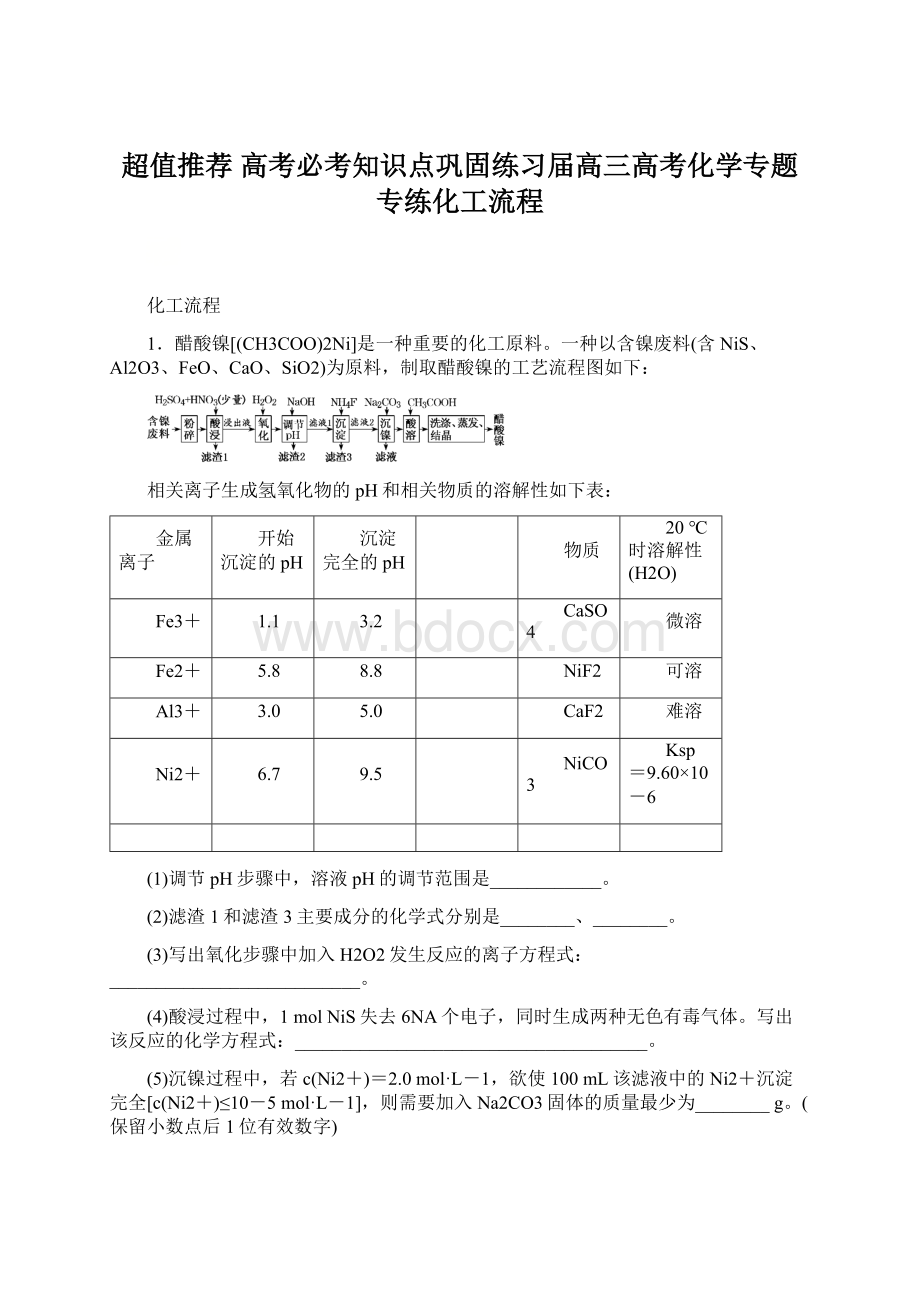
一种以含镍废料(含NiS、Al2O3、FeO、CaO、SiO2)为原料,制取醋酸镍的工艺流程图如下:
相关离子生成氢氧化物的pH和相关物质的溶解性如下表:
金属离子
开始沉淀的pH
沉淀完全的pH
物质
20℃时溶解性(H2O)
Fe3+
1.1
3.2
CaSO4
微溶
Fe2+
5.8
8.8
NiF2
可溶
Al3+
3.0
5.0
CaF2
难溶
Ni2+
6.7
9.5
NiCO3
Ksp=9.60×10-6
(1)调节pH步骤中,溶液pH的调节范围是____________。
(2)滤渣1和滤渣3主要成分的化学式分别是________、________。
(3)写出氧化步骤中加入H2O2发生反应的离子方程式:
___________________________。
(4)酸浸过程中,1molNiS失去6NA个电子,同时生成两种无色有毒气体。
写出该反应的化学方程式:
______________________________________。
(5)沉镍过程中,若c(Ni2+)=2.0mol·L-1,欲使100mL该滤液中的Ni2+沉淀完全[c(Ni2+)≤10-5mol·L-1],则需要加入Na2CO3固体的质量最少为________g。
(保留小数点后1位有效数字)
(6)保持其他条件不变,在不同温度下对含镍废料进行酸浸,镍浸出率随时间变化如图。
酸浸的最佳温度与时间分别为________℃、________min。
2.硫酸锌可用于制造锌钡白、印染媒染剂等。
用锌白矿(主要成分为ZnO,还含有Fe2O3、CuO、SiO2等杂质)制备ZnSO4·7H2O的流程如下:
相关金属离子生成氢氧化物沉淀的pH(开始沉淀的pH按金属离子浓度为1.0mol·L-1计算)如表所示:
金属离子
开始沉淀的pH
沉淀完全的pH
Fe3+
1.1
3.2
Fe2+
5.8
8.8
Zn2+
6.4
8.0
(1)“滤渣1”的主要成分为________(填化学式)。
“酸浸”过程中,提高锌元素浸出率的措施有:
适当提高酸的浓度、____________(填一种)。
(2)“置换”过程中,加入适量的锌粉,除与溶液中的Fe3+、H+反应外,另一主要反应的化学方程式为______________________________________。
(3)“氧化”一步中,发生反应的离子方程式为________________________________。
溶液pH控制在[3.2,6.4)之间的目的是____________________________________。
(4)“母液”中含有的盐类物质有____________(填化学式)。
3.某科研小组采用如下方案回收一种光盘金属层中的少量Ag(金属层中其他金属含量过低,对实验的影响可忽略)。
已知:
①NaClO溶液在受热或酸性条件下易分解,如:
3NaClO===2NaCl+NaClO3
②AgCl可溶于氨水:
AgCl+2NH3·H2OAg(NH3)
+Cl-+2H2O
③常温时N2H4·H2O(水合肼)在碱性条件下能还原Ag(NH3)
:
4Ag(NH3)
+N2H4·H2O===4Ag↓+N2↑+4NH
+4NH3↑+H2O
(1)“氧化”阶段需在80℃条件下进行,适宜的加热方式为________________。
(2)NaClO溶液与Ag反应的产物为AgCl、NaOH和O2,该反应的化学方程式为__________________________________。
HNO3也能氧化Ag,从反应产物的角度分析,以HNO3代替NaClO的缺点是___________________________________________。
(3)为提高Ag的回收率,需对“过滤Ⅱ”的滤渣进行洗涤,并_____________________。
(4)若省略“过滤Ⅰ”,直接向冷却后的反应容器中滴加10%氨水,则需要增加氨水的用量,除因过量NaClO与NH3·H2O反应外(该条件下NaClO3与NH3·H2O不反应),还因为______________________________。
(5)请设计从“过滤Ⅱ”后的滤液中获取单质Ag的实验方案:
______________(实验中须使用的试剂有:
2mol·L-1水合肼溶液,1mol·L-1H2SO4)。
4.以工业生产硼砂所得废渣硼镁泥为原料制取MgSO4·7H2O的过程如图所示:
硼镁泥的主要成分如下表:
MgO
SiO2
FeO、Fe2O3
CaO
Al2O3
B2O3
30%~40%
20%~25%
5%~15%
2%~3%
1%~2%
1%~2%
回答下列问题:
(1)“酸解”时应该加入的酸是________,“滤渣1”中主要含有________(写化学式)。
(2)“除杂”时加入次氯酸钙、氧化镁的作用分别是___________、__________________。
(3)判断“除杂”基本完成的检验方法是______________________________。
(4)分离滤渣3应趁热过滤的原因是____________________________________。
5.“分子筛”是一种具有多孔结构的铝硅酸盐(NaAlSiO4·nH2O),其中有许多笼状孔穴和通道能让直径比孔穴小的分子通过而将大的分子留在外面,故此得名。
利用铝灰(主要成分为Al、Al2O3、AlN、FeO等)制备“分子筛”的一种工艺如下:
(1)分子筛的孔道直径为4A称为4A型分子筛;当Na+被Ca2+取代时就制得5A型分子筛,当Na+被K+取代时就制得3A型分子筛。
要高效分离正丁烷(分子直径为4.65A)和异丁烷(分子直径为5.6A)应该选用________型的分子筛。
(2)铝灰在90℃时水解的化学方程式为____________________________;“水解”采用90℃而不在室温下进行的原因是_________________________________。
(3)“酸溶”时,为降低生产成本,应选择的酸为__________,理由是_____________。
(4)“氧化”时,发生的主要反应的离子方程式为____________________________。
(5)该工艺中滤渣的成分是________。
(6)“胶体”调节pH后过滤所得“晶体”需洗涤,如何证明该晶体已经洗涤干净?
_____________________________________________________________________。
6.PFS是水处理中重要的絮凝剂,下图是以回收的废铁屑为原料制备PFS的一种工艺流程。
(1)酸浸槽以及聚合釜中用到的酸应是________;PFS中铁元素的化合价为________;在酸浸槽中,为了提高浸出率,可以采取的措施有________________(写两条)。
(2)若废铁屑中含有较多铁锈(Fe2O3·xH2O),则酸浸时反应的化学方程式有______________。
(3)如果反应釜中用H2O2作氧化剂,则反应的离子方程式为_______________;生产过程中,发现反应釜中产生了大量的气体,且温度明显升高,其原因可能是_________________。
(4)聚合釜中溶液的pH必须控制在一定的范围内。
如果溶液酸性过强,造成的后果是____________________。
如果溶液酸性太弱又会生成大量的氢氧化铁沉淀。
若溶液中Fe3+的浓度为1mol·L-1,当Fe3+开始沉淀时,溶液的pH约为________。
[已知Fe(OH)3的Ksp≈1.0×10-39]。
7.工业上利用粗ZnO(含FeO、CuO)制取金属锌的流程如下(部分步骤省略):
已知:
几种离子形成氢氧化物沉淀时的pH如下表:
待沉淀的离子
Fe2+
Fe3+
Zn2+
Cu2+
开始沉淀时pH
6.3
1.5
6.2
5.2
沉淀完全时pH
9.7
3.2
8.0
6.4
请回答下列问题:
(1)酸浸粗氧化锌的过程中,为了加快酸浸速率,可采取的措施有__________________________________
(写出一点即可)。
(2)步骤A的目的是将Fe2+氧化为Fe3+,并全部形成Fe(OH)3沉淀,为了暂不形成Cu(OH)2、Zn(OH)2,该步骤需控制溶液pH的范围是______________,该步骤中加入H2O2发生反应的离子方程式为_______________________________________。
(3)步骤D的操作名称为________________________________________________。
(4)由粗ZnO制取单质锌的另一种方法是将粗ZnO(含FeO、CuO)溶于NaOH溶液,ZnO全部转化为Na2[Zn(OH)4]溶液,该反应的化学方程式为_________________________;然后将FeO、CuO过滤除去;再用惰性电极电解该滤液,阳极上逸出无色无味气体,阴极上析出锌,则阴极电极反应式为_____________________________________________。
参考答案
1.醋酸镍[(CH3COO)2Ni]是一种重要的化工原料。
一种以含镍废料(含NiS、Al2O3、FeO、CaO、SiO2)为原料,制取醋酸镍的工艺流程图如下:
相关离子生成氢氧化物的pH和相关物质的溶解性如下表:
金属离子
开始沉淀的pH
沉淀完全的pH
物质
20℃时溶解性(H2O)
Fe3+
1.1
3.2
CaSO4
微溶
Fe2+
5.8
8.8
NiF2
可溶
Al3+
3.0
5.0
CaF2
难溶
Ni2+
6.7
9.5
NiCO3
Ksp=9.60×10-6
(1)调节pH步骤中,溶液pH的调节范围是____________。
(2)滤渣1和滤渣3主要成分的化学式分别是________、________。
(3)写出氧化步骤中加入H2O2发生反应的离子方程式:
___________________________。
(4)酸浸过程中,1molNiS失去6NA个电子,同时生成两种无色有毒气体。
写出该反应的化学方程式:
______________________________________。
(5)沉镍过程中,若c(Ni2+)=2.0mol·L-1,欲使100mL该滤液中的Ni2+沉淀完全[c(Ni2+)≤10-5mol·L-1],则需要加入Na2CO3固体的质量最少为________g。
(保留小数点后1位有效数字)
(6)保持其他条件不变,在不同温度下对含镍废料进行酸浸,镍浸出率随时间变化如图。
酸浸的最佳温度与时间分别为________℃、________min。
【答案】
(1)5.0≤pH<6.7
(2)SiO2、CaSO4 CaF2
(3)2Fe2++H2O2+2H+===2Fe3++2H2O
(4)NiS+H2SO4+2HNO3===NiSO4+SO2↑+2NO↑+2H2O (5)31.4 (6)70 120
【解析】
(1)~(3)制取醋酸镍的工艺流程可解读为