高中化学选修四期末复习知识点总结docWord文档下载推荐.docx
《高中化学选修四期末复习知识点总结docWord文档下载推荐.docx》由会员分享,可在线阅读,更多相关《高中化学选修四期末复习知识点总结docWord文档下载推荐.docx(23页珍藏版)》请在冰豆网上搜索。
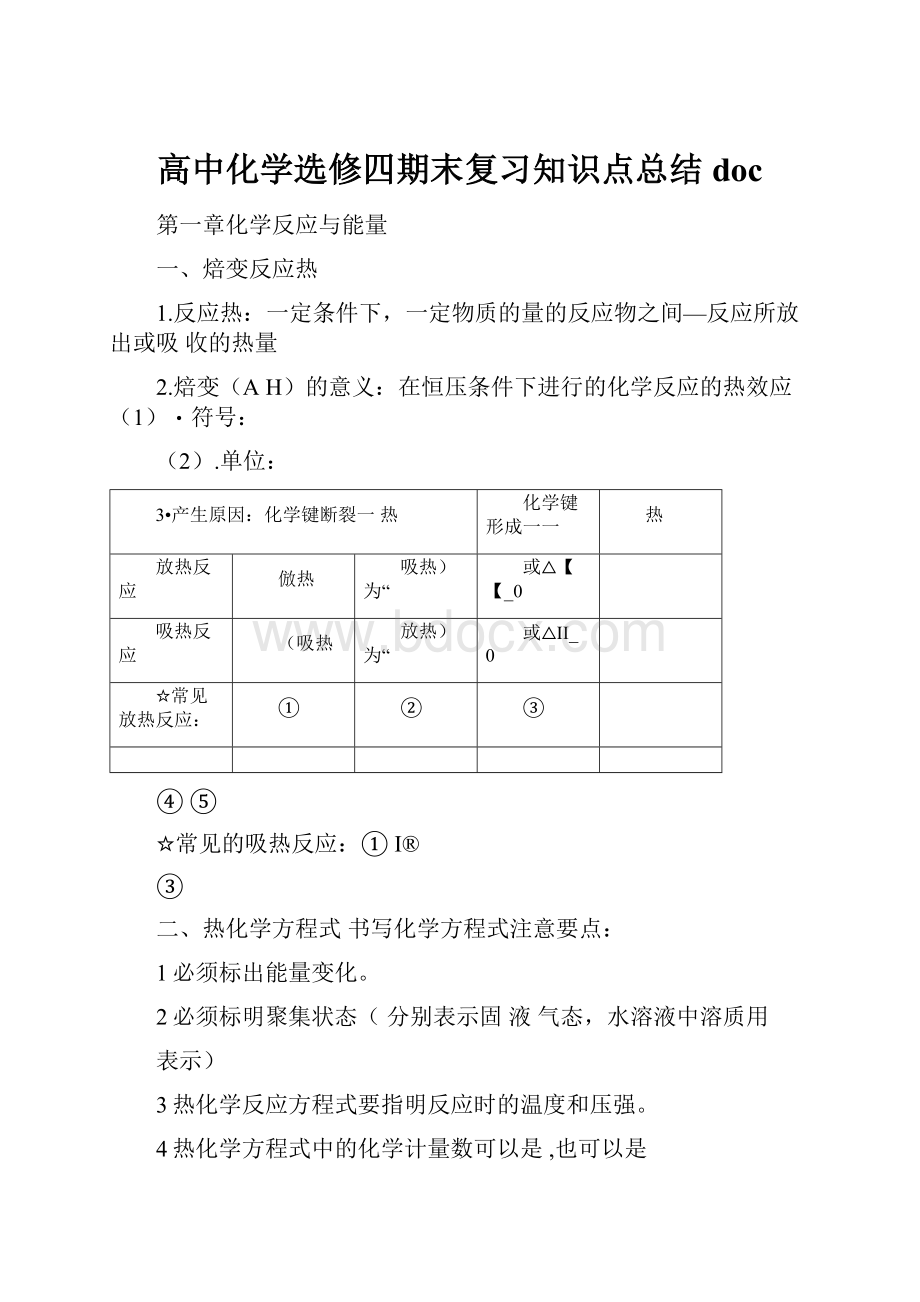
盐酸(0.50mol/L)氢氧化钠溶液(0.55mol/L)
实验步骤:
计算公式:
误差分析
五、盖斯定律
1.内容:
化学反应的反应热只与反应(各反应物)和(各生成
物)有关,而与具体反应进行的途径无关,如果一个反应可以分几步进行,则O
2.使用方法
3.反应热的计算
第二章化学反应速率和化学平衡
一、化学反应速率
1.化学反应速率(v)
(1)定义:
衡量反应快慢,单位时间内反应物或生成物的量的变化
(2)表示方法:
单位时间内反应浓度的减少或生成物浓度的增加来表示
⑶计算公式:
(u:
平均速率,浓度变化)单位:
⑷影响因素:
①决定因素(内因):
(决定因素)
②条件因素(外因):
反应所处的条件2.反应物浓度、气体压强、
温度、催化剂对反应速率的影响
条件变化
单位体积内分子总数
活化分子百分数
单位体积内
活化分子总数
V变化
光、电磁波、超声波、固体反应物颗粒大小、溶剂等
(1)固体和液体,市于压强对浓度儿乎无影响,反应速率不变。
(2)、惰性气体对于速率的影响
1恒温恒容吋:
充入惰性气体一总压增大,但是各分压不变,各物质浓度不变一反应速率不变
2恒温恒体时:
充入惰性气体一体积增大一各反应物浓度减小一反应速率减慢
二、化学平衡
(_)1.定义:
2、化学平衡的特征
逆(研究前提是反应)
等(的正逆反应速率相等)
动(动态平衡)
定(各物质的浓度与质量分数)
变(条件改变,平衡发生变化)
3、判断平衡的依据判断可逆反应达到平衡状态的方法和依据
例举反应
mA(g)+nB(g)〜pC(g)+qD(g)
混合物体系中各成分的含量
①各物质的物质的量或各物质的物质的量的分数一定
平衡
②各物质的质量或各物质质量分数一定
()
③各气体的体积或体积分数一定
④总体积、总压强、总物质的量一定
正、逆反应速率的关系
①在单位时间内消耗了mmolA同时生成mmolA,即V(正)二V(逆)
②在单位时间内消耗了nmolB同时消耗了pmolC,则V(正)=V(逆)
()
@V(A):
V(B):
V(C):
V(D)=m:
n:
p:
q,V(正)不一定等于V(逆)
不一定平衡
④在单位时间内生成nmolB,同时消耗了qmolD,因均指V(逆)
压强
①m+nHp+q时,总压强一定(其他条件一定)
②m+n二p+q时,总压强一定(其他条件一定)
混合气体平均相对分子质量
Mr
①Mr—定时,只有当m+nHp+q时
②Mr—定时,但m+n二p+q时
温度
任何反应都伴随着能量变化,当体系温度一定时1其他不变)
体系的密度
密度一定
其他
如体系颜色不再变化等
(二)影响化学平衡移动的因素
1、浓度对化学平衡移动的影响⑴其他条件不变,增大反应物的浓度或减少生成物
的浓度,平衡向移动;
增大生成物的浓度或减小反应物
的浓度,平衡向移动。
(2)增加固体或纯液体的量,由于浓度不变,所以平衡移动
(3)溶液中的反应,如稀释溶液,反应物浓度减小,生成物浓度也减小,V正减
小,V逆也减小,但是减小的程度不同,平衡向方程式中计量数之和大的方向移动。
2、温度对化学平衡移动的影响
其他条件不变,温度升高平衡向移动,温度降低平衡向方向移动。
3、压强对化学平衡移动的影响
其他条件不变,增大压强,平衡向移动;
减小压强,平衡向移动。
注意:
(1)改变压强不能使无气态物质存在的化学平衡发生移动
(2)气体减压或增压与溶液稀释或浓缩的化学平衡移动规律相似
4.催化剂:
由于催化剂対正反应速率和逆反应速率影响的程度是的,所以平
衡。
但是使用正催化剂可以达到平衡所需的时间
5.勒夏特列原理(平衡移动原理):
如果改变影响平衡的条件Z—(如温度,压强,
浓度),平衡向着能的方向移动。
三、化学平衡常数(符号)
(一)定义:
一定温度下,达到化学平衡时,
比值。
(二)使用化学平衡常数K应注意的问题:
1、表达式中各物质的浓度是o
2、K只与有关,与反应物或生成物的浓度无关。
3、反应物或生产物中固体或纯液体,由于其浓度是固定不变的。
4、稀溶液屮进行的反应,如有水参加,水的浓度不必写在平衡关系式屮。
(三)化学平衡常数K的应用:
1、化学平衡常数值的大小是可逆反应的标志。
K值越大,说明平衡时
的浓度越大,它的进行的程度越大,即该反应进行得越完全,反应物转化
率越—o反之,则相反。
一般地,K>
105时,该反应就进行得基本完全了。
2、利用K值做标准,可判断正在进行的可逆反应是否平衡及建立平衡的方向。
(Q:
浓度积)
QK:
反应向正反应方向进行;
反应处于平衡状态;
反应向逆反应方向进行
3、利用K值可判断反应的热效应
若温度升高,K值增大,则正反应为反应
若温度升高,K值减小,则正反应为反应
*四、等效平衡
1、概念:
一定条件下(定温、定容或定温、定压),同一可逆反应经不同途径达到平衡后,任何相同组分的百分含量均相同,这样的化学平衡互称为等效平衡。
2、分类
(1)等温,等容条件下的等效平衡
第一类:
对于反应前后气体分子数改变的可逆反应:
第二类:
对于反应前后气体分子数不变的可逆反应:
(2)等温,等压的等效平衡:
五、化学平衡图像问题
看懂图像(面、线、点、势)-联想规律…分析判断
六、化学反应进行的方向
反应爛变与反应方向:
(1)爛:
一个状态函数,用来描述体系的混乱度,符号为S.单位:
J-mol^K1
(2)体系趋向于有序变为无序,导致体系的嬌增加,这叫做原理,也是反
应方向判断的依据。
.
(3)同一物质,气态、液态、固态时嬌值关系为S(g)S(l)S(s)
2、反应方向判断依据
在温度、压强一定的条件下,化学反应的判断依据为:
AG二AH-TAS0
AH-TAS0
(1)为负,
(2)AH为正,
反应能自发进行
反应达到平衡状态
反应不能自发进行
△S为正时,任何温度反应都能自发进行AS为负时,任何温度反应都不能自发进行
第三章水溶液中的离子平衡
一、弱电解质的电离
1、定义:
电解质:
在中或状态下能导电的-
非电解质:
强电解质:
C
弱电解质:
—
下列物质中HCkNaOH、NaCLBaSO4、HCIO、NH3・出0、Cu(OH)2、H20、SO3、C02.CCI4、
CH2=CH2属非电解质的有:
属强电解质的有:
O
属弱电解质的有:
2、电解质与非电解质本质区别:
电解质的强弱与导电性、溶解性关。
3、电离平衡:
在一定的条件下,当时,电离
过程就达到了平衡状态。
4、影响电离平衡的因素:
A、温度:
电离一般_热,升温电离平衡向移动。
B、浓度:
浓度越大,电离程度;
溶液稀释时,电离平衡向移动。
C、同离子效应:
加入与弱电解质具有相同离子的电解质,会电离。
D、其他外加试剂:
加入能与弱电解质电离的某种离子反应的物质,电离。
5、电离方程式的书写:
用可逆符号弱酸的电离要分布写(第一步为主)
6、电离常数:
在一定条件下,弱电解质在达到电离平衡时,溶液中电离所生成的各种离子浓度的乘积,跟溶液中未电离的分子浓度的比是一个常数。
叫做电离平衡常数,(一般用Ka表示酸,Kb表示碱。
)
表示方法:
AB'
'
A*+B「Ki=
7、影响因素:
a、电离常数的大小主要由物质的本性决定。
b、电离常数受温度变化影响,不受浓度变化影响,在室温下一般变化不大。
C、同一温度下,不同弱酸,电离常数越大,其电离程度越大,酸性越强。
如:
H2SO3>
H3PO4>
HF>
CH3COOH>
H2CO3>
H2S>
HCIO
二、水的电离和溶液的酸碱性
1、水电离平衡:
:
只2°
水的离子积:
Kw=;
25°
C时,;
KW==
Kw只与温度有关,温度一定,则Kw值一定
Kw不仅适用于纯水,适用于任何稀溶液(酸、碱、盐)
2、水电离特点:
(1)可逆
(2)吸热(3)极弱
3、影响水电离平衡的外界因素:
1酸、碱:
水的电离
2温度:
水的电离(因为水的电离是热的)
3能水解的盐:
4、溶液的酸碱性和pH:
(1)pH=1
(2)pH的测定方法:
酸碱指示剂中皐橙、石蕊、酚駄。
变色范围:
甲基橙3.1-4.4(橙色)石蕊5.0-8.0(紫色)酚酿8.2T0.0(浅红
色)
pH试纸_操作,
①事先不能用水湿润PH试纸;
②广泛pH试纸只能读取整数値或范围
三、混合液的pH值计算方法
1、强酸与强酸的混合:
(先求[『]混:
将两种酸屮的『离子物质的量相加除以总体
积,再求其它)[曲混=([H^M+[H+]2V2)/(V1+V2)
2、强碱与强碱的混合:
(先求[OHT混:
将两种酸中的0K离子物质的量相加除以总体积,再求其它)[0町混=([OH]M+[OH]2V2)/(V1+V2)(注意:
不能直接计算[H+]混)
3、强酸与强碱的混合:
(先据H++OH==H20计算余下的『或OH,①『有余,则用余下的『数除以溶液总体积求[H]混;
OR有余,则用余下的0K数除以溶液总体
积求[0H]混,再求其它)
四、稀释过程溶液pH值的变化规律:
1、强酸溶液:
稀释10"
倍时,pH稀pH原+n(但始终不能7)
2、弱酸溶液:
3、强碱溶液:
倍时,pH稀pH據一n(但始终不能7)
4、弱碱溶液:
稀释诃倍吋,pH稀pH^-n(但始终不能7)
5、不论任何溶液,稀释时pH均是向7靠近(即向中性靠近);
任何溶液无限稀释后pH均接近7
6、稀释时,弱酸、弱碱和水解的盐溶液的pH变化—,强酸、强碱变化—。
五、酸碱中和滴定:
1、中和滴定的原理
实质:
H++OFT二出0即酸能提供的『和碱能提供的OH物质的量o
2、中和滴定的操作过程:
(1)滴定管的刻度,0刻度在—,往下刻度标数越来越大,全部容积它的最大刻度值。
滴泄时,所用溶液不得超过最低刻度,不得一次滴定使用两滴定管酸
(或碱),也不得中途向滴定管中添加。
(2)药品:
标准液;
待测液;
指示剂。
(3)准备过程:
准备:
检漏、、、、赶气泡、调液面。
(4)实验过程及滴定终点的判断
3、酸碱中和滴定的误差分析
误差分析:
利用门酸c酸V酸初碱c碱碱进行分析
六、盐类的水解
-
2、水解的实质:
水溶液中盐电离出来的弱离子跟水电离出来的『或OK结合,破坏
水的电离,使平衡向移动,水的电离。
3、盐类水解规律:
1有—才水解,无弱不水解,越弱越水解;
谁—显谁性,同强显中性。
2多元弱酸根,浓度相同时正酸根比酸式酸根水解程度大,碱性更强。
(如:
Na2CO3
>
NaHCO3)
4、盐类水解的特点:
(1)
(2)(3)
5、影响盐类水解的外界因素:
1温度:
温度越水解程度越大(水解吸热,越热越水解)
2浓度:
浓度越小,水解程度越(越稀越水解)
3酸碱:
促进或抑制盐的水解(『促进水解而阳离子水解;
6、酸式盐溶液的酸碱性:
1只电离不水解:
如HSO,显酸性
2电离程度〉水解程度,显性(如:
HSO3-、H2PO4_)
3水解程度〉电离程度,显性(如:
HCO(、HS*、HPO42_)
7、双水解反应:
(1)构成盐的阴阳离子均能发生水解的反应。
双水解反应相互促进,水解程度较大,有的甚至水解完全。
(2)常见的双水解反应完全的为:
Fe*与AIO2\CO32_(HCO3));
A产与AIO2\CO32(HCO3)^S2'
(HS)>
SO32(HSO3)o其特点是相互水解成沉淀或气体。
离子方程式配平依据是两边电荷平衡,如:
2A产+3S2'
+6H2O==2AI(OH)3I+3H2St
8、盐类水解的应用:
水解的应用
实例
原理
净水
明矶净水
、
去油污
用热碱水冼油污物品
CO产+出0仝HCOs+OFT
药品的保存
①配制FeCh溶液时常加入少量盐酸
②配制NazCOj溶液时常加入少量NaOH
C0f+氏0、iICO;
+OH
制备无水盐
由MgCl2创2O制无水MgCl2在HC1气流中加热
若不然,则:
MgCl2・6H2O亠Mg(OH)2+2HC1+4出0Mg(OH)2丄亠MgO+HvO
泡沫灭火器
用A12(S0»
3与NaHCOs溶液混合
比较盐溶液中离子浓度的大小
比较NH4C1溶液屮离子浓度的大小
7时+出0=:
NH:
}・出0+『c(Cl)>
c(NH;
)>
c(H)>
c(OH)'
9、水解平衡常数(KQ
强碱弱酸盐:
Kh=Kw/Ka强酸弱碱盐:
Kh=Kw/Kb<
Kw为该温度下水的离子积,
Ka为该条件下该弱酸电离平衡常数;
心为该条件下该弱碱的电离平衡常数)
7.电离、水解方程式的书写原则
1、多元弱酸(多元弱酸盐)的电离(水解)的书写原则:
分步书写
不管是水解还是电离,都决定于第一步,第二步一般相当微弱。
2、多元弱碱(多元弱碱盐)的电离(水解)书写原则:
一步书写
八、溶液中微粒浓度的大小比较
基本原则:
抓住溶液中微粒浓度必须满足的三种守恒关系:
1电荷守恒:
任何溶液均显电性,各阳离子浓度与其所带电荷数的乘积之和
=各阴离子浓度与其所带电荷数的乘积之和
2物料守恒:
(即原子个数守恒或质量守恒)
某原子的总量(或总浓度)=其以各种形式冇在的所有微粒的呈(或浓度)Z和
3质子守恒:
即水电离出的『浓度与0K浓度相等。
九、难溶电解质的溶解平衡
1、难溶电解质的溶解平衡的一些常见知识
(1)溶解度_小于O.Olg的电解质称难溶电解质。
(2)反应后离子浓度降至以下的离子反应为完全反应。
如酸碱中和时[『]
降至10-7mol/L<
10-5mol/L,故为完全反应,用“二”,常见的难溶物在水中的离子浓度均远低于10'
5mol/L,故均用“二”。
(3)难溶并非不溶,任何难溶物在水屮均存在溶解平衡。
(4)掌握三种微溶物质:
(5)溶解平衡常为吸热,但Ca(OH)2为放热,升温其溶解度减少。
(6)溶解平衡存在的一般前提是:
存在沉淀,否则不存在平衡。
2、溶解平衡方程式的书写
注意在沉淀后用⑸标明状态,并用"
Ag2S(s)=hAg*(aq)+S2(aq)
3、沉淀生成的三种主要方式
(1)加沉淀剂法:
Ksp越小,沉淀越完全;
沉淀剂过塑能使沉淀更完全。
(2)调pH值除某些易水解的金属阳离子:
如除去MgCb溶液中FeCb可以
加入
(3)氧化还原沉淀法:
(4)同离子效应法
4、沉淀的溶解:
沉淀的溶解就是使溶解平衡正向移动。
常采用的方法有:
①酸碱;
②氧化还原;
③
5、沉淀的转化:
溶解度大的生成溶解度小的,溶解度小的生成溶解度更小的。
AgNO3―AgCI()—Br(淡黄色)一gl(黄色)一Ag2S(黑色)
6、溶度积(Ksp)
⑴表达式:
AmBn⑸三二mAn+(aq)+nBm(aq)
Ksp=[c(An+)]m-[c(Bm)]n
⑵影响溶解平衡的因素:
决定因素是
外因:
①浓度:
加水,平衡向方向移动。
②温度:
升温,多数平衡向方向移动。
⑶、溶度积规则
Qc(离子积)KSP
QcKsp
QcKsp
有沉淀析出
平衡状态
未饱和,继续溶解第四章电化学基础
1.原电池:
化学能转化为电能的装置叫做原电池
2、组成条件:
①②
3、电子:
外电路:
极一一导线一一—极
内电路:
盐桥中—离子移向负极的电解质溶液,—离子移向正极溶液。
4、电极反应:
以锌铜原电池为例:
负极:
反应:
正极:
总反应式:
5、正、负极的判断:
(1)从电极材料:
一般为负极;
或金属为负极,非金属为正极°
(2)从电子的流动方向和电流方向
(3)从发生反应
(4)根据电解质溶液内离子的移动方向
(5)根据实验现象
2.化学电池
1、电池的分类:
化学电池、太阳能电池、原子能电池
2、化学电池:
借助于化学能直接转变为电能的装置
3、化学电池的分类:
一次电池、二次电池、燃料电池
一次电池
1、常见一次电池:
碱性锌镭电池、锌银电池、锂电池等
二次电池又叫充电电池
1•铅蓄电池的电极反应
放电:
负极(铅):
正极(氧化铅):
充电:
阴极:
阳极:
两式可以写成一个可逆反应:
PbO2+Pb+2H2SO4上皂2PbSO4I+2H2O
2.目前已开发出新型蓄电池:
银锌电池、镉镰电池、氢線电池、锂离子电池、聚合物锂离子电池
燃料电池
1、燃料电池:
使燃料与氧化剂反应直接产生电流的一种化学电池
2、电极反应:
一般燃料电池发生的电化学反应的最终产物与燃烧产物相同,可根据燃烧反应写出总的电池反应,但不注明反应的条件。
,负极发生氧化反应,正极发生还原反应,不过要注意一般电解质溶液要参与电极反应。
以盘氧燃料电池为例,钳为正、负极,介质分为酸性、碱性和中性。
当电解质溶液呈酸性时:
正极:
当电解质溶液呈碱性时:
正极:
甲烷燃料电池是用金属钳片插入KOH溶液作电极,在两极上分别通甲烷和氧气。
电极反应式为:
负极:
;
O
电池总反应式为:
3、燃料电池的优点:
能量转换率高、废弃物少、运行噪音低
3.电解原理
1、电解池:
把电能转化为化学能的装置电解槽
2、电解:
直流电通过电解质溶液,在阴阳两极引起氧化还原反应的过程
3、放电:
当离子到达电极吋,失去或获得电子,发生氧化还原反应的过程
4、电子流向:
(电源)负极一(电解池)阴极一(离子定向运动)电解质溶液一(电解池)阳极—(电源)正极
5、电极名称及反应:
与直流电源的相连的电极,发生反应
6、电解CuCH溶液的电极反应:
)
电解质溶液的导电过程,就是电解质溶液的电解过程
阴极(阳离子)放电顺序
Ag+>
Hg2+>
Fe3+>
Cu2+>
H+)>
Pb2+>
Sn2+>
Fe2+>
Zn2+>
AI3+>
Mg2+>
Na+>
Ca2+>
K+
阳极放电顺序
惰性电极时:
S2>
r>
Br>
cr>
OH>
含氧酸根离子>
F(SO327MnO4*>
OH)
活性电极吋:
电极本身溶解放电
注意先要看电极材料,是惰性电极还是活性电极,若阳极材料为活性电极(Fe、Cu)等金屈,则阳极反应为电极材料失去电子,变成离子进入溶液;
若为惰性材料,则根据阴阳离子的放电顺序,依据阳氧阴还的规律来书写电极反应式。
用惰性电极电解电解质溶液规律
电解类型
电解质分类
电极反应特点
pH变化
溶液复原应加
四、电解原理的应用
1、电解饱和食盐水以制造烧碱、氯气和氢气
2、电镀
(1)应用电解原理在某些金属表而镀上一薄层其他金属或合金的方法
(2)、电极、电解质溶液的选择:
(镀层金属)M—ne一二二
待镀金属(镀件):
Mn++ne-==M
电解质溶液:
含有镀层金屈离子的溶液做电镀液
(3)、电镀应用之一:
铜的精炼
;
阴极:
电解质溶液:
3、电冶金
(1)、电冶金:
使矿石中的金屈阳离子获得电子,从它们的化合物中还原出来用于冶炼活泼金属,如钠、镁、铝
(2)、电解氯化钠:
通电前,氯化钠高温下熔融:
NaCI=Na++C厂通直流电后:
☆规律总结:
原电池、电解池、电镀池的判断规律
(1)若无外接电源,又具备组成原电池的三个条件即为原电池。
(2)若有外接电源,两极插入电解质溶液中,则可能是电解池或电镀池;
当阴极为金属,阳极亦为金属且与电解质溶液中的金属离子属同种元素吋,则为电镀池。
(3)若多个单池相互串联,又有外接电源时,则与电源相连接的装置为电解池或电镀池。
若无外接电源时,先选较活泼金属电极为原电池的负极(电子输出极),有关装置为原电池,其余为电镀池或电解池。
☆
☆原电池,电解池,电镀池的比较
类别
原电池
电解池
电镀池
定义
(装置特点)
将化学能转变成电能的装置
将电能转变成化学能的装置
应用电解原理在某些金属表面镀上一侧层英他金属
是否是自发反应
装置特征
有电源,两级材料可同可不同
形成条件
活动性不同的两极电解质溶液形成闭合回路
镀层金属接电源正极,待镀金屈接负极;
电镀液必须