《基础实验操作及装置改进二附答案》主观题精选精练Word文件下载.docx
《《基础实验操作及装置改进二附答案》主观题精选精练Word文件下载.docx》由会员分享,可在线阅读,更多相关《《基础实验操作及装置改进二附答案》主观题精选精练Word文件下载.docx(24页珍藏版)》请在冰豆网上搜索。
使内外压强平衡(5)浓硫酸(6)将右侧注射器的活塞向右拉,松手,活塞恢复至原处
(7)促进微溶的硫酸钙溶解,使硫酸继续与碳酸钙反应
(8)VmL−(V1mL+V2mL);
×
100%
(9)样品中的碳酸钙能全部与稀硫酸反应,测定的结果更准确
【解析】【解答】
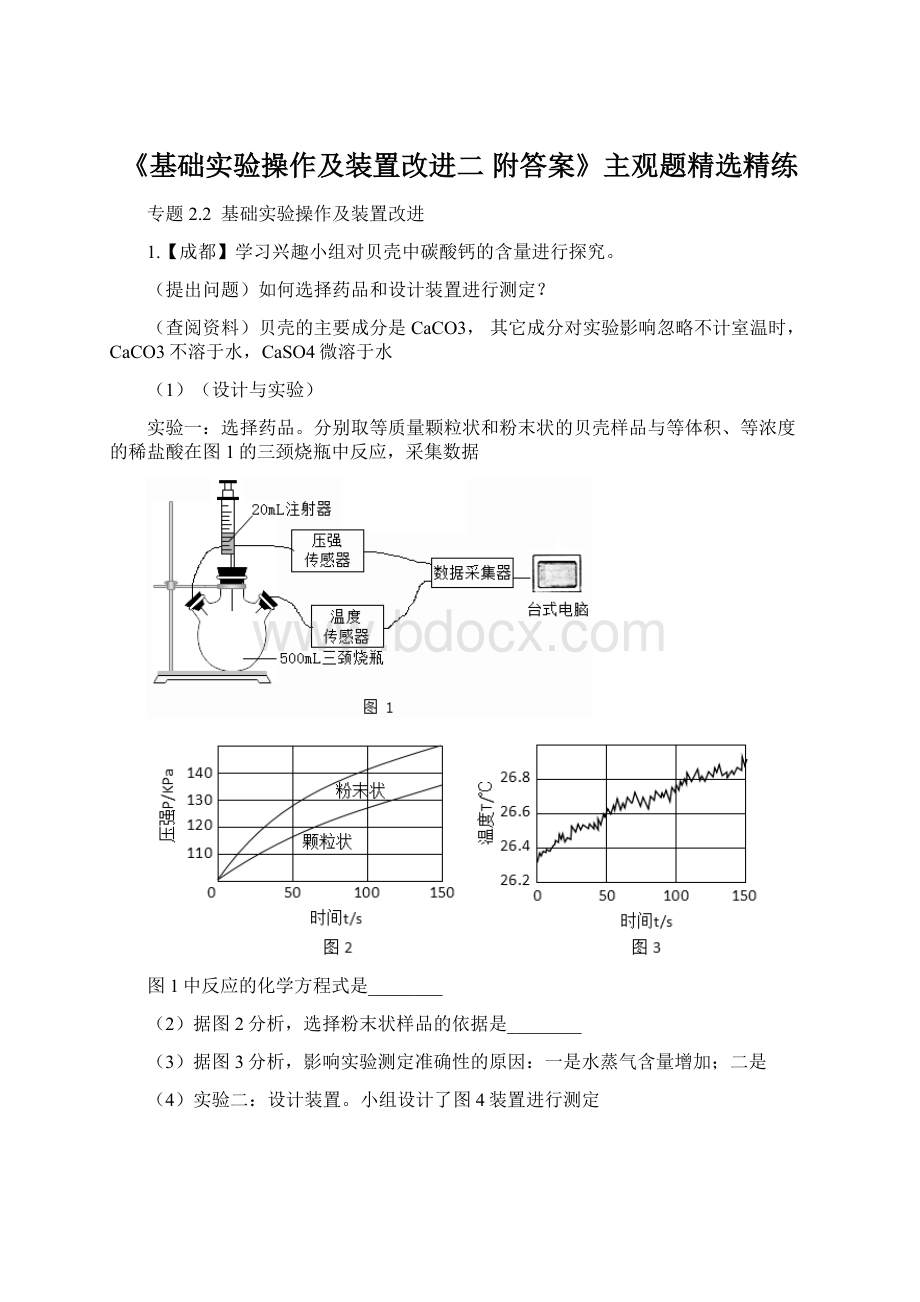
(1)由题意可知,图1中的反应是贝壳中的碳酸钙与盐酸反应生成氯化钙、水和二氧化碳,故反应的化学方程式写为:
CaCO3+2HCl=CaCl2+H2O+CO2↑。
(2)由图2可知,粉末状贝壳与盐酸反应的时间短,说明单位时间内,反应效率更高,故填单位时间内,反应效率更高。
(3)由图3可知,随反应时间的延长,浓盐酸挥发出来的HCl气体增加,也能影响实验测定准确性,故填浓盐酸挥发出来的HCl气体增加。
(4)稀硫酸与碳酸钙反应生成硫酸钙、水和二氧化碳,观察到的现象是试管中出现气泡,量气管内液面下降,水准管内液面上升,故填试管中出现气泡,量气管内液面下降,水准管内液面上升;
由题意可知,影响实验测定准确性的因素包括压强,读数前调节水准管与量气管液面相平可以使内外压强平衡,避免压强不同对实验的准确性产生干扰,故填使内外压强平衡。
(5)试剂a为浓硫酸,用浓硫酸吸收生成二氧化碳中的水分,避免水分对测定二氧化碳产生干扰,故填浓硫酸。
(6)检查该装置气密性的方法是连接装置,将右侧注射器的活塞向右拉,松手,如果活塞恢复至原处,证明装置不漏气,故填将右侧注射器的活塞向右拉,松手,活塞恢复至原处。
(7)氯化铵溶液,发现又产生气泡,说明加入氯化铵后硫酸与碳酸钙继续反应,说明氯化铵能够促进硫酸钙的溶解,故填促进微溶的硫酸钙溶解,使硫酸继续与碳酸钙反应。
(8)实验后收集到的气体包括二氧化碳和空气,其中空气的体积=V1mL+V2mL,所以反应生成CO2体积=VmL−(V1mL+V2mL),故填VmL−(V1mL+V2mL);
由化学方程式CaCO3+H2SO4=CaSO4+H2O+CO2↑可知,参加反应的碳酸钙与生成的二氧化碳的质量比=100:
44,消耗碳酸钙的质量为
g,样品碳酸钙质量分数表达式=
100%,故填
100%。
(9)与实验二相比,实验三的优点是样品中的碳酸钙能全部与稀硫酸反应,测量的结果更准确,故填样品中的碳酸钙能全部与稀硫酸反应,测定的结果更准确。
2.【菏泽】现有氯酸钾、过氧化氢溶液、二氧化锰、稀硫酸、稀盐酸、石灰石,及下列仪器:
(1)仪器⑥的名称________。
(2)利用上述药品,从①一⑦中选择仪器,可以制取一瓶较干燥氧气或二氧化碳,你选择的仪器是________(填序号),其反应的化学方程式为________(选写一个)。
(3)小明用A、B两种仪器组装了一套发生装置,这套装置与你的装置相比,具有的优点是(任写一条)。
(4)小明利用混有CO2的CO气体还原Fe2O3,并验证反应后的气体产物,现有下列实验装置(可重复选用),按气体流向从左到右,装置的连接顺序依次是:
乙________丁。
【答案】
(1)锥形瓶
(2)①②⑥⑦;
或
(3)可以控制反应速率
(4)乙→甲→丙→甲→丁
(1)仪器⑥的名称是锥形瓶;
(2)氧气可用过氧化氢与二氧化锰制得,该反应属于固液不加热反应,氧气不易溶于水,密度比空气大,可用排水法或向上排空气法收集,向上排空气法制得的氧气比较干燥,根据所给仪器,可选择①②⑥⑦;
过氧化氢在二氧化锰的催化下分解为水和氧气,该反应的化学方程式为:
;
实验室通常用石灰石(或大理石)与稀盐酸反应制取二氧化碳,该反应属于固液不加热反应,且二氧化碳溶于水、密度比空气大,应用向上排空气法收集,故根据所给仪器,可选择①②⑥⑦;
石灰石的主要成分是碳酸钙,碳酸钙和稀盐酸反应生成氯化钙、二氧化碳和水,该反应的化学方程式为:
(3)该仪器可通过注射器控制药品的滴加速率,从而控制反应速率,故填:
可以控制反应速率;
(4)一氧化碳中混有二氧化碳,二氧化碳会干扰反应后气体产物的验证,故应先除去二氧化碳,氢氧化钠能与二氧化碳反应,可除去二氧化碳,故应先将混合气体通入氢氧化钠溶液,然后用氢氧化钙溶液验证二氧化碳是否除尽,然后通入丙,使一氧化碳与氧化铁反应生成铁和二氧化碳,然后用氢氧化钙溶液检验生成的气体二氧化碳,最后用气囊收集尾气。
,防止一氧化碳散逸到空气中,污染空气,故填:
乙→甲→丙→甲→丁。
3.【成都】配制100g质量分数为16%的Na2CO3溶液,用于演示灭火器原理。
回答下列问题
(1)计算Na2CO3的质量为________g,称量Na2CO3的仪器名称是________
(2)20℃时,Na2CO3的溶解度为,⑤中的溶液________(填“是”或“不是”)该物质的饱和溶液
(3)将烧杯中溶液倒入吸滤瓶的操作是________。
从橡胶管喷出大量液体的原因是________
(4)酒精(C2H5OH)可作燃料,在空气中完全燃烧的化学方程式是________。
酒精燃烧失火,可用干粉灭火器灭火。
NaHCO3是干粉的主要成分,俗称是________。
用干粉灭火器灭火的正确操作顺序是________→________→________(填序号)
【答案】
(1);
托盘天平
(2)不是
(3)将烧杯尖嘴紧挨着吸滤瓶口,缓慢倾倒;
浓盐酸与碳酸钠溶液剧烈反应,产生二氧化碳,使瓶内压强迅速增大
(4)
;
小苏打;
c;
b;
a
【解析】
(1)Na2CO3的质量=100g×
16%=16g;
称量Na2CO3的仪器名称为托盘天平。
(2)20℃时,Na2CO3的溶解度为21.5g。
实验只称量了16gNa2CO3溶解于84g水中,此时的溶解度为
,小于21.5g,故不是该物质的饱和溶液。
(3)将烧杯中溶液倒入吸滤瓶的操作是将烧杯尖嘴紧挨着吸滤瓶口,缓慢倾倒;
从橡胶管喷出大量液体的原因是浓盐酸与碳酸钠溶液剧烈反应,产生二氧化碳,使瓶内压强迅速增大。
(4)酒精(C2H5OH)在空气中完全燃烧生成二氧化碳和水,化学方程式为
NaHCO3是干粉的主要成分,俗称是小苏打;
用干粉灭火器灭火的正确操作顺序是拔出保险销、解脱喷管、按下压把,对准火焰根部喷射,故顺序为c、b、a。
4.【常州】如图是初中化学常用实验装置(夹持装置已省略)。
(1)仪器a的名称是________。
(2)该装置用于实验室制取CO2:
装置甲中发生反应的化学方程式为。
(3)该装置用于实验室制取干燥的O2:
乙中存放的试剂为________。
检验丙中气体是否收集满的方法是________。
(4)该装置用于实验室制取干燥的H2:
对装置所作的简单改动可以是________。
(5)该装置用于混合物中物质含量测定:
在丙装置后连接量气装置,取黄铜(铜锌合金)粉末于锥形瓶中,加入足量稀硫酸,待完全反应后,根据气体体积换算得到生成的氢气质量为,则该混合物中铜的质量分数为多少?
(写出计算过程)
【答案】
(1)分液漏斗
(2)CaCO3+2HCl=CaCl2+H2O+CO2↑
(3)浓硫酸;
将带火星的木条放在丙装置右侧导管口,若木条复燃,则集满
(4)将原来乙装置短导管与丙装置长导管相连的胶皮管拆开,改成用胶皮管将乙装置的短导管与丙装置的短导管相连
(5)解:
设:
该混合物中锌的质量为x。
解得
该混合物中铜的质量分数为:
答:
该混合物中铜的质量分数为67.5%。
(1)根据图示,仪器a的名称是:
分液漏斗。
(2)装置甲适用于固液反应,不需要加热制取气体,实验室常用大理石(或石灰石)和稀盐酸反应制取CO2,符合该装置要求。
大理石的主要成分是碳酸钙,碳酸钙和稀盐酸反应生成氯化钙、水和二氧化碳,故装置甲中发生反应的化学方程式为:
(3)该装置如果用于实验室制取氧气,则是利用过氧化氢溶液在二氧化锰催化作用下分解生成氧气,装置甲排出的气体中含有水蒸气。
根据装置乙的特点,乙中的干燥剂必须是液态,浓硫酸常温下是液态,且氧气不跟浓硫酸反应,因此制取干燥的O2,乙中存放的试剂为:
浓硫酸。
因为氧气能使带火星的木条复燃,故检验丙中氧气是否收集满的方法是:
将带火星的木条放在丙装置右侧导管口,若木条复燃,则集满。
(4)因为实验室常用锌和稀硫酸在常温下反应制取氢气,氢气也不跟浓硫酸反应,所以装置甲和装置乙不需要改动。
又因为氢气的密度比空气小,所以用装置丙收集氢气必须是“短进(氢气)长出(空气)”,因此该装置用于实验室制取干燥的H2,对装置所作的简单改动是:
将原来乙装置短导管与丙装置长导管相连的胶皮管拆开,改成用胶皮管将乙装置的短导管与丙装置的短导管相连。
5.【安顺】根据如图回答问题。
(1)反应原理
①加热高锰酸钾、分解过氧化氢溶液或加热氯酸钾均可产生氧气,其中分解过氧化氢溶液和加热氯酸钾时,加入二氧化锰在反应中起的作用是________。
三种方法中,写出其中一个反应的化学方程式________。
②石灰石和稀盐酸反应产生二氧化碳的化学方程式为。
(2)制取O2和CO2。
连接如图的装置完成实验。
反应物
装置(填“甲”或“乙”)
物质
B作用
C作用
________
水
接水
石灰石和稀盐酸
乙
干燥CO2
【答案】
(1)催化作用;
(或
);
(2)H2O2溶液和二氧化锰;
甲;
收集O2;
浓H2SO4;
收集二氧化碳
(1)①分解过氧化氢溶液和加热氯酸钾时,二氧化锰是催化剂,故加入二氧化锰在反应中起的作用是:
催化作用;
过氧化氢在二氧化锰的催化下受热分解为水和氧气,该反应的化学方程式为:
高锰酸钾受热分解为锰酸钾、二氧化锰和氧气,该反应的化学方程式为:
氯酸钾在二氧化锰的催化下受热分解为氯化钾和氧气,该反应的化学方程式为:
②石灰石的主要成分是碳酸钙,碳酸钙和稀盐酸反应生成氯化钙、二氧化碳和水,该反应的化学方程式为:
(2)该装置是固液不加热反应制取氧气,适用于过氧化氢与二氧化锰制取氧气,故反应物是:
H2O2溶液和二氧化锰;
所连接装置内所加的物质是水,故应连接甲装置,氧气的密度比水小,从a端进入,是排水法收集氧气,
故填:
收集氧气;
制取二氧化碳,
反应物是:
石灰石和稀盐酸,连接装置乙,长进短出,故是洗气,可在装置乙中加浓硫酸,浓硫酸具有吸水性,且不与二氧化碳反应,可用于干燥二氧化碳,二氧化碳的密度比空气大,可用向上排空气法收集,故C的作用是收集二氧化碳,故填:
浓硫酸;
收集二氧化碳。
6.【安顺】化学是一门以实验为基础的学科。
请结合下列实验装置图回答问题:
(1)写出图中①、②两种仪器的名称:
①________,②________。
(2)某同学用高锰酸钾加热制取氧气,反应的化学方程式为;
应选择的发生装置为________(填字母),收集装置为________(填字母)。
(3)A装置与C装置比较,A装置的优点是可以控制反应的发生和停止。
请写出一个利用A装置此优点的反应化学方程式________。
(4)实验室可用金属与浓硫酸反应制取SO2气体,金属锌和金属铜都能与浓硫酸反应制SO2气体。
欲制取一瓶纯净的SO2气体,最好选择金属________(填“锌”或“铜”),选择理由是。
【答案】
(1)铁架台;
集气瓶
(2)
B;
D(填“F”或“D或F”均可)
(3)
(答案合理均可)
(4)Cu;
随着反应的进行,浓硫酸会变成稀硫酸,锌能与稀硫酸反应产生氢气,使得SO2不纯,而铜不与稀硫酸反应
(1)①是铁架台,②是集气瓶;
故答案为:
铁架台;
集气瓶;
(2)高锰酸钾在加热的条件下生成锰酸钾、二氧化锰和氧气,反应的化学方程式为:
,该反应属于固、固加热型,适合用装置B作发生装置;
氧气的密度比空气大,不易溶于水,可用装置D或F收集;
D(填“F”或“D或F”均可);
(3)实验室常用大理石(或石灰石)和稀盐酸反应制取二氧化碳,常用稀硫酸和锌反应制取氢气,都是颗粒状固体和液体反应,都可以通过A控制反应的发生与停止。
碳酸钙和稀盐酸反应生成氯化钙、水和二氧化碳,反应的化学方程式为:
稀硫酸和锌反应生成硫酸锌和氢气,反应的化学方程式为:
(答案合理均可);
(4)欲制取一瓶纯净的SO2气体,最好选择金属是铜,因为随着反应的进行,浓硫酸会变成稀硫酸,锌能与稀硫酸反应生成氢气,使的二氧化硫不纯,而铜不与稀硫酸反应,故答案为:
Cu;
随着反应的进行,浓硫酸会变成稀硫酸,锌能与稀硫酸反应产生氢气,使得SO2不纯,而铜不与稀硫酸反应。
7.【巴中】化学所取得的丰硕成果与实验的重要作用分不开,根据下列实验装置回答问题。
(1)写出仪器a的名称:
________。
(2)实验室用B装置制取氧气,发生的化学反应方程式为,其基本反应类型为________反应。
若要收集瓶氧气可选用的收集装置为________(选填编号)。
(3)若要制取并收集一瓶纯净、干燥的二氧化碳气体(常混有少量水蒸气和氯化氢气体),装置连接的正确顺序是________(选填字号)
①产生气体→F→D②产生气体→G→D③产生气体→F→G→D④产生气体→G→F→D
【答案】
(1)铁架台
(2)
分解;
C或D(3)④
(1)仪器a的名称为铁架台;
(2)用B装置是固液不加热型的发生装置,则应用过氧化氢制取氧气,发生反应的化学方程式为
,该反应是一种反应物产生了两种生成物的反应,其基本反应类型为分解反应。
由于氧气密度比空气略大,不易溶于水,可以用排水法或向上排空气法收集氧气,则选用的收集装置为C或D;
(3)产生二氧化碳后,要先用饱和碳酸氢钠溶液除去氯化氢气体,再用浓硫酸除去水蒸气,如果顺序颠倒,就不能除去水了;
由于二氧化碳的密度比空气大,能溶于水,所以只能用向上排空气法收集,所以装置连接的正确顺序是:
产生气体→G→F→D;
8.【青岛】近年来,我国高铁飞速发展,已成为世界上唯一高铁成网运行的国家。
(1)请回答下列问题。
实验一
实验二
实验三
实验操作
实验现象
蜡烛火焰________
软塑料瓶变瘪程度较大的是________
(选填“甲”或“乙”)
干石蕊纸花不变色,湿石蕊纸花变红色
实验结论
①二氧化碳的密度比空气大;
②二氧化碳既不能燃烧,也不能支持燃烧
二氧化碳能与氢氧化钠发生反应
(2)制造高铁列车使用了多种材料。
下列高铁列车的部件中,其主要材料属于金属材料的是_____(选填字母序号)。
A.玻璃车窗
B.镁铝合金车体C.塑料小桌板
D.涤纶座套
(3)高铁电路多用铜质导线,这是利用了铜的延展性和________性。
(4)高铁刹车片由合金锻钢制作,时速300公里以上的列车紧急制动时,轮毂盘面和刹车片的温度瞬间达到700℃以上,合金锻钢应该具备耐磨和________等特性。
(5)建造高铁需要消耗大量的铝、铁等金属。
工业炼铁的原理是氧化铁(Fe2O3)和一氧化碳在高温条件下反应,其化学方程式为。
(6)车身表面烤漆不仅美观,还能起到防锈的作用。
其防锈的原理是。
(7)目前世界上已有50%以上的铁得到了回收利用。
回收利用废旧金属的社会意义是________(写出一条即可)。
【答案】
(1)由下到上依次熄灭;
乙;
二氧化碳能与水反应
(2)B(3)导电
(4)耐高温(5)
(6)隔绝水和氧气
(7)节约金属资源(合理即可)
【解析】【解答】实验一:
由于二氧化碳既不能燃烧,也不能支持燃烧,且二氧化碳的密度比空气大。
实验现象:
蜡烛火焰由下到上依次熄灭;
实验二:
甲中50mL水溶解等体积的二氧化碳,瓶内气压减小程度低,乙中二氧化碳能与氢氧化钠发生反应,生成了碳酸钠和水,瓶中气压减小程度大,所以软塑料瓶变瘪程度较大的是乙;
实验三:
第1支试管中干石蕊纸花不变色,说明二氧化碳不能使干石蕊纸花不变色,第2支试管中,二氧化碳与湿石蕊纸花中的水反应产生碳酸,碳酸使湿石蕊纸花变红色,说明二氧化碳能与水反应;
(2)A、玻璃车窗,属于无机非金属材料,不正确;
B、镁铝合金车体,是金属材料,正确;
C、塑料小桌板,是合成材料,不正确;
D、涤纶座套,是合成材料,不正确。
B。
(3)高铁电路多用铜质导线,这是利用了铜的延展性和导电性;
(4)列车紧急制动时,轮毂盘面和刹车片的温度瞬间达到700℃以上,合金锻钢应该具备耐磨和耐高温等特性;
(5)工业炼铁的原理是氧化铁(Fe2O3)和一氧化碳在高温条件下反应,其化学方程式为:
其防锈的原理是隔绝水和氧气;
(7)金属矿物的储量有限,而且不可再生,我们必须保护金属资源并进行废旧金属的回收利用,回收利用废旧金属可以节约金属资源、节约冶炼金属所需的能源、能降低成本,减少环境污染等。
9.【青岛】实验室制取气体时需要的部分装置如下图所示,请回答下列问题。
(信息)二氧化碳不易溶于饱和碳酸氢钠溶液。
(1)实验室中可用过氧化氢溶液与二氧化锰制取氧气,反应的化学方程式为,应选用的发生装置是________(选填装置字母序号)。
(2)实验室中用石灰石和稀盐酸制取一瓶干燥、纯净的二氧化碳气体,所选装置的连接顺序为:
气体发生装置→________→________→D(选填装置字母序号)。
(3)确定实验室制取气体的反应原理时,下列因素中不需要考虑的是___(选填字母序号)。
A.药品容易获得,能生成所要制取的气体B.反应条件易于控制,反应速率适中
C.操作简便易行,安全可靠,节能环保D.所要制取气体的颜色和气味
【答案】
(1)
B
(2)G;
F(3)D
(1)实验室中可用过氧化氢溶液与二氧化锰制取氧气,反应的化学方程式为RC
,反应物是固体和液体,且反应条件不需加热,故发生装置应选择B。
(2)实验室中用石灰石和稀盐酸制取一瓶干燥、纯净的二氧化碳气体,所以制得的二氧化碳气体在收集前要进行除杂和干燥,除杂是用饱和的碳酸氢钠溶液除去气体中的氯化氢气体,再用浓硫酸对气体进行干燥,故所选装置的连接顺序为:
气体发生装置→G→F→D。
(3)A、需考滤药品是否容易获得,能否生成所要制取的气体,A正确;
B、需考滤反应条件是否易于控制,反应速率适中,B正确;
C、需考滤操作简便易行,安全可靠,节能环保,C正确;
D、不需考滤要制取气体的颜色和气味,气体的颜色和气味是物理性质,与制取气体的方法、原理和操作过程没有关系,D不正确。
10.【金昌】实验室常用下列装置制取气体,请你根据所学知识回答有关问题。
(1)写出图中标有序号的仪器名称:
①________;
②________;
(2)实验室用装置A来制取氧气,但装置A有明显不正确,请你指出不正确________,若按该装置操作的后果是。
(3)实验室常用装置B来制取氧气,其反应的化学方程式为,收集装置选________。
实验室选用装置B或装置C还可以制取CO2,其反应药品是________,与装置B相比,装置C的一个突出优点是。
【答案】
(1)试管;
锥形瓶
(2)试管口高于试管底部;
冷凝水倒流,试管炸裂
(3)2H2O2
2H2O+O2↑;
E或F;
石灰石或大理石和稀盐酸;
可控制反应的发生和停止
(1)由图可知①为试管;
②为锥形瓶,故填:
试管;
锥形瓶。
(2)试管口需低于试管底部,否则容易造成冷凝水倒流试管炸裂,故填:
试管口高于试管底部;
冷凝水倒流,试管炸裂。
(3)过氧化氢制氧气,不需要加热,可用B做发生装置,过氧化氢在二氧化锰的催化下分解为水和氧气,该反应的化学方程式为2H2O2
2H2O+O2↑,氧气密度比空气大,不易溶于水,可用排水法或向上排空气法收集,故收集装置选E或F;
实验室用石灰石或大理石和稀盐酸制取二氧化碳,在装置C中,固体药品放在多孔隔板上,液体药品从长颈漏斗中加入。
反应开始后,关闭开关时,试管中的气体增多,压强增大,把液体压入长颈漏斗,固体和液体分离,反应停止,打开开关时,气体导出,试管中的气体减少,压强减小,液体和固体混合,反应进行。
实验室常用装置C代替装置B制取气体,装置C的优点是可以随时控制反应的发生与停止,
2H2O2
可控制反应的发生和停止。
11.【日照】在实验室里,用下图所示的装置进行有关实验。
请回答下列问题:
(1)用加热高锰酸钾的方法制取氧气,组装发生装置应选择________(填写字母标号,下同),反应化学方程式为。
(2)用混合过氧化氢溶液和硫酸铜溶液的方法制取氧气,为了便于控制反应,组装发生装置应选择________,硫酸铜溶液的作用是。
(3)用加热无水醋酸钠和碱石灰固体混合物的方法制取甲烷,组装发生装置应选择________,上述装置中,能用于收集甲烷的是________。
(4)选用上述装置并进行改进,设计了如图所示装置制取二氧化碳,该发生装置的优点是可以控制反应随时发生或停止,节约药品。
使反应停止的操作是。
【答案】
(1)BD;
(2)AC;
催化作用(3)BD;
E、F
(4)抽拉(或提起)粗铜丝,使小布袋与液体脱离接触
(1)用加热高锰酸钾的方法制取氧气,属于固体