对硝基乙酰苯胺的制备与纯化Word文档格式.docx
《对硝基乙酰苯胺的制备与纯化Word文档格式.docx》由会员分享,可在线阅读,更多相关《对硝基乙酰苯胺的制备与纯化Word文档格式.docx(15页珍藏版)》请在冰豆网上搜索。
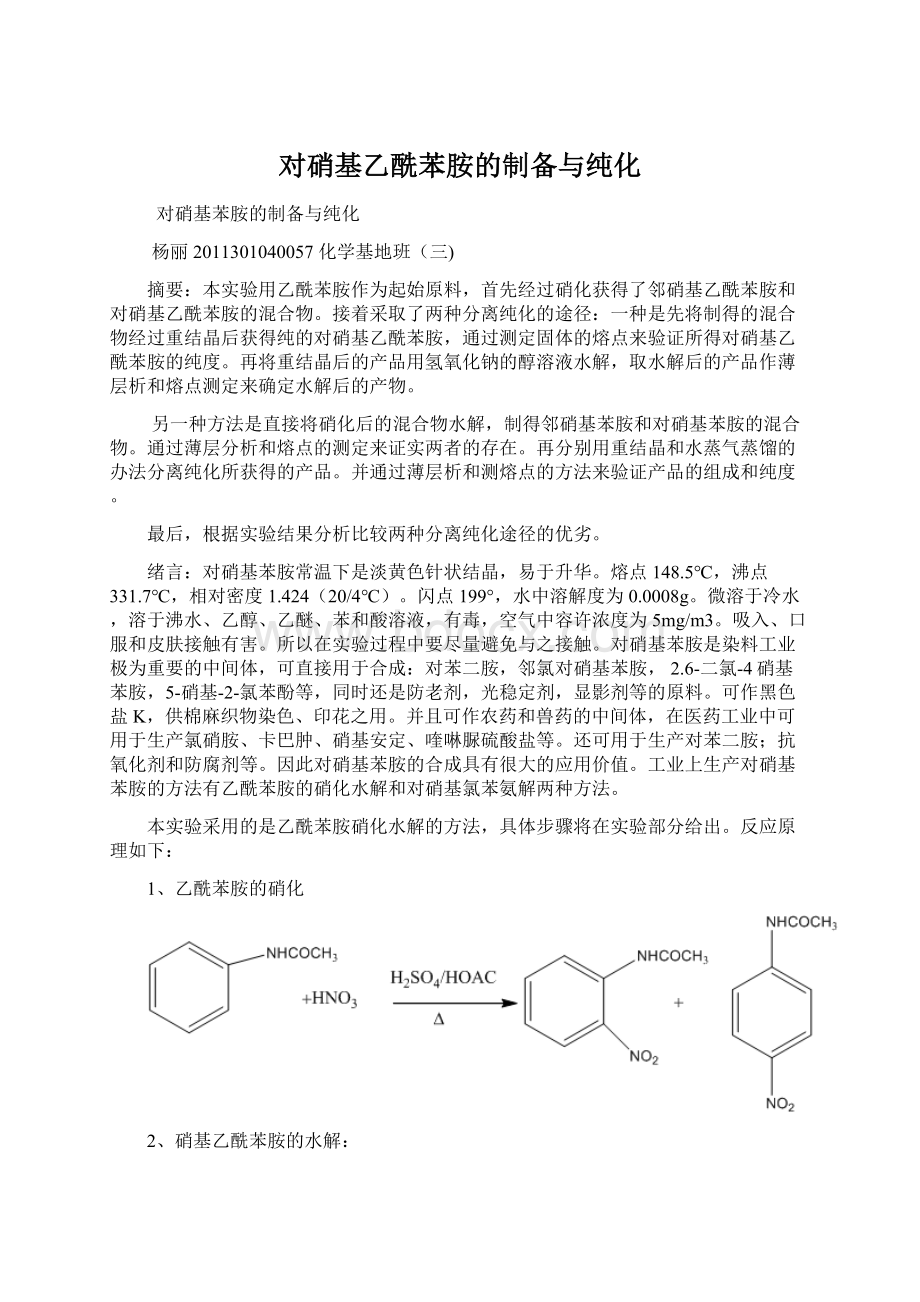
1、乙酰苯胺的硝化
2、硝基乙酰苯胺的水解:
而纯化和分离的办法主要采取了薄层析、重结晶、水蒸气蒸馏三种办法。
三者的分离原理如下。
薄层析:
薄层色谱(TLC)是用来鉴别产物成分与辨别产物纯度的有效方法。
不同物质的极性不同因此与展开剂的作用力不同,当物质随展开剂攀援而上时会由于攀援速度不同而分离开来。
溶剂前沿与起始线间距离品点与起始线距离
溶剂前沿
样样品点与起始线间距离品点与起始线距离
起始线
重结晶:
重结晶是纯化静态物质的普适的、最常用的方法之一。
用适当的溶剂把
含有杂质的晶体溶解,配成接近沸腾的浓溶液,趁热滤去不溶性杂质,使滤液冷却析出结晶,以达到纯化晶体的目的。
水蒸气蒸馏:
有机物与水一起共热,当体系总的蒸气压等于大气压力时,体系沸腾,此时,有机物在低于100oC的温度下随蒸气一起蒸出来,这样的操作叫做水蒸气蒸馏。
♦水蒸气蒸馏的用途及适用场合:
水蒸气蒸馏是用来分离和提纯液态或固态有机化合物的一种方法,常用于下列场合:
(1)某些沸点高的有机化合物,在常压蒸馏虽可与副产品分离,但易将其破坏。
(2)混合物中含有大量树枝状杂质或不挥发性杂质,采用蒸馏、萃取等方法都难于分离;
(3)从较多固体反应物中分离出被吸附的液体。
♦被提纯物质必须具备以下几个条件:
(1)不溶或难溶于水;
(2)共沸腾下与水不发生化学反应;
(3)在100oC左右时,必须具有一定的蒸气压[至少666.5~1333Pa(5~10mmHg)]
实验参数表格:
名称
分子量
性状
折光率
比重
熔点
(oC)
沸点
溶解度(/100g)
水
醇
醚
乙酰苯胺
135.17
白色有光泽片状结晶
1.5860
1.219
114.3
304
0.46(20oC)
36.9
(20oC)
溶
临硝基乙酰苯胺
180.16
淡黄色片状或棱状晶体
1.4149
94
100
(0.133KPa)
溶于沸水微溶于冷水
溶于乙醇
溶于乙醚
对硝基乙酰苯胺
无色晶体
1.41
215.6
(1.06x10-3KPa)
溶于热水
邻硝基苯胺
138.13
橙黄色针状晶体
1.44
69.7
284.5
微溶于冷水溶于沸水
易溶于乙醚
对硝基苯胺
淡黄色针状晶体,易升华
1.424
148.5
331.7
0.0008g(冷水)
溶于沸水
实验内容:
实验流程图
邻、对硝基苯胺
测熔点测熔点薄层析
重结晶
水蒸汽蒸馏
水解
对硝基苯胺
测熔点薄层析
薄层析
测熔点
实验步骤
1、乙酰苯胺的硝化:
在100mL三口烧瓶中放入5.00g制得的乙酰苯胺,加入10.0mL冰醋酸。
安装上电磁搅拌装置。
在三颈瓶口分别装上温度计、回流冷凝管、恒压滴液漏斗。
在恒压漏斗中加入4.0mL浓硝酸(比重为1.14g/mL,0.03mol)和8.0mL浓硫酸(比重为1.84g/mL)配成混酸。
三颈瓶外用电热煲控温在50±
5oC,边搅拌边缓慢加入混酸(约需20min),加完后60oC左右继续反应1小时。
然后将反应液倒入20g碎冰中,即有黄色沉淀析出,过滤、水洗至中性。
实验装置图
(一)硝化装置
2、硝基乙酰苯胺的水解:
将得到的固体均分为两份,一份进行重结晶,粗产品转移到50ml烧瓶中,加入约10mL乙醇,在搅拌下加热至沸腾。
观察有未溶解的固体,再补加乙醇约8mL后固体全部溶解,最后补加了5mL乙醇。
稍冷后,加入0.5g活性炭,并煮沸10min。
在保温漏斗中趁热过滤除去活性炭。
滤液倒入热的烧杯中。
然后自然冷却至室温,冰水冷却,待结晶完全析出后,进行抽滤。
用少量冷水洗涤滤饼两次,压紧抽干。
将结晶转移至表面皿中,烘干后测定重结晶后固体的熔点,再将重结晶后的固体用自配的氢氧化钠醇溶液在加热沸腾的情况下回流水解半小时,再加入3.0mL水加热沸腾的情况下回流水解20min。
再将溶液稍冷后倒入20g冰水中,过滤,用水洗至弱碱性,烘干得水解产物。
取水解后的产物做薄层分析和熔点测定。
水解装置+重结晶装置实验装置
(二)
2.2取另一份直接水解,水解方法与2.1中一样,水解之后仍将固体均分为两分,一份进行重结晶,重结晶的方法与2.1类似,只是乙醇的用量减半。
再将重结晶的样品烘干测定熔点,并做薄层分析。
将另一半固体进行水蒸气蒸馏,将蒸馏后收集到的馏分每次用10mL氯仿分两次萃取。
将萃取所得液体再次蒸馏,直至烧瓶内溶剂仅剩3mL自然冷却至室温,将所得样品进行薄层分析。
蒸馏装置萃取装置
实验装置(三)
实验结果与讨论:
1.实验结果:
1.1熔点测定结果
物质
T初(oC)
T全(oC)
熔距ΔT(oC)
标准熔点T(oC)
(初产品重结晶)
165.0
193.0
28.0
168.0
190.0
22.0
(重结晶加水解)
144.0
149.0
5.0
143.0
152.0
9.0
直接水解的初产
品
60.0
63.0
3.0
61.0
2.0
水解+重结晶后
的产品
59.0
65.0
6.0
66.0
(水解+水蒸气蒸馏)
145.0
4.0
146.0
150.0
1.2薄层析结果:
Rf值
样点黄色深浅
样点性状
重结晶再水解产品
样点1
0.59
颜色很浅,
椭球状
纯邻硝基苯胺
0.63
颜色深
样点2
0.28
颜色极深
长条楔形
纯对硝基苯胺
直接水解的初产品
0.61
颜色浅
水解+重结晶后的产品
0.56
颜色很浅
对硝基苯胺(水解+水蒸气蒸馏)
无
0.27
邻硝基苯胺(水解+水蒸气蒸馏)
0.54
0.26
2、实验讨论
(1)熔点测定分析
由硝化产物直接重结晶得到的对硝基乙酰苯胺的熔点测定结果来看,熔程长,熔点相较于标准的对硝基乙酰苯胺的熔点-215.6oC来说偏低了许多。
造成该实验结果的主要原因有:
①从得到的产品的晶型来看,产品呈土黄色泥状,基本看不出晶态。
而晶体的晶型对晶体的熔点有很大的影响,我所得到的产品更偏向于是多晶或非晶,所以熔程较长。
②熔点低说明所含的杂质多,重结晶的效果欠佳,包含的杂质初步判断为临硝基乙酰苯胺。
判断的理由是硝化过程中,在酸的作用下会有少量的乙酰苯胺被水解生成苯胺,但由于量少,在重结晶的过程中会全部溶解于溶剂中,不会给实验结果带来很大影响,而含量较多的邻硝基乙酰苯胺则会因为重结晶的的效果不佳而使得实验结果偏低。
③熔点仪的温度计测温不准,造成所得数值偏低,这在其他的几个熔点测定实验中也可以看出。
④晶体不够干燥。
①、②两个解释最本质的原因是重结晶的过程中所加的溶剂量不够,溶剂用量不足会使得邻硝基乙酰苯胺在低温时并不能完全溶解在溶剂中,而随着对硝基乙酰苯胺一起析出,再加上晶体析出过程中,由于溶剂量过少,溶质析出过快,成核密度太大,微粒不能形成晶体而是以沉淀形式存在,且相对表面积增大,吸附现象严重,总的结果就是熔程长、熔点偏低。
(2)薄层析结果分析
①从薄层析结果来看,邻硝基苯胺的样点随溶剂移动的速度更快,比移值更大,
是由于邻硝基苯胺的极性比对硝基苯胺小,因此与吸附剂的结合力更弱,在吸附与脱吸的交替过程中脱吸占上风,因此与溶剂一起攀爬的速度快于对硝基苯胺。
②薄层析中,硝化后重结晶再水解的样品的样点拉得很长,并不是清晰的一点,说明产品纯度不高。
除了有邻硝基苯胺和对硝基苯胺外还有其他有色杂质,这可能是硝化过程中由于温度控制不当,有多硝基化合物生成。
多硝基化合物的生成会使得产品颜色加深,而我所得到的产品颜色确实很深。
由此观之确实有少量多硝基化合物存在。
(3)综合分析
1、为什么要用氢氧化钠醇溶液作为水解试剂:
胺基具有给电子性会使酰基碳钝化,因此水解所需的条件要剧烈一些,氢氧化钠醇溶液碱性强,水解效果好,以乙醇作溶剂提供了一个均相体系使反应更容易发生。
2、水解产品分析
重结晶后水解的产品中对硝基苯胺占绝大部分,但仍有少量的邻硝基苯胺,这从薄层析和熔点测定的结果中都可以看出。
薄层析结果显示样品存在两个样点,一个与纯的邻硝基苯胺样点移动的速度一致,但颜色很浅;
一个与纯的对硝基苯胺样点移动的速度一致,但颜色深。
熔点测定时,熔点与对硝基苯胺的熔点十分接近。
这两个实验结果都表明产物主要是对硝基苯胺。
造成最终的产品中仍有邻硝基苯胺的原因很大一部分在于重结晶时的效果不好,有邻硝基乙酰苯胺,所以在水解之后产品不纯。
直接水解后的样品熔程短,熔点为62oC,十分接近邻硝基苯胺的熔点,而薄层色谱中样品仍有两个样点,一个与纯的邻硝基苯胺样点移动的速度一致,颜色很深;
一个与纯的对硝基苯胺样点移动的速度一致,但颜色很浅。
由熔点测定结果和薄层色谱结果可以得出,直接水解的产物中邻硝基苯胺居多。
将初产品重结晶后,测得的熔点为63oC,相比于未重结晶的产品更接近纯的邻硝基乙酰苯胺的熔点,但改善不大。
除了熔点改善不大之外,薄层色谱也十分相近。
另外还有明显的熔程变长。
而理论上重结晶后应该会使得熔程变短,熔点更接近真实值,所以实验结果与理论之间出现了悖论。
这其中的原因是我在直接水解之后,将水解后的产品自然放置了一周,因此晶体的析出极其缓慢,成核密度低,形成的晶体大,晶型单一,所以直接得到的粗产品的熔程较短。
而相较于重结晶时,晶体的及时其析出,晶型肯定比初产品差,这从外观也可以得到验证:
粗产品为暗红色棱状晶体,而重结晶后是暗红色粉末状固体。
而熔点改善小也是由于粗产品结晶过程长晶粒大,吸附包夹极少,纯度高,所以重结晶所能做的改善很小。
在水蒸气蒸馏试验中,我得到了0.13g对硝基苯胺,通过熔点的测定结果和薄层析的结果证实了它是比较纯的对硝基苯胺。
而邻硝基苯胺几乎没有,在蒸发掉溶剂之后只在瓶壁上析出了少量固体,通过薄层分析证实了它是邻硝基苯胺,而且纯度很高。
由水蒸气蒸馏实验可以得出一个与粗产品分析完全相反的结论:
直接水解之后的产品中主要是对硝基苯胺。
将粗产品分析与水蒸气蒸馏实验结果相比较不难看出他们之间存在明显的悖论:
前者说明水解产物主要是邻硝基苯胺,而后者又证实主要是对硝基苯胺。
为什么会出现如此背道而驰的实验现象呢?
首先,我们来看为什么邻硝基苯胺量会如此之多,这与温度控制有莫大关系。
首先,在硝化的过程中我控温在63oC左右,但有时不慎温度会飙升到70oC以上,由于温度越高越有利于邻硝基乙酰苯胺的生成,所以在硝化之后邻硝基乙酰苯胺含量较高。
但由直接重结晶的结果来看邻位虽然含量较高,但仍不至于完全盖过对硝基乙酰苯胺。
所以除了邻硝基乙酰苯胺本身量多之外,更重要的原因在于我的水解过程。
由直接重结晶再水解的结果来看可以排除水解试剂氢氧化钠醇溶液的影响,那么唯一可能带来该实验现象的就是我在析出晶体时实际上分了两步,第一步是水解之后我放至室温时有固体析出,但量很少,所以我将溶液抽滤后,并未直接弃去滤液,而是将他收集在250mL烧杯中,放置了一周,第二周发现烧杯中析出了大量暗红色晶体,我将其抽滤后,用该晶体作了薄层析和熔点测定。
以及重结晶。
而将一周前析出的样品作了水蒸气蒸馏实验。
由我的实验过程,就不难看出问题的关键在于我做粗产品分析以及重结晶的样品与做水蒸气蒸馏的样品不同。
前者是放置一周后析出的固体,后者是水解后直接洗出的固体。
究其本质原因就在于邻硝基苯胺的水溶性比对硝基苯胺的水溶性高,这与两者的极性所导致的效果恰好相反:
邻硝基苯胺的极性小,对硝基苯胺的极性大,根据相似相容原理,邻硝基苯胺更易溶于水。
所以在溶剂量大,温度高的情况下邻硝基苯胺首先析出,而对硝基苯胺不析出。
因此我提出了另一种解释,对硝基苯胺中,对硝基苯胺分子间的氢键相对来说比较强,与对硝基苯胺与水分子间的氢键相比不可忽略。
而邻硝基苯胺没有自身分子间的氢键而只与水分子间形成氢键,所以临硝基乙酰苯胺在水中的溶解度大。
同时将溶液放置很长时间后,溶剂挥发掉了,温度又进一步降低,自然地邻硝基苯胺就析出了,这也是为什么会造成水蒸气蒸馏结果和粗产品分析结果与重结晶结果之间存在悖谬的原因。
其实在实验之初,就出现过类似现象。
也就是在硝化之后,抽滤时,首先析出的固体是浅黄色的,但是将滤液放置一段时间后,再将其抽滤,析出的固体就是橙黄色甚至是暗红色的了。
很显然,浅黄色说明对硝基乙酰苯胺的量较多,而暗红色说明邻硝基乙酰苯胺的量多,也就是说总是存在邻硝基乙酰苯胺后析出,对硝基乙酰苯胺先析出的现象,造成该现象的原因与邻硝基苯胺和对硝基苯胺谁先析出的原因是一样的。
该实验之所以可以通过水蒸气蒸馏来分离邻硝基苯胺与对硝基苯胺,是由于在一个大气压下,邻硝基苯胺的饱和蒸汽压大于对硝基苯胺,因此在温度低于一百摄氏度时邻硝基苯胺先随水蒸气一起蒸出,如此便将邻硝基苯胺与对硝基苯胺分离开来。
比较两种合成和纯化路线的实验结果,从熔点值和薄层分析来看,先纯化后水解的办法比先水解后纯化的方法实验结果差,所得产品纯度低。
这是因为先纯化得到的对硝基乙酰苯胺在水解的过程中会再一次引入杂质,导致先前的纯化所起的作用不大,要想得到纯的对硝基苯胺仍然需要进一步纯化。
对比水蒸气蒸馏和重结晶的结果,水蒸气蒸馏所得产品的薄层析结果更纯,说明水蒸气蒸馏纯化比重结晶纯化效果要好。
但是重结晶的实验操作比水蒸气蒸馏更简单。
综合上述实验结果,对硝基乙酰苯胺最好的合成及纯化路线是先硝化再水解,再进行水蒸气蒸馏。
附录:
实验仪器:
50ml、100mL圆底烧瓶、100mL、50mL三口烧瓶、10ml量筒、玻璃棒、磁子、回流冷凝管、直型冷凝管、尾接管、温度计、电磁加热搅拌器、布氏漏斗、抽滤瓶、50mL、100mL、250ml烧杯各一个、滤纸、表面皿、10ml及25ml及50ml锥形瓶、滴管、熔点仪、pH试纸、层析板、毛细管、熔点管、层析缸、棉花、水蒸汽发生装置
实验试剂:
5.00g乙酰苯胺,浓硫酸,浓硝酸,冰醋酸,氢氧化钠固体,乙醇,石油醚,乙酸乙酯,氯仿
所用层析液是:
体积比石油醚:
乙酸乙酯=5:
2
实验现象:
熔点及性状
土黄色固体
土黄色泥状固体
暗红色晶状固体
暗红色固体
暗红色针状晶体
薄层分析:
注:
在薄层析板前端的点叫做样点1,邻硝基苯胺。
在薄层析板后端的点叫样点2,对硝基苯胺