山东省淄博市高青县最新九年级第一次模拟考试化学试题Word下载.docx
《山东省淄博市高青县最新九年级第一次模拟考试化学试题Word下载.docx》由会员分享,可在线阅读,更多相关《山东省淄博市高青县最新九年级第一次模拟考试化学试题Word下载.docx(13页珍藏版)》请在冰豆网上搜索。
C.乙醛一种有机物D.乙醛中碳和氢的原子个数比为l:
3
5.下列用途利用了物质的物理性质的是
A.氧气用作助燃剂B.生石灰用作干燥剂
C.活性炭用作吸附剂D.氮气用作保护气
6.高锰酸钾(化学式为KMnO4)是一种消毒药品。
在高锰酸钾中,锰元素的化合价为
A.+5B.+7C.+3D.+1
7.CH4和某种氮的氧化物反应的化学方程式为CH4+2口催化剂N2+CO2+2H2O,则框内物质的化学式是
A.NOB.NO2C.N2OD.N2O5
8.下列化学方程式书写正确的是
A.NaCO3+2HCl=NaCl+H2O+CO2↑B.CuSO4+2NaOH=CuOH↓+Na2SO4
C.CO2+Ca(OH)2=CaCO3↓+H2OD.Fe2O3+6HCl=2FeC12+3H2O
9.健康的生活离不开化学,下列说法正确的是()
A.油脂是重要的营养物质,可大量摄入油脂
B.为保持肉制品鲜美,在香肠中加过量的亚硝酸钠
C.为预防甲状腺肿大,应在食盐中添加大量的碘元素
D.人误食重金属盐中毒后,服用鸡蛋清可减轻毒性
10.中和反应在工农业生产和日常生活中有广泛的用途.下列应用一定与中和反应原理无关的是()
A.施用熟石灰改良酸性土壤
B.用胃舒平(主要成分氢氧化铝)治疗胃酸过多
C.用熟石灰和硫酸铜配制波尔多液
D.用NaOH溶液洗涤石油产品中的残余硫酸
11.只用一种试剂就可以把盐酸、氢氧化钠溶液、石灰水区分开来,该试剂是()
A.二氧化碳B.石蕊试液C.碳酸钠溶液D.氯化钡溶液
12.下列对实验现象的分析合理的是
A.向某无色溶液中滴入酚酞试液,呈红色,证明该溶液是碱溶液
B.向某无色溶液中滴入硝酸银溶液,产生白色沉淀,证明该溶液是盐酸
C.某白色固体与熟石灰混合后加热,产生可使湿润的红色石蕊试纸变蓝色的气体,证明该固体是铵盐
D.向某固体中加入稀盐酸,产生无色气体。
证明该固体中一定含有碳酸根离子
13.强化安全意识,提升安全素养。
下列采取的安全措施错误的是()
A.不必检纯度,直接点燃氢气
B.在火灾逃生时用湿毛巾捂住口鼻
C.在加油站张贴严禁烟火标志
D.在燃气灶的厨房内上方安装报警器
14.除去下列物质中含有的少量杂质,所用试剂或方法正确的是
序号
混合物(括号内为杂质)
除杂试剂或方法
A
Fe粉(Cu)
CuSO4溶液
B
NaCl(沙子)
加水溶解,过滤、蒸发结晶
C
Na2SO4溶液(Na2CO3)
过量稀盐酸
D
除去KCl溶液中少量CuCl2
滴加NaOH溶液,至不再生成沉淀,过滤
A.AB.BC.CD.D
二、多选题
15.右图是KNO3和NaCl的溶解度曲线。
下列说法中正确的是
A.NaCl的溶解度受温度的影响变化不明显
B.KNO3的溶解度大于NaCl的溶解度
C.t1℃时,100gKNO3的饱和溶液中含有20gKNO3
D.t2℃时,NaCl的饱和溶液与KNO3的饱和溶液中溶质的质量分数相等
三、填空题
16.镓(元素符号为Ga)原子的结构示意图如图所示:
,则镓元素属于_____(填“金属”或“非金属”)元素。
在化学反应中镓原子与铝原子的性质相似,原因是_______________。
写出氢氧化镓和稀盐酸反应的化学方程式______________。
17.食品包装袋中的“双吸剂”用于防潮和抗氧化,该“双吸剂”是_________,用于食品保鲜的化学反应的原理是___________________。
取少量“双吸剂”中的物质放入试管中,加入稀盐酸,观察到有少量气泡生成,反应完毕溶液变为黄色,写出反应的化学方程式_________,__________。
18.向碳酸钠溶液中滴加2滴酚酞试液,溶液变为______色,说明溶液显______性。
向盛有澄清石灰水的试管中滴加碳酸钠溶液,观察到的现象是____________,反应的化学方程式为________________。
四、推断题
19.甲、乙、丙是初中常见物质,它们经一步反应的转化关系如右下图所示,其中部分反应物、生成物及反应条件已略去。
(1)若反应皆为化合反应,且均在点燃条件下发生,则丙的化学式为_______,则乙转化为丙的反应为_________(填“吸热”或“放热”)反应。
(2)若反应皆为置换反应,且均在溶液中进行,甲、乙、丙都为金属,则它们的金属活动性由强到弱的顺序是____________(用“甲”、“乙”、“丙”表示)。
(3)若反应皆为复分解反应,乙为白色难溶物。
甲为常见的酸,甲、乙、丙含相同的原子团,丙溶液为蓝色,则丙生成乙的化学方程式为__________________________(写出一个即可)。
五、实验题
20.根据下图回答问题。
(1)如图1,观察到的现象是_____________________,反应的化学方程式是___________,瓶底留少量水的目的是_______________,通过实验可知,可燃物燃烧的条件是____________。
(2)如图2,验证CO2与NaOH、Ca(OH)2都能发生反应。
分别向甲、乙两个瓶中注入少量、等体积的两种溶液,观察实验现象。
I:
甲中反应的化学方程式是___________。
说明CO2能与Ca(OH)2反应的实验现象是__________。
II:
下列实验现象中,一定能说明“CO2与NaOH发生了化学反应”的是_____(填序号)。
a.U型管中红墨水左低右高b.U型管中红墨水左高右低c.U型管中红墨水液面没有发生改变
21.下图是实验室制取气体的常用装置。
(1)写出标号仪器的名称:
b__________。
(2)实验室常用过氧化氢溶液在二氧化锰催化作用下制取二氧化碳气体,反应的化学方程式为______,反应类型为_______反应,选用的发生装置为_______(填序号),若用C装置收集一瓶氧气,验满的方法是___________。
(3)小明同学用浓盐酸和大理石反应制取二氧化碳,将生成的二氧化碳通入新配制的澄清石灰水中,没有发现变浑浊现象,原因可能是___________,若用A装置加热氯酸钾和二氧化锰的混合物制取氧气,同时生成氯化钾,反应的化学方程式为_____________________。
六、计算题
22.纯碱在生成过程中常混有少量氯化钠,实验中学化学兴趣小组的同学要测定某品牌纯碱样品中碳酸钠的质量分数。
他们称取11g样品放入烧杯中,逐滴加入稀盐酸至不再产生气泡为止,共消耗稀盐酸64.7g,烧杯中没有残留物,称得反应后溶液的质量为71.3g。
(1)生成二氧化碳的质量为___________g。
(2)计算样品中碳酸钠的质量分数为_____________。
(写出计算过程)
参考答案
1.D
【解析】
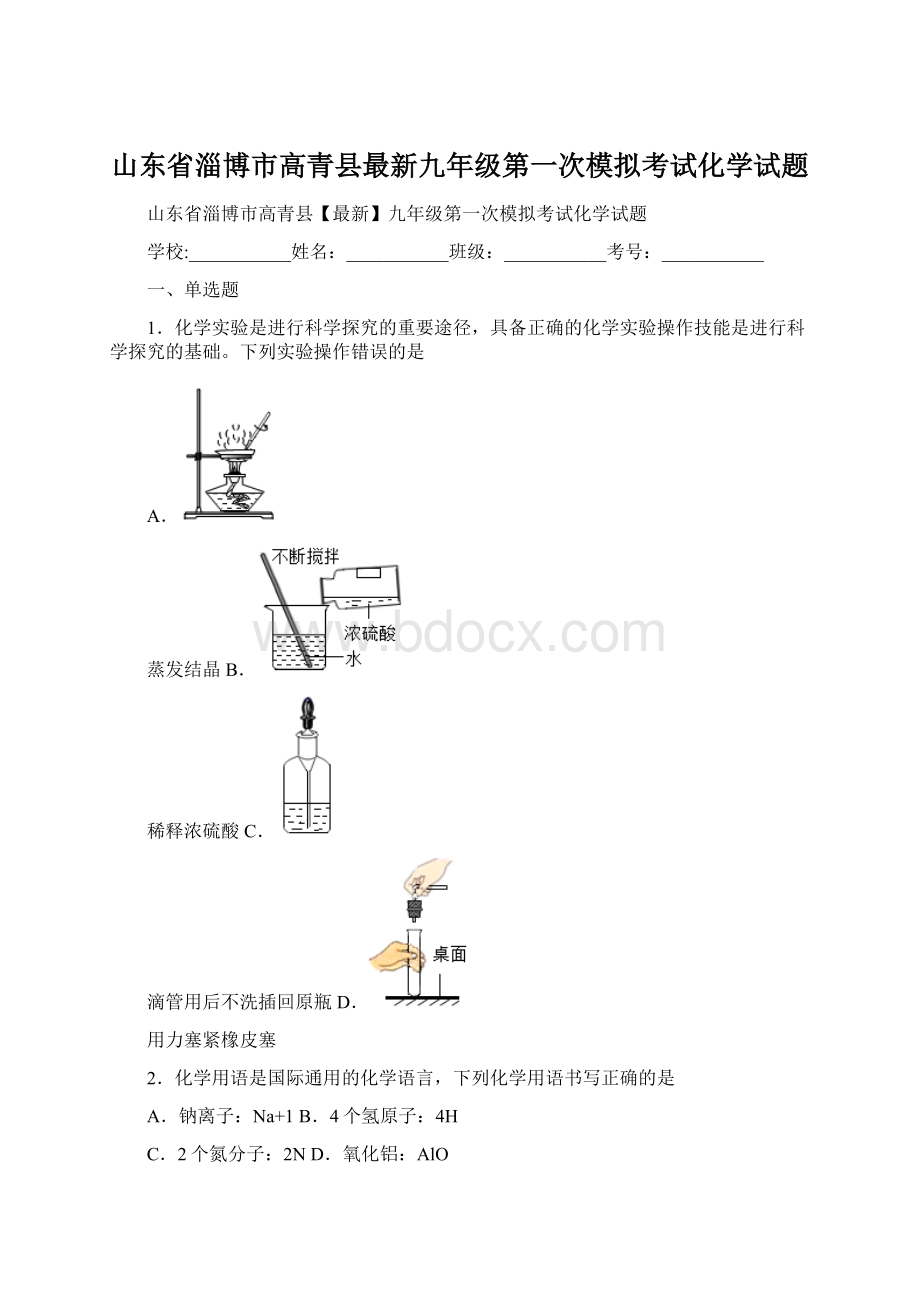
A、蒸发结晶,应玻璃棒搅拌,故A正确;
B、稀释浓硫酸应把浓硫酸倒入水中,并玻璃棒不断搅拌,故B正确;
C、滴管用后不洗插回原瓶,这是滴瓶专用滴管,不用清洗,故C正确;
D、胶塞插入试管,手握胶塞,向一个方向用力旋转,试管不应接触桌面,故D错误。
点睛∶严格按照实验要求规范实验操作是顺利完成实验的重要保证。
滴瓶专用滴管,不用清洗。
稀释浓硫酸应把浓硫酸倒入水中。
2.B
A、钠离子:
Na+,1往往省略,故A错误;
B、4个氢原子:
4H,原子讲种类,讲个数,符号前面数字表示原子个数,故B正确;
C、2个氮分子:
2N2,氮气属于双原子分子,分子讲种类,讲个数,符号前面数字表示分子个数,故C错误;
D、氧化铝:
Al2O3,化合物化学式的书写应符合正负总价代数和为零原则,故D错误。
点睛∶分子,原子和离子均属于微观离子,讲种类,讲个数,符号前面数字表示微粒个数。
化合物化学式的书写应符合正负总价代数和为零的原则。
3.A
A、水结冰体积膨胀——温度降低,分子间隔变大,故A错误;
B、“八月桂花香”——分子在不断的运动,故B正确;
C、水烧开后易把壶盖冲起——温度升高,分子间隙变大,体积变大,故C正确;
D、氧气和液氧都可助燃——相同物质的分子,化学性质相同,物质的结构决定物质的性质,故D正确。
点睛∶物质的结构决定物质的性质。
分子的基本性质是⑴质量非常小,体积很小;
⑵不断运动;
⑶分子间有间隔。
4.A
A.乙醛由三种元素组成,B.
,乙醛中碳元素的质量分数最大;
C.除一氧化碳、二氧化碳、碳酸、碳酸盐以外的含碳化合物称为有机物。
,乙醛一种有机物;
D.化学式中元素符号右下角的数字为一个分子中原子个数,所以乙醛中碳和氢的原子个数比为l:
3。
选A
5.C
【分析】
物理性质是指物质不需要经过化学变化就直接表现出来的性质,化学性质是指物质经过化学变化表现出来的性质。
【详解】
A、氧气用作助燃剂,本身不能燃烧,可以支持帮助其他物质燃烧,属于化学性质;
B、生石灰用作干燥剂,生石灰与水反应生成熟石灰,属于化学性质;
C、活性炭用作吸附剂,吸附性属于物理性质;
D、氮气用作保护气,氮气常温下化学性质比较稳定,属于化学性质。
故选C。
6.B
化合物中正负总价代数和为零,根据这一原则,可以确定化合物中某元素的化合价。
设高锰酸钾(化学式为KMnO4)中锰元素的化合价为x,根据化合物中正负总价代数和为零原则:
﹙+1﹚+x+﹙-2﹚×
4=0,x=+7。
故选B。
7.B
试题分析:
化学变化前后各种原子的个数不变,反应后有2N、C、4H、4O,而反应前有4H、一个C原子,反应前后差2N、4O,所以框内物质的化学式为NO2,故选B
考点:
质量守恒定律的应用
8.C
化学方程式的书写应遵循两个原则:
(1)以客观事实为依据;
(2)遵循质量守恒定律。
A、Na2CO3+2HCl=2NaCl+H2O+CO2↑,故A错误;
B、CuSO4+2NaOH=Cu﹙OH﹚2↓+Na2SO4,故B错误;
C、CO2+Ca(OH)2=CaCO3↓+H2O,故C正确;
D、Fe2O3+6HCl=2FeC13+3H2O,故D错误。
9.D
A、油脂是重要的营养物质,可适量摄入油脂,错误;
B、亚硝酸钠致死量是3克,在香肠中加适量的亚硝酸纳,可保持肉制品鲜美,错误;
C、为预防甲状腺肿大,应在食盐中添加适量的碘元素,错误;
D、重金属盐能使蛋白质变性,鸡蛋清含有蛋白质,人误食重金属盐中毒后,服用鸡蛋淸可减轻毒性,正确。
故选D。
10.C
A、氢氧化钙与酸性物质发生中和反应,该应用一定与中和反应原理有关,不符合题意;
B、氢氧化铝与胃液的主要成分盐酸反应,为中和反应,该应用一定与中和反应原理有关,不符合题意;
C、用熟石灰、硫酸铜和水配制波尔多液,是碱与盐的反应,不符合中和反应的概念,该应用一定与中和反应原理无关,符合题意;
D、用NaOH溶液洗涤石油产品中的残余硫酸,氢氧化钠溶液与硫酸反应,属于中和反应,该应用一定与中和反应原理有关,但不符合题意;
故选:
C。
11.C
A、二氧化碳能使石灰水变浑浊,氢氧化钠和二氧化碳反应但是无现象,二氧化碳不会与盐酸反应,不能鉴别,故A错误;
B、石蕊在氢氧化钠和氢氧化钙中都显蓝色,不能鉴别,故B错误;
C、碳酸钠和盐酸会生成二氧化碳,和氢氧化钠不反应,和澄清石灰水生成白色沉淀,现象不同,可以鉴别,故C正确;
D、氯化钡和三种物质都不反应,不能鉴别,故D错误;
12.C
A、向某无色溶液中滴入酚酞试液,呈红色,证明该溶液是碱性溶液,不一定是碱,故A错误;
B、向某无色溶液中滴入硝酸银溶液,产生白色沉淀,证明该溶液是盐酸或盐酸盐,故B错误;
C、某白色固体与熟石灰混合后加热,产生可使湿润的红色石蕊试纸变蓝色的气体,应是氨气,氨气溶于水生成氨水,氨水呈碱性,氨气遇湿润的红色石蕊试纸变蓝色,证明该固体是铵盐,故C正确;
D、向某固体中加入稀盐酸,产生无色气体。
证明该固体中不一定含有碳酸根离子,也可能是活泼金属,故D错误。
13.A
A、氢气具有可燃性,点燃前要验纯,否则可能会发生爆炸,错误;
B、在火灾逃生时用湿毛巾捂住口鼻,以免吸入大量的可吸入颗粒物和毒气,正确;
C、加油站空气中含有可燃性气体,在加油站张贴严禁烟火标志,正确;
D、甲烷的密度比空气小,故在燃气灶的厨房内上方安装报警器,正确。
故选A。
14.B
根据原物质和杂质的性质选择适当的除杂剂和分离方法,所谓除杂(提纯),是指除去杂质,同时被提纯物质不得改变。
除杂质题至少要满足两个条件:
①加入的试剂只能与杂质反应,不能与原物质反应;
②反应后不能引入新的杂质。
A、Fe粉能与CuSO4
溶液反应生成硫酸亚铁溶液和铜,反而会把原物质除去,不符合除杂原则,故选项所采取的方法错误。
B、氯化钠易溶于水,沙子难溶于水,可采取加水溶解、过滤、蒸发结晶的方法进行分离除杂,故选项所采取的方法正确。
C、Na2CO3能与过量稀盐酸反应生成氯化钠、水和二氧化碳,能除去杂质但引入了新的杂质氯化钠,不符合除杂原则,故选项所采取的方法错误。
D、CuCl2能与氢氧化钠溶液反应生成氢氧化铜沉淀和氯化钠,能除去杂质但引入了新的杂质氯化钠,不符合除杂原则,故选项所采取的方法错误。
B。
15.AD
NaCl的溶解度受温度的影响变化不明显;
在温度大于t2时,KNO3的溶解度大于NaCl的溶解度;
t1℃时,100g水的饱和溶液中含有20gKNO3;
t2℃时,NaCl的饱和溶液与KNO3的饱和溶液中溶质的质量分数相等。
故选AD.
溶解度与曲线
16.金属最外出电子数相同3HCl+Ga﹙OH﹚3=3H2O+GaCl3
由题中信息知,镓元素属于金属元素。
在化学反应中镓原子与铝原子的性质相似,原因是最外出电子数相同,原子最外层电子数决定元素的化学性质。
氢氧化镓和稀盐酸反应的化学方程式是3HCl+Ga﹙OH﹚3=3H2O+GaCl3。
点睛∶原子最外层电子数决定元素的化学性质。
化学方程式的书写应遵循两个原则⑴以客观事实为依据;
⑵遵循质量守恒定律。
17.铁吸收包装袋中的水分和氧气Fe+2HCl=FeCl2+H2Fe2O3+6HCl=2FeCl3+3H2O
食品包装袋中的“双吸剂”用于防潮和抗氧化,该“双吸剂”是铁,铁可以与空气中氧气,水蒸气反应生成铁锈。
用于食品保鲜的化学反应的原理是吸收包装袋中的水分和氧气,食品变质是一种缓慢氧化。
取少量“双吸剂”中的物质放入试管中,加入稀盐酸,观察到有少量气泡生成,反应完毕溶液变为黄色,反应的化学方程式是Fe+2HCl=FeCl2+H2↑,Fe2O3+6HCl=2FeCl3+3H2O,氯化铁溶液呈黄色。
点睛∶铁属于活泼金属,与盐酸起置换反应;
铁在潮湿的空气中生成铁锈,铁锈与盐酸反应生成氯化铁黄色溶液。
18.红碱生成白色沉淀Na2CO3+Ca(OH)2=CaCO3↓+2NaOH
碳酸钠溶液呈碱性,遇酚酞试液变红,溶液变为红色,说明溶液显碱性。
向盛有澄清石灰水的试管中滴加碳酸钠溶液,观察到的现象是生成白色沉淀,反应的化学方程式为Na2CO3+Ca(OH)2=CaCO3↓+2NaOH。
点睛∶碳酸钠溶液呈碱性,遇酚酞试液变红。
碳酸钠溶液与澄清石灰反应生成碳酸钙白色沉淀。
19.CO吸收甲乙丙CuSO4+BaCl=BaSO4↓+CuCl2
根据所学知识和题中信息知,甲、乙、丙是初中常见物质,它们经一步反应的转化关系。
(1)若反应皆为化合反应,且均在点燃条件下发生,则丙的化学式为CO,则乙转化为丙的反应为吸热反应,二氧化碳和碳反应生成一氧化碳,吸热。
(2)若反应皆为置换反应,且均在溶液中进行,甲、乙、丙都为金属,则它们的金属活动性由强到弱的顺序是甲>乙>丙,排在前面金属可以把排在其后面的金属从它的盐溶液中置换出来。
甲为常见的酸,甲是硫酸、乙是硫酸钡、丙是氯化铜,甲、乙、丙含相同的原子团,丙溶液为蓝色,则丙生成乙的化学方程式为CuSO4+BaCl2=BaSO4↓+CuCl2。
点睛∶金属活动顺序表的应用⑴排在氢前面的金属可以与稀硫酸或盐酸反应置换出氢气,排在氢后面的金属则不能⑵排在前面金属可以把排在其后面的金属从它的盐溶液中置换出来⑶从左到右金属活动性越来越弱。
20.红热的铁丝剧烈燃烧,火星四射,生成黑色固体,放出大量的热3Fe+2O2点燃Fe3O4防止瓶底炸裂可燃物温度达到着火点2NaOH+CO2=Na2CO3+H2O石灰水变浑浊bc
根据所学知识和题中信息知,
(1)如图1,观察到的现象是红热的铁丝剧烈燃烧,火星四射,生成黑色固体,放出大量的热。
反应的化学方程式是3Fe+2O2点燃Fe3O4,瓶底留少量水的目的是防止瓶底炸裂,生成的四氧化三铁熔融物温度较高。
_,通过实验可知,可燃物燃烧的条件是可燃物温度达到着火点。
甲中反应的化学方程式是2NaOH+CO2===Na2CO3+H2O。
说明CO2能与Ca(OH)2反应的实验现象是石灰水变浑浊,二氧化碳与Ca(OH)2反应生成碳酸钙白色沉淀。
CO2与NaOH发生反应生成碳酸钠和水,没有明显现象,一定能说明“CO2与NaOH发生了化学反应”的是①U型管中红墨水左高右低,二氧化碳与氢氧化钠反应,使甲容器内气压减小;
②U型管中红墨水液面没有发生改变,甲和乙中二氧化碳均反应。
点睛∶铁丝在氧气中剧烈燃烧,火星四射,生成黑色固体,放出大量的热。
瓶底留少量水,防止瓶底炸裂。
21.集气瓶2H2O2MnO22H2O+O2↑分解B将带火星的木条放在集气瓶口,若木条复燃,证明已满浓盐酸具有挥发性,使溶液呈局部酸性2KClO3
2KCl+3O2↑
根据所学知识和题中信息知,
(1)标号仪器的名称:
b集气瓶。
(2)实验室常用过氧化氢溶液在二氧化锰催化作用下制取二氧化碳气体,反应的化学方程式为2H2O2MnO22H2O+O2↑,反应类型为分解反应,一种物质分解生成了两种物质;
选用的发生装置为B,固体和液体反应不需加热制取气体。
若用C装置收集一瓶氧气,验满的方法是将带火星的木条放在集气瓶口,若木条复燃,证明已满,这是我们检验氧气常用的方法。
(3)用浓盐酸和大理石反应制取二氧化碳,将生成的二氧化碳通入新配制的澄清石灰水中,没有发现变浑浊现象,原因可能是浓盐酸具有挥发性,使溶液呈局部酸性,若用A装置加热氯酸钾和二氧化锰的混合物制取氧气,同时生成氯化钾,反应的化学方程式为2KClO3
2KCl+3O2↑。
点睛∶用浓盐酸和大理石反应制取二氧化碳,将生成的二氧化碳通入新配制的澄清石灰水中,往往检查不到石灰水变浑浊,主要原因是浓盐酸具有挥发性,使溶液呈局部酸性。
22.
(1)4.4;
(2)96.4%
(1)根据质量守恒定律知,生成二氧化碳的质量为11g+64.7g-71.3g=4.4g。
(2)解∶设样品中碳酸钠的质量分数为x
Na2CO3+2HCl==2NaCl+H2O+CO2↑
10644
11g×
x4.4g
=
,x=96.4%。
答∶
(1)生成二氧化碳的质量为4.4g;
(2)样品中碳酸钠的质量分数为96.4%。
点睛∶灵活应用质量守恒定律,正确书写化学方程式是顺利完成本题的重要保证。