高考化学专题复习分类练习 铁及其化合物推断题综合解答题附答案解析Word文档下载推荐.docx
《高考化学专题复习分类练习 铁及其化合物推断题综合解答题附答案解析Word文档下载推荐.docx》由会员分享,可在线阅读,更多相关《高考化学专题复习分类练习 铁及其化合物推断题综合解答题附答案解析Word文档下载推荐.docx(15页珍藏版)》请在冰豆网上搜索。
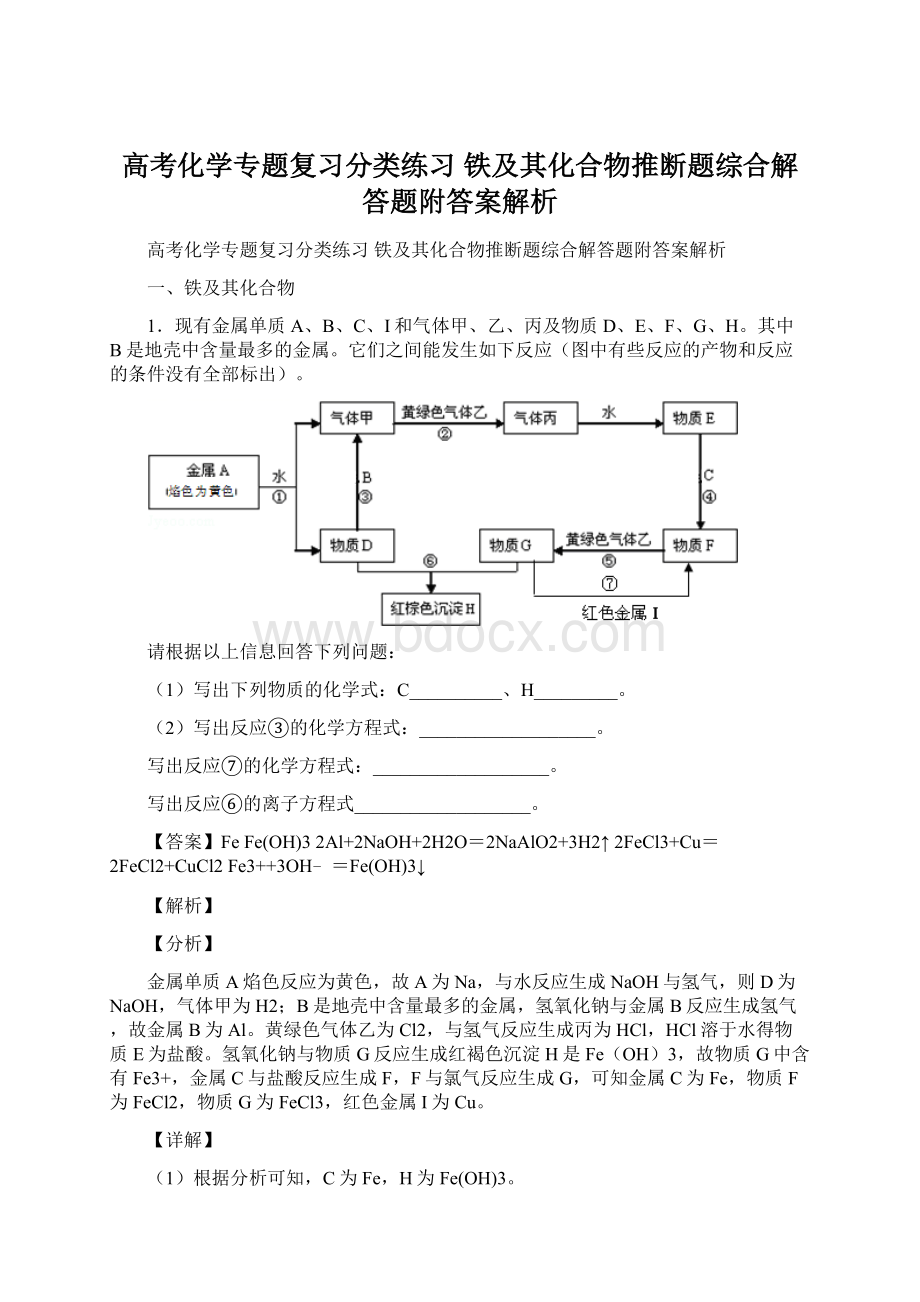
。
请根据以上信息完成下列各题:
B_______、丙__________。
(2)写出黄绿色气体乙的一种用途___________,反应过程⑦可能观察到的实验现象是______。
对应的化学方程式是_______。
(3)反应③中的离子方程式是_________。
【答案】AlHCl杀菌消毒、强氧化剂、漂白白色沉淀迅速变成灰绿色,最终变成红褐色4Fe(OH)2+O2+2H2O=4Fe(OH)32Al+2OH-+2H2O=2AlO2-+3H2↑
金属A颜色反应为黄色证明A为金属Na,Na与水反应生成气体甲为H2,D为NaOH;
金属B和氢氧化钠溶液反应产生H2,说明B为金属Al,黄绿色气体乙为Cl2,气体甲是H2,H2和Cl2反应生成丙为HCl,HCl溶于水得到的物质E为盐酸溶液,盐酸与金属C反应产生F溶液是金属氯化物,该氯化物与Cl2还可以反应产生G,G与NaOH溶液反应生成红褐色沉淀H为Fe(OH)3,则G为FeCl3,推断物质F为FeCl2;
判断C为Fe,以此解答该题。
根据上述分析可知A是Na,B是Al,C为Fe,气体甲是H2,气体乙是Cl2,气体丙是HCl;
D是NaOH,E是盐酸,F是FeCl2,G是FeCl3,H是Fe(OH)3。
(1)根据上述分析可知,物质B是Al,丙是HCl;
(2)黄绿色气体乙是Cl2,该物质可以与水反应产生HCl和HClO,HClO具有强氧化性,可作氧化剂,氧化一些具有还原性的物质,也用于杀菌消毒或用于物质的漂白;
(3)FeCl2与NaOH溶液发生反应:
FeCl2+2NaOH=Fe(OH)2↓+2NaCl,Fe(OH)2具有还原性,容易被溶解在溶液中的氧气氧化,发生反应:
4Fe(OH)2+O2+2H2O=4Fe(OH)3,固体由白色迅速变为灰绿色,最后变为红褐色,因此可观察到的实验现象是白色沉淀迅速变成灰绿色,最终变成红褐色;
(4)反应③是Al与NaOH溶液发生反应产生NaAlO2和H2,反应的离子方程式为:
2Al+2OH-+2H2O=2AlO2-+3H2↑。
【点睛】
本题是无机物推断,物质的颜色及转化关系中特殊反应是物质推断的突破口,再结合转化关系推断,需要学生熟练掌握元素化合物知识,试题培养了学生的分析能力及逻辑推理能力。
3.现有X、Y、Z三种非金属元素,A、B、C三种金属元素,有:
①X、Y、Z的单质在常温下均为气体;
②X的单质在Z的单质中燃烧,火焰呈苍白色。
产物XZ的水溶液可使石蕊试液变红;
③2molX的单质可与1molY的单质化合生成2molX2Y,X2Y在常温下为液体;
④Z的单质溶于X2Y中所得的溶液具有漂白性;
⑤A的单质可以在Z的单质中燃烧,生成黑棕色固体,该固体溶于水得到棕黄色溶液;
⑥B与Z可形成化合物BZ3,向BZ3的溶液中逐滴滴加NaOH溶液,先生成白色沉淀后沉淀逐渐溶解;
⑦C的单质与Y的单质反应可能得到两种产物,其中一种为淡黄色固体M
请回答下列问题:
(1)写出下列物质的化学式:
XZ__________,X2Y__________,M__________
(2)Z的单质溶于X2Y中所得溶液中起漂白作用的物质是__________(填化学式)
(3)A的单质与Z的单质反应的化学方程式为__________
(4)BZ3与过量的NaOH溶液反应的离子方程式为__________
(5)X的单质与Z的单质的混合气体经点燃充分反应后,冷却至室温,再通入足量的NaOH溶液中,气体被完全吸收,则原混合气体中X的单质与Z的单质的体积关系可能为__________(用相应化学式表示X、Z的单质)
【答案】HClH2ONa2O2HClO2Fe+3Cl2
2FeCl3Al3++4OH-=
+2H2OV(H2):
V(Cl2)≤1:
1
现有X、Y、Z三种非金属元素,A、B、C三种金属元素,有①X、Y、Z的单质在常温下均为气体;
②X的单质在Z的单质中燃烧,火焰呈苍白色,产物XZ的水溶液可使石蕊试液变红,则XZ为HCl,得出X为H,Z为Cl;
③2molX的单质可与1molY的单质化合生成2molX2Y,X2Y在常温下为液体,则X2Y为H2O,Y为O;
④Z的单质溶于X2Y中所得的溶液具有漂白性;
⑤A的单质可以在Z的单质中燃烧,生成黑棕色固体,该固体溶于水得到棕黄色溶液,则为氯化铁溶液,即A为Fe;
⑥B与Z可形成化合物BZ3,向BZ3的溶液中逐滴滴加NaOH溶液,先生成白色沉淀后沉淀逐渐溶解,则B为Al;
⑦C的单质与Y的单质反应可能得到两种产物,其中一种为淡黄色固体M,则M为过氧化钠,则C为Na。
⑴根据分析得出下列物质的化学式:
XZ为HCl,X2Y为H2O,M为Na2O2;
故答案为:
HCl;
H2O;
Na2O2。
⑵Z的单质溶于X2Y反应生成盐酸和次氯酸,次氯酸起漂白作用;
HClO。
⑶A的单质与Z的单质反应是铁与氯气反应生成氯化铁,其化学方程式为2Fe+3Cl2
2FeCl3;
2Fe+3Cl2
2FeCl3。
⑷氯化铝与过量的NaOH溶液反应生成偏铝酸钠和水,其离子方程式为Al3++4OH-=AlO2-+2H2O;
Al3++4OH-=AlO2-+2H2O。
⑸X的单质与Z的单质的混合气体经点燃充分反应生成HCl,H2+Cl2
2HCl,反应后冷却至室温,再通入足量的NaOH溶液中,气体被完全吸收,氯化氢和氢氧化钠反应生成氯化钠和水,氯气也要与氢氧化钠溶液反应生成氯化钠、次氯酸钠和水,因此氯气过量或刚好生成HCl,气体都能完全被吸收,故原混合气体中X的单质与Z的单质的体积关系可能为V(H2):
V(Cl2)≤1:
1;
V(H2):
1。
4.现有金属单质A、B和气体甲、乙、丙及物质C、D、E、F、G,它们之间能发生如图反应(图中某些反应的产物及条件没有全部标出)
根据以上信息填空:
A______G__________;
(2)纯净的气体甲在气体乙中燃烧的现象:
______________________________________;
(3)写出下列反应的离子方程式:
反应①_________________________;
反应④____________________________;
【答案】NaFe(OH)3产生苍白色火焰,放出大量的热,出现白雾2Na+2H2O=2Na++2OH-+H2↑2Fe2++Cl2=2Fe3++2Cl-
【解析】金属A焰色反应为黄色,故A为金属Na;
由反应①Na+H2O→气体甲+C,则甲为H2,C为NaOH;
乙是黄绿色气体,则乙为Cl2;
反应②:
气体甲+气体乙→气体丙,即H2+Cl2→HCl,则丙为HCl;
红褐色沉淀G为Fe(OH)3;
反应⑤:
物质C+物质F→沉淀G,即NaOH+F→Fe(OH)3,可推断F中含有Fe3+;
反应④:
物质E+Cl2→物质F,则E中含有Fe2+;
反应③:
丙的水溶液D+金属B→物质E,可推断金属B为Fe,则E为FeCl2,F为FeCl3。
(1)根据上述分析可知A为Na;
G为Fe(OH)3;
(2)气体甲为H2,气体乙为Cl2,氢气在氯气中燃烧的现象为:
产生苍白色火焰,放出大量的热,出现白雾;
(3)反应①为钠和水的反应,离子方程式为:
2Na+2H2O=2Na++2OH-+H2↑;
反应④为FeCl2与的反应,离子方程式为:
2Fe2++Cl2=2Fe3++2Cl-。
5.某淡黄色固体A(仅含三种元素,式量小于160)可用于制药,为探究其组成和性质,设计并完成如下实验:
已知:
①上述流程中所涉及的反应都充分进行。
②B、C、D均为常见气体。
相同情况下气体B的密度大气体C。
③黑色固体
溶于盐酸后滴加KSCN,无明显现象,加适量氯水后,溶液变红。
请问答:
(1)写出气体B的电子式__,固体A的化学式是__。
(2)黑色固体E与足量浓硝酸反应的离子反应方程式是__。
【答案】
FeC2O43FeO+10H++NO3-=NO+3Fe3++5H2O
B、C、D均为常见气体说明D单质为氧气,物质的量为
,相同情况下气体B的密度大气体C则说明B为二氧化碳,B与过氧化钠反应,则C为一氧化碳,气体物质的量为
由于生成0.1mol氧气,根据2CO2+2Na2O2=2Na2CO3+O2,因此二氧化碳的物质的量为0.2mol,CO物质的量为0.2mol,黑色固体E溶于盐酸后滴加KSCN,无明显现象,说明无铁离子,加适量氯水后,溶液变红,说明原物质为FeO,则m(FeO)=28.8g−0.2mol×
28g∙mol−1−0.2mol×
44g∙mol−1=14.4g,则FeO物质的量
,因此n(Fe):
n(C):
n(O)=0.2mol:
(0.2mol+0.2mol):
(0.2mol+0.2mol+0.2mol×
2)=1:
2:
4,则化学式为FeC2O4。
⑴气体B为二氧化碳,其电子式
,根据上面分析得到固体A的化学式是FeC2O4;
;
FeC2O4。
⑵黑色固体E即FeO与足量浓硝酸反应生成硝酸铁、一氧化氮和水,其离子反应方程式是3FeO+10H++NO3-=NO+3Fe3++5H2O;
3FeO+10H++NO3-=NO+3Fe3++5H2O。
6.已知有以下物质相互转化:
请回答下列问题:
(1)写出B的化学式___________,D的化学式为____________;
(2)写出由E转变成F的化学方程式________。
(3)写出D转化成H的离子方程式_________。
(4)除去溶液B中混有的少量G溶液的最适宜方法是________。
【答案】FeCl2KCl4Fe(OH)2+O2+2H2O=4Fe(OH)3Ag++Cl-=AgCl↓向溶液B中加入足量铁粉,再经过滤操作
D和硝酸银、稀硝酸的混合溶液反应生成沉淀H和焰色反应呈紫色的溶液可知,H为AgCl,D为KCl,白色沉淀E在空气中变成红褐色沉淀F可知E为Fe(OH)2,F为Fe(OH)3,所以G为FeCl3,A为Fe,B为FeCl2,C为NaOH,据此解答。
(1)由分析可知,B为FeCl2,D为KCl,故答案为:
FeCl2;
KCl;
(2)E为Fe(OH)2,F为Fe(OH)3,反应的方程式为:
4Fe(OH)2+O2+2H2O=4Fe(OH)3,故答案为:
4Fe(OH)2+O2+2H2O=4Fe(OH)3;
(3)D为KCl,H为AgCl,D转化为H的离子方程式为:
Ag++Cl-=AgCl↓,故答案为:
Ag++Cl-=AgCl↓;
(4)FeCl2中混有的少量FeCl3,可用过量的铁粉将FeCl3转化为FeCl2,过量的铁粉用过滤除去,故答案为:
向溶液B中加入足量铁粉,再经过滤操作。
白色沉淀迅速变为灰绿色,最后变为红褐色所涉及的反应正是E到F:
4Fe(OH)2+2H2O+O2=4Fe(OH)3。
7.A、B、C、D、E、F六种物质的相互转化关系如下图所示(反应条件未标出),其中反应①是置换反应。
(1)若A是常见的金属单质,D、F是气态单质,反应①在水溶液中进行,则反应②(在水溶液中进行)的离子方程式是__________。
(2)若B、C、F都是气态单质,且B有毒,③的反应中还有水生成,反应②需要放电才能发生,A、D相遇有白烟生成,则A、D反应产物的电子式是________,反应③的化学方程式是____。
(3)若A、D、F都是短周期元素组成的非金属单质,且A、D所含元素同主族,A、F所含元素同周期,则反应①的化学方程式是________。
【答案】2Fe2++Cl2=2Fe3++2Cl-
4NH3+5O2
4NO+6H2O2C+SiO2
2CO↑+Si
(1).A是常见的金属单质,D、F是气态单质,反应①为置换反应且在水溶液中进行,由转化关系可知,A为变价金属,F具有强氧化性,则A为Fe,F为Cl2、B为HCl、C为氯化亚铁、D为氢气、E为氯化铁,反应②(在水溶液中进行)的离子方程式是:
2Fe2++Cl2=2Fe3++2Cl-,故答案为:
2Fe2++Cl2=2Fe3++2Cl-;
(2).B、C、F都是气态单质,B有毒,则B为氯气,反应②需要放电条件才能发生,为氮气与氧气反应,③反应中有水生成,可以推知C为N2,F为O2,E为NO,A为NH3,反应①为置换反应,A、D相遇有白烟生成,可推知D为HCl,A与D反应产物为氯化铵,电子式为
,反应③的化学方程式是:
4NH3+5O2
4NO+6H2O,故答案为:
4NO+6H2O;
(3).A、D、F都是短周期元素组成的非金属单质,且A、D所含元素同主族,A、F所含元素同周期,反应①为置换反应,考虑是碳与二氧化硅反应生成硅与CO,碳与F反应生成E,CO与F生成E,则F为氧气,通过验证符合图示转化关系,则反应①的化学方程式是2C+SiO2
2CO↑+Si,故答案为:
2C+SiO2
2CO↑+Si。
8.从某矿渣(成分为NiFe2O4(铁酸镍)、NiO、FeO、CaO、SiO2等)中回收NiSO4的工艺流程如图:
(NH4)2SO4在350℃分解生成NH3和H2SO4;
NiFe2O4在焙烧过程中生成NiSO4、Fe2(SO4)3。
回答下列问题:
(1)“研磨”的目的是___。
(2)矿渣中部分FeO在空气焙烧时与H2SO4反应生成Fe2(SO4)3的化学方程式为____。
(3)“浸泡”过程中Fe2(SO4)3生成FeO(OH)的离子方程式为___。
“浸渣”的成分除Fe2O3、FeO(OH)、CaSO4外还含有___(填化学式)。
(4)向“浸取液”中加入NaF以除去溶液中Ca2+,溶液中c(F-)至少为___mol·
L-1时,可使钙离子沉淀完全。
[已知Ca2+浓度小于1.0×
10-5mol·
L-1时沉淀完全;
Ksp(CaF2)=4.0×
10-11]
(5)萃取可用于对溶液中的金属离子进行富集与分离:
Fe2+(水相)+2RH(有机相)
FeR2(有机相)+2H+(水相)。
萃取剂与溶液的体积比(
)对溶液中Ni2+、Fe2+的萃取率影响如图所示,
的最佳值为___。
在___(填“强碱性”“强酸性”或“中性”)介质中“反萃取”能使有机相再生而循环利用。
(6)若将流程图中浸泡步骤改为如图步骤(前后步骤不变)。
依据下表数据判断,调pH范围为___。
【答案】增大接触面积,加快反应速率4FeO+6H2SO4+O2
2Fe2(SO4)3+6H2OFe3++2H2O
FeO(OH)+3H+SiO22.0×
10-30.25强酸性3.7≤pH<
7.1
某矿渣的主要成分是NiFe2O4(铁酸镍)、NiO、FeO、CaO、SiO2等,加入硫酸铵研磨后,600°
C焙烧,已知:
(NH4)2SO4在350℃以上会分解生成NH3和H2SO4;
NiFe2O4在焙烧过程中生成NiSO4、Fe2(SO4)3,在90°
C的热水中浸泡过滤得到浸出液,加入NaF除去钙离子,过滤得到滤液加入萃取剂得到无机相和有机相,无机相通过一系列操作得到硫酸镍,有机相循环使用,据此分析解答。
(1)焙烧前将矿渣与(NH4)2SO4混合研磨,混合研磨的目的是增大接触面积,加快反应速率,使反应更充分;
(2)矿渣中部分FeO在空气焙烧时与H2SO4反应生成Fe2(SO4)3的化学方程式为4FeO+6H2SO4+O2
2Fe2(SO4)3+6H2O;
(3)“浸泡”过程中Fe2(SO4)3生成FeO(OH)的离子方程式为:
Fe3++2H2O
FeO(OH)+3H+;
根据分析,浸渣”的成分除Fe2O3、FeO(OH)、CaSO4外还含有
SiO2;
(4)向“浸取液”中加入NaF以除去溶液中Ca2+,已知Ca2+浓度小于1.0×
L-1时沉淀完全,溶液中c(F−)=
=
≈2×
10−3mol/L,故溶液中c(F-)至少为2×
10−3mol/L;
(5)本工艺中,萃取剂与溶液的体积比(
)对溶液中Ni2+、Fe2+的萃取率影响如图所示,最佳取值是亚铁离子不能被萃取,镍离子被萃取,
的最佳取值是0.25;
由Fe2+(水相)+2RH(有机相)⇌FeR(有机相)+2H+(水相)可知,加酸,增大氢离子的浓度,使平衡逆向移动,可生成有机相,则应在强酸性介质中“反萃取”能使有机相再生而循环利用;
(6)若将流程图中浸泡步骤改为如图步骤(前后步骤不变),亚铁离子被双氧水氧化为铁离子,除杂过程中要将铁离子除去但不能使镍离子沉淀,依据下表数据判断,pH=3.7时铁离子完全沉淀,pH=7.1时镍离子开始沉淀,则调节pH范围为3.7≤pH<
7.1。
9.稀土元素包括钪、钇和镧系(含Ce、Eu)共17种元素,是重要的战略资源,我省稀土资源非常丰富.某彩色电视机显示屏生产过程中产生大量的废荧光粉末含(Eu2O3、SiO2、Fe2O3、CeO2、MnO等物质).某课题组以此粉末为原料,设计如下工艺流程对资源进行回收,得到较为纯净的CeO2和Eu2O3(氧化铕).
CeO2不溶于桸硫酸,也不溶于NaOH溶液,Eu2O3可溶于稀硫酸
(1)往滤渣中加稀硫酸和H2O2进行酸浸,反应的离子方程式____________。
为了提高酸浸率,可以适当提高反应温度,但温度偏高浸出率反而会减小,其原因是________________________________。
(2)有机物HR能将Ce3+从水溶液中萃取出来.该过程可表示为:
Ce3+(水层)+3HR(有机层)
CeR3(有机层)+3H+(水层)。
向CeR3(有机层)中加入稀硫酸进行反萃取能获得较纯的含Ce3+水溶液,从平衡角度解释其原因:
________________________。
(3)流程中由含Ce3+滤液生成Ce(OH)4的离子方程式____________________。
(4)取上述流程中得到的Ce(OH)4产品0.52g,加硫酸溶解后,用浓度为0.1000mol•L-1FeSO4标准溶液滴定至终点时,铈被还原为Ce3+,消耗24.00mL标准溶液。
该产品中Ce(OH)4的质量分数为___________。
(5)已知含Ce3+溶液也可以先加碱调pH后再通入氧气氧化可得到Ce(OH)4。
298K时,Ksp[Ce(OH)3]=5×
10-20,若溶液中c(Ce3+)=0.05mol•L-1,加碱调节pH到_____时Ce3+开始沉淀(忽略加碱过程中溶液体积变化).
(6)萃取剂对金属离子的萃取率与pH的关系如图所示.流程中为了用萃取剂除去金属杂质离子,进行萃取2最适宜的pH是_______(填选项序号).其原因是_____。
A.2.0左右B.3.0左右C.5.0左右
【答案】2CeO2+H2O2+6H+=2Ce3++O2↑+4H2O温度升高,H2O2受热易分解,造成浸出率偏低;
加入稀硫酸时,c(H+)增大,平衡向形成Ce3+的方向移动,4Ce3++O2+12OH-+2H2O=4Ce(OH)496%8B使Fe3+、Mn2+完全除去,并防止Eu3+被萃取导致损失
废荧光粉末含(Eu2O3、SiO2、Fe2O3、CeO2、MnO等物质),加入硫酸,滤液含有Eu3+、Fe3+、Mn2+等,经萃取,可除去Fe3+、Mn2+等,加入氨水,可生成Eu(OH)3,加热分解可生成Eu2O3;
滤渣中含有CeO2、SiO2,加入稀硫酸和过氧化氢,经萃取、反萃取,可得到含有Ce3+的溶液,加入氢氧化钠并通入氧气,可生成Ce(OH)4,加热可生成CeO2。
(1)在酸浸时发生的离子反应为2CeO2+H2O2+6H+=2Ce3++O2↑+4H2O,H2O2受热易分解,为防止其分解,则温度不宜太高,故答案为:
2CeO2+H2O2+6H+=2Ce3++O2↑+4H2O;
温度升高,H2O2受热易分解,造成浸出率偏低;
(2)根据平衡Ce3+(水层)+3HR(有机层)
CeR3(有机层)+3H+(水层),向CeR3(有机层)中加入稀硫酸时,c(H+)增大,平衡向形成Ce3+的方向移动,则Ce3+从水溶液中被萃取出来,故答案为:
加入稀硫酸时,c(H+)增大,平衡向形成Ce3+的方向移动;
(3)流程中Ce3+与氧气、氢氧化钠反应生成Ce(OH)4,离子方程式为4Ce3++O2+12OH-+2H2O=4Ce(OH)4,故答案为:
4Ce3++O2+12OH-+2H2O=4Ce(OH)4;
(4)Ce(OH)4加硫酸溶解后,被FeSO4还原为Ce3+,则有Ce(OH)4~Ce3+~FeSO4,则n[Ce(OH)4]=0.1×
24×
10-3mol=2.4×
10-3mol,m[Ce(OH)4]=2.4×
10-3mol×
208g/mol=0.4992g,该产品的纯度为:
,故答案为:
96%;
(5)298K时,Ksp[Ce(OH)3]=5×
10-20,若溶液中c(