海口市度九年级下学期期中考试化学试题B卷Word格式.docx
《海口市度九年级下学期期中考试化学试题B卷Word格式.docx》由会员分享,可在线阅读,更多相关《海口市度九年级下学期期中考试化学试题B卷Word格式.docx(15页珍藏版)》请在冰豆网上搜索。
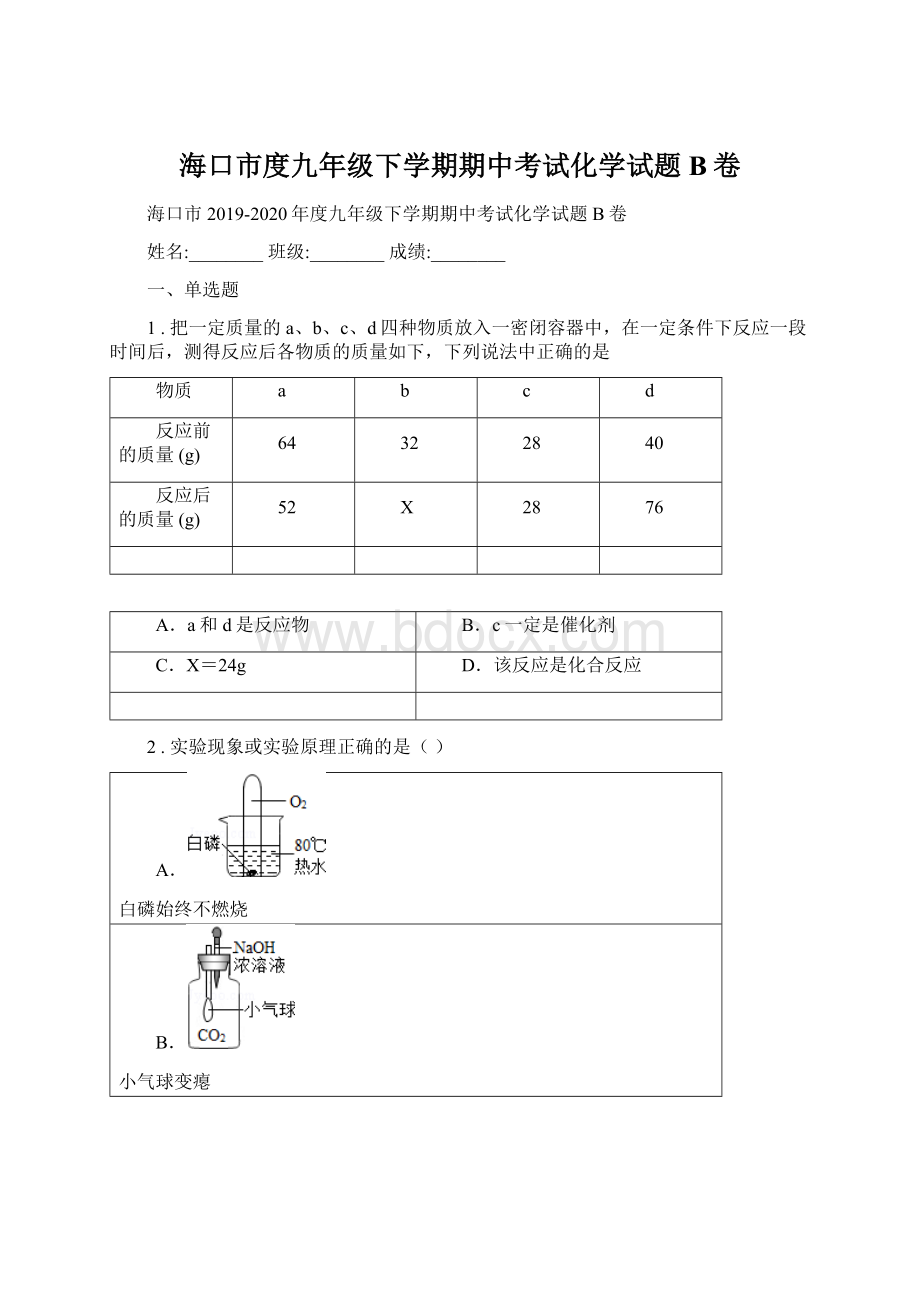
小气球变瘪
C.
U型管内液面左低右高
D.
验证Fe、Cu、Ag的金属活动性强弱
3.下图是氨气和氧气在点燃条件下,发生化学反应时部分微观示意图。
下列说法正确的是
A.反应中各元素的化合价均发生变化
B.该反应属于置换反应
C.生成物种两种物质的质量比为3:
1
D.该反应中分子、原子都发生了改变
4.下图为甘氨酸分子结构模型,下列有关甘氨酸的叙述正确的是()
A.一个甘氨酸中分子含有1个氧分子
B.一个甘氨酸分子由10个元素组成
C.甘氨酸是由碳、氢、氧、氮四种原子构成的
D.甘氨酸中碳元素与氢元素的质量比为24:
5
5.小金在实验室完成了两个有关“水变化”的实验得出的结论合理的是()
A.实验二说明水中含有H2和O2
B.电解水连接电源正极的管内产生O2
C.两个实验变化前后分子种类都改变
D.玻璃管b中的气体具有可燃性
6.在我们学过的化学知识中,有许多物质“名不副实”。
下列说法错误的是
A.“纯碱”不是碱
B.“醋酸”不是酸
C.“水银”不是银
D.“干冰”不是冰
7.打火机是常用的点火工具,其结构如图所示,
下列说法不正确的是
A.打火机的制作材料包括无机非金属材料、金属材料、有机高分子材料
B.打着火后,铁制挡风罩没有燃烧,说明燃烧需要的条件之一是物质具有可燃性
C.松开开关即可熄灭火焰,其灭火原理与森林着火时设置隔离带的灭火原理相同
D.燃料丁烷是从石油中分离出来的,属于化石燃料
8.金刚石、石墨、C60的化学性质相似,物理性质却有很大差异。
原因是:
()
A.构成它们的原子不同
B.构成它们的原子数目不同
C.构成它们的原子大小不同
D.构成它们的原子排列的方式不同
9.下图所示物质的用途中,主要是利用其化学性质的是()
用石墨做干电池的电极
用氢气做高能燃料
用金刚石刀划破玻璃
用大理石做天安门的华表
10.生活中的下列变化只涉及物理变化的是
A.酿酒
B.动植物呼吸
C.菜刀生锈
D.石蜡熔化
11.科学家采用“组合转化”技术,可将二氧化碳在一定条件下转化为重要的化工原料乙烯,其反应的微观过程如图所示。
下列说法不正确的是()
A.微粒所表示的物质中氧化物有2种
B.无机物在一定条件下可转化为有机物
C.参加反应的两种分子的个数比是1:
4
D.乙烯的化学式为C2H4
12.运用化学知识可以解决许多实际问题。
下表中完全正确的一组是:
安全常识
区分常见物质
天然气泄漏——立即打开换气扇
油锅着火——立即用水扑灭
预防煤气中毒——确保烟道畅通
O2和CO2——用澄清石灰水
H2和N2——闻气味
食盐和白醋——观察颜色
物质的性质与用途
日常生活经验
N2性质稳定——作保护气
H2具有可燃性——作气体燃料
CO具有还原性——冶炼金属
去除衣服上油污——用汽油洗涤
使篝火更旺——把木柴架空
硬水软化——加入明矾
A.A
B.B
C.C
D.D
13.已知同温同压下,气体的分子个数之比等于气体体积之比。
密闭容器中氢气在一定量的氧气中完全燃烧时,常温下测得氢气的体积与剩余气体体积的关系如图所示。
下列说法错误的是()
A.B点表示的意义是氢气和氧气恰好完全反应
B.氧气的起始体积为2mL
C.AB段表示剩余气体为氧气
D.C点表示剩余气体体积为(x-2)mL
14.以下说法正确的是
A.CO是一种有毒的气体,它有害无利
B.易燃易爆物应露天存放,紧密堆积
C.燃烧固体燃料需要架空,目的是增大可燃物与空气的接触面积
D.造成酸雨的主要气体是SO2和CO2
15.物质的性质在很大程度上决定了物质的用途。
下列物质的性质与用途对应关系错误的是
A.金刚石硬度大—切割玻璃
B.生石灰能与水反应—作食品干燥剂
C.铜有导热性—作电线
D.干冰升华时吸收大量的热—作致冷剂
16.如图是四位同学讨论某个化学方程式的场景。
他们所描述的化学方程式是()
A.2CO+O2
2CO2
B.C+O2
CO2
C.S+O2
SO2
D.2H2+O2
2H2O
17.纳米材料被誉为21世纪最有前途的新型材料。
纳米碳管是一种由碳原子构成的直径为几个纳米(1nm=10-9m)的空心管。
A.纳米碳管是一种新型的有机化合物
B.纳米碳管如果完全燃烧,生成物是二氧化碳
C.纳米碳管材料管道多,表面积大,吸附能力强
D.纳米碳管在常温下化学性质稳定
18.下列物质中,属于纯净物的是()
A.液氧
B.矿泉水
C.食醋
D.稀有气体
19.近期微博热传的“苯宝宝表情包”是一系列苯的衍生物配以相应的文字形成的,如图所示的六氯苯,其化学式为
A.六氯苯属于有机化合物
B.六氯苯是由碳和氯气组成的
C.六氯苯是由6个碳原子和6个氯原子构成的
D.六氯苯中碳元素与氯元素的质量比为6:
17
20.从环境保护角度考虑,下列燃料中最理想的是
A.酒精
B.天然气
C.煤气
D.氢气
二、填空题
21.我国著名化学家侯德榜先生发明了“侯氏制碱法”,其原理中重要的一步是向饱和食盐水中先后通入足量NH3和CO2制备NaHCO3,化学方程式:
NaCl+NH3+CO2+H2O=NaHCO3↓+NH4Cl某兴趣小组在实验室模拟该过程,请结合具体的步骤回答下列问题:
Ⅰ.气体制备
(1)二氧化碳气体制备
实验室常采用石灰石与稀盐酸反应制备CO2,其化学方程式为_____________。
应选择的气体收集装置为______(选填装置对应的字母)。
(2)氨气制备:
实验室常用硫酸吸收氨气,防止污染空气,实验室制备NH3的反应原理为:
Ca(OH)2(固)+2NH4Cl(固)
CaCl2+2H2O+2NH3↑。
现要制备并干燥NH3,所选装置的正确连接顺序为_____→______(选择装置对应的字母)。
实验室制备O2也可用上述制备NH3的发生装置,写出用该发生装置制备O2的化学方程式__________。
II.NaHCO3制备:
NaHCO3
NH4Cl
溶解度/g(20℃)
9.6
37.2
(3)根据表格中的溶解度数据,解释20℃产物中NaHCO3能够先从溶液中结晶析出的原因________。
(4)该过程中另一产物NH4Cl在农业生产中常被用作______________。
22.科学实践活动课上同学们做了很多有趣的实验,了解了很多科学知识。
(一)图A为水果电池实验,该实验中,化学能转变为
。
(二)图B为干冰中倒入热水后,产生了类似于舞台上云雾缭绕的现象。
该实验说明干冰具有的性质是
干冰的这一性质,还可用于
(三)图C为同学们用白糖、果汁、小苏打(NaHCO3)、柠檬酸(C6H8O7)及矿泉水自制的饮料。
(1)原料中的柠檬酸和小苏打粉末混合后溶于水,可以发生以下反应,请将化学方程式补充完整。
3NaHCO3+C6H8O7====C6H5O7Na3+
+3CO2↑
(2)上述反应所涉及到的物质中,属于有机物的是
(写化学式)。
23.如图为某矿泉水的标签.请回答:
(1)该矿泉水属于______(填“纯净物”或“混合物”);
(2)该矿泉水里含有“MgSO4”,“MgSO4”读作____;
(3)该矿泉水显____(填“酸性”或“碱性”);
(4)镁离子的结构示意图是________。
24.红磷燃烧除需要达到着火点外,还需满足的条件是______________________;
该反应的文字表达式为__________________________;
用红磷做“测定空气里氧气含量”的实验时,若红磷的量不足,所测得氧气的体积分数___(填“偏大"
、“偏小"
或“不变”)。
25.
(1)请选择下列物质填入相应横线上(填序号):
A氧气
B二氧化碳
C氮气
D氦气
常用作食品包装保护气的是________;
用于医疗急救的是________;
用澄清石灰水检验的气体是________;
用于填充探空气球的是________;
(2)下列各图中○和●分别表示不同的原子,请回答问题,用字母序号填空:
属于纯净物的有________;
属于混合物的有________;
26.已知在反应3A+2B=2C+D中,反应物A、B的质量比为3︰4。
当反应生成C和D的质量共140g时,消耗B的质量为____g。
三、实验题
27.下列是实验室制取气体的常用装置图。
请根据下图回答问题:
(1)写出仪器a、b的名称:
a
,b
(2)若实验室用高锰酸钾制取氧气,应选择的发生装置及收集装置是
(填序号)。
表示其反应原理的化学方程式为
(3)实验室制取二氧化碳的发生装置及收集装置为
四、简答题
28.根据如图所示实验回答问题。
(1)A中铜片上的白磷燃烧而热水中的白磷不燃烧,说明燃烧的条件之一是_____。
(2)B中水的作用是_____。
(3)C中实验现象是_____。
(4)D中当观察到蒸发皿中出现_____时,停止加热。
29.能源的利用与社会可持续发展密切相关。
(1)煤燃烧时产生NO2、_____等气体,这些气体或气体在空气中发生反应后的生成物溶于雨水,会形成酸雨。
(2)在一定条件下,甲烷(CH4)和水反应(未配平)的微观示意图如图所示。
①W表示的物质的化学式是_____。
②该反应中两种生成物Z和W的分子个数比为_____。
(3)实验室可用锌和稀硫酸反应制取氢气。
写出该反应的化学方程式:
_____。
目前,氢气作为新能源在生活和生产中还未能广泛应用,其原因是_____。
(4)在高温下,工业上以赤铁矿(主要成分是Fe2O3)和一氧化碳反应来炼铁的化学方程式为_____。
30.在成都市公交车燃烧事故的原因调查中,多项证据显示,有人携带汽油上车。
(1)当空气中悬浮着一定量的汽油时,一个小火星就足以使其燃烧,这说明汽油的着火点较_____(选填“高”或“低”)。
(2)加油站必备的消防用品之一是沙子,用沙子灭火的原理是____________________。
(3)这次事故引发了人们对公共交通消防安全问题的讨论,下列观点合理的是_______。
A.公交车上要配备消防器材
B.公交车上坐椅用阻燃材料制成
C.对司乘人员进行消防安全知识培训
31.实验室部分装置如图所示,请回答下列问题。
(1)若用KMnO4制取O2,应选用发生装置________(填编号),应选用收集装置_____或
_____(填编号),反应的化学方程式是___________。
(2)若用100g含杂质5%的石灰石和盐酸制取CO2(假设杂质不与盐酸反应,石灰石的体积约为34cm3),应选用发生装置_____(填编号),反应的化学方程式是______________,其中CaCO3与CO2的质量比为_________,反应后最多能生成______gCO2(结果取整数)。
(3)在实验室制取二氧化碳的研究中,进行了如下实验:
实验编号
药品
甲
乙
丙
丁
mg石灰石
块状
粉末状
wg盐酸
稀盐酸
浓盐酸
①若要研究盐酸的浓、稀对反应的影响,可选择实验甲与______对照(选填实验编号)。
②除盐酸的浓稀外,上述实验研究的另一个影响反应的因素是_____________________。
32.二氧化碳和一氧化碳虽只有一字之差,但它们化学性质相差很大。
(1)有人认为,二者就像孪生兄弟,这是因为___________________________________;
(2)二氧化碳能与水反应,一氧化碳难溶于水。
二氧化碳与水反应的化学方程式_______;
(3)区别一氧化碳和二氧化碳的方法不能用________(填序号);
A.闻气味
B.通入澄清的石灰水
C.点燃
D.通入紫色石蕊溶液
(4)过多的二氧化碳加剧了“温室效应”,写出一条控制二氧化碳排放的措施___________。
33.根据下图回答相关问题。
(1)小孩“血铅超标”中的“铅”指的是_________(填“原子”、“元素”或“单质”),工厂方面的辩解错在哪里?
_______________。
(2)请用文字表述“火场逃生”方法__________________,_______________。
五、推断题
34.I、如图分别是水蒸气液化、水电解的微观示意图,据此回答:
(1)从微观角度解释图甲,图乙的本质区别是_______。
(2)图乙所示化学变化中一定不变的粒子是_______。
II、A、B、C、D是初中化学常见的物质,这四种物质中均含有同一种元素。
其中A是无色气体单质。
B,C均为氧化物,且B为有毒气体,D是大理石的主要成分。
它们之间的转化关系如图所示(图中反应条件及部分反应物、生成物已省略)。
(1)写出物质A的化学式__________;
它的用途有________。
(2)写出实验室用D制备C的化学方程式__________。
六、计算题
35.氢化钠(NaH)是重要的制氢剂,与水接触时,发生如下反应:
请回答下列问题:
(1)氢化钠中钠元素的质量分数是__________(结果精确0.1%)。
(2)若制取100g氢气,需要氢化钠的质量是________?
36.菱铁矿(主要成分是碳酸亚铁)是炼铁的原料之一,现取20.0g菱铁矿,向其中加入足量稀硫酸,充分反应(菱铁矿中的杂质不参加反应,且难溶于水),测得固体质量与所加稀硫酸的质量关系如图所示。
(1)20.0g菱铁矿中FeCO3的质量分数为________%。
(2)列式计算,恰好完全反应时所得溶液的质量。
______
(3)向上述所得溶液中加入____________g水,能得到10%的硫酸亚铁溶液,用于缺铁花卉的营养液。