出血热接种附表Word文件下载.docx
《出血热接种附表Word文件下载.docx》由会员分享,可在线阅读,更多相关《出血热接种附表Word文件下载.docx(10页珍藏版)》请在冰豆网上搜索。
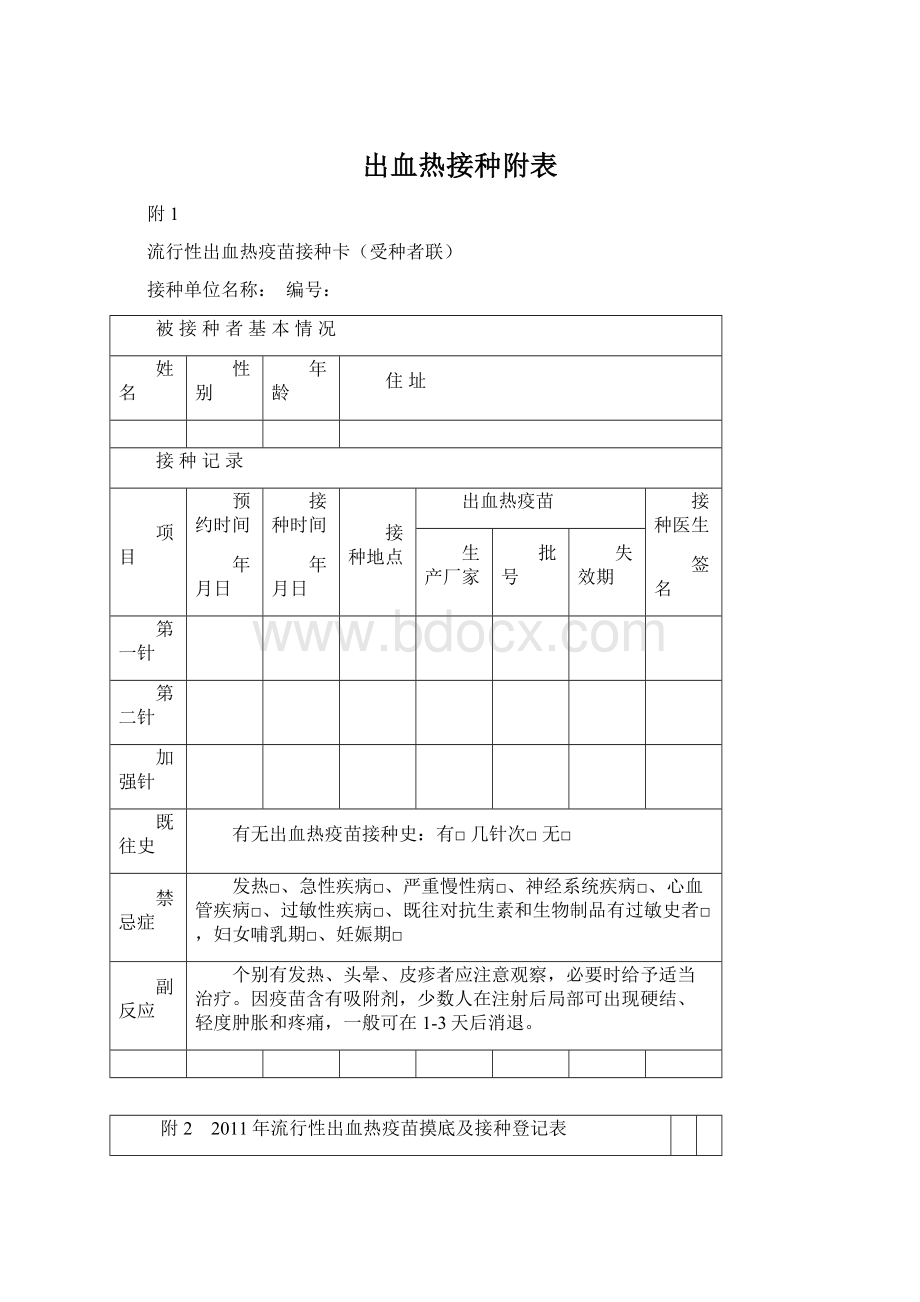
副反应
个别有发热、头晕、皮疹者应注意观察,必要时给予适当治疗。
因疫苗含有吸附剂,少数人在注射后局部可出现硬结、轻度肿胀和疼痛,一般可在1-3天后消退。
附22011年流行性出血热疫苗摸底及接种登记表
宝鸡市县/区乡/镇/社区村/居委会编号
序
号
门
牌
户主
姓名
16-60
岁
人数
16-60岁人员
性
别
户籍
出血热疫苗接种史
有无接种禁忌症
是否需要接种
第一针接种
第二针接种
接种对象签名
本地
暂驻
全程
未全程
未接种
疫苗批号
第三针
注:
1、常住、暂驻人员均纳入摸底登记和接种;
2、家庭16-60岁人员各占一行;
3、户籍中的本地/暂驻栏划“√”;
4、出血热疫苗接种史划“√”;
5、有无接种禁忌症填“有、无”;
6、是否需要接种填“是、否”。
摸底人签名:
联系电话:
年月日
附32011年出血热疫苗接种汇总表
宝鸡市县/区乡/镇/社区村/居委会编号
序号
村/乡镇名称
摸底人数
16-60岁人员数
出血热疫苗接种史
实际接种人数
备注
不全程
加强
汇总单位(盖章):
汇总填表人签名:
联系电话:
填报时间:
年月日
附42011流行性出血热疫苗接种抗体形成率监测表
宝鸡市县/区乡/镇/社区村/居委会编号
门牌
出生
接种前抗体水平
所用疫苗生产厂家
首针
基础免疫后抗体水平
加强接种后抗体水平
采血时间
检测结果
1、所选观察对象必须为常住户口;
2、接种应完成全程3针次;
3、检测结果不填,由省上统一填写反馈;
4、采血3次,分别在接种前、基础免疫2针次后一个月、加强接种后一个月完成,将表和血样一同送检。
填表人签名:
填表时间:
宝鸡市流行性出血热疫苗
疑似预防接种异常反应应急处置预案
流行性出血热疫苗是一种安全有效的疫苗,但仍有少数人在接种后会出现一些轻微的不良反应,还有可能出现罕见的严重症状。
为有效应对和处置接种可能引起的不良反应,保证本次流行性出血热疫苗群体性预防接种工作的顺利实施,根据《全国疑似预防接种异常反应监测方案》要求,特制定本预案。
一、目的
1、预防或尽可能减少接种后异常反应的发生,保护受种者健康;
2、及时调查、处理和上报可能出现的预防接种异常反应,防止事态进一步扩大。
二、组织及人员安排
市、县级均成立由卫生行政部门、临床(内科、传染病科、急诊科等)、药品检验和流行病学专家组成的流行性出血热疫苗预防接种异常反应调查处置组织,负责可能发生的预防接种异常反应的诊断和处理工作。
市级成立流行性出血热疫苗疑似预防接种异常反应处理小组、医疗救治小组和调查诊断小组(见附1、2、3),各县区也要结合实际成立相应组织,分级负责接种不良反应的调查、诊断和处理工作。
各乡镇卫生院至少向每个接种点配备一名经验丰富的内科医生,对发生的疑似接种异常反应病例及时进行初步诊断、现场治疗和处理。
三、报告范围与程序
1、报告范围
流行性出血热疫苗预防接种过程中或接种后发生的怀疑与预防接种有关的反应包括不良反应(一般反应、异常反应)、疫苗质量事故、接种事故、偶合症和心因性反应,共五类。
其中应报告的不良反应包括:
短暂中度以上发热(腋温≥38.6℃)、局部中度以上红肿(直径>2.5cm)、过敏性皮疹(荨麻疹)、过敏性休克、过敏性紫癜、周围神经炎。
2、报告程序与时限
疑似预防接种异常反应报告实行属地化管理。
疫苗接种单位和个人发现属于报告范围的疑似预防接种异常反应(包括接到受种者或其监护人的报告)应在48小时内填写疑似预防接种异常反应个案报告卡(附4),向当地县级卫生行政部门、药品监督管理部门和疾控机构报告;
发现怀疑与预防接种有关的死亡、严重残疾、群体性反应、对社会有重大影响的疑似预防接种异常反应时,在2小时内填写疑似预防接种异常反应个案报告卡或群体性疑似预防接种异常反应登记表(附5),以电话等最快方式报告。
县级卫生行政部门、药品监督管理部门在2小时内向上级部门报告。
县级疾控机构经核实后立即通过“全国预防接种信息管理系统”进行网络直报。
对于死亡或群体性疑似预防接种异常反应,同时还应当按照《突发公共卫生事件应急条例》的有关规定进行报告。
市疾控中心应每天上网对县级报告的个案进行审核,监测分析辖区内疑似预防接种异常反应发生情况。
四、调查处理
1、县级卫生行政部门、药品监督管理部门接到疑似预防接种异常反应报告后,对需要进行调查诊断的疑似预防接种异常反应(除明确诊断的一般反应如单纯发热、接种部位的红肿、硬结等)交由县级疾控机构组织专家进行调查诊断。
县级疾控机构应当在48小时内组织开展调查,应当核实疑似预防接种异常反应的基本情况、发生时间和人数、主要临床表现、初步临床诊断、疫苗接种等,收集相关资料,在调查开始后3日内初步完成疑似预防接种异常反应个案调查表的填写,并通过全国预防接种信息管理系统进行网络直报。
怀疑与预防接种有关的死亡、严重残疾、群体性反应、对社会有重大影响的疑似预防接种异常反应,由市级疾控机构在接到报告后立即组织预防接种异常反应调查诊断专家组进行调查,并将事件处理过程及结果及时上报省疾控中心,如需技术援助,立即向上级提出请求。
2、接种点在疑似预防接种异常反应发生后,接种组医务人员必须尽快做出初步判断和报告,并立即对发生异常反应的病例给予对症治疗、处理(参考附6);
对接种点无法处理的异常反应病例,立即请求乡镇卫生院和县级救治小组派经验丰富的内科医生帮助处理;
同时,各接种点必须保存所有可能与异常反应发生相关的物证(疫苗、注射器等)。
3、如果发现怀疑与疫苗或注射器有关的多例类似反应者,接种单位应立即暂停接种,保存相关物品,及时报告上级机构,并协助调查处理。
4、各级疑似预防接种异常反应调查诊断小组成员在整个调查过程中,要把握好与患者亲属交流的尺度。
在工作未完成前,任何单位和个人不得急于下结论,以预防接种异常反应调查诊断小组的结论为准。
同时做好媒体风险沟通。
五、物资储备
1、县级必须至少准备一辆救护车,在群体性免疫接种实施期间随时待命,一旦需要,能立即赶赴现场。
2、接种点必须储备所需的急救器械和药品(5%或10%葡萄糖液体、1:
1000肾上腺素针剂、抗过敏药物及其它常规急救药品)。
3、指定市中心医院为流行性出血热疫苗接种严重异常反应病例的市级救治医院。
各县区也应确定当地医疗救治点,保证所有需救治接种异常反应病例及时得到妥善处理。
附4
疑似预防接种异常反应个案报告卡
编码
□□□□□□□□□□□□□□
2.
姓名*
3.
性别*
1男
2女
□
4.
出生日期*
年
月
日
□□□□/□□/□□
5.
职业
□□
6.
现住址
7.
联系电话
8.
监护人
9.
可疑疫苗接种情况(按最可疑的疫苗顺序填写)
疫苗
名称
*
规格
(剂/支或粒)
生产
企业
批号
接种
日期
组织
形式
剂次
剂量
(ml或粒)*
途径
接
部位
1
2
3
10.
反应发生日期*
11.
发现/就诊日期*
12.
就诊单位
13.
主要临床经过*
发热(腋温℃)*
137.1-37.5
237.6-38.5
3≥38.6
4无
局部红肿(直径cm)*
1≤2.5
22.6-5.0
3>5.0
局部硬结(直径cm)*
14.
初步临床诊断
15.
是否住院*
1是
2否
16.
病人转归*
1痊愈2好转3后遗症4死亡5不详
17.
初步分类*
1一般反应
2待定
18.
反应获得方式
1被动监测
2主动监测
19.
报告日期*
20.
报告单位*
21.
报告人
22.
说明:
*为关键项目
附5
群体性疑似预防接种异常反应登记表
群体性疑似预防接种异常反应编码:
县国标码□□□□□□-首例发生年份□□□□-编号□□
发生地区:
疫苗名称*:
生产企业*:
规格(剂/支或粒):
有无批签发合格证:
接种单位:
接种人数*:
反应发生人数*:
报告单位*:
报告人:
联系电话:
编码
出生日期
接种日期
接种组织形式
接种剂次
接种剂量
接种途径
接种部位
反应发生日期
发现/就诊日期
是否住院
病人转归
反应获得方式
报告日期
调查日期
发热(腋温℃)*
局部红肿(直径cm)*
作出结论的组织
组织级别
反应分类
最终临床诊断
说明:
*为关键项目。
附6
流行性出血热疫苗预防接种不良反应处理方法(参考)
反应
临床表现
处理方法
常见
不良反应
发热:
轻度(37.1-37.5℃),很少超过3天
轻度全身反应时加强观察,一般不需处理,适当休息,多喝水,防止继发其他疾病
注射部位出现疼痛、发痒、局部硬结、轻度肿胀
一般不需处理,在1-3天内即自行消退
罕见
中度(37.6-38.5℃)、重度(≥38.6℃)发热,很少超过3天
给予物理方法或药物进行对症处理,防止发生高热惊厥或继发其他疾病。
高热不退或伴有其他并发症,应密切观察,及时入院治疗
局部中度以上红肿(直径>2.5cm),一般在3天内即可自行消退
一般不需任何处理,经过适当的休息即可恢复正常。
反应较重的局部红肿可用干净的毛巾热敷,每日数次,每次10-15分钟可助消退
极罕见
过敏性皮疹:
个别接种者在接种后72小时内出现荨麻疹
应及时就诊,给予抗过敏治疗
过敏性休克:
一般在接种后1小时内发生
应及时抢救,注射肾上腺素进行治疗
过敏性紫癜
应及时就诊,应用皮质固醇类药物给予抗过敏规范治疗,防止并发紫癜性肾炎
周围神经炎
应及时就诊