GSP认证检查指导原则修改项目Word文档格式.docx
《GSP认证检查指导原则修改项目Word文档格式.docx》由会员分享,可在线阅读,更多相关《GSP认证检查指导原则修改项目Word文档格式.docx(12页珍藏版)》请在冰豆网上搜索。
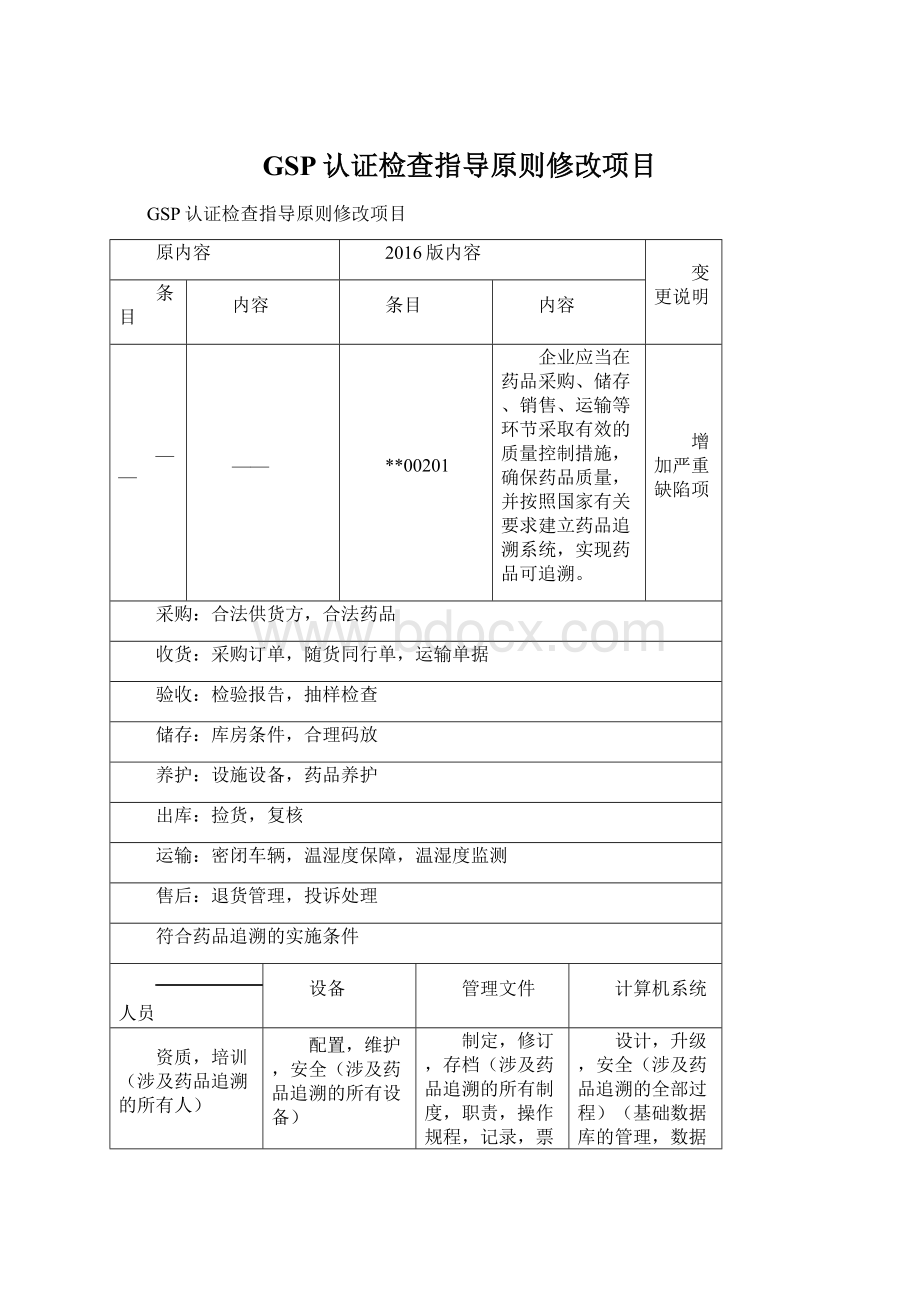
检验报告,抽样检查
储存:
库房条件,合理码放
养护:
设施设备,药品养护
出库:
捡货,复核
运输:
密闭车辆,温湿度保障,温湿度监测
售后:
退货管理,投诉处理
符合药品追溯的实施条件
人员
设备
管理文件
计算机系统
资质,培训(涉及药品追溯的所有人)
配置,维护,安全(涉及药品追溯的所有设备)
制定,修订,存档(涉及药品追溯的所有制度,职责,操作规程,记录,票据,报告,档案等)
设计,升级,安全(涉及药品追溯的全部过程)(基础数据库的管理,数据的关联性,可控性,查询性
人员培训有药品追溯的内容
设备维护记录
药品追溯管理规定进存销运所有记录齐全可追溯
计算机系统的升级维护及数据库的管理
*02208
经营疫苗的还应当配备2名以上专业技术人员专门负责疫苗质量管理和验收工作,专业技术人员应当具有预防医学、药学、微生物学或者医学等专业本科以上学历及中级以上专业技术职称,并有3年以上从事疫苗管理或者技术工作经历。
从事疫苗配送的,还应当配备年以上从事疫苗管理或者技术工作经历。
专业技术人员应当具有预防医学、药学、微生物学或者医学等专业本科以上学历及中级以上专业技术职称,并有3年以上从事疫苗管理或者技术工作经历。
变更为“从事疫苗配送”
1.检查疫苗配送资格备案资料
2.检查人员资质是否合规
3.检查人员工作经历是否合规
*03601
(二十一)执行药品电子监管的规定;
(二十一)药品追溯的规定;
变更为“药品追溯的规定;
”
1.检查是否有制度
2.检查制度的内容是否全面
3.检查制度的执行
*04901
经营冷藏、冷冻药品的,应当配备与其经营规模和品种相适应的冷库。
*04901
变为“储存,运输;
规模适应(储得进、配得出、存得下)
品种适应(品种的储存温度与储存温度适应)
1、检查企业冷库容积及冷藏药品的经营情况(最高到货数量、周转天数、冷库的利用率等),核查是否相适应
2、检查冷库的分区是否齐全(收货验收、储存、包装材料预冷、装箱发货、待处理药品存放等区域)
3、检查企业经营品种的温度范围,核查企业冷库设置是否符合要求
新修订GSP将第四十九条修改为:
“储存、运输冷藏冷冻药品的,应当配备以下设施设备
*04902
经营疫苗的,应当配备两个以上独立冷库(其中一个为备用库)。
**04902
储存疫苗的,应当配备两个以上独立冷库。
变更为严重缺陷项,经营变成储存
1、检查储存疫苗企业批件备案情况
2、检查是否配备了2个以上独立冷库
3、设定温度是否涵盖了所储存疫苗的温度区间
4、冷库是否全部经过了验证
5、两个冷库温控系统是否相互独立
*05701
企业应当建立能够符合经营全过程管理及质量控制要求的计算机系统,实现药品质量可追溯,并满足药品电子监管的实施条件。
企业应当建立能够符合经营全过程管理及质量控制要求的计算机系统,实现药品可追溯。
将电子监管内容变更为药品追溯
1、检查基础数据库的生成之前是否经过质管部门审核
2、检查采购数据是否由基础数据库弓|入
3、检查收货验收环节是否能查看采购记录
4、检查验收记录是否从采购记录引入
5.检查养护计划是否从库存记录弓|出
6.检查销售记录是否从库存记录弓|入
7、检查随货同行单的生成方式,核查出库复核记录的来源
*06101
企业采购药品应当确定供货单位的合法资格;
确定所购入药品的合法性;
核实供货单位销售人员的合法资格。
**06101
变更为严重缺陷项
1、抽查实货或者抽查发票、付款流向等,核查购货单位是否经过审核
2、抽查实货或者采购、验收等记录,核查药品是否经过审核
3、抽查销售人员的授权委托书,核查对销售人员是否进行了审核
*06601
企业采购药品时应当向供货单位索取发票。
**06601
检查发票的索取情况,对于没有发票的情形有合理的解释
*06901
发生灾情、疫情、突发事件或者临床紧急救治等特殊情况,以及其他符合国家有关规定的情形,企业可采用直调方式购销药品,将已采购的药品不入本企业仓库,直接从供货单位发送到购货单位,并建立专门的采购记录,保证有效的质量跟踪和追溯。
*06901
除发生灾情、疫情、突发事件或者临床紧急救治等特殊情况,以及其他符合国家有关规定的情形外,企业不得采用直调方式购销药品。
拆分为*06901和06902两条
6902
企业在上述特殊情况下,采取将已采购的药品不入本企业仓库,直接从供货单位发送到购货单位的直调方式购销药品的,应当建立专门的采购记录,保证有效的质量跟踪和追溯。
1.核查企业是否有直调的行为
2.如有直调是否有专门的采购记录
*08101
对实施电子监管的药品,应当按规定进行药品电子监管码扫码,并及时将数据上传至中国药品电子监管网系统平台。
删除
08201
对未按规定加印或者加贴中国药品电子监管码,或者监管码的印刷不符合规定要求的,应当拒收。
08202
监管码信息与药品包装信息不符的,应当及时向供货单位查询,未得到确认之前不得入库,必要时向当地药品监督管理部门报告。
08402
购货单位应当严格按照《规范》的要求验收药品和进行药品电子监管码的扫码与数据上传。
*10201
对实施电子监管的药品,应当在出库时进行扫码和数据上传。
11201
企业委托运输药品应当有记录,实现运输过程的质量追溯。
委托运输记录至少包括发货时间、发货地址、收货单位、收货地址、货单号、药品件数、运输方式、委托经办人、承运单位等内容,采用车辆运输的,还应当载明车牌号,并留存驾驶人员的驾驶证复印件。
10901
企业运输药品应当有记录,实现运输过程的质量追溯,运输记录应当至少保存5年。
明确了运输记录
11202
委托运输记录应当至少保存5年。
10902
附录变更部分附录
(一)冷藏冷冻药品的储存与运输管理
检查项目
所对应附录检查内容
05101
运输冷藏、冷冻药品的冷藏车及车载冷藏箱、保温箱应当符合药品运输过程中对温度控制的要求。
企业运输冷藏、冷冻药品,应当根据药品数量、运输距离、运输时间、温度要求、外部环境温度等情况,选择适宜的运输工具和温控方式,确保运输过程温度符合要求。
*05101
变更为主要缺陷项目
抽查企业冷链药品销售记录,出库复核记录及运输记录,核查运输工具及温度控制情况
附录变更部分附录
(二)药品经营企业计算机系统
10105
启运时应当做好运输记录,内容包括运输工具和启运时间。
系统应当按照《规范》要求,生成药品运输记录。
10001
企业应当按照质量管理制度的要求,严格执行运输操作规程,并采取有效措施保证运输过程中的药品质量与安全。
药品批发企业系统应当对药品运输的在途时间进行跟踪管理,对有运输时限要求的,应当提示或警示相关部门及岗位人员。
检查项目移除“启运时应当做好运输记录,内容包括运输工具和启运时间。
”检查内容合并
10301
抽查运输记录,核查企业运输管理。
是否有在途时限的要求,超时限的处理
附录变更部分附录(四)药品收货与验收
04708
库房应当有验收的专用场所。
1.药品待验区域有明显标识,并与其他区域有效隔离。
2.待验区域符合待验药品的储存温度要求。
3.验收设施设备清洁,不得污染药品。
4.待验区按规定配备药品电子监管码扫码与数据上传设备。
删除第四条电子监管码相关内容,其他内容不变