高中化学《离子晶体》教案9 新人教版选修3Word下载.docx
《高中化学《离子晶体》教案9 新人教版选修3Word下载.docx》由会员分享,可在线阅读,更多相关《高中化学《离子晶体》教案9 新人教版选修3Word下载.docx(15页珍藏版)》请在冰豆网上搜索。
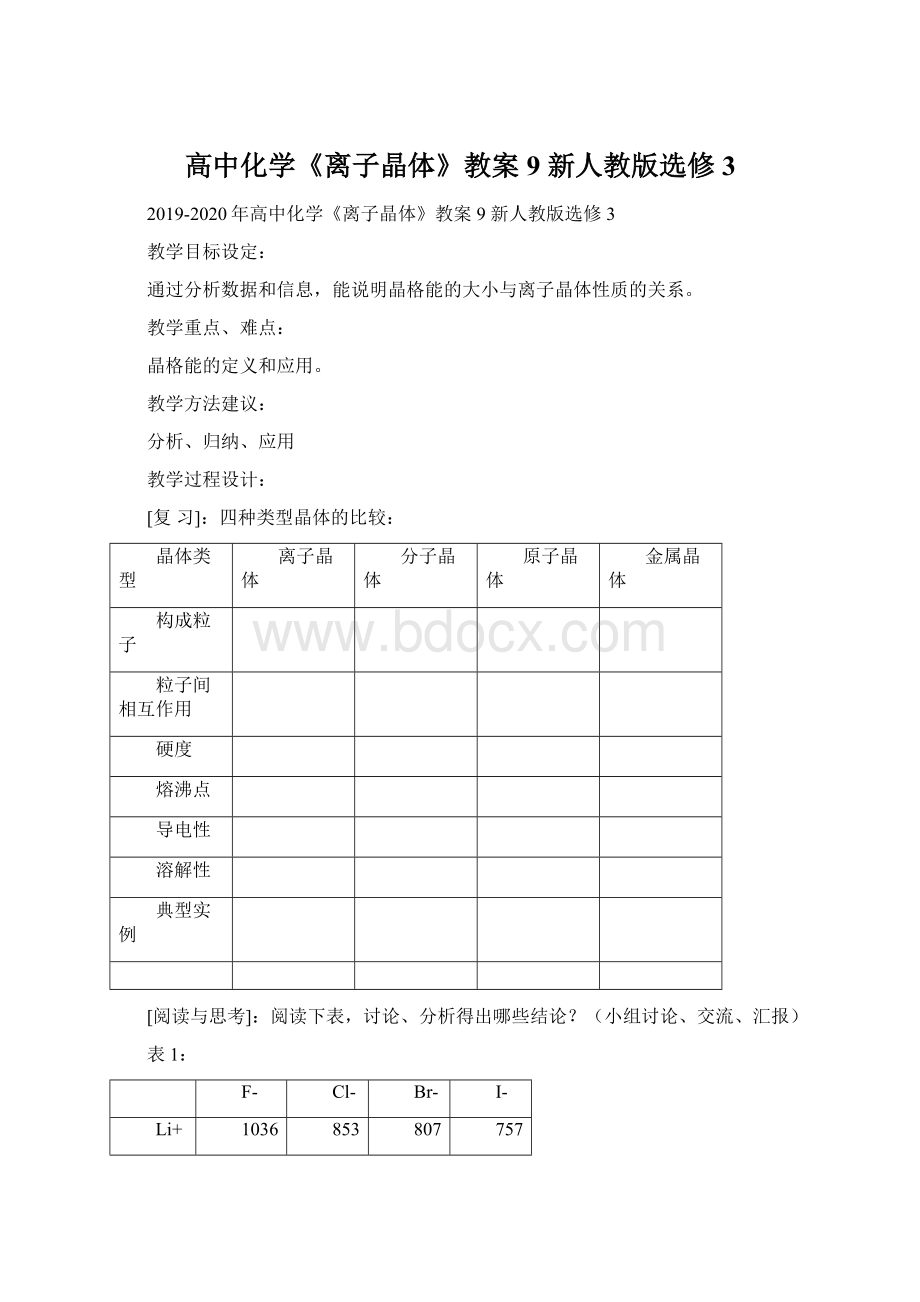
747
704
K+
821
715
682
649
Cs+
785
689
660
630
Rb+
740
659
631
604
表2:
AB型离子晶体
离子电荷
晶格能(KJ/mol
熔点
摩氏硬度
NaF
1
993
3.2
NaCl
801
2.5
NaBr
<
NaI
661
MgO
2
3791
2852
6.5
CaO
3401
2614
4.5
SrO
3223
2430
3.5
BaO
3054
1918
3.3
[板书]:
二、晶格能
1、定义:
气态离子形成1mol离子晶体时释放的能量。
2、规律:
(1)离子电荷越大,离子半径越小的离子晶体的晶格能越大。
(2)晶格能越大,形成的离子晶体越稳定,熔点越高,硬度越大。
[科学视野]:
阅读P84----科学视野,从中你知道了什么?
3、岩浆晶出规则:
晶格能高的晶体,熔点较高,更容易在岩浆冷却过程中先结晶析出。
(美国矿物学家鲍文)
教学习题设计:
1、下列大小关系正确的是
A、晶格能:
NaCl<
NaBrB、硬度:
MgO>
CaO
C、熔点:
NaI>
NaBrD、熔沸点:
CO2>
2、已知:
三种氟化物的晶格能如下表:
晶格能(KJ/mol)
Mg2+
2957
Al3+
5492
三种氟化物的晶格能的递变原因是。
3、已知:
硅酸盐和石英的晶格能如下表:
硅酸盐矿物和石英
橄榄石
4400
辉石
4100
角闪石
3800
云母
长石
2400
石英
2600
回答下列问题:
(1)橄榄石和云母晶出的顺序是。
(2)石英总是在各种硅酸盐析出后才晶出的原因是。
(3)推测云母和橄榄石的熔点顺序为,硬度大小为。
4、下表列出了钠的卤化物和硅的卤化物的熔点:
NaX
995
775
651
SiX4
SiF4
SiCl4
SiBr4
SiI4
—90.2
—70.4
5.2
120.5
(1)钠的卤化物的熔点比相应的硅的卤化物的熔点高很多,其原因是。
(2)NaF的熔点比NaBr的熔点高的原因是。
SiF4的熔点比SiBr4的熔点低的原因是。
(3)NaF和NaBr的晶格能的高低顺序为,硬度大小为。
2019-2020年高中化学《离子晶体》教案设计新人教版选修4
一、教材内容分析
本节知识是中学化学结构理论的重要组成部分。
本节在复习化学键等知识的基础上引入分子间作用力,氢键,晶体结构等基本概念和基本理论,并运用化学键理论和晶体结构理论分析晶体结构与其性质的关系。
本节是中学化学教学的重点和难点,也是历年来高考的热点。
二、教学目标(知识,技能,情感态度、价值观)
知识与技能:
以NaCl晶体为例掌握离子晶体内部结构特点。
使学生掌握离子晶体的基本物理性质。
过程与方法:
了解研究物质结构的基本方法和实验手段,并体会到构建主义的学习方法。
同时感受探究式学习的过程。
情感态度与价值观:
培养学生敢于质疑、勤于思索、勇于创新、积极实践的科学态度。
体验发现的乐趣。
三、学习者特征分析
学生相对基础薄弱,自控力较差。
结合教材的特点及所设计的教学方法,力求把教师的讲授转变为启发诱导,把学生的被动接受转化为主动探索。
以教师为主导,学生为主体,促使学生去动眼看,动手做,动口说,动脑想,使学生的学习过程与认识过程统一为一个整体。
四、教学策略选择与设计
1.以老师为桥梁,通过创设情景引入课题,引导学生提出问题-分析问题-解决问题这一模式进行螺旋教学,以突破教学重点,并调动学生探究的积极性。
2.以多媒体作为教学的辅助手段,增强课堂密度和授课内容的直观性。
3.采用“启发——讨论”式教学方法,在课堂上既有教师提问又有学生提问,既有师生交流又有生生交流。
同时在教学中穿插化学史讲授,让学生在人类文化背景下构建化学课程。
五、教学环境及资源准备
多媒体教室教学。
氯化钠和氯化铯的晶体结构模型
课题:
第四节离子晶体(第一课时)
授课班级
课时
教
学
目
的
知识
与
技能
1、理解离子晶体的结构模型及其性质的一般特点。
2、了解离子晶体中离子晶体配位数及其影响因素。
3、了解决定离子晶体结构的重要因素。
过程
方法
通过学习离子晶体的结构与性质,培养运用知识解决实际问题的能力,培养学生的空间想像能力
情感
态度
价值观
通过学习离子晶体的结构与性质,激发学生探究热情与精神。
进一步认识“结构决定物质性质”的客观规律
重点
离子晶体的结构模型及其性质的一般特点;
离子晶体配位数及其影响因素;
难点
知
识
结
构
板
书
设
计
第四节离子晶体
一、离子晶体
1.定义:
由阳离子和阴离子通过离子键结合而成的晶体。
2.构成微粒:
阴阳离子
3.微粒间的作用:
阴阳离子间以离子键结合,离子内可能有共价键
4.配位数:
与中心离子(或原子)直接成键的离子(或原子)称为配位离子(原子)。
5.结构模型:
(1)氯化钠晶体
(2)氯化铯晶体
6.影响因素:
(1)几何因素:
晶体中正负离子的半径比(r+/r-)。
(2)电荷因素:
正负离子的电荷比。
(3)键性因素:
离子键的纯粹程度。
7.离子晶体特点:
(1)较高的熔点和沸点,难挥发、难于压缩。
(2)硬而脆
(3)不导电,但熔化后或溶于水后能导电。
(4)大多数离子晶体易溶于极性溶剂中,难溶于非极性溶剂中。
教学过程
教学步骤、内容
教学方法、手段、师生活动
[复习]分子晶体、原子晶体、金属晶体的有关理论。
[过渡]在晶体中,若微粒为离子,通过离子键形成的晶体为离子晶体,今天我们来研究离子晶体。
[板书]
[讲]在离子晶体中,阴阳离子间只存在离子键。
不存在分子,而化学式表示为晶体中阴阳离子个数的最简化。
阴阳离子采用不等径密堆积。
[讲]离子晶体不一定含有金属阳离子,如NH4Cl为离子晶体,不含有金属阳离子,但一定含有阴离子。
[讲]离子晶体种类繁多,结构多样,图3—27给出了两种典型的离子晶体的晶胞。
我们来研究晶体中的配位数(在离子晶体中离子的配位数(缩写为CN)是指一个离子周围最邻近的异电性离子的数目)。
[展示]NaCl和CsCl的晶胞:
[科学探究]p78
1、CsCl、NaCl的阳离子和阴离子的比例都是l:
l,同属AE型离子晶体。
参考图3—27、图3-28,数一数这两种离子晶体中阳离子和阴离子的配位数,它们是否相等?
并填表。
阴离子的配位数
阳离子的配位数
6
CsCl
8
2、你认为什么因素决定了离子晶体中离子的配位数?
利用相关数据计算,并填表:
ZnS
r+/r-=0.2-0.4
r+/r-=0.52
r+/r-=0.93
C.N=4
C.N=6
C.N=8
[投影]探究练习参考资料:
离子
Na+
Cs+
Cl-
离子半径/pm
95
169
18l
[讲]显而易见,NaCl和CsCl是两种不同类型的晶体结构。
晶体中正负离子的半径比(r+/r-)是决定离子晶体结构的重要因素,简称几何因素。
4.配位数:
[讲]配位离子的数目称为配位数。
5.结构模型:
[投影]
[讲]由下图氯化钠晶体结构模型可得:
每个Na+紧邻6个Cl-,每个Cl-紧邻6个Na+(上、下、左、右、前、后),这6个离子构成一个正八面体。
设紧邻的Na+与Cl-间的距离为a,每个Na+与12个Na+等距离紧邻(同层4个、上层4个、下层4个)。
由均摊法可得:
该晶胞中所拥有的Na+数为4个,Cl-数为4个,晶体中Na+数与Cl-数之比为1:
1,则此晶胞中含有4个NaCl结构单元。
(2)氯化铯晶体
[讲]每个Cs+紧邻8个Cl-,每个Cl-紧邻8个Cs+,这8个离子构成一个正立方体。
设紧邻的Cs+与Cs+间的距离为a,则每个Cs+与6个Cs+等距离紧邻(上、下、左、右、前、后)。
晶体中的Cs+与Cl-数之比为1:
1。
[讲]上面两例中每种晶体的正负离子的配位数相同,是由于正负离子电荷(绝对值)相同,于是正负离子的个数相同,结果导致正负离子配位数相等,如在NaCl中,Na+扩和C1-的配位数均为6。
如果正负离子的电荷不同,正负离子的个数必定不相同,结果,正负离子的配位数就不会相同。
这种正负离子的电荷比也是决定离子晶体结构的重要因素,简称电荷因素。
例如,在CaF2晶体中,Ca2+和F-的电荷比(绝对值)是2:
l,Ca2+和F-的个数比是l:
2,如图3—29所示。
Ca2+的配位数为8,F-的配位数为4。
此外,离子晶体的结构类型还取决于离子键的纯粹程度(简称键性因素)。
6.影响因素:
[讲]离子键无饱和性和方向性,但成键时因离子半径决定了阴阳离子参加成键的数目是有限的。
阴阳离子半径比值越大,配位数就越大。
[讲]在离子晶体中,离子间存在着较强的离子键,要克服离子间的相互作用使物质熔化和沸腾,就需要较多的能量。
因此,离子晶体具有较高的熔点、沸点和难挥发的性质。
7.离子晶体特点:
[讲]离子晶体的熔沸点,取决于构成晶体的阴阳离子间的离子键的强弱,而离子键的强弱,又可用离子半径衡量,通常情况下,同种类型的离子晶体,离子半径越小,离子键越强,熔沸点越高。
[讲]离子晶体中,由于离子键的强烈作用,离子晶体表现出较高的硬度,当晶体受到冲击力作用时,部分离子键发生断裂,导致晶体破碎。
(2)硬而脆,无延展性
[讲]离子晶体中阴阳离子交替出现,层与层之间如果滑动,同性离子相邻而使斥力增大导致不稳定,所以离子晶体无延展性。
[讲]由于离子晶体中离子键作用较强,离子晶体不能自由移动,即晶体中无自由移动离子,因此,离子晶体不导电。
当升高温度时,阴阳离子获得足够能量克服了离子间相互作用,成为自由移动的离子,在外界电场作用下,离子定向移动而导电。
离子化合物溶于水时,阴阳离子受到水分子作用变成了自由移动的离子(或水合离子),在外界电场作用下,阴阳离子定向移动而导电。
[讲]当把离子晶体放在水中时,极性水分子对离子晶体中的离子产生吸引,使晶体中的离子克服离子间的作用而离开晶体,变成在水中自由移动的离子。
[小结]化学变化过程一定发生旧化学键的断裂和新化学键的形成,但破坏化学键或形成化学键的过程却不一定发生化学变化。
[自学]p79科学视野—复杂离子的晶体
碳酸盐在一定温度下会发生分解,如大家熟悉的碳酸钙煅烧得到石灰(CaO),这是由于碳酸钙受热,晶体中的碳酸根离子会发生分解,放出二氧化碳。
实验证明,碳酸盐的阳离子不同,热分解的温度不同。
碳酸盐
MgCO3
CaCO3
SrCO3
BaCO3
热分解温度/℃
402
900
1172
1360
阳离子半径/pm
66
99
112
135
教学回顾:
第四节离子晶体(第二课时)
高二
(2)
袁顺来
理解离子晶体的晶格能与性质的关系。
离子晶体的晶格能与性质的关系。
1.定义:
晶格能是指1mol的离子化合物中的阴阳离子,由相互远离的气态,结合成离子晶体时所释放出的能量或拆开1mol离子晶体使之形成气态阴离子和阳离子所吸收的能量。
单位是kJ/mol
2.影响因素:
离子的电荷和阴阳离子的大小。
3.规律:
晶格能越大,形成的离子晶体越稳定,而且熔点越高,硬度越大。
[讲]最能反映离子晶体稳定性的数据是它们的晶格能。
离子晶体的品格能的定义是气态离子形成l摩离子晶体释放的能量,通常取正值,表3—8给出了某些离子晶体的晶格能数据。
[板书]
[投影]
F—
C1一
Br—
I—
Li+
K+
Rb+
1036
923
821
785
740
853
786
715
689
659
807
747
682
660
63l
757
704
649
630
604
[讲]晶格能与离子电荷的乘积成正比,与阴阳离子的大小成反比。
[观察]分析晶格能大小与晶体稳定性关系。
[讲]晶格能的数据可以用来说明许多典型的离子晶体的物理化学性质的变化规律。
[自学]p81科学视野—岩浆晶出规则与晶格能
[问题]1.什么是岩浆晶出?
2.岩浆晶出顺序与晶格能的关系?
[投影]岩浆:
[小结]晶格能越大,越早析出晶体。
越早达到饱和,越易析出。