高考化学人教大一轮全程复习构想 课时训练6 金.docx
《高考化学人教大一轮全程复习构想 课时训练6 金.docx》由会员分享,可在线阅读,更多相关《高考化学人教大一轮全程复习构想 课时训练6 金.docx(12页珍藏版)》请在冰豆网上搜索。
高考化学人教大一轮全程复习构想课时训练6金
课时训练6 钠及其重要化合物
一、选择题(本题包括12小题,每小题4分,共48分,每小题只有一个选项符合题目要求)
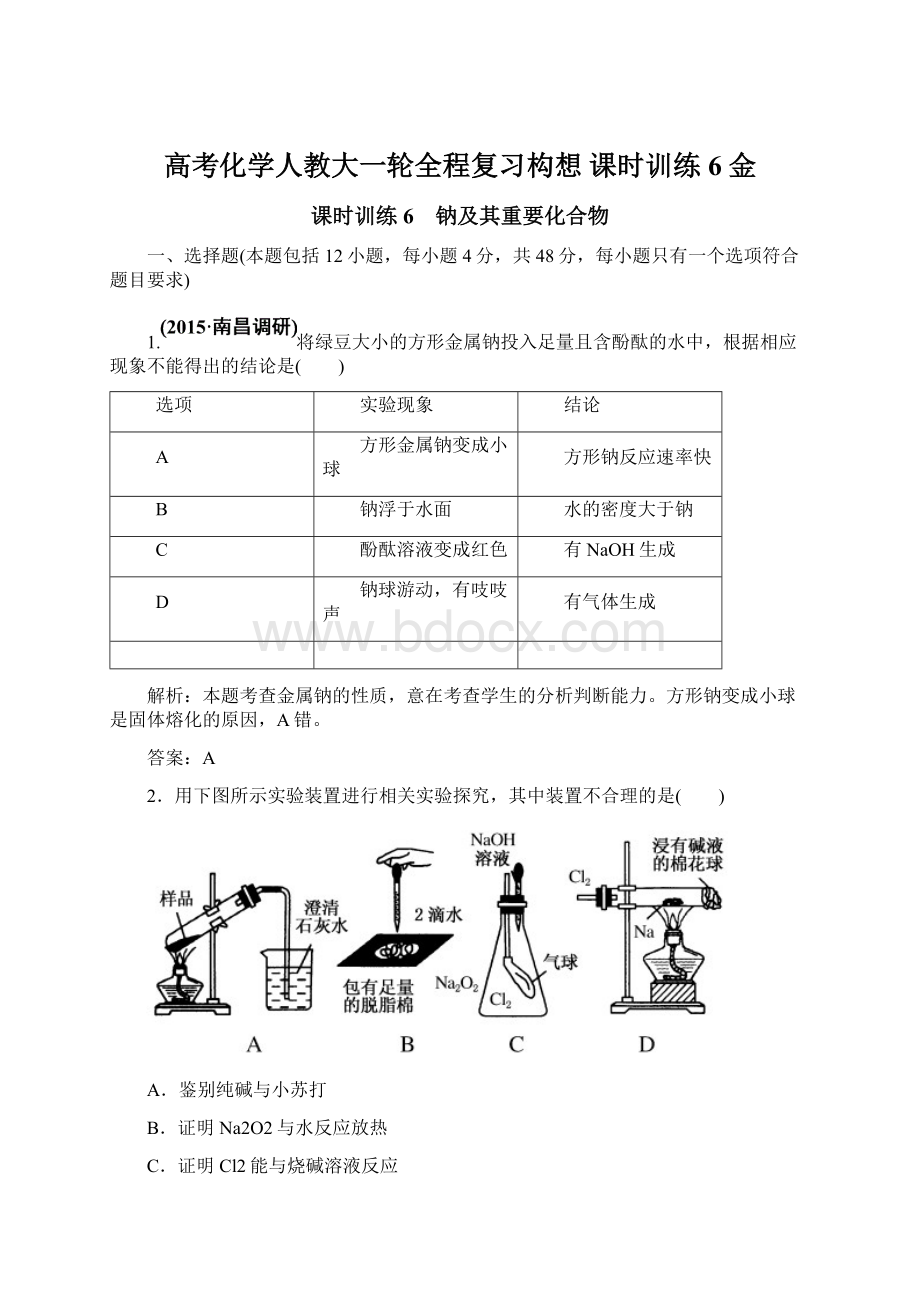
1.将绿豆大小的方形金属钠投入足量且含酚酞的水中,根据相应现象不能得出的结论是( )
选项
实验现象
结论
A
方形金属钠变成小球
方形钠反应速率快
B
钠浮于水面
水的密度大于钠
C
酚酞溶液变成红色
有NaOH生成
D
钠球游动,有吱吱声
有气体生成
解析:
本题考查金属钠的性质,意在考查学生的分析判断能力。
方形钠变成小球是固体熔化的原因,A错。
答案:
A
2.用下图所示实验装置进行相关实验探究,其中装置不合理的是( )
A.鉴别纯碱与小苏打
B.证明Na2O2与水反应放热
C.证明Cl2能与烧碱溶液反应
D.探究钠与Cl2反应
解析:
加热固体时,试管口不能向上倾斜,A项设计错误;B项中脱脂棉燃烧、C项中气球变大,能表明Na2O2与水反应放热、Cl2能被NaOH溶液吸收;D项能进行Na与Cl2反应。
答案:
A
3.下列各组物质相互混合反应,既有气体生成,最终又有沉淀生成的是( )
①金属钠投入到CuSO4溶液 ②过量NaOH溶液和明矾溶液 ③明矾溶液和NaHCO3溶液 ④Na2O2投入FeCl2溶液 ⑤金属钠投入到碳酸氢钙溶液
A.①②③B.③④
C.②③D.①③④⑤
解析:
①金属钠与水剧烈反应,生成NaOH,并放出氢气,生成的NaOH与CuSO4反应生成Cu(OH)2沉淀;②NaOH和明矾电离的Al3+反应,首先生成Al(OH)3沉淀,Al(OH)3能与过量的NaOH反应生成NaAlO2而溶解;③明矾与HCO二者混合水解相互促进,最终生成Al(OH)3沉淀和CO2气体;④Na2O2与水反应生成NaOH和O2,NaOH与Fe2+反应生成Fe(OH)2,Fe(OH)2最终被氧化成Fe(OH)3沉淀;⑤Na与水反应生成NaOH和H2,NaOH与碳酸氢钙反应,生成CaCO3沉淀。
答案:
D
4.下列实验操作正确的是( )
编号
实验
操作
A
观察钠与水反应的现象
用镊子从煤油中取出金属钠,切下绿豆大小的钠,小心放入装满水的烧杯中
B
检验NaHCO3与Na2CO3溶液
用小试管分别取少量溶液,然后滴加澄清石灰水
C
证明Na2O2与CO2是放热反应
Na2O2用棉花包裹,放入充满CO2的集气瓶中,棉花燃烧说明是放热反应
D
检验Na2CO3与K2CO3溶液
用铂丝分别蘸取溶液,在酒精灯外焰上灼烧,直接观察火焰的颜色
解析:
应将钠表面的煤油用纸吸干且烧杯中不能装满水,A错误;B项都有白色沉淀产生,错误;Na2O2与CO2反应生成氧气,如果棉花燃烧说明达到了着火点,能证明是放热反应,C正确;观察钾的焰色反应应该透过蓝色钴玻璃,D错误。
答案:
C
5.如图所示,两圆圈相交的部分表示圆圈内的物质相互发生的反应。
已知钠及其氧化物的物质的量均为0.1mol,水的质量为100g。
下列说法正确的是( )
A.反应③最多能产生0.05molO2
B.反应①的离子方程式为Na+2H2O===Na++2OH-+H2↑
C.Na2O2中阴阳离子数目之比为11
D.①、②、③充分反应后所得溶液中溶质的质量分数:
①>②>③
解析:
本题考查钠及其化合物的相关知识,意在考查学生对相关知识的掌握情况。
0.1molNa2O2与100gH2O反应,H2O过量,反应③最多能产生0.05molO2,选项A正确;反应①的离子方程式应为2Na+2H2O===2Na++2OH-+H2↑,选项B错误;Na2O2中阴阳离子数目之比为12,选项C错误;①、②、③充分反应后所得溶液中溶质(NaOH)的质量分数从大到小:
③=②>①,选项D错误。
答案:
A
6.过氧化钠与CO2作用,反应的化学方程式为2Na2O2+2CO2===2Na2CO3+O2↑。
当0.2molNaO2与足量CO2完全反应后,下表对生成物Na2CO3和O2的描述中正确的是( )
Na2CO3的质量
关于O2的描述
A
21.2g
O2的摩尔质量是36g·mol-1
B
21.6g
生成标准状况下O2的体积为2.24L
C
21.6g
O2的摩尔质量是34g·mol-1
D
22.4g
生成标准状况下O2的体积为2.24mL
解析:
NaO2与CO2的反应实质是-1价的氧发生歧化反应,反应方程式为2NaO2+2CO2===2Na2CO3+18O2,其中生成物Na2CO3中有1个为18O,氧气为18O2,则当0.2molNaO2与足量CO2完全反应后,生成Na2CO3的质量为21.6g,生成标准状况下O2的体积为2.24L。
答案:
B
7.下列事实及其解释不正确的是( )
A.滴有酚酞的NaHCO3溶液呈浅红色,微热后红色加深,是因为NaHCO3分解生成了Na2CO3
B.钠保存在煤油中,是因为煤油不与钠发生反应,钠比煤油密度大,煤油可以使钠隔绝空气和水蒸气
C.用洁净的玻璃管向包有Na2O2的脱脂棉吹气,脱脂棉燃烧,说明CO2、H2O与Na2O2的反应是放热反应
D.钠长期暴露在空气中的产物是Na2CO3,原因是钠与氧气生成的Na2O与水和二氧化碳反应
解析:
A项,对滴有酚酞的NaHCO3溶液微热,红色加深,是因为HCO的水解程度增大,溶液碱性增强。
答案:
A
8.为了使宇航员在飞船中得到一个稳定的、良好的生存环境,一般在飞船内安装盛有Na2O2或K2O2颗粒的装置,它的用途是产生氧气。
下列关于Na2O2的叙述正确的是( )
A.Na2O2中阴、阳离子的个数比为11
B.Na2O2分别与水及CO2反应产生相同量的O2时,需要水和CO2的质量相等
C.Na2O2分别与水及CO2反应产生相同量的O2时,转移电子的物质的量相等
D.Na2O2的漂白原理与SO2的漂白原理相同
解析:
Na2O2的电子式为Na+[]2-Na+,故阴、阳离子的个数比为12,A错误;生成相同量的O2时,消耗水和二氧化碳的物质的量相同,但质量不同,B项错;由得失电子守恒知两者转移电子的物质的量相同,C项正确;Na2O2因具有强氧化性而有漂白性,SO2的漂白原理是其与有色物质化合生成不稳定的无色物质,故二者的漂白原理不同,D项错误。
答案:
C
9.一定物质的量的Cl2与NaOH溶液反应,所得产物中NaClO和NaClO3的物质的量之比为35,则参加反应的Cl2与NaOH的物质的量之比为( )
A.811B.35
C.12D.94
解析:
Cl2与NaOH溶液的反应中Cl2既是氧化剂又是还原剂,显然产物中还存在NaCl,在NaClO、NaClO3、NaCl中n(Na)n(Cl)=11,根据元素守恒,则n(Cl2)n(NaOH)=n(Cl)n(Na)=12。
答案:
C
10.我国化学家侯德榜根据NaHCO3的溶解度比NaCl、Na2CO3、NH4HCO3、NH4Cl的都小的性质,运用CO2+NH3+H2O+NaCl===NaHCO3↓+NH4Cl的反应原理制备纯碱。
下面是实验室进行模拟实验的生产流程示意图:
饱和食盐水A和食盐的饱和溶液悬浊液晶体纯碱
则下列叙述错误的是( )
A.气体A是NH3,气体B是CO2
B.第Ⅲ步得到的晶体是发酵粉的主要成分
C.第Ⅲ步操作用到的主要玻璃仪器是烧杯、漏斗、玻璃棒
D.第Ⅳ步操作的主要过程有溶解、蒸发、结晶
解析:
“侯氏制碱法”是先制得氨化的饱和食盐水,再往其中通入CO2(即往饱和食盐水中依次通入足量的NH3、CO2,不能先通入CO2后通NH3,因为NH3在水中的溶解度远远大于CO2,先将溶液氨化后,吸收CO2的效果更好),第Ⅱ步得到NaHCO3悬浊液,第Ⅳ步将NaHCO3加热分解,以得到Na2CO3。
答案:
D
11.为除去括号内的杂质,所选用的试剂或方法不正确的是( )
A.Na2CO3粉末(NaHCO3) 加热
B.NaHCO3溶液(Na2CO3) 应通入过量的CO2气体
C.Na2O2粉末(Na2O) 将混合物在氧气中加热
D.Na2CO3溶液(Na2SO4) 加入适量Ba(OH)2溶液,过滤
解析:
A项,NaHCO3受热分解生成Na2CO3,从而除去杂质;B项,Na2CO3与CO2、H2O反应生成NaHCO3;C项,Na2O与O2反应可生成Na2O2;D项,Na2SO4与Ba(OH)2反应,生成NaOH,又引入新的杂质。
答案:
D
12.将等物质的量的金属Na、Mg、Al分别与100mL2mol·L-1的盐酸反应,实验测得生成气体的体积V(已折合为标准状况)与时间t的关系如图所示,则下列说法错误的是( )
A.x=2.24
B.钠的物质的量为0.2mol
C.反应时,Na、Mg、Al均过量
D.曲线b为Mg与盐酸反应的图像
解析:
由图像可以看出,生成气体的体积相等,则盐酸完全反应,x=2.24,A正确。
根据生成的H2为2.24L,可知Na失去0.2mol电子,则钠的物质的量为0.2mol,B正确。
反应时如果钠过量,则钠会与水反应,生成的气体必多于2.24L,故C错误。
根据反应速率可知曲线a、b、c依次是Na、Mg、Al与盐酸反应的图像,D正确。
答案:
C
二、非选择题(本题共4小题,共52分)
13.(14分)A、B、C、D、E、F六种物质在一定条件下有如图所示相互转化关系,所有反应物和生成物均已给出。
(1)若B是一种淡黄色固体,绿色植物的光合作用和呼吸作用可实现自然界中D、E的循环,反应③是呼吸面具中发生的反应。
则A的化学式为________,F的化学式为________,反应①的离子方程式为______________________________。
(2)若D能使淀粉溶液变为蓝色,B的焰色反应为黄色,反应①、②、③均为溶液中的置换反应,A、D、E为卤素单质。
则A、D、E的氧化性由强到弱的顺序为________________(用序号表示),其中A的化学式是__________;反应②的化学方程式为________________________。
写出工业上获得E的化学方程式:
________________________。
解析:
(1)A为H2O、B为Na2O2、C为NaOH、D为O2、E为CO2、F为Na2CO3。
(2)D能使淀粉溶液变为蓝色,则D为I2;B的焰色反应为黄色,反应①②③均为溶液中的置换反应,A、D、E为卤素单质,结合转化关系知A为Br2、B为NaI、C为NaBr、E为Cl2、F为NaCl。
工业上获得氯气的方法是电解饱和食盐水(氯碱工业)。
答案:
(1)H2O
(2)Na2CO3 2Na2O2+2H2O===4Na++4OH-+O2↑
(2)E>A>D Br2 Cl2+2NaBr===2NaCl+Br2 2NaCl+2H2O2NaOH+Cl2↑+H2↑
14.(10分)
Na与FeSO4溶液反应,一般很难完整地观察到反应全过程的有关现象。
有人用如图所示装置进行实验改进:
先将试管内新制备的FeSO4溶液液面上覆盖一薄层汽油,然后将试管放入烧杯中,待试管内汽油层消失后,往试管内投入一小粒钠,并迅速塞上带导管的单孔塞。
(1)实验中汽油的作用是________________________________________________________________________。
(2)加入钠后观察到液面上有大量气泡逸出,溶液中有________色沉淀生成。
(3)如果往试管中加入汽油后立即投入钠粒可能发生爆炸,其原因是________________