人教版学年中考二模化学试题A卷模拟Word格式文档下载.docx
《人教版学年中考二模化学试题A卷模拟Word格式文档下载.docx》由会员分享,可在线阅读,更多相关《人教版学年中考二模化学试题A卷模拟Word格式文档下载.docx(12页珍藏版)》请在冰豆网上搜索。
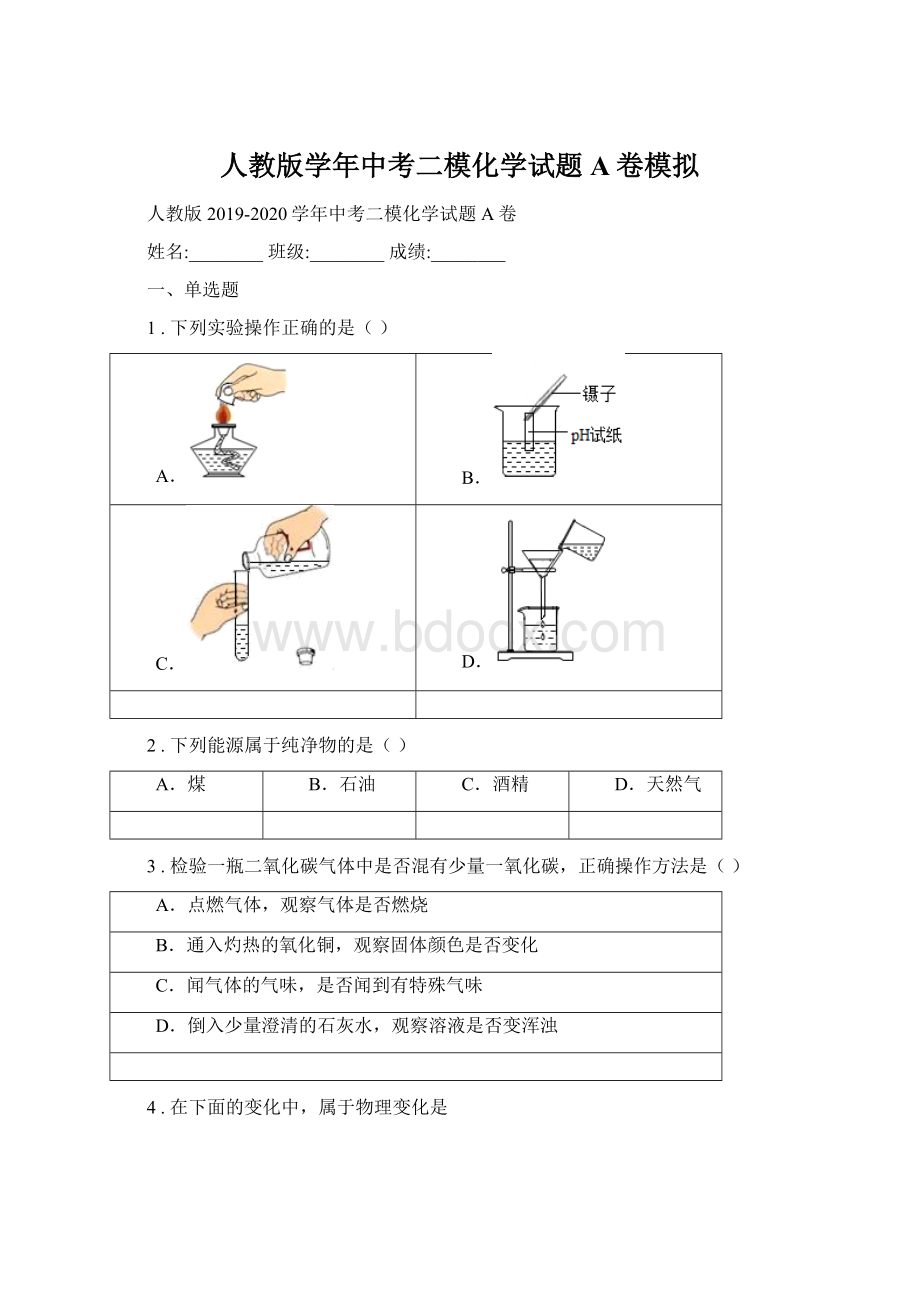
B.纸张燃烧
C.牛奶变酸
D.水分蒸发
5.2017年6月1日,特朗普宣布美国退出《巴黎协定》,引起国际社会强列反响,使能源和环境问题再次成为热点。
下列观点或做法完全正确的是()
A.保护空气
B.爱护水资源
a.禁燃烟花爆竹——降低PM2.5
b.CO2增多——酸雨
c.SO2排放——温室效应
a.用淘米水浇花——节约用水
b.活性炭——除自来水异味
c.污水处理——防止水污染
C.垃圾处理
D.能源利用
a.焚烧垃圾——减少“白色污染”,环保
b.回收废电池——保护土壤
c.禁烧秸秆——减轻雾霾
a.发现大量可燃冰——无能源危机
b.太阳能路灯——节能环保
c.车用乙醇汽油——无尾气污染
A.A
B.B
C.C
D.D
6.下列有关比较正确的是
A.铁合金中的含碳量:
生铁>
钢
B.地壳中元素的含量:
铝>
氧
C.铁在不同溶液中的锈蚀程度:
河水>
海水
D.铁矿石中铁元素的质量分数:
赤铁矿(Fe2O3)>
磁铁矿(Fe3O4)
7.下列物质的用途与性质对应关系错误的是()
A.铜丝作导线﹣铜具有良好的导电性
B.液氧作火箭助燃剂﹣氧气可支持燃烧
C.干冰用于人工降雨﹣二氧化碳能与水反应
D.氮气作保护气﹣氮气常温下化学性质稳定
8.现有甲、乙、丙三种金属,把乙放入丙盐溶液中,有丙析出;
丙在加热的条件下能与氧气反应,甲即使在高温时也不能与氧气反应。
根据以上实验事实,甲、乙、丙三种金属的活动性顺序是
A.乙、丙、甲
B.丙、乙、甲
C.丙、甲、乙
D.甲、丙、乙
9.下列符号中只具有微观意义的是()
A.2H
C.H
10.人的健康离不开化学,下列叙述错误的是()
A.水果蔬菜可以为人体提供维生素,也可以提供一定量的纤维素
B.健康人体胃液的pH范围在0.9-1.5
C.在人体中若缺少微量元素锌,会引起影响生长发育,造成思维迟钝
D.碳、氢、氧、氯都是人体所需的常量元素
11.等质量的镁、铝、铁三种金属与足量的稀盐酸充分反应,生成氢气的质量与消耗金属的质量对应关系正确的是
12.下列五种物质中均含有碘元素,它们按碘的化合价的顺序排列:
①KI②I2③HIO④X⑤NaIO4。
则根据这种排列规律,X不可能是
A.KIO3
B.AgI
C.I204
D.I205
13.取实验室中部分变质的NaOH样品配成溶液,向其中滴加过量的稀硫酸,下列图象中正确反应其中变化的是()
二、多选题
14.烧杯中盛有BaCl2和HCl的混合溶液100.0g,向其中滴加溶质质量分数为10.0%的Na2CO3溶液,烧杯中溶液的质量与滴加溶液的质量关系如图所示。
下列说法正确的是()
A.ab段产生白色沉淀
B.bc段溶液质量增加86.3g
C.c点对应溶液的溶质质量分数为7.5%
D.向d点溶液中滴加酚酞试液,溶液显红色
15.在密闭容器内进行某化学反应,测量反应前(t0)、反应中(t1)、反应后(t2)三个时刻甲乙丙丁4种物质的质量分数,得到质量分数分布图分别如下:
下列说法错误的是()
A.该反应中,乙是反应物,丁是生成物
B.t1时刻,甲和乙的质量比为5:
7
C.若丙是Cu,丁是二氧化碳,则甲、乙的化学计量数之比为2:
1
D.若反应前物质总质量为100克,如果再增加20g甲,则甲与乙可恰好完全反应
三、填空题
16.用你学到的知识填写下列表格
实验类别
反应符号表达式
反应现象
基本反应类型
1.红磷在空气中燃烧
_____
2.木炭在氧气中燃烧
3.硫粉在氧气中燃烧
4.铁线在氧气中燃烧
(1)铁丝在燃烧时,绕成螺旋状的目的是_____,待_____时将铁丝伸入集气瓶,集气瓶底放少量水的目的是:
_____,若瓶底放了细沙,集气瓶仍炸裂了,则可能原因是_____。
(2)硫粉燃烧集气瓶底放少量水的目的是:
_____。
17.从H、C、O、N、S、Cu、Na元素中选择适当的元素,按要求用化学用语填空。
(1)配制波尔多液的盐______;
(2)小苏打中的阴离子______;
(3)炉具清洁剂中的碱______;
(4)硫酸铵中氮元素的化合价______;
(5)碘酒中的溶剂燃烧的反应______;
(6)有蓝色沉淀参加的中和反应______。
18.除杂的原则是:
在除去杂质的同时可以引入新的杂质,如果不得已引入了杂质,也要易于和原物质分离。
(______)
19.将一定质量的甲、乙、丙、丁四种物质放入密闭容器中,在一定条件下反应一段时间后,测得反应前后各物质的质量如下表:
物质
甲
乙
丙
丁
反应前的质量/g
6
3
17
25
反应后的质量/g
待测
11
34
(1)由表格可知,该反应属于_________反应(填基本反应类型)
(2)反应中乙和丙的质量比为______________。
20.中国石化2018年3月26日宣布,我国首个大型页岩气田——涪陵页岩气田如期建成年产能100亿立方米,相当于建成一个千万吨级的大油田。
(1)页岩气是一种非常规天然气,属于_______(填“可再生”或“不可再生”)资源。
(2)实验室制备甲烷气体,常采用排水法或向下排空气法收集,说明甲烷具有哪些物理性质:
____________________________________。
(3)甲烷与水蒸气高温下反应能生成一种有毒气体和一种单质,该反应的化学方程式为_______________________________________。
(4)页岩气是一种非常规天然气,作燃料燃烧时火焰发黄,这是应采取的措施是____。
21.根据图中a、b、c三种固体的溶解度曲线,回答问题。
(1)N点的意义是_______________________________。
(2)温度为t1℃时,a、b、c三种物质的溶解度从大到小的顺序是____________。
(3)将t3℃时a、b、c三种物质的饱和溶液都降温到t1℃,三种溶液中溶质的质量分数由大到小的顺序为____________。
四、实验题
22.化学是一门以实验为基础的科学,请结合图示回答问题:
(1)图中仪器①的名称是_____.
(2)实验室用高锰酸钾制取氧气的化学反应方程式为_____。
(3)实验室制取二氧化碳,选择发生装置B,其优点是_____
。
该反应的化学方程式为_____。
(4)实验室中常用氯化铵和熟石灰的固体混合物加热制取氨气.通常状况下,氨气是一种无色、有刺激性气味的气体,极易溶于水,密度比空气小.实验室欲制取氨气,可选择的发生装置是_____(填序号),若用装置D收集一瓶氨气,则氨气应从_____(填“a”或“b”)端通入,多余的氨气应进行处理,防止污染环境.
(5)某些大理石中含少量硫化物,使制得的CO2中混有H2S气体。
欲获取纯净、干燥的CO2,需对发生装置中产生的气体进行除杂,实验装置如下:
查阅资料:
I.H2S能与NaOH等碱溶液、CuSO4溶液反应。
Ⅱ.CO2中混有的HC1气体可用饱和NaHCO3溶液吸收。
装置甲中所盛试剂应选用_____(填字母)。
A浓硫酸
BNaOH溶液
C澄清石灰水
DCuSO4溶液
五、推断题
23.A、B、C、D、E是初中化学常见的物质,它们的转化关系如图所示(“→”表示物质间转化关系,部分反应物、生成物及反应条件已略去).其中A、B、E均为氧化物,且B、E组成元素相同,C、D为不同类别的化合物,D在工业上广泛用于玻璃、造纸、纺织和洗涤剂的生产等。
则C的化学式是_____;
B的一种用途是_____;
B→E反应过程中会_____(填“吸收”或“放出”)热量;
由B转化为A化学方程式_____。
六、计算题
24.汽油是混合物,其组成可把它看作C8H16,密度约为0.7kg/L。
(1)C8H16的相对分子质量为_________;
(2)C8H16中碳元素的质量分数约为_________(计算结果保留至0.1%);
(3)请依据C8H16与氧气反应的化学方程式计算:
一辆百公里油耗为10L的汽车每公里排放二氧化碳多少克_________?
(假设汽油充分燃烧生成二氧化碳和水)
25.向盛有锌粒的试管中逐滴加入稀硫酸,产生气体的质量与加入稀硫酸质量的关系如图所示。
请计算:
(1)锌粒反应结束时,产生氢气的质量为_____。
(2)原稀硫酸溶液的溶质质量分数_____。
七、综合题
26.二氧化碳与我们生活息息相关,兴趣小组利用图9装置进行多角度探究。
(资料查阅)1.浓盐酸具有挥发性,能挥发出氯化氢气体
2、HCl与AgNO3溶液发生反应,生成白色沉淀(白色沉淀为不溶于水也不溶于酸的AgCl)。
3、盐酸可与石灰水反应:
Ca(OH)2+2HCl═CaCl2+2H2O
探究一 气体的制取
(1)写出图中①的仪器名称:
(2)用装置A制取二氧化碳的反应化学方程式是_____。
若装置A用于实验室制取氧气,则反应化学方程式是_____。
(3)生活中有许多物品可以代替实验仪器。
关闭K2和K3,打开K1,若用装置F所示的医用塑料袋排空气法收集CO2,则F装置_____(填“a”或“b”)端与B装置相连。
探究二
气体的性质检验
打开K2、关闭K1和K3,用于检验制取的二氧化碳性质。
(4)若装置C中是紫色石蕊试剂,可观察到_____(填现象),证明二氧化碳与水发生了反应。
若装置C中试剂是澄清石灰水,则该反应的化学方程式是_____。
(5)小强将制取的二氧化碳通入澄清石灰水中,未见浑浊,小强认为是使用的盐酸浓度过高,挥发进入石灰水中。
要验证是否是上述原因,设计实验方案为:
探究三 测定气体生成的反应速率
关闭K1、K2,打开K3,可测一段时间内生成二氧化碳气体的速率。
所测得数据如下:
稀盐酸的体积(mL)
(反应前)
大理石质量(g)(反应前)
E装置收集的液体量(mL)
反应时间(s)
50
5.0
37.8
100
(6)由实验数据可知,生成CO2的体积为_____mL。
(7)若生成气体的反应速率用公式v=△V/△t表示(△V表示生成气体的体积、△t表示反应所用的时间),则生成的二氧化碳的速率为_____mL/s。
(8)有同学认为,图中的测量方法容易带来误差,请指出造成误差的原因_____(写一点)。
参考答案
1、
2、
3、
4、
5、
6、
7、
8、
9、
10、
11、
12、
13、
4、答案:
略