合肥市度九年级上学期期末化学试题I卷Word格式.docx
《合肥市度九年级上学期期末化学试题I卷Word格式.docx》由会员分享,可在线阅读,更多相关《合肥市度九年级上学期期末化学试题I卷Word格式.docx(10页珍藏版)》请在冰豆网上搜索。
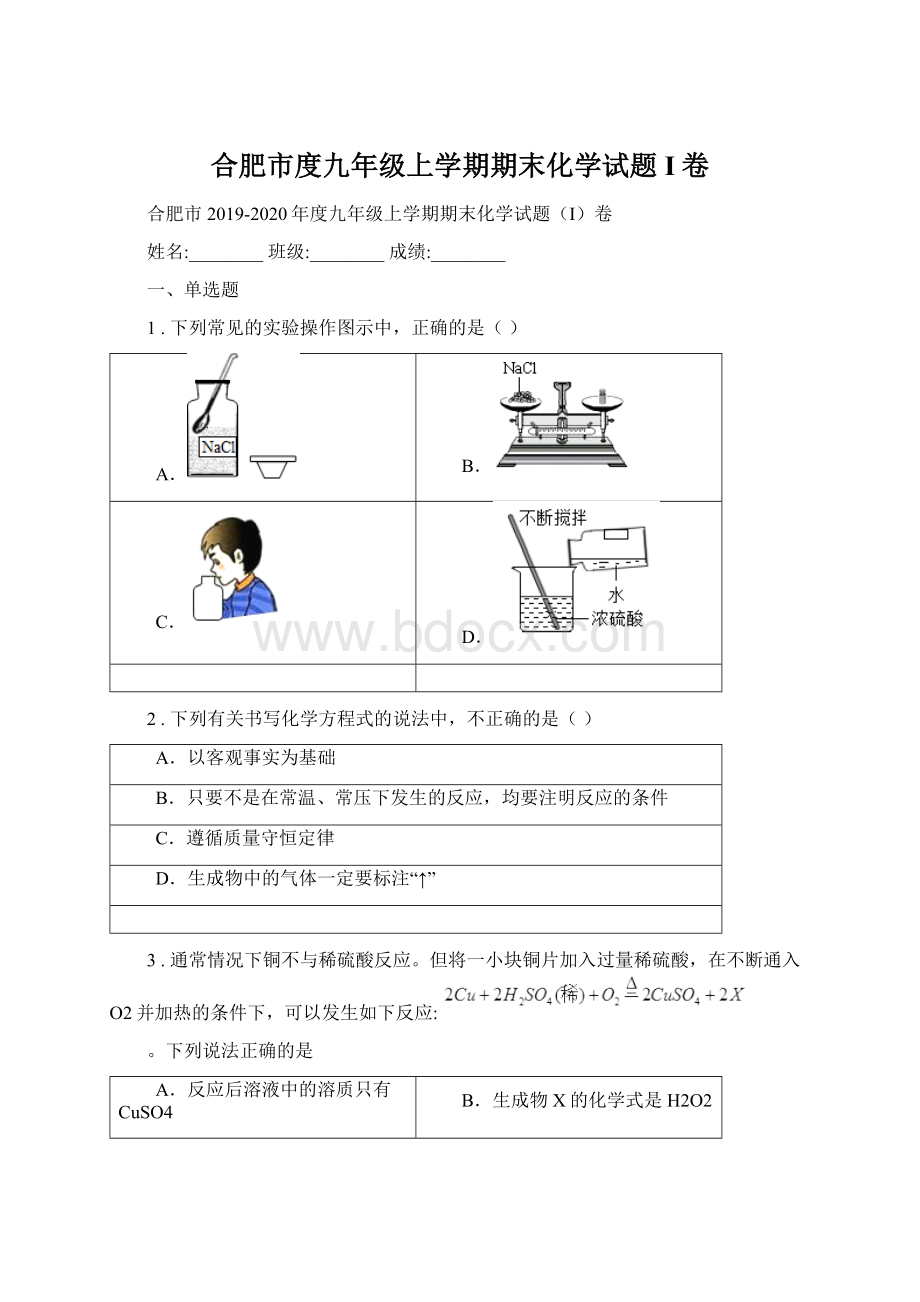
。
下列说法正确的是
A.反应后溶液中的溶质只有CuSO4
B.生成物X的化学式是H2O2
C.反应后溶液由无色变为蓝色
D.反应后溶液质量减少
4.如图表示X、Y、Z三种物质的溶解度曲线,下列说法错误的是
A.Y中含有少量X,用海水晒盐的原理提纯Y
B.t3°
C时,X、Y的饱和溶液降温到t2°
C,析出晶体较多的是x
C.t1°
C时,三种物质的饱和溶液升温到t2°
C,溶液中溶质质量分数的大小关系是Y>
X>
Z
D.t3°
C时,等质量的X、Y分别配成该温度下的饱和溶液,所得溶液质量X<
Y
5.下列著名诗词中不涉及化学变化的是
()
A.千锤万凿出深山,烈火焚烧若等闲
B.春蚕到死丝方尽,蜡炬成灰泪始干
C.爆竹声中一岁除,春风送暖入屠苏
D.千里冰封,万里雪飘
6.在大气层中,因CO2的含量不断增加而引起“温室效应”,造成大气中CO2含量增加的主要原因是()
A.由于动植物呼吸作用增加
B.由实验室逸出的CO2增加
C.由于森林绿化面积迅速递减,使得自然界吸收CO2的能力降低
D.由于大量燃烧含碳燃料
7.下列连线错误的是()
A.人类的营养物质﹣甲醛和一氧化碳
B.空气中的主要成分﹣氮气和氧气
C.二氧化硫、二氧化氮排入大气中﹣形成酸雨
D.有机化合物﹣都含有碳元素
8.以甲为原料合成化工产品丁的微观过程如图所示,下列说法正确的是()
A.乙、丁为氧化物
B.转化①中乙和丙的分子个数之比为1∶1
C.该反应前后原子总数发生了改变
D.该过程体现了无机物与有机物可相互转化
9.下列实验中,能够达到实验目的的是()
A.制备Cu(OH)2固体:
用CuO与适量NaOH溶液混合
B.鉴别稀H2SO4和稀盐酸:
取样,分别滴加Ba(NO3)2溶液
C.除去CO中的少量CO2气体:
将气体通过灼热的CuO粉末
D.分离MnO2和KCl固体混合物:
加入足量的水溶解,过滤
10.下列对实验现象的描述正确的是()
A.在空气中加热铜丝,生成黑色固体
B.蜡烛在氧气中燃烧,产生蓝色火焰
C.将银丝伸入稀盐酸中,产生大量气泡
D.KNO3固体与熟石灰混合研磨,产生刺激性气味气体
11.催产素(oxytocin)的化学式为C43H66N12O12S2,下列有关说法不正确的是
A.催产素分子中碳、氢、氮、氧、硫的原子个数比为43:
66:
12:
2
B.催产素由碳、氢、氮、氧、硫五种元素组成
C.催产素中硫元素质量分数为
D.催产素的相对分子质量是1006
12.宋代著名的医学家宋慈编写的《洗冤集录》中有“银针验毒”的记载,“银针验毒”的原理之一是:
4Ag+2H2S+O2=2X(黑色)+2H2O下列说法中正确的是()
A.X为Ag2S
B.金属活动性:
Ag>Cu
C.反应中H2S和O2的质量比为17:
16
D.反应前后,银元素、氧元素的化合价均没有改变
二、填空题
13.根据下图中KNO3和NaCl两种物质的溶解度曲线,回答下列问题。
(1)10℃时,20gKNO3放入50g水中,形成溶液的质量为_________g;
(2)保持溶液的溶质质量分数不变,将接近饱和的KNO3溶液变成饱和溶液的方法是_______;
(3)若KNO3中含有少量NaCl,提纯KNO3采取的方法是______(选填“蒸发结晶”或“降温结晶”)。
14.日常生活中的不少用品与水银有关,温计就是其中之一。
小明偶患感冒,量体温时不小心将体温计滑落摔碎,地面上散落许多水银珠。
小明想:
水银有毒吗?
怎样清理?
经网络搜寻,小明获取以下有关水银的资料:
水银学名为汞(Hg),常温下是银白色液体,密度大,受热易蒸发且吸附性特别好,不溶于水,及汞的大多数化合物有毒。
在化合物中常表现为+2价,能与硫反应生成不易溶于水的无毒物质——硫化汞(HgS)。
依据以上信息,完成下面问题:
(1)小明关掉室内所有热源,这样做的目的是________________________;
(2)小明戴上手套以避免________________,用小勺把水银收集到盛有水的玻璃瓶中,送交实验室。
(3)小明从实验室带回了硫磺粉,他向不易收集的细小水银珠布上撒硫磺粉降低危害,他的依据是_________________________________(用化学方程式表示).
15.下图是一些微粒的结构示意图和硒元素的相关信息,回答下列问题:
(1)A、B、C中属于阳离子的是_____,其离子符号为_____。
(2)硒元素属于_____(填“金属”或“非金属”)元素,硒元素和钠元素组成化合物的化学式为_____。
(3)下图是某个反应的微观示意图:
①请将图示后两个方框中的微观粒子示意图补画完全,使反应成立______。
②请用化学方程式表示该反应_____。
16.下列是实验室常用的几种仪器,请回答有关问题.
粗盐中含少量Ca2+、Mg2+、SO42﹣和泥沙等杂质,粗盐精制的过程中涉及常规操作步骤有:
(1)①加水溶解;
②依次加入过量的BaCl2、NaOH、Na2CO3溶液;
③
;
④加入适量的
⑤
、冷却结晶(填试剂或操作名称).
(2)过滤用到的玻璃仪器有:
、
.
(3)蒸发时
(填“能”或“不能”)将溶液直接蒸干.
(4)配置1000g5.85%的NaCl溶液,需
gNaCl;
在准确称取固体后,用量筒量取水时,仰视读数,则所配置溶液溶质质量分时
(填“偏高”或“偏低”)
17.
(1)用适当的数字和符号填空:
①二个钠离子_____;
②三个氢氧根离子_____;
③硝酸铵中显﹣3价的氮元素___________;
(2)选择适当物质的序号填空。
A.二氧化碳
B.小苏打
C.硝酸钾
D.氮气
E.熟石灰
F.聚乙烯
①可用于人工降雨的是____________;
②农业上可作复合肥的是______________;
③可用于食品膨松剂的是__________;
④常用于保护蔬菜瓜果的气体是_________;
⑤用作食品包装材料的____________;
⑥可用作改良酸性土壤的是___________。
三、实验题
18.实验室常选用下图中部分装置制取并收集气体,请回答问题:
(1)写出图中标有数字的仪器名称:
①___________,②___________;
(2)用高锰酸钾制取氧气,发生装置应选______,该反应的方程式为:
_______,若用D装置收集O2,集满O2的集气瓶应______放在桌面上(填“正”或“倒”);
(3)若用B装置制取二氧化碳,有关反应的方程式是:
________,如果想要收集到干燥的二氧化碳气体,还需要E、F装置,正确的连接顺序是a-____-_____-____;
(4)装置B与装置C相比较,装置C的优点是:
___________。
19.在实验课上,老师让同学们分组实验探究,自己设计实验证明氢氧化钠与盐酸恰好完全反应。
下面是来自不同小组的三位同学的实验过程,请你帮他们分析解决实验中遇到的问题。
(1)小明同学先按右图所示的方法向试管中加入约2毫升的NaOH溶液,再加几滴酚酞,溶液呈红色,又按下图的方法逐滴加入稀盐酸,直到溶液刚好变无色为止。
请指出小明的操作错误:
______________________________________________.
(2)小华同学向试管中加入约2毫升的NaOH溶液,又加入了一些稀盐酸,突然记起还没有加酚酞,于是加了几滴酚酞,溶液呈无色,他认为两者恰好完全反应。
他的结论是否正确?
____________________________________.
(3)小红同学向试管中加入约2毫升的NaOH溶液,再加几滴酚酞,溶液呈红色,又按正确方法逐滴加入稀盐酸,边加边振荡,直到溶液刚好变无色为止。
可是发现加盐酸时有气泡产生。
请帮她分析一下产生气泡的原因________________________(写一点就行)。
请帮他们写出NaOH溶液与稀盐酸反应的化学方程式____________________________________.
四、流程题
20.如图是利用海水提取粗盐的过程。
(1)图中①是_____池(填“蒸发”或“冷却”)。
(2)在①中,海水中氯化钠的质量分数逐渐_____(填“增大”或“减小”)。
(3)母液为氯化钠的_____溶液(填“饱和”或“不饱和”)。
(4)实验室要配制100g溶质质量分数为3%的氯化钠溶液。
具体步骤:
①计算:
需要氯化钠的质量_____g②称量固体氯化钠③量取一定体积的水④_____。
五、计算题
21.有一赤铁矿样品(主要成分为Fe2O3),某学校化学兴趣小组为了测得样品中氧化铁的质量分数,进行了如下探究:
小明取10g赤铁矿样品(杂质不溶于水和酸),不断加入稀盐酸到固体的质量不再减少,加入稀盐酸的量如图所示()
(1)赤铁矿中氧化铁的质量分数是_____。
(2)计算所使用的稀盐酸的溶质质量分数_____。
22.工业上冶炼150吨含杂质为2%的生铁,需要含杂质20%的赤铁矿石多少吨?
参考答案
1、
2、
3、
4、
5、
6、
7、
8、
9、
10、
11、
12、