高考化学实验题归类总结七物质的性质实验精Word文档格式.docx
《高考化学实验题归类总结七物质的性质实验精Word文档格式.docx》由会员分享,可在线阅读,更多相关《高考化学实验题归类总结七物质的性质实验精Word文档格式.docx(9页珍藏版)》请在冰豆网上搜索。
B.用锌片做阳极,铁片做阴极,电解氯化锌溶液,铁片表面出现一层锌
C.把铜片插入三氯化铁溶液中,在铜片表面出现一层铁
D.把锌粒放入盛有盐酸的试管中,加入几滴氯化铜溶液,气泡放出速率加快
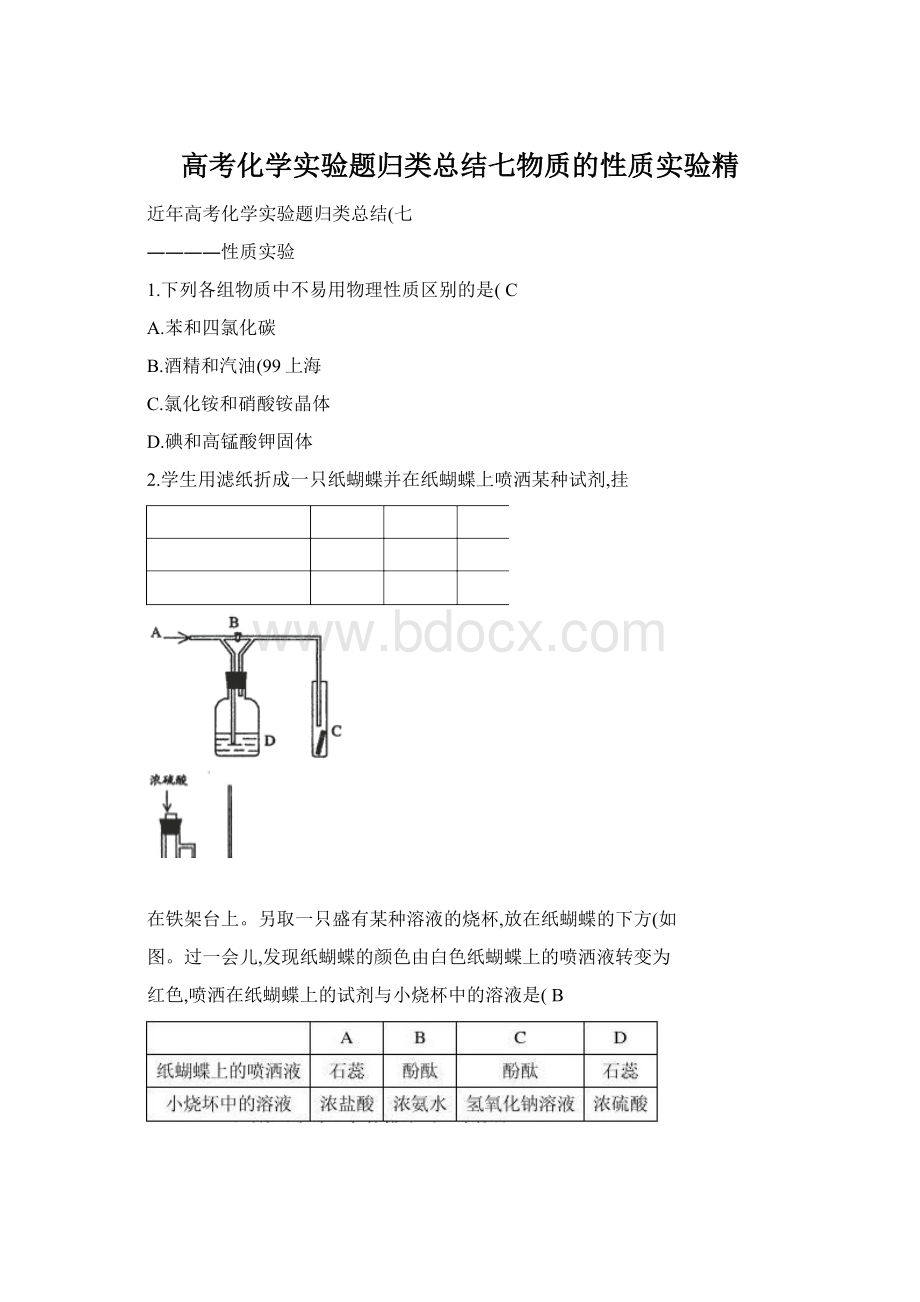
4.右图是一种试验某气体化学性质的实验装置,图中B为开关。
如先打开B,在A处通入干燥氯气,C中红色布条颜色无变化;
当关闭B时,C处红色布条颜色褪去。
则D瓶中盛有的溶液是(B
A.浓H2SO4
B.饱和NaCl溶液(03上海理综化
C.浓NaOH溶液
D.浓NaBr溶液
5.右图小试管中盛有几毫升水,与大试管连通的U型细玻管内放有少量的水(已染成红色。
如沿小试管壁小心地慢慢注入3mL浓硫酸,静置片刻后,U型细玻管中可观察到的液面现象是(B
A.左高右低
B.左低右高
C.左右一样高
D.来回振动
6.都能用图示装置进行喷泉实验的一组气体是(A
A.HCl和CO2
B.NH3和CH4
C.SO2和CO
D.NO2和NO(94上海
7.A是一种白色晶体,它与浓氢氧化钠溶液共热,放
出无色气体B。
用圆底烧瓶收集干燥的B。
按下图装置仪器,
挤压滴管的胶头时,可以得到蓝色喷泉;
A与浓硫酸反应,
放出无色气体C。
用圆底烧瓶收集干燥的C,仍按下图装置
仪器,挤压滴管的胶头时,可以得到红色喷泉。
(1A的化学式是__________________。
(01春京
(2可用于除去B中水分的干燥剂是_______________。
收集气体B的方法是___________________。
(3收集气体C的方法是___________________。
19.(1NH4Cl
(2碱石灰(或答生石灰、KOH固体等任一种不与氨反应的干燥剂;
向下排气法
(3向上排气法
7.某学生课外活动小组利用右图所示装置分别做如下实验:
(1在试管中注入某红色溶液,加热试管,溶液颜色逐渐变浅,冷却
后恢复红色,则原溶液可能是________________溶液;
加热时溶液由
红色逐渐变浅的原因是:
_________________________________
____________________________________________________。
(2在试管中注入某无色溶液,加热试管,溶液变为红色,冷却后恢复无色,则此溶液可能是________________溶液;
加热时溶液由无色变为红色的原因是:
_______________
________________________________________________________________________。
答案(1稀氨水和酚酞;
稀氨水中的NH3气逸出,所以溶液的颜色变浅(2溶有SO2的品红;
SO2气体逸出,品红溶液恢复红色
8.图(Ⅰ中瓶a内放入20mL6mol/L盐酸,b是未充气的气球,里边放有4g碳酸钙粉末,将它紧紧套在瓶a口上,胶管c套在瓶的侧口,并用弹簧夹d夹紧(瓶口和瓶侧都不漏气。
将图(Ⅰ的装置在托盘天平上称量,质量为W1g。
根据实验现象填写下列空白:
(95MCE
(1把气球b中的碳酸钙粉末小心地倒入瓶中,立即产生许多气泡,气球逐渐胀大(图Ⅱ。
反应结束后,再次称量,质量为W2g。
则W1和W2的关系为。
(2取25mL6mol/LNaOH溶液。
先用滴管取少量NaOH溶液,滴管插入胶管c口(为便于操作,可以适当倾斜瓶a,注意防止漏气。
打开d,将溶液挤入瓶中,立即夹紧d。
可以看到瓶内产生少量白色沉淀,轻轻摇动瓶a,沉淀随即消失。
用同样方法再加入少量NaOH溶液,又产生白色沉淀,轻摇,沉淀又消失。
使沉淀消失的反应的化学方程式是
。
(3将全部NaOH溶液很快加入瓶中,夹紧d,瓶内产生大量白色沉淀,不再溶解,此时瓶内温度(填“不变”、“降低”或“升高”。
(4继续轻摇瓶a,气球逐渐缩小,直至恢复反应前的下垂状。
写出这时发生的反应的化学方程式。
答案.(1W2=W1(或回答相等(2Ca(OH2+2HCl=CaCl2+2H2O(3升高(42NaOH+CO2=Na2CO3+H2O;
Ca(OH2+CO2=CaCO3↓+H2O;
(注:
第2个化学方程式可写成Na2CO3+Ca(OH2=CaCO3↓+2NaOH
9.将氯气用导管通入较浓的NaOH和H2O2混合液中,在导管口与混合液的接触处有闪烁的红光出现,这是因为通氯气后混合液中产生的ClO-被H2O2还原,发生激烈反应,产生能量较高的氧分子,它立即转变为普通氧分子,将多余的能量以红光放出。
进行此实验,所用的仪器及导管如图。
(92MCE
根据要求填写下列空白:
(1组装氯气发生器时,应选用的仪器及导管(填写图中编号是。
(2实验进行中,按气流方向从左到右的顺序,气体流经的各仪器及导管的编号依次是。
(3仪器①的橡皮塞上应有个孔,原因是。
(4实验时,仪器①中除观察到红光外还有现象。
(5实验需用约10%H2O2溶液100mL,现用市售30%(密度近似为1g/cm3H2O2来配制,其具体配制方法是。
(6实验时仪器中ClO-与H2O2反应的离子方程式是。
答案.(1③②⑤(不要求顺序
(2②⑤⑥④①或②⑤⑥④
(32;
使瓶内外压强相等(写出其它合理的与大气相通的方法,如多孔也算对。
(4冒气泡
(5用量筒量取33(或34mL30%H2O2溶液加入烧杯中,再加入67(或66mL水(或加水稀释至100mL,搅拌均匀
(6ClO-+H2O2=Cl-+O2↑+H2O
10.根据右图实验,填空和回答下列问题:
(93MCE
(1烧瓶中所发生的主要化学反应的化学方程式是_____________________________。
装置(Ⅱ的烧杯中冷水所起的作用是,装置(Ⅲ的烧杯中液体的作用是。
(2进行此实验时,烧瓶内的橡皮塞最好用锡箔包住,用橡皮管连接的两玻璃管口要相互紧靠,这是因为。
(3装置(Ⅲ的烧杯中使用倒置漏斗可防止液体倒吸,试简述其原因。
答案.(12NaBr+3H2SO4+MnO22NaHSO4+MnSO4+2H2O+Br2↑或2NaBr+
2H2SO4+MnO2Na2SO4+MnSO4+2H2O+Br2↑或NaBr+3H2SO4(浓NaHSO4+
HBr↑(或2NaBr+3H2SO4(浓
Na2SO4+2HBr↑和4HBr+MnO2MnBr2+2H2O+Br2↑;
冷凝;
吸收未冷凝的气体
(2溴蒸气会腐蚀橡皮塞和橡皮管
(3当气体被吸收时,液体上升到漏斗中,由于漏斗的容积较大,导致烧杯中液面下降,使漏斗口脱离液面,漏斗中的液体又流回烧杯内,从而防止了倒吸。
评分要点:
①漏斗容积较大,②烧杯中液面下降,使漏斗口脱离液面(或使液面低于漏斗口
11.(1为证明有关物质的性质,某学生设计了如图所示的装置。
(95上海
当打开活塞C,使液体A与搁板H上的固体B相遇时即有气体产生,并发现D中蜡烛(含C20—30的烷烃慢慢熄灭;
关闭C打开E时,则看到G中蜡烛燃得更亮。
请写出该生在装置中有关仪器内盛放的物质:
A,B,F。
用化学方程式表示上述实验中发生的有关反应
答案.(1稀盐酸;
CaCO3;
Na2O2(注:
答稀硝酸、BaCO3、CaSO3且组合合理CaCO3+2HCl=CaCl2+H2O+CO2↑;
2Na2O2+2CO2=2Na2CO3+O2;
2Na2O2+2H2O=4NaOH+O2↑;
CxHy+(x+4yO2→xCO2+2
yH2O;
或以x为20—30的烷烃分子式表示也可12.某课外活动小组加热炭粉(过量和氧化铜的混合物,再用下图装置,对获得的铜粉(含炭样品进行实验。
图中铁架台等装置已略去。
请你帮助他们完成下列实验报告。
(1实验目的:
。
(2)实验用品:
仪器:
天平、分液漏斗、锥形瓶、硬质玻璃管、干燥管、酒精灯、洗气瓶等药品;
红褐色铜粉(含炭)样品、过氧化氢溶液、二氧化锰、碱石灰、浓硫酸等(3)实验内容:
(00上海)实验步骤在C中加入样品粉末Wg,D中装入药品后并称量为m1g,连接好仪器后,检查气密性。
打开A的活塞,慢慢滴加溶液。
对C进行加热。
当C中药品充分反应后,关闭A的活塞,停止加热。
冷却后,称量D的质量为m2g。
(4)计算:
样品中铜的质量分数:
(5)问题和讨论:
实验完成后,老师评议说:
按上述实验设计,即使C中反应完全、D中吸收完全,也不会得出正确的结果。
经讨论,有同学提出在B与C之间加入一个装置。
再次实验后,得到了较正确的结果。
那么,原来实验所测得的铜的质量分数偏小的原因可能是。
在B与C之间加入的装置可以是(3〕B、E中气泡产生C中红褐色粉末变成黑色(1分)MnO22H2O2¾
¾
®
2H2O+O2
实验现象有关化学方程式(用含W、m1、m2的代数式表示),其中盛放的药品是。
答案.
(1)测定铜粉样品中铜的质量分数¾
2Cu+O2¾
D2CuO¾
C+O2¾
DCO2(4)W-(m2-m1´
W1244(5)偏小;
水蒸汽通过C被D中碱石灰吸收洗气瓶;
浓硫酸(或干燥管;
碱石灰)