初三一模分类汇编基础实验Word文档下载推荐.docx
《初三一模分类汇编基础实验Word文档下载推荐.docx》由会员分享,可在线阅读,更多相关《初三一模分类汇编基础实验Word文档下载推荐.docx(21页珍藏版)》请在冰豆网上搜索。
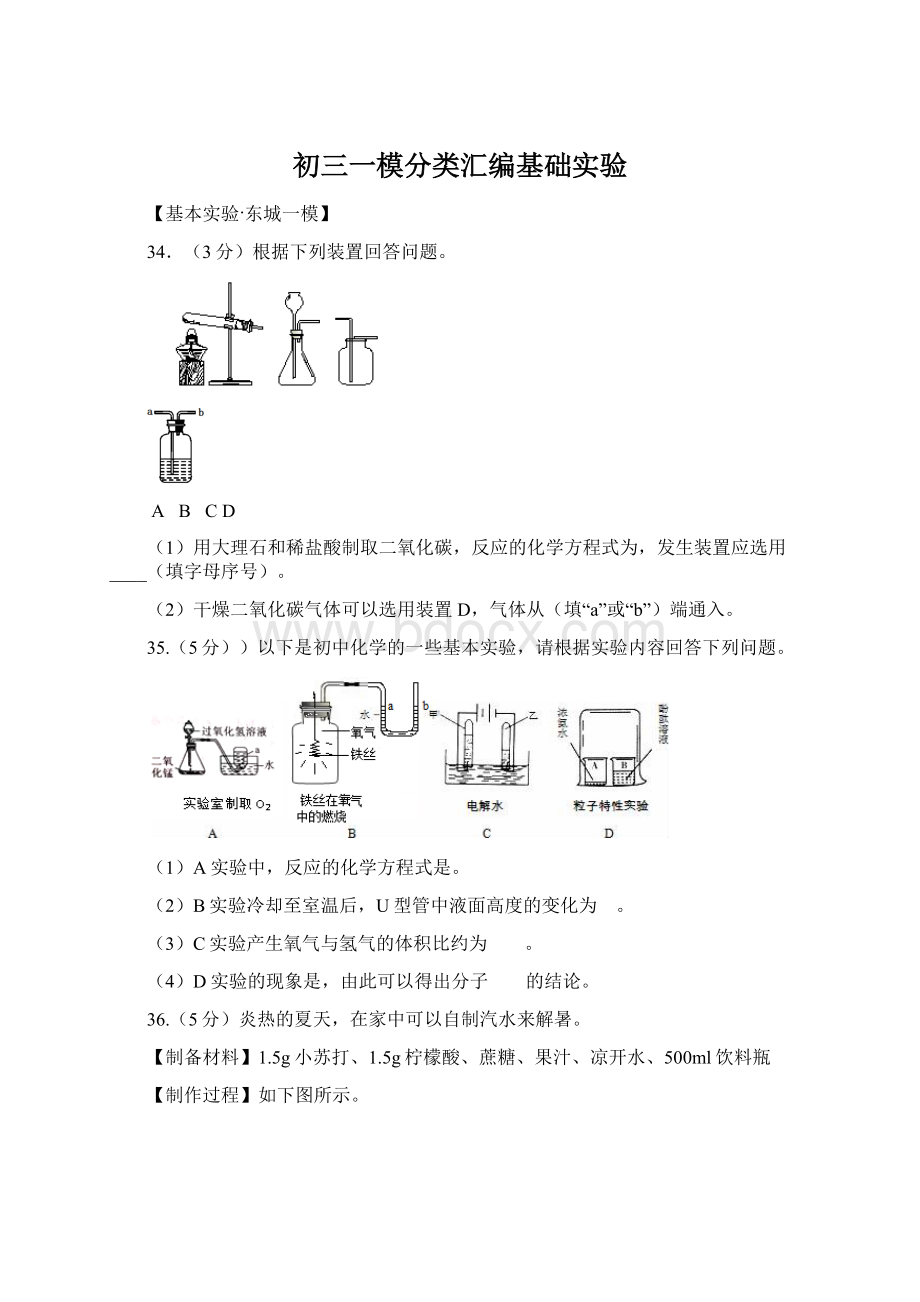
(1)步骤①中使用玻璃棒的目的是_____。
(2)步骤②中过滤器的制作如右图,正确的顺序
是_____(填序号)。
(3)步骤③的名称是_____。
当观察到_____时,停止加热。
(4)在上述粗盐提纯的过程中,利用到氯化钠的物理性质有_____(答一条即可)。
36.(2分)为了探究盐酸和氢氧化钠是否发生反应,设计并进
行了如图所示的实验。
实验中可观察到的现象是_____,该现象能证明盐酸和氢氧
化钠发生了化学反应,其理由是_____。
37.(3分)以铁、铜、铝为例探究金属的物理性质。
老师给同学们提供了下列实验用品:
铁丝、铜丝、铝丝、铝块、电池、小灯泡、酒精灯、火柴、镊子等。
(1)将铝块拉成丝、砸成片,说明铝具有的物理性质是_____。
(2)同学们要测试金属铜的导电性,可选取铜丝、电池和_____。
(3)证明铝比铁的导热性强。
分别在长度和直径都相同的铝丝和铁丝的一端各
滴上一滴石蜡,……,观察到铝丝上石蜡比铁丝上的石蜡先熔化,说明铝
的导热性比铁强。
请补全实验操作_____。
34.(5分)
(1)试管
(2)2KMnO4K2MnO4+MnO2+O2↑氧气不易溶于水
(3)CaCO3+2HClCaCl2+CO2↑+H2O将燃着的木条放于集气瓶瓶口
35.(5分)
(1)加快溶解
(2)CAB(3)蒸发有较多的固体析出
(4)氯化钠能溶于水
36.(2分)溶液由红色变为无色氢氧化钠能使酚酞溶液变为红色,溶液由红色变为无色,
说明氢氧化钠已反应完
37.(3分)
(1)延展性
(2)小灯泡
(3)用酒精灯同时加热铝丝和铁丝的另一端
【基本实验·海淀一模】
35.(4分)根据下图回答问题。
(1)写出一个实验室制氧气的化学方程式,并选择相应的发生装置。
①化学方程式:
。
②发生装置:
(2)实验室收集二氧化碳用装置C而最好不用装置D的原因是。
(3)木炭在氧气中燃烧的实验现象是。
36.(3分)配制20%的NaCl溶液100g。
序号
①
②
③
④
操作
(1)用托盘天平称取所需的氯化钠,发现指针向右偏转,接下来的操作是(填
字母序号)。
A.继续添加氯化钠B.减少砝码
(2)用量筒量取水的体积为mL(ρ水≈1g/cm3)。
(3)该实验的正确操作顺序为(填数字序号)。
37.(3分)为了验证铁、铜、银的金属活动性强弱,同学们设计了如下图所示的两步实验。
第1步
(1)第1步实验的目的是,可观察到的现象是。
(2)第2步实验中,为了达到实验目的,溶液甲可以是(填字母序号)。
A.稀盐酸B.FeSO4溶液C.CuSO4溶液D.ZnSO4溶液
38.(2分)某同学利用如下实验研究酸的性质,并进行未知物检验。
实验
现象
红色固体消失,溶液变黄
固体表面有气泡产生,澄清石灰水变浑浊
(1)进行实验①、②的目的是。
(2)依据实验③、④的现象,可得出关于方解石和云白石成分的结论是。
35.
(1)(①、②均正确,但不对应,共得1分)
△
2KMnO4====K2MnO4+MnO2+O2↑
A
MnO2
2KClO3====2KCl+3O2↑
2H2O2======2H2O+O2↑
B
(2)二氧化碳密度比空气大,且不与空气中的物质反应,因此可以用装置C
收集,而二氧化碳能溶于水,因此最好不用装置D收集
(3)木炭剧烈燃烧、发出白光、放出热量(剧烈燃烧、放出热量答出一点即可)
36.
(1)A
(2)80
(2)②③④①
37.
(1)验证铜、银的金属活动性强弱
铜丝表面覆盖一层灰黑色固体,溶液由无色变成蓝色(答出1点即可)
(2)ABC
38.
(1)探究酸能否与氧化铁反应(或其他合理答案)
(2)含有碳酸盐(或其他合理答案)
【基本实验·朝阳一模】
33.(4分)利用如图所示的实验装置回答有关问题。
(1)装置A是用软塑料管自制的气体发生装置,若利用锌和稀硫酸反应制取氢气,药品加入完毕后,接下来的操作是 ,收集氢气。
该装置还可用于制取的气体是。
(2)若用装置B收集的氧气不纯,原因可能是 (写一种)。
(3)用装置C收集氧气,验满时将带火星的木条放在 (填“a”或“b”)处。
34.(3分)为研究实验室制取二氧化碳的适宜条件,进行如下实验。
实验编号
药品
甲
乙
丙
丁
1g大理石
块状
粉末状
10g盐酸(过量)
稀盐酸
浓盐酸
(1)大理石与盐酸反应的化学方程式为 。
(2)实验甲与 对照,是为了研究固体反应物颗粒大小对反应速率的影响。
(3)上述实验中,另一个影响反应速率的因素是 。
35.(4分)根据下图所示实验,回答以下问题。
(1)A装置中发生反应的化学方程式为。
(2)将紫色石蕊溶液浸泡并晾干的小花,一半喷水后放入集气瓶B中,该实验的目的是。
(3)用C装置测定空气中氧气的体积分数,实验时在粗铜丝末端的燃烧匙中放足量白磷,按图连好仪器,点燃酒精灯加热铜丝一端,白磷燃烧。
①白磷燃烧的化学方程式为。
②整个实验过程中,瓶内水面的变化是。
36.(3分)某同学用实验测定氢氧化钠溶液是否变质,实验过程如下图所示。
(1)配制上图实验所用的稀盐酸,需要溶质质量分数为36.5%的浓盐酸g。
(2)步骤2中最终产生气体g。
(3)该氢氧化钠溶液变质的原因为(用化学方程式表示)。
33.(4分)
(1)挤压塑料管的下端,使液体与固体接触O2或CO2
(2)没等有连续气泡冒出就开始收集;
或收集前集气瓶中的水没有装满。
(3)a
34.(3分)
(1)CaCO3+2HCl═CaCl2+H2O+CO2↑
(2)丙(3)盐酸的浓度
35.(4分)
(1)2H2O通电2H2↑+O2↑
(2)证明二氧化碳能与水反应
(3)①4P+5O2点燃2P2O5②先下降后上升
36.(3分)
(1)50
(2)4.4(3)CO2+2NaOH=Na2CO3+H2O
【基本实验·丰台一模】
32.(5分)根据下列仪器回答问题。
ABCD
(1)仪器A的名称是。
(2)实验室用高锰酸钾制取氧气的化学方程式为,若选择导管D,收集氧气的方法为。
(填“排水法”或“向上排空气法”)
(3)实验室制取二氧化碳的化学方程式为,若发生装置选择了B、C,则胶塞应选择(填“单孔”或“双孔”)。
33.(3分)根据下图所示实验,回答问题。
ABC
(1)实验A可以证明水由组成。
(2)实验B中发生反应的化学方程式为。
(3)实验C可以得出的结论是。
34.(2分)某化学课外小组通过如下实验探究铁生锈的条件。
(1)通过对比实验A和B可以得出的结论是。
(2)得出“铁生锈需要与水接触”这一结论所依据的实验现象是。
35.(2分)某小组同学想要养海鱼,查资料得知浓度为3%的氯化钠溶液较为合适,因此想要配制400克此溶液。
(1)需要氯化钠的质量是克。
(2)称量氯化钠固体时,天平指针向右偏离,如图所示,接下来应该进行的操作是。
32.
(1)试管
(2)2KMnO4====K2MnO4+MnO2+O2↑排水法
点燃
(3)CaCO3+2HCl===CaCl2+CO2↑+H2O双孔
33.
(1)氢元素和氧元素
(2)3Fe+2O2====Fe3O4
(3)铁比铜活泼
34.
(1)铁生锈需要与氧气接触
(2)B中固体表面产生红棕色物质,C中无明显变化
35.
(1)12
(2)向左盘加氯化钠固体
【基本实验·石景山一模】
35.(4分)根据下图回答问题。
ABCDE
(1)实验室用高锰酸钾制取氧气时,选用的收集装置是(填序号,下同)。
反应的化学方程式为。
(2)实验室用大理石和稀盐酸制取二氧化碳时,选用的发生装置是。
如图E所示,将二氧化碳倒入烧杯中,观察到燃烧的蜡烛自下而上依次熄灭,说明二氧化碳具有的性质是。
36.(2分)研究物质的组成。
红磷
图1图2
(1)图1实验中,根据,证明水由氢、氧两种元素组成。
(2)用如图2所示的装置可以粗略的测定空气的组成,其结论是。
碳酸钠粉末
37.(3分)实验小组同学做了如下实验,验证质量守恒定律。
盐酸
红热玻璃管
(1)A实验中,红磷燃烧的化学方程式为_______。
(2)以上2个实验能验证质量守恒定律的是_______(填序号),另一个实验不能验证的原因是_______。
38.(2分)研究燃烧的条件。
(1)铜片上的白磷发生燃烧,说明铜具有的性质是_______。
(2)通过对比________,可以说明可燃物燃烧需要氧气。
39.(3分)为探究铁、铜、银三种金属的活动性顺序,设计了A、B两个方案。
请从两个方案中任选1个作答,若两个均作答,按方案A计分。
方案A
方案B
(1)实验中发生反应的化学方程式为______。
(2)实验中观察到的现象是______。
(3)该方案______(填“能”或“不能”)验证三种金属的活动性。
35.(4分)
(1)C2KMnO4△K2MnO4+MnO2+O2↑
(2)B不可燃也不支持燃烧,且密度比空气大
36.(2分)
(1)水通电分解只生成氢气和氧气
(2)空气中氧气的体积分数约为1/5
37.(3分)
(1)4P+5O2点燃2P2O5
(2)A反应后称量的不是所有生成物的总质量
38.(2分)
(1)导热性
(2)图1水中白磷不燃烧和铜片上的白磷燃烧
或图2水中白磷通氧气前不燃烧、通氧气后燃烧
39.(3分)
39-A:
(1)Fe+CuSO4=FeSO4+Cu
(2)
中无明显变化,
中铁片表面覆盖一层红色物质,溶液由蓝色变成浅绿色
(3)能
39-B:
(1)Fe+2HCl=FeCl2+H2↑
中均无明显变化,
中有气泡冒出,溶液由无色变成浅绿色(3)不能
【基本实验·房山一模】
34.(4分)实验室制取气体所需装置如下图所示。
(1)用大理石和稀盐酸制取二氧化碳时,所选用的发生装置是_________,其反应的化
学方程式为_________。
(2)用高锰酸钾制取氧气时,所选用的收集装置是C或_________。
将带火星的木条接
近集气瓶口,看到木条_________,证明氧气已收集满。
35.(3分)根据下列实验示意图回答相关问题。
(1)实验A中,观察到的现象是_________,发生反应的化学方程式为_________。
(2)实验B的目的是_________。
36.(2分)去除粗盐中泥沙的主要操作步骤如下图所示。
(1)实验的正确操作顺序是_________(填序号)。
(2)C中玻璃棒的作用是_________。
37.(3分)现用溶质质量分数为36.5%的浓盐酸配制100g溶质质量分数为7.3%的稀盐酸。
(1)配制的稀盐酸中溶质的质量为_________g。
(2)用量筒量取所需浓盐酸与水的体积时,视线要与量筒内液体凹液面的_________保
持水平,再读出液体的体积。
(3)将两种液体都倒入_________(填仪器名称)中,用玻璃棒搅拌,使溶液混合均匀。
(4)将配制好的溶液倒入试剂瓶中,盖好瓶塞并贴上标签,备用。
34.
(1)BCaCO3+2HCl===CaCl2+CO2↑+H2O
(2)D复燃
35.
(1)铁丝剧烈燃烧、火星四射、放热、生成黑色固体3Fe+2O2====Fe3O4
(2)探究分子不断运动(或验证浓盐酸具有挥发性或验证浓盐酸显酸性等)
36.
(1)ACB
(2)引流37.
(1)7.3
(2)最低处(3)烧杯
【基本实验·燕山一模】
31.(2分)实验与案例分析:
案例一案例二
(1)案例一探究人体呼出气体中二氧化碳含量比空气中的高,实验条件除了要控制两个盛装气体样品的集气瓶大小规格相同外,还要控制相同。
(2)案例二用玻璃杯迅速扣住燃烧的蜡烛,并使杯口始终浸没在水中。
描述此实验实验现象:
32.(3分)化学是以实验为基础的科学,根据下列实验回答下列问题:
(1)该实验的实验目的是__________________________,
(2)当恰好完全反应时锥形瓶中的现象是:
_____________________________,
(3)图中所示称量的质量是_______g。
32.
(1)滴入澄清石灰水的量
(2观察到蜡烛熄灭,水进入玻璃杯,最终杯中液面高于碗中液面
33.
(1)验证质量守恒定律(探究酸和碱发生反应,验证盐酸和氢氧化钠能否发生反应)
(2)溶液有红色变为无色(3)103.2g
【基本实验·顺义一模】
32.(4分)请从32-A或32-B两题中任选1个作答,若两题均作答,只一组计分。
32-A
32-B
该装置可用于实验室制取氧气。
(1)仪器a的名称是__________。
(2)反应的化学方程式为______。
(3)氧气可用排水法,还可以用的__________方法收集。
(4)当用排水法收集满气体后,应先将导气管移出水槽,再熄灭酒精灯,原因是______。
该装置可用于实验室制取二氧化碳并探究二氧化碳的性质
(2)制取CO2反应的化学方程式为___________。
(3)收集二氧化碳的方法是__________。
(4)将二氧化碳通入澄清石灰水中,观察到的现象是__________。
35.(4分)实验室有一瓶未知浓度的氯化钠溶液,小丽要测定其溶质的质量分数。
实验步骤:
(1)取样:
小丽测得该NaCl溶液的密度为1.2g/cm3,决定量取出50克氯化钠溶液作为样品量取时用到的仪器有________。
(2)获取溶质:
从氯化钠溶液中得到氯化钠的方法是__________。
(2)称量食盐:
小丽加了一个砝码,待天平静止时,出现如图所示的情况,小丽接下来的操作是:
________。
读数,得到氯化钠的质量。
(3)小丽发现有少量氯化钠粘在玻璃棒等器皿上,这对测定结果的影响是________(写“偏大”或“偏小”)。
36.(4分)对比是科学研究中常用的方法,下图所示的实验均用到对比的方法。
(1)甲用于探究分子的运动,观察到的现象是__________。
对比A和B烧杯的现象,你得出的结论是__________。
(2)乙实验中应用对比得出的结论是__________。
(3)丙实验用于探究物质的溶解,实验目的是__________。
32.(4分)A
(1)酒精灯
(2)2KMnO4
K2MnO4+MnO2+O2↑(3)向上排空气
(4)防止水倒吸炸裂试管
B
(1)试管
(2)CaCO3+2HCl=CaCl2+CO2↑+H2O(3)向上排空气(4)澄清石灰水变浑浊
33.(4分)
(1)量筒、胶头滴管
(2)蒸发溶剂(3)将10g砝码换成5g砝码(4)偏小
34.(4分)
(1)B中变红,A、C无明显现象;
不同物质的分子运动速率不同
(2)CO2的密度比空气大(3)探究物质的溶解能力与溶剂的种类是否有关
【基本实验·通州一模】
33.(2分)根据下图回答问题。
(1)要将橡胶塞塞进试管口时,下面哪个操作是正确的?
(填序号)
桌面
AB
(2)用集气瓶收集满气体后,要用玻璃片盖住瓶口,玻璃片一面光滑,一面粗糙,我们通常用的一面接触集气瓶口,以减少气体溢出。
35.(3分)化学小组同学用右图所示装置探究铁的金属活动性。
(1)若要证明Fe在金属活动性顺序中位于氢前,X可用。
(2)若X为少量硫酸铜溶液,该反应的化学方程式为;
待充分反应后,取出未反应完的铁片,再将金属R放入到反应后溶液中,观察到R表面有黑色固体析出。
根据上述实验现象,得出Fe、Cu、R的金属活动性顺序:
>>
36.(2分)可以利用右图所示装置探究燃烧的条件。
在两支三角架上分别放置两个铁丝网,在上面放置三团医用脱脂棉A、B、C。
其中棉花B中放置一支温度计,棉花C上罩一只小烧杯,并在A、C处铁丝网下各放置酒精灯。
同时点燃酒精灯,一段时间后棉花A燃烧,B没变化,C底部变黑但不燃烧。
(1)能说明燃烧需要温度达到可燃物的着火点的实验现象为。
(2)当把小烧杯拿下后,发现C能燃烧,说明燃烧所需要的一个条件是。
33.
(1)A
(2)粗糙一面
34.
(1)溶解
(2)玻璃棒(3)0.9g
35.
(1)稀盐酸/稀硫酸
(2)Fe+CuSO4=Cu+FeSO4(3)R>
Fe>
Cu
36.
(1)A处棉花燃烧,B处棉花没变化
(2)与氧气充分接触
【基本实验·延庆一模】
34.(4分)实验小组同学在实验室用高锰酸钾制取氧气,并验证氧气的化学性质。
(1)图A是小瑛同学进行“高锰酸钾制取氧气”的发生装置。
该装置有一处明显错误,
为使装置正确,她应调节的旋钮是_________(填序号),调整正确后,A中发生反应的化学方程式为_________________________________________。
(2)图B是木炭在氧气中燃烧,观察到的现象是______________________,为进一步证明木炭与氧气发生了化学反应,应继续进行的实验操作是_________________。
35.(3分)某化学兴趣小组的同学用下列操作进行粗盐(含有难溶性杂质)提纯实验。
请回答下列问题:
(1)粗盐提纯实验的步骤是______________________(填序号,下同)。
(2)操作④中用玻璃棒的作用是
__________________________
(3)用上述所得的精盐配制50g16%的氯化钠溶液经检测,溶质质量分数偏小,其原因可能有
______________________。
①氯化钠固体仍然不纯
②称量时砝码端忘垫质量相同的纸片
③量取水时,仰视读数
④装瓶时,有少量溶液洒出
36.(4分)在科学实践活动中,同学们做了两个有关干冰的有趣实验,如下图所示:
(1)实验一玻璃杯C中的现象是_________________________________________,发生反应的化学方程式为____________________________________________。
(2)实验二中蜡烛熄灭,说明二氧化碳所具有的性质的是____________________;
上层脱脂棉燃烧,说明二氧化碳与过氧化钠(Na2O2)发生了放热反应,并产生了一种气体,该气体是______。
34.
附:
35题分析方法:
眼睛与刻度相连,然后延长到页面凹液面,观察到凹液面所对应的刻度,看比42大还是小,即可。
(4分)
(1)ab2KMnO4K2MnO4+MnO2+O2↑
(2)剧烈燃烧,发出白光向反应后的集气瓶中注入澄清石灰水
35.(3分)
(1)
(2)引流(3)
36.(4分)
(1)红色逐渐消失,溶液变浑浊后又变澄清Ca(OH)2+CO2===CaCO3↓+H2O
(2)二氧化碳不燃烧,也不支持燃烧。
氧气