人教版学年九年级下学期中考一模化学试题A卷Word文档下载推荐.docx
《人教版学年九年级下学期中考一模化学试题A卷Word文档下载推荐.docx》由会员分享,可在线阅读,更多相关《人教版学年九年级下学期中考一模化学试题A卷Word文档下载推荐.docx(14页珍藏版)》请在冰豆网上搜索。
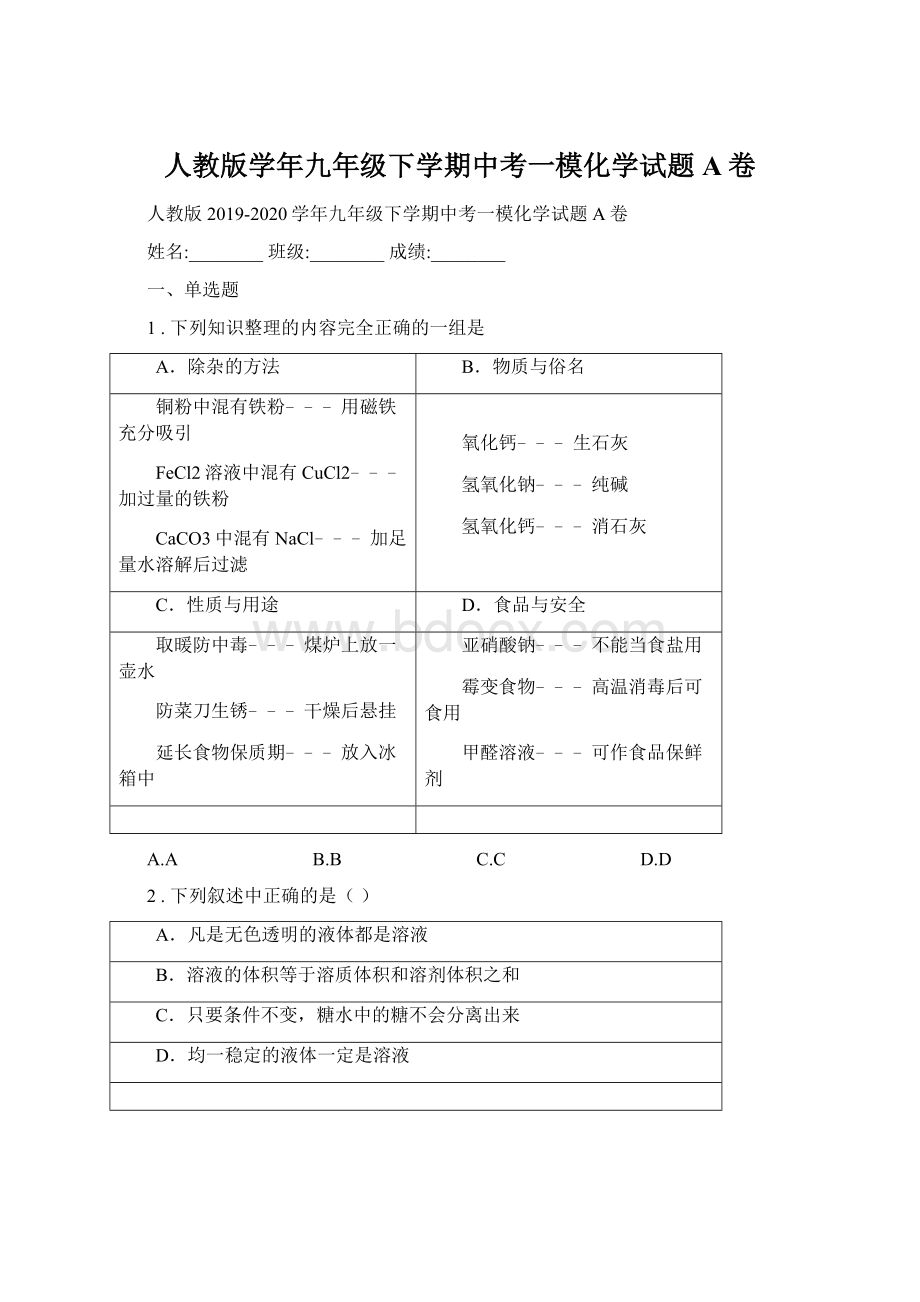
C.C
D.D
2.下列叙述中正确的是()
A.凡是无色透明的液体都是溶液
B.溶液的体积等于溶质体积和溶剂体积之和
C.只要条件不变,糖水中的糖不会分离出来
D.均一稳定的液体一定是溶液
3.2018年10月24日,港珠澳大桥正式通车。
实现了香港、珠海、澳门的1小时生活圈,整个工程从提出设想到正式通车,前后经历了35个年头。
下列相关说法不正确的是()
A.此项工程对提升珠江三角洲地区的综合竞争力,保持港澳的长期繁荣稳定,打造港澳大湾区具有重耍战略意义。
B.路面上铺的沥青是利用石油为原料通过分馏得到的产品
C.大桥上五彩缤纷的霓虹灯主要是利用稀有气体通电时会发出不同颜色的光的原理制成的
D.大桥的海底隧道部分由33节钢筋混凝土结构的沉管对接而成,钢筋混凝土属于金属材料
4.在pH=1的溶液中,下列物质能大量共存,且溶液为无色的是()
A.NaOH、NaCl、K2SO4
B.MgSO4、Cu(NO)3、KCl
C.KNO3、ZnCl2、Ca(NO3)2
D.CaCl2、(NH4)2SO4、K2CO3
5.如图是甲、乙两种固体物质的溶解度曲线。
下列说法正确的是
A.t1℃时,向100克水中加入20克甲,充分溶解后所得溶液是饱和溶液
B.甲饱和溶液从t2℃降温至t1℃,溶液的质量不变
C.乙饱和溶液温度降低,有晶体析出,是化学变化
D.当甲中含有少量乙时,可用降低甲饱和溶液温度的方法提纯甲
6.分类、归纳等是化学学习的常用方法。
下列分类、归纳中正确的是()
A.金属材料:
生铁、钛合金
B.复合肥料:
KNO3、CO(NH2)2
C.人体必需微量元素:
Ca、Se
D.有机物:
C2H5OH、H2CO3
7.下列物质在
的溶液中能够大量共存,且形成无色溶液的是()
A.
,
B.
C.
D.
8.化学是你,化学是我,化学深入我们生活,下列说法正确的是()
A.腌制的泡菜虽然富含亚硝酸盐,但多吃无妨
B.焊接金属时用氧气做保护气
C.pH值大于7的溶液不一定是碱溶液
D.铵态氮肥与熟石灰混合使用可以明显提高肥效
9.根据下列实验方案进行实验,不能达到相应实验目的的是
测定空气中氧气的含量
检验氧气是否收集满
验证物质燃烧需要氧气
探究影响物质溶解性的因素
10.图是恒温下模拟海水晒盐过程的示意图,下列说法不正确的是()
A.四杯溶液中溶质质量分数最小的是甲
B.四杯溶液中丙和丁的溶质质量分数相等
C.四杯溶液中溶质质量分数丙一定大于乙
D.四杯溶液中溶质海盐的溶解度相同
11.将化学知识应用于生活,能提高我们的生活质量,下列做法中正确的是()
A.用甲醛浸泡水产品,光鲜!
B.清理沼气池时,用火把照明,亮堂!
C.随意丢弃废旧电池,方便!
D.少开私家车,多乘公交车,“低碳”!
12.现有一定质量氧化铁、氧化铜和氧化铝的混合物,加入7.3%的稀盐酸100g,恰好完全反应,则反应后溶液中溶剂质量为()
A.101.8g
B.94.5g
C.92.7g
D.95.5g
13.如图是A、B、C三种物质的溶解度曲线图,下列说法一定正确的是
A.将三种物质的饱和溶液分别由60℃降温到20℃,A溶液中析出的晶体质量最大
B.C可能是氢氧化钙溶液
C.采用蒸发结晶的方法除去A溶液中混有的少量B
D.60℃时,等质量的A、C饱和溶液中,水的质量是A<C
14.化学兴趣小组的同学利用废铜制取硫酸铜,设计了如下两个方案:
方案一:
Cu
CuO
CuSO4
方案二:
CuSO4 [Cu+2H2SO4(浓)
CuSO4+SO2↑+2H2O]
比较上述两个方案,你认为方案一的优点是()
①节约能源 ②不产生污染大气的二氧化硫 ③提高硫酸的利用率 ④提高铜的利用率
A.②③
B.①②③
C.①③④
D.①②③④
15.下列有关溶液的叙述错误的是()
A.溶液都是无色透明的
B.雪碧是均一、稳定的混合物
C.固体NaOH溶于水时,溶液温度升高
D.一定条件下,饱和溶液和不饱和溶液可以相互转化
16.合理施肥是农业生产中的重要措施。
下列化肥属于复合肥料的是
A.尿素[CO(NH2)2]
B.硫酸钾(K2SO4)
C.硝酸钾(KNO3)
D.磷酸钙[Ca3(PO4)2]
17.室温时,有两瓶硝酸钾溶液,一瓶为饱和溶液(溶质的质量分数为40%),另一瓶为10%的溶液。
下列实验操作中,无法区分这两种溶液的是()
A.室温时,蒸发少量水
B.加入少量硝酸钾晶体
C.略降低温度
D.加一定量的水
18.下列有关物质的性质、用途等说法正确的是()
①干冰用于人工降雨
②石墨可作电极
③氧气可用作燃料
④稀盐酸可以用来除铁锈
⑤活性炭作口罩滤芯
⑥生活中可用氢氧化钠来除去炉具上的油污,也可治疗胃酸过多
A.①②③④⑤⑥
B.①②③④
C.①②④⑤
D.②④⑥
19.下列关于溶液的说法正确的是
A.均一、稳定的液体一定是溶液
B.碘酒中的溶质是酒精
C.用汽油洗去衣服上的油污是乳化现象
D.相同温度,溶质相同的饱和溶液溶质的质量分数一定比不饱和溶液大
20.下图是a、b两种固体物质的溶解度曲线,从图中获得的信息不正确的是
A.a、b两种固体物质的溶解度均随温度升高而增大
B.t℃时,a、b的饱和溶液蒸发等质量的水,析出a、b的质量相等
C.升高温度,均可使a、b的饱和溶液变为不饱和溶液
D.将等质量的a、b分别加入100g水中,充分溶解,所得溶液溶质质量分数相等
二、填空题
21.现欲配制70g溶质质量分数为20%的氢氧化钠溶液,该实验的部分操作如下图所示:
(1)需要称取氢氧化钠的质量是14g(使用了砝码和游码),若称量时出现了右盘高的现象(如图A),接下来的操作应该是___________;
A.向右移动游码
B.左盘中增加氢氧化钠
C.左盘中减少氢氧化钠
(2)若按照图B的方法量取水,会使配制的溶液质量分数______(选填“偏大”或“偏小”);
(3)D中所贴标签有一项内容不正确,请加以改正___________;
(4)若要将已配好的70g溶质质量分数为20%的氢氧化钠溶液,稀释成10%的氢氧化钠溶液,需要加水__________g。
22.通过学习化学,同学们明白了很多道理,请从微观(分子或原子)角度来解决下列化学问题。
⑴一氧化碳和二氧化碳化学性质不同的原因是
⑵混合物和纯净物的不同之处是
⑶打气筒能将空气压入足球内
三、简答题
23.AgNO3、Cu(NO3)2、Mg(NO3)2的混合溶液中加入一定量的锌粉并充分反应,过滤得滤渣和滤液。
(1)往滤液中加盐酸,若无明显现象,请分析滤液中一定含有溶质的成分_____。
(2)猜想:
滤液中溶质为AgNO3、Zn(NO3)2、Mg(NO3)2,请分析该猜想不合理的原因_____。
24.化学与生活息息相关,请用化学知识解释下列问题:
(1)“铁强化酱油”可补充人体所需的铁元素,铁元素摄入不足可能会引起哪种疾病?
______________
(2)塑料的用途广泛,请写出塑料的一条优点。
(3)喝了汽水后常常会打嗝,这是为什么?
四、科学探究题
25.化学小组应用如图所示的装置进行相关实验(夹持仪器略去,K1、K2、K3均关闭,装置内所示药品的量可认为是实验中某一状态下的量),已知装置内的药品,甲:
稀盐酸;
乙中为无色气体;
分液漏斗中为红色的溶液;
丙:
石灰水,依据相关信息回答问题:
(碳酸钠溶液呈碱性)
(1)打开K3,将丁向外拉,丙中长导管口有气泡冒出,且出现白色浑浊现象,则乙中的无色气体是___,丙中出现白色浑浊的原因是____。
(用化学方程式回答)
(2)关闭K3,打开K2(分液漏斗上端的玻璃塞处于打开状态),当分液漏斗内的红色溶液全部进入到乙中时,关闭K2,振荡乙一会儿后,打开K1,可观察到甲中的现象是____,乙中有气体产生,且溶液由红色变为无色,产生气体的化学方程式是____,从物质性质的角度解释溶液由红色变为无色的原因是___。
26.小明在做铁与硫酸溶液反应的实验时,发现生成的气体有刺激性气味,于是进行了探究。
(提出问题)铁与硫酸溶液反应生成的气体为什么有刺激性气味?
(查阅资料)
(1)6H2SO4(浓)+2Fe
Fe2(SO4)3+6H2O+3SO2↑
(2)SO2可使品红溶液的红色褪去。
(进行猜想)铁与不同浓度的硫酸溶液反应,生成的气体产物中可能有二氧化硫。
(实验探究)小明用图甲所示的装置进行实验,并将E中收集到的气体进行如图乙所示的爆鸣实验。
请帮助小明完成下表:
A中硫
酸浓度
实验现象
A中生成气体成分
B中品
红溶液
D中品
爆鸣实验
实验一
98%
__________
不褪色
无爆鸣声
只有SO2
实验二
45%
稍有褪色
有爆鸣声
实验三
25%
_________
只有H2
(实验结论)铁与不同浓度的硫酸溶液反应,生成的气体产物可能不同,当硫酸浓度达到足够大时,生成的气体产物中有二氧化硫。
(交流反思)
(1)写出实验三中铁与硫酸反应的化学方程式:
_________________。
写出实验二中发生爆鸣反应的化学方程式:
____________________。
(2)实验一中C装置的作用是_______________________________。
(拓展延伸)小明又将A装置进行了如右图所示的改过。
试分析增加的导管伸入液面以下的原因是____________________________________________。
该导管所起的作用是__________________________________。
五、计算题
27.黄铜是铜、锌合金,它用于制造机器、电器零件等。
为测定某黄铜样品中铜的质量分数,取10g该黄铜样品加入到稀硫酸中,恰好完全反应,产生氢气0.1g。
试求:
(1)该黄铜样品中锌的质量__________。
(2)该黄铜样品中铜的质量分数__________。
28.小明将30%的H2O2溶液加水稀释,并用其制取O2。
(1)稀释过程中要用到的实验仪器有________(填序号)。
a.量筒b.烧杯c.托盘天平d.玻璃棒e.漏斗f.胶头滴管
(2)用稀释后的H2O2溶液按图所示实验,分析并计算稀释后的溶液中溶质的质量分数________。
六、科普阅读题
29.食醋中一般含有3%-5%的醋酸,醋酸的化学名称叫乙酸(CH3COOH),是无色、有刺激性气味的液体,能溶于水。
食醋可以除去水壶内的水垢,水垢的主要成分是碳酸钙。
除水垢时,可在水壶中加入水,倒人适量醋,浸泡一段时间,不溶于水的碳酸钙会转变成可溶于水的醋酸钙而被除掉,化学方程式为CaCO3+2CH3COOH=(CH3COO)2Ca+H2O+CO2↑。
在熬制骨头汤时,常常在汤中加入少量食醋,因为骨头中含有不溶于水的磷酸钙,当磷酸钙与醋酸作用时生成可溶于水的磷酸二氢钙,能够增加汤内的含钙量,促进人体对钙、磷的吸收和利用。
食醋不仅在厨房中大显身手,还是一种杀菌剂,冬天在屋子里熬醋可以杀灭细菌,对抗感冒有很大作用。
饮酒过量的人可以用食醋来解酒,因为乙酸能跟乙醇发生酯化反应生成乙酸乙酯(CH3COOC2H5)和水,从而达到解酒的目的。
家用铝制品不能用来盛放食醋,以免铝被腐蚀。
根据文章内容,回答下列问题:
(1)乙酸属于_________(填“有机物”或“无机物”)。
(2)食醋能用来解酒的原因是_________________________。
(3)用铁锅炒菜时,放一点食醋能补铁,用化学方程式解释原因___________。
(4)用食醋除去水壶内的水垢,该反应属于基本反应类型中的_________。
七、综合题
30.钠及其化合物是中学化学学习和研究的重要内容.
(1)如图1是钠的原子结构示意图,钠在反应中失电子后形成离子的符号是_____.
(2)钠在氯气中燃烧生成氯化钠,化学方程式为_____.
(3)配制一瓶符合如图2所示的氯化钠溶液,需氯化钠_____g;
小明同学配制的氯化钠溶液质量分数偏小了,请写出他操作中可能出现的错误(提示:
1g以下用游码,至少答出两点)_____.
(4)如何测定一瓶苏打水的酸碱度(写出实验操作步骤)_____.
(5)小苏打受热分解生成碳酸钠、二氧化碳和水,化学方程式为_____.
(6)钛和钛合金性能优良,广泛用于航空、造船和化学工作中.工业上常用钠来制取钛,在高温时,钠与四氯化钛(TiCl4)反应生成氯化钠和钛.若用该方法制取2.4kg钛,理论上需要钠的质量是多少_____?
参考答案
1、
2、
3、
4、
5、
6、
7、
8、
9、
10、
11、
12、
13、
14、
15、
16、
17、
18、
19、
20、