高三化学教案离子反应3 最新文档格式.docx
《高三化学教案离子反应3 最新文档格式.docx》由会员分享,可在线阅读,更多相关《高三化学教案离子反应3 最新文档格式.docx(16页珍藏版)》请在冰豆网上搜索。
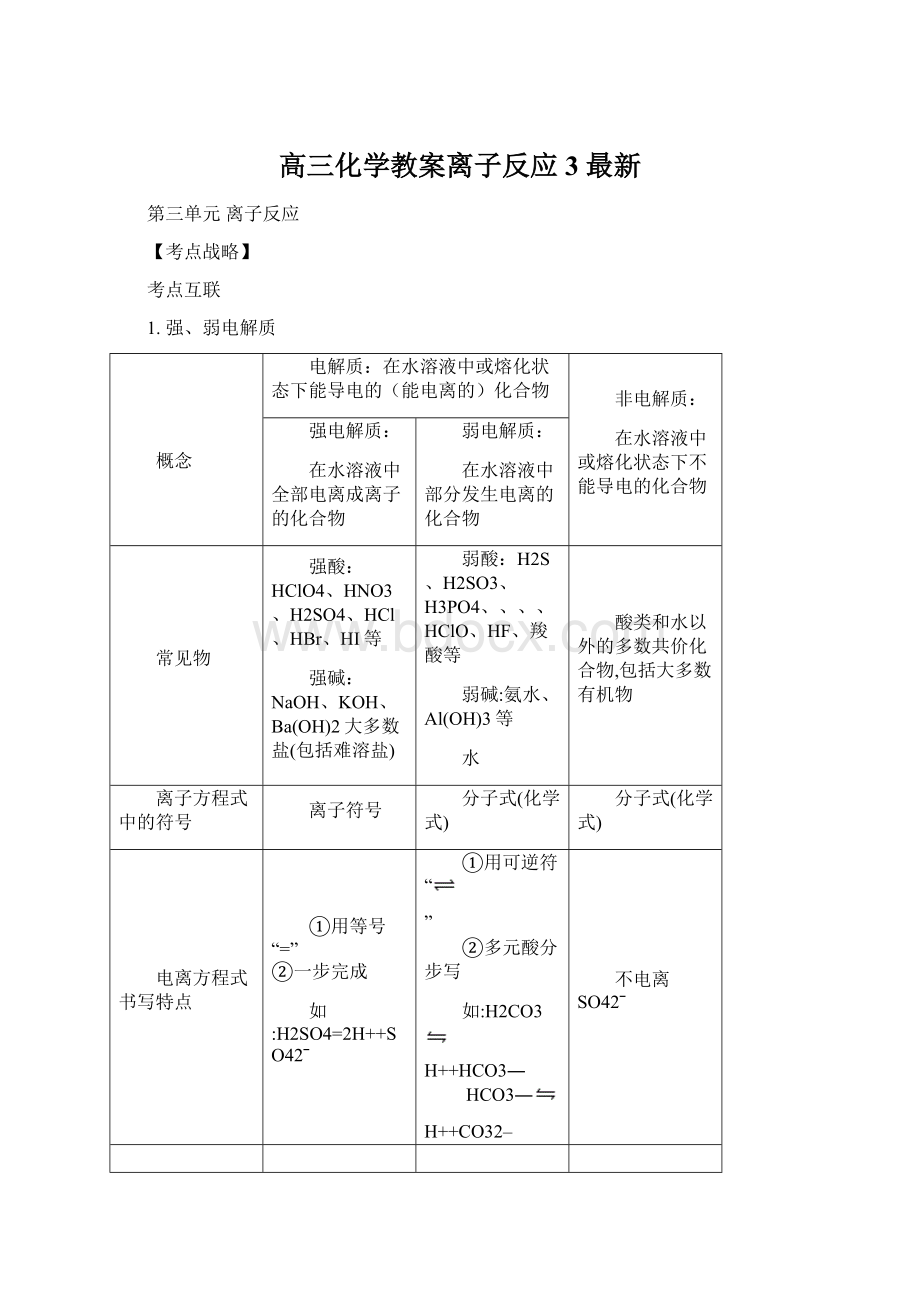
弱酸:
H2S、H2SO3、H3PO4、、、、HClO、HF、羧酸等
弱碱:
氨水、Al(OH)3等
水
酸类和水以外的多数共价化合物,包括大多数有机物
离子方程式中的符号
离子符号
分子式(化学式)
电离方程式书写特点
①用等号“=”
②一步完成
如:
H2SO4=2H++SO42ˉ
①用可逆符“
”
②多元酸分步写
H2CO3
H++HCO3―
HCO3―
H++CO32–
不电离SO42ˉ
注意:
电解质和非电解质都是化合物,不包括单质,也不是指溶液。
2.离子反应、离子方程式
概念有离子参加的反应叫离子反应。
离子反应
本质溶液中某些离子能相互作用,使这些离子的浓度减小。
(1)生成难溶性物质;
(2)生成难电离的物质(弱电解质);
发生条件(3)生成挥发性物质(气体);
(4)能发生氧化还原反应(氧化剂的氧化性强于氧化产物,或还原剂的还原性强于还原产物;
(5)能发生其它反应,如Fe3+与SCN―结合成难电离的FeSCN2+离子。
离子方程式
概念用实际参加反应的离子的符号表示离子反应的式子。
书写方法
写,写出正确的化学方程式;
拆,把易溶强电解质的化学式改写成离子符号;
删,把没有参加反应的离子从方程式两边删去;
查,检查方程式两边原子及电荷数是否相等.。
意义不仅表示一定物质间的特定反应,还能表示同一类反应。
考点解说
1.溶液导电性。
溶液导电是离子导电。
常见电解质在水溶液中都有导电性,但熔化态时则不尽相同,酸类物质在熔化态时一般认为不存在离子,不导电;
而碱与盐可导电。
以此可区分离子化合物和共价化合物。
溶液的导电性与离子浓度有密切关系,离子浓度变大时,导电性一般增强,但不等于电解质强其溶液导电性就强,因为强电解质溶液在浓度很小时离子浓度也会很小,从而导电性也会很弱。
2.离子方程式的书写。
离子方程式的书写难点是确定物质的书写形式。
其要领是“实事求是”,即按物质的主要存在形式写,一般规则是:
易溶的强电解质(强酸、强碱、易溶盐)通常应写成离子形式,难溶,难电离和气态物质都写成化学式。
有几种具体情况说明如下:
(1)非离子反应,如气体、固体间的反应,即使是易溶的强电解质也不能写成离子方程式,如HCl和NH3两种气体反应。
但熔融状态的电解质反应可写成离子方程式,如电解熔融的氧化铝制取金属铝。
(2)有的反应,虽然反应物都不能写成离子的形式,但实质仍是离子反应,如果生成物以离子形式存在,仍应写成离子符号。
如金属钠与水反应。
(3)浓硫酸与固体(如NaCl、Cu)反应时,虽有离子存在,但按主要存在形式应写分子式。
(4)弱酸(包括中强酸)的酸式盐“拆”写时,其阴离子应写成酸式根的形式,如HCO3ˉ、HPO42―,但硫酸的酸式盐如NaHSO4应拆写成Na++H++SO42ˉ。
(5)微溶物处理:
微溶反应物,以溶液形式存在时(如澄清石灰水)写成离子符号,以悬浊液形式存在时则写成化学式;
微溶生成物,通常以化学式表示。
3.离子方程式的正误判断。
对已给出的离子方程式作正误判断是最常见的题型之一。
依据一定的顺序由简及繁的检查,有利于快速准确地解题.检查的重点有:
(1)查有没有配平(原子平,电荷平,得失电子平.重点是电荷是否配平);
(2)查物质的书写形式是否符合规定;
(3)查与客观事实是否相符,如能否反应,是否离子反应,生成物是不是符合事实等。
某些随加液顺序不同而反应不同或与反应物用量有关的反应要特别注意生成物的合理性。
另外还有如稀碱溶液与铵盐溶液反应,常温下生成物不应写成“NH3↑”,而应写成NH3·
H2O;
浓硫酸与固体(如食盐或铜)反应时,不写成离子符号;
盐类水解一般应该用可逆符号而不应用等号。
有的错误仅据表面形式检查不易查出,如硫酸与氢氧化钡溶液反应错写成:
H++SO42ˉ+Ba2++OHˉ==H2O+BaSO4↓,若自己根据书写步骤写出正确的离子方程式,便可发现应该写成:
2H++SO42ˉ+Ba2++2OHˉ==H2O+BaSO4↓。
4.离子共存问题。
如果两种或多种离子在水溶液里符合离子反应发生的条件,则发生离子反应而不能(大量)共存,反之则能共存.离子不能共存的常见实例有:
不能大量共存的原因
常见实例
(1)结合成难溶物或微溶物
如SO42ˉ不能与Ba2+、Ca2+、Ag+共存
OH-、CO32-不能与Mg2+、Fe2+、Fe3+、Al3+、Zn2+、Cu2+等共存
Ag+不能与Cl―、Br―、I―共存(详见课本溶解性表)
(2)生成挥发性物质
如CO32–、SO32―、S2–、HCO3―、HSO3―、HS―等与H+不能共存
(3)结合成难电离的物质(水,弱酸和弱碱)
H+与OH-结合成水
H+与PO43ˉ、CH3COO_、F―、ClO―、AlO2―、C6H5-O―结合成弱酸
OH-与酸式根如HCO3―、HSO3―、H2PO4―生成水
OH-与NH4+结合成NH3·
H2O
(4)发生氧化还原反应
MnO4―、ClO―、NO3―(有H+时)与S2―、I―、Fe2+、SO32―等不能共存。
(5)能结合成络合物
如Fe3+与SCN―不能共存
(6)发生双水解反应
Fe3+、Al3+与AlO2―、S2–、CO32ˉ、C6H5-O―不能共存
【命题战略】
高考经典聚焦
一、选择题(每小题有1-2个正确选项)
1.下列物质的水溶液能导电,但属于非电解质的是(2000•上海)
A.CH3CH2COOHB.Cl2C.NH4HCO3D.SO2
2.下列离子方程式中正确的是(2003•上海)
A.过量的NaHSO4与Ba(OH)2溶液反应:
Ba2++2OH-+2H++SO42-→BaSO4↓+2H2O
B.NH4HCO3溶液与过量NaOH溶液反应:
NH4++OH-→NH3↑+H2O
C.苯酚钠溶液中通入少量CO2:
-O-+CO2+H2O→
-OH+HCO3-
D.FeBr2溶液中通入过量Cl2:
2Fe2++2Br-+2Cl2→2Fe3++Br2+4Cl-
3.下列反应的离子方程式书写正确的是(2000•全国)
A.向饱和碳酸氢钙溶液中加入饱和氢氧化钙溶液Ca2++HCO3-+OH-==CaCO3↓+H2O
B.金属铝溶于氢氧化钠溶液Al+2OH-==AlO2-+H2↑
C.用氢氧化钠溶液吸收二氧化碳2OH-+CO2==CO32-+H2O
D.Fe2(SO4)3的酸性溶液中通入足量硫化氢Fe3++H2S==Fe2++S↓+2H+
4.下列离子方程式书写正确的是(2002•上海)
A.FeCl2溶液中通入Cl2:
Fe2++Cl2==Fe3++2Cl-
B.澄清石灰水与少量小苏打溶液混合:
Ca2++OH-+HCO3-==CaCO3↓+H2O
C.FeS固体放入稀硝酸溶液中:
FeS+2H+==Fe2++H2S↑
D.AlCl3溶液中加入过量氨水:
Al3++4OH-==AlO2-+2H2O
5.下列各组离子在溶液中能大量共存的是(2000•上海)
A.Ca2+、HCO3-、Cl-、K+B.Al3+、AlO2-、HCO3-、Na+
C.Fe2+、NH4+、SO42-、S2-D.Fe3+、SCN-、Na+、CO32-
6.下列离子在溶液中因发生氧化还原反应而不能大量共存的是(2001·
上海)
A.H3O+、NO3ˉ、Fe2+、Na+B.Ag+、NO3ˉ、Clˉ、K+、
C.K+、Ba2+、OHˉ、SO42ˉD.Cu2+、NH4+、Brˉ、OHˉ
二、非选择题
7.请指出H+、Na+、K+、Al3+、Clˉ、S2ˉ、AlO2ˉ各种离子中,所有不能两两共存于同一溶液中的离子____________________(1996·
全国)
8.
(1)向NaHSO4溶液中,逐滴加入Ba(OH)2溶液至中性,请写出发生反应的离子方程式:
______________________________
(2)在以上中性溶液中,继续滴加Ba(OH)2溶液请写出此步反应的离子方程式:
______________(1997·
高考命题预测
由历届高考经典回顾可以看出,命题热点有:
(1)溶液导电性;
(2).离子方程式的书写;
(3).离子方程式的正误判断;
(4).离子共存。
这些热点在今年高考中还会有所表现,且难度有可能加大。
离子共存问题的题型历年来多数为选择题,偶尔也有填空题出现。
难度增大的方法主要在增加题干条件,如溶液强酸性、pH=13、无色透明、指示剂显某种颜色、发生氧化还原反应、“由水电离出的c(H+)=1×
10-14mol/L------”等等。
离子方程式考点命题频率最高的题型是正误判断的选择题,其次是书写离子方程式的填空题。
较高难度的题主要表现在与反应物用量有关的方程式。
一、选择题(有1-2个正确选项)
9.加入铝能放出H2的溶液中可能共存的离子组是
A.NH4+、NO3ˉ、CO32ˉ、Na+B.Na+、Ba2+、Mg2+、HCO3ˉ
C.NO3ˉ、Ca2+、Al3+、ClˉD.NO3ˉ、K+、AlO2ˉ、OHˉ
10.下列反应属于氧化还原反应,且离子方程式正确的是
A.金属钾与硫酸铜溶液反应:
2K+Cu2+=Cu+2K+
B.氯气与水反应:
Cl2+H2O=2H++Clˉ+ClOˉ
C.氢氧化钠溶液吸收二氧化硫:
2OHˉ+SO2+H2O=SO32ˉ+2H2O
D.铁粉加入硫酸铁溶液中:
Fe+2Fe3+=3Fe2+
11.下列对溶液导电性的推测不正确的是
A.饱和碘水很稀,导电性很弱,I2易溶于CCl4,所得饱和溶液导电性较强
B.常温下饱和的苯酚溶液导电性较弱,向苯酚的浑浊液中滴加NaOH溶液,导电性增强
C.向氨水中通CO2气体,溶液的导电性增强
D.发生中和反应时,生成盐是强电解质,所以溶液的导电性一定增强
12.醋酸铅(CH3COO)2Pb是一种易溶于水的盐类,实验测得其水溶液的导电性很弱。
实验室常利用湿润的的醋酸铅试纸检验H2S气体,是利用醋酸铅与氢硫酸反应生成深黑色的PbS沉淀。
该反应属于离子互换反应,它的离子方程式书写形式符合规定的是
A.Pb2++S2ˉ=PbS↓B.(CH3COO)2Pb+S2ˉ=PbS↓+2CH3COO_
C.Pb2++H2S=PbS↓+2H+D.(CH3COO)2Pb+H2S=PbS↓+2CH3COOH
二、非选择题
13.有一固体混合物,可能由碳酸钠、硫酸钠、硫酸铜、氯化钙、氯化钠等物质组成。
为鉴别它们,做了如下实验①将固体混合物溶于水,搅拌后,得无色溶液。
②在①所得溶液中滴加氯化钡溶液,有白色沉淀生成。
③过滤,然后在此白色沉淀中加入足量稀硝酸,沉淀完全消失。
(1)由此推断,固体混合物中肯定有__________,肯定没有__________可能会有__________
(2)写出上述过程可能发生反应的离子方程式_______