届嘉惠中学第一次理科综合能力测试Word文档格式.docx
《届嘉惠中学第一次理科综合能力测试Word文档格式.docx》由会员分享,可在线阅读,更多相关《届嘉惠中学第一次理科综合能力测试Word文档格式.docx(16页珍藏版)》请在冰豆网上搜索。
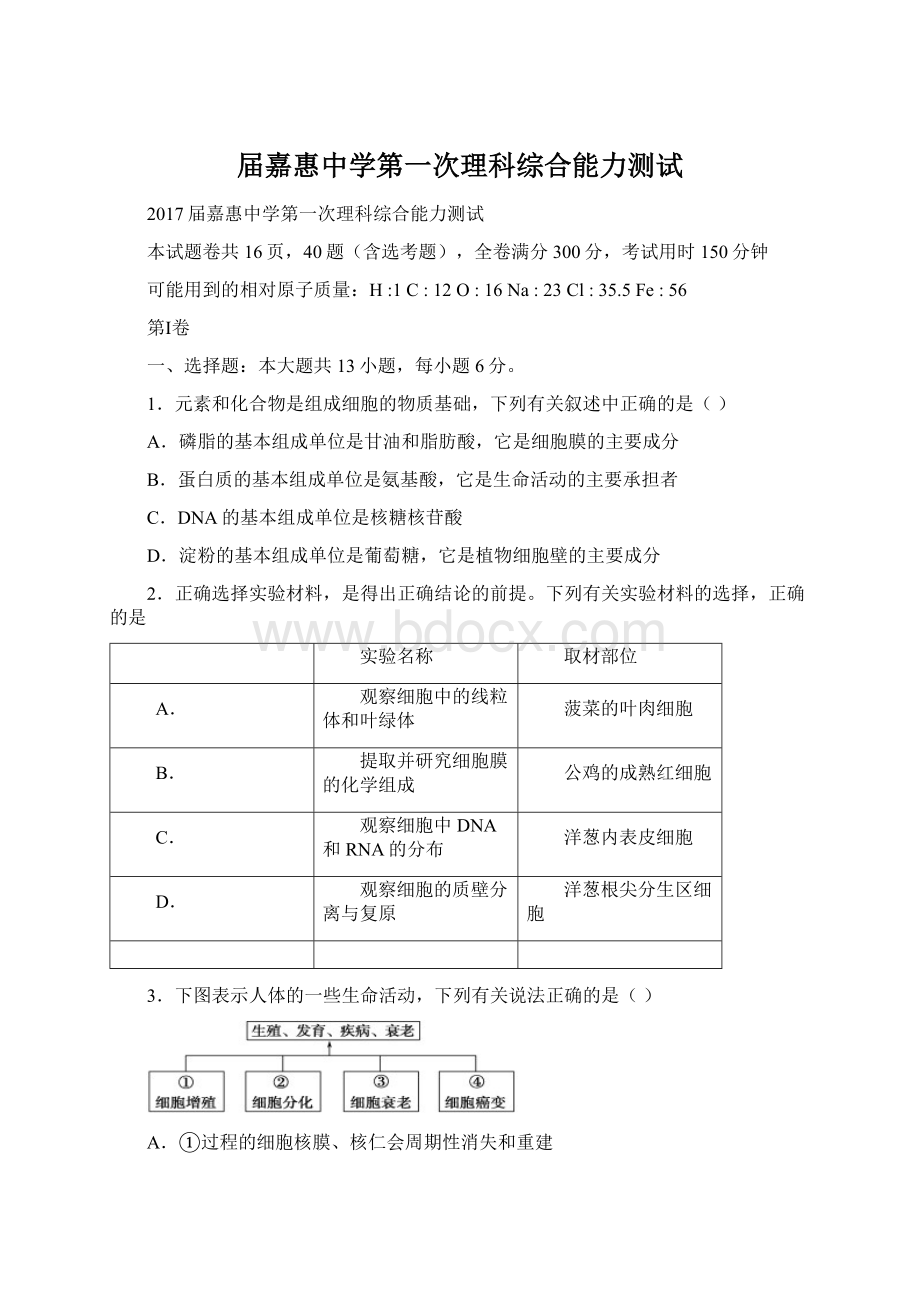
实验名称
取材部位
A.
观察细胞中的线粒体和叶绿体
菠菜的叶肉细胞
B.
提取并研究细胞膜的化学组成
公鸡的成熟红细胞
C.
观察细胞中DNA和RNA的分布
洋葱内表皮细胞
D.
观察细胞的质壁分离与复原
洋葱根尖分生区细胞
3.下图表示人体的一些生命活动,下列有关说法正确的是()
A.①过程的细胞核膜、核仁会周期性消失和重建
B.②过程细胞中的遗传物质发生改变
C.③过程中细胞膜通透性下降,物质运输功能降低
D.④过程中原癌基因和抑癌基因发生突变
4.下列有关生物的遗传信息的叙述,错误的是
A.生物的遗传信息储存在DNA或RNA的核苷酸序列中
B.与翻译相比,遗传信息转录时特有的碱基配对方式是T—A
C.分子水平上遗传信息的传递过程中均可能发生基因突变
D.遗传信息从RNA—蛋白质,实现了基因对生物体性状的控制
5.下列有关遗传物质是核酸的实验证据的叙述,正确的是
A.格里菲思的肺炎双球菌的体内转化实验证明R型细菌中存在转化因子
B.艾弗里的肺炎双球菌体外转化实验运用了物质提纯和鉴定技术、同位素示踪技术和细菌培养技术等
C.赫尔希和蔡斯的噬菌体浸染细菌的实验过程是:
标记噬菌体→噬菌体与细菌混合培养→搅拌、离心→检测放射性
D.库兰特用烟草花叶病毒(TMV)的重建实验证明了DNA是遗传物质
6.枯草杆菌野生型与某一突变型的差异见下表:
下列叙述正确的是
A.S12蛋白结构改变使突变型具有链霉素抗性
B.链霉素通过与核糖体结合抑制其转录功能
C.突变型的产生是由于碱基对的缺失所致
D.链霉素可以诱发枯草杆菌产生相应的抗性突变
7、下列说法正确的是
A.汽油是纯净物,乙醇汽油是混合物
B.饱和(NH4)2SO4溶液和饱和CuSO4溶液都能使蛋白质溶液产生沉淀,且原理相同
C.将铜片在酒精灯上加热变黑后迅速插入乙醇溶液中,铜片恢复红色且质量不变
D.乙烯、植物油和苯都能与氢气发生加成反应,是因为其结构中都含有碳碳双键
8.有关化学用语正确的是
A.Cl-的电子排布式:
1s22s22p63s23p6B.乙醇的结构简式:
C2H6O
C.硫离子的结构示意图:
D.四氯化碳的电子式:
9、设NA代表阿伏加德罗常数的值,下列说法不正确的是
A.标准状况下,22.4LNO和11.2L氧气混合,气体的分子总数约为1.5NA个
B.非标准状况下,1mol某气体体积可能约为22.4L
C.常温常压下,氧气和臭氧的混合物16g中约含有NA个氧原子
D.17gNH3所含共用电子对数为3NA
10、下列方程式表达正确的是
A.硫酸铜水解:
Cu2++2H2O===Cu(OH)2↓+2H+
B.用氢氧化钠溶液除去铝表面的氧化膜:
Al2O3+2OH-=2AlO2-+H2O
C.用稀氢氧化钠溶液吸收二氧化氮:
2OH-+2NO2=NO3-+NO↑+H2O
D.甲烷的标准燃烧热为-890.3kJ·
mol-1,则甲烷燃烧的热化学方程式可表示为:
CH4(g)+2O2(g)=CO2(g)+2H2O(g)
△H=-890.3kJ·
mol-1
11、生产、生活离不开化学。
下列说法错误的是
A.“低碳生活”有利于减缓全球气候变暖和环境恶化的速度
B.燃料电池的燃料都在负极发生反应
C.纯碱可用于生产玻璃,其溶液也可用于除去物品表面的油污
D.工业上常用高纯硅制造光导纤维
12、在pH=1的含有Mg2+、Fe2+、Al3+三种阳离子的溶液中,可能大量存在的阴离子是
①Cl-;
②NO3-;
③SO42-;
④S2-
A.①②
B.①③
C.③④
D.②③
13.短周期金属元素甲~戊在元素周期表中的相对位置如右表所示,下面判断正确的是
A.原子半径:
丙<丁<戊B.金属性:
甲>丙
C.氢氧化物碱性:
丙>丁>戊D.最外层电子数:
甲>乙
14.在2014年的某省抗洪战斗中,一摩托艇要到正对岸抢救物质,关于该摩托艇能否到达正对岸的说法中正确的是( )
A.只要摩托艇向正对岸行驶就能到达正对岸
B.只有摩托艇的速度大于水流速度,摩托艇才能到达正对岸
C.虽然水流有较大的速度,但只要摩托艇向上游某一方向行驶,一定能到达正对岸
D.不论摩托艇怎么行驶,都可能到达正对岸
15.某同学在单杠上做引体向上,在下列四个选项中双臂用力最小的是( )
A.
B.
C.
D.
16.倾角为α、质量为M的斜面体静止在水平桌面上,质量为m的木块静止在斜面体上.下列结论正确的是( )
A.桌面对斜面体的支持力大小是(M+m)g
B.桌面对斜面体的摩擦力大小是mgsinαcosα
C.木块受到的摩擦力大小是mgcosα
D.木块对斜面体的压力大小是mgsinα
17.如图所示,一光滑小球静止放置在光滑半球面的底端,用竖直放置的光滑挡板水平向右缓慢地推动小球,则在小球运动的过程中(该过程小球未脱离球面),木板对小球的推力F1、半球面对小球的支持力F2的变化情况正确的是( )
A.F1增大,F2减小
B.F1减小,F2增大
C.F1减小,F2减小
D.F1增大,F2增大
18.若在某行星和地球上相对于各自的水平地面附近相同的高度处、以相同的速率平抛一物体,它们在水平方向运动的距离之比为2:
.已知该行星质量约为地球的7倍,地球的半径为R.由此可知,该行星的半径约为( )
A.R
B.R
C.2R
D.R
19.如图,小球沿斜面向上运动,依次经a、b、c、d到达最高点e.已知ab=bd=8m,bc=1m,小球从a到c和从c到d所用的时间都是2s,设小球经b、c时的速度分别为vb、vC,则( )
A.de=8m
B.vC=4m/s
C.vb=m/s
D.从d到e所用的时间是3s
20.如图所示,在光滑四分之一圆弧轨道的顶端a点,质量为m的物块(可视为质点)由静止开始下滑,经圆弧最低点b滑上粗糙水平面,圆弧轨道在b点与水平轨道平滑相接,物块最终滑至c点停止.若圆弧轨道半径为R,物块与水平面间的动摩擦因数为μ,下列说法正确的是( )
A.物块滑到b点时的速度为
B.物块滑到b点时对b点的压力是3mg
C.c点与b点的距离为
D.整个过程中物块机械能损失了mgR
21.一辆小汽车在水平路面上由静止启动,在前5s内做匀加速直线运动,5s末达到额定功率,之后保持以额定功率运动.其v-t图象如图所示.已知汽车的质量为m=2×
103Kg,汽车受到地面的阻力为车重的0.1倍,取重力加速度g=10m/s2,则以下说法正确的是( )
A.汽车在前5s内的牵引力为6×
103N
B.0~t0时间内汽车牵引力做功为mvm2
C.汽车的额定功率为50kw
D.汽车的最大速度为30m/s
第II卷(非选择题共174分)
三、非选择题:
包括必考题和选考题两部分。
第22题~第32题为必考题,每个试题考生都必须做答。
第33题~第40题为选考题,考生根据要求做答。
(一)必考题(共129分)
22.在“探究恒力做功与动能改变的关系”实验中(装置如图甲):
①下列说法哪一项是正确的______.(填选项前字母)
A.平衡摩擦力时必须将钩码通过细线挂在小车上
B.为减小系统误差,应使钩码质量远大于小车质量
C.实验时,应使小车靠近打点计时器由静止释放
②图乙是实验中获得的一条纸带的一部分,选取O、A、B、C计数点,已知打点计时器使用的交流电频率为50Hz.则打B点时小车的瞬时速度大小为______m/s(保留三位有效数字).
23、“验证力的平行四边形定则”的实验情况如图甲所示,其中A为固定橡皮筋的图钉,O为橡皮筋与细绳的结点,OB和OC为细绳。
图乙是在白纸上根据实验结果画出的图。
(1)图乙中的F与F′两力中,方向一定沿AO方向的是_______。
(2)本实验采用的科学方法是_______。
A.理想实验法
B.等效替代法
C.控制变量法
D.建立物理模型法
(3)某同学在做该实验时认为:
A.拉橡皮条的细绳长一些,实验效果较好
B.拉橡皮条时,弹簧秤、橡皮条、细绳应贴近木板且与木板平面平行
C.橡皮条弹性要好,拉结点到达某一位置O时,拉力要适当大些,且拉力F1和F2的夹角越大越好
D.在实验中O点位置不能变
E.细绳可以用弹性绳代替
其中不正确的是______(填入相应的字母)。
24(14分)如图所示,质量m=1.1kg的物体(可视为质点)用细绳拴住,放在水平传送带的右端,物体和传送带之间的动摩擦因数μ=0.5,传送带的长度L=5m,当传送带以v=5m/s的速度做逆时针转动时,绳与水平方向的夹角θ=37°
.
已知:
g=l0m/s2,sin37°
=0.6,cos37°
=0.8.求:
(1)传送带稳定运动时绳子的拉力T;
(2)某时刻剪断绳子,求物体运动至传送带最左端所用时间.
25(18分)、如图所示,小物块A在粗糙水平面上做直线运动,经距离时与另一小物块B发生碰撞并粘在一起以速度v飞离桌面,最终落在水平地面上。
已知=5.0m,s=0.9m,A、B质量相等且m=0.10kg,物块与桌面间的动摩擦因数µ
=0.45,桌面高h=0.45m。
不计空气阻力,重力加速度g=10m/s2。
求:
(1)A、B一起平抛的初速度v;
(2)小物块A的初速度v0。
26(14分)短周期元素形成的常见非金属固体单质A与常见金属单质B,在加热条件下反应生成化合物C,C与水反应生成白色沉淀D和气体E,D既能溶于强酸,也能溶于强碱。
E在足量空气中燃烧产生刺激性气体G,G在大气中能导致酸雨的形成。
请回答下列问题:
(1)组成单质A的元素位于周期表中第周期,第族。
(2)B与氢氧化钠溶液反应的化学方程式为:
。
(3)G与氯酸钠在酸性条件下反应可生成消毒杀菌剂二氧化氯。
该反应的氧化产物为,当生成2二氧化氯时,转移电子。
(4)将G气体通入BaCl2溶液中没有明显现象,若加入H2O2溶液则有__________
写出相关的化学反应方程式为:
。
27.(14分)亚氯酸钠(NaClO2)是一种重要的含氯消毒剂,主要用于水的消毒以及砂糖、油脂的漂白与杀菌。
以下是过氧化氢法生产亚氯酸钠的工艺流程图:
①NaClO2的溶解度随温度升高而增大,适当条件下可结晶析出NaClO2•3H2O。
②纯ClO2易分解爆炸,一般用稀有气体或空气稀释到10%以下安全。
③160g/LNaOH溶液是指160gNaOH固体溶于水所得溶液的体积为1L。
(1)160g/