非金属及其化合物推断题Word格式文档下载.doc
《非金属及其化合物推断题Word格式文档下载.doc》由会员分享,可在线阅读,更多相关《非金属及其化合物推断题Word格式文档下载.doc(7页珍藏版)》请在冰豆网上搜索。
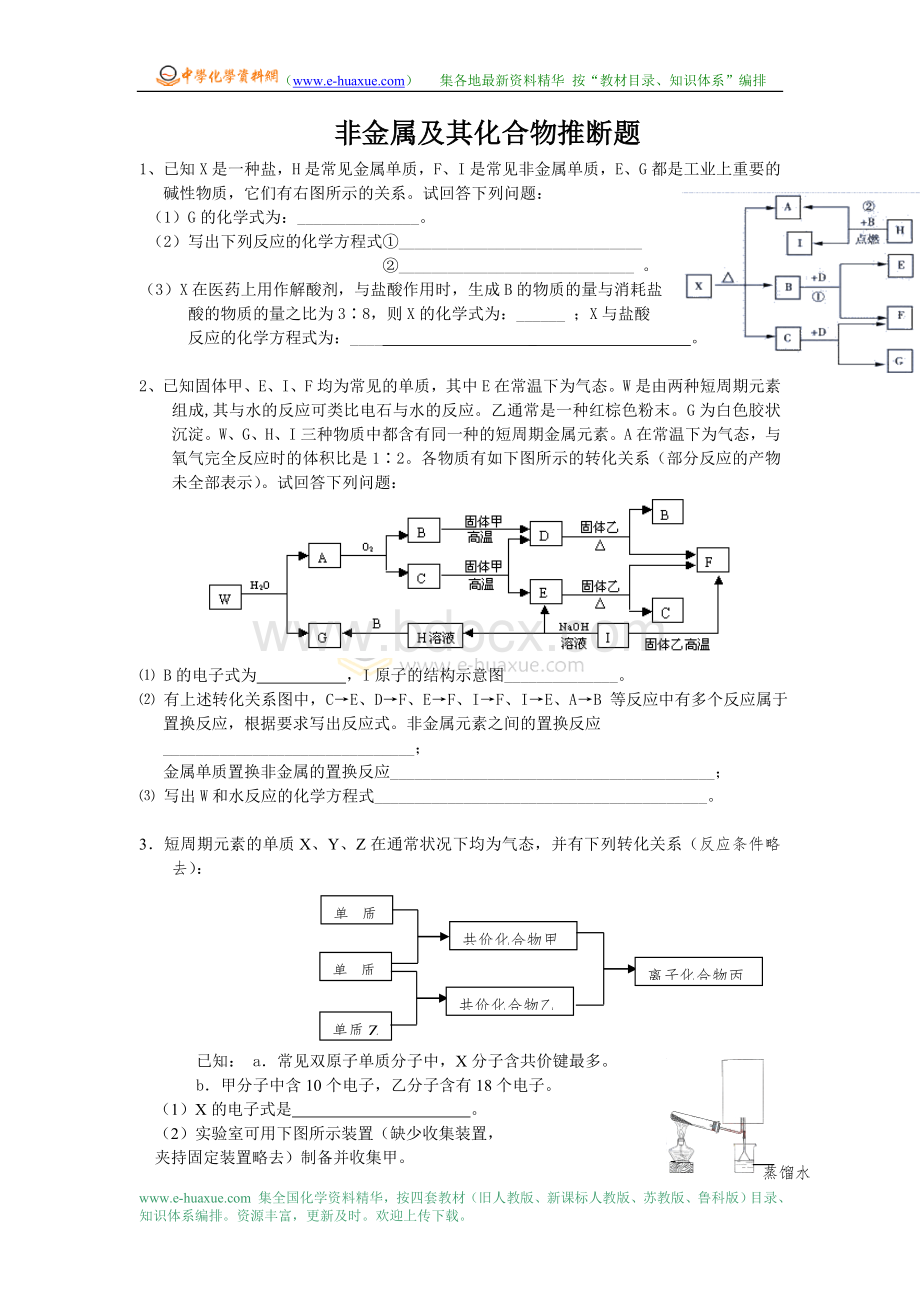
G为白色胶状沉淀。
W、G、H、I三种物质中都含有同一种的短周期金属元素。
A在常温下为气态,与氧气完全反应时的体积比是1∶2。
各物质有如下图所示的转化关系(部分反应的产物未全部表示)。
⑴B的电子式为,I原子的结构示意图______________。
⑵有上述转化关系图中,C→E、D→F、E→F、I→F、I→E、A→B等反应中有多个反应属于置换反应,根据要求写出反应式。
非金属元素之间的置换反应_______________________________;
金属单质置换非金属的置换反应________________________________________;
⑶写出W和水反应的化学方程式_________________________________________。
3.短周期元素的单质X、Y、Z在通常状况下均为气态,并有下列转化关系(反应条件略去):
单质X
单质Y
单质Z
共价化合物甲
共价化合物乙
离子化合物丙
蒸馏水
(滴有酚酞)
已知:
a.常见双原子单质分子中,X分子含共价键最多。
b.甲分子中含10个电子,乙分子含有18个电子。
(1)X的电子式是。
(2)实验室可用下图所示装置(缺少收集装置,
夹持固定装置略去)制备并收集甲。
①在图中方框内绘出用烧瓶收集甲的仪器装置简图。
②试管中的试剂是(填写化学式)。
③烧杯中溶液由无色变为红色,其原因是(用电离方程式表示) 。
(3)磷在Z中燃烧可生成两种产物,其中一种产物丁分子中各原子最外层不全是8电子结构,丁的化学式是。
(4)nmol丁与nmol丙在一定条件下反应,生成4nmol乙和另一化合物,该化合物蒸气的密度是相同状况下氢气的174倍,其化学式是。
4、如下图是中学化学中常见物质之间的一些反应关系,其中部分产物未写出。
常温下X和H是固体,B和G是液体,其余均为气体,1molX分解得到A、B、C各1mol。
试回答下列各题:
(1)写出下列物质的化学式:
X________,B________。
(2)写出下列反应的化学方程式:
①H+G―→A+F:
__________________________________________________________。
②C+D―→E:
(3)写出下列反应的离子方程式:
G+Cu―→E:
___________________________________________________________。
5.下图分别代表有关反应中的一种物质,请填下以下空白。
(1)①、③、⑤的化学式分别是、、。
(2)⑧与⑨反应的化学方程式是。
(3)用“双线桥”表示过氧化钠与②反应中的电子转移的方向和数目。
6.已知A为常见金属,X、Y为常见非金属,X、E、F、G常温下为气体,C为液体,B是一种盐,受热极易分解,在工农业生产中用途较广(如被用作某些电池的电解质)。
现用A与石墨作电极,B的浓溶液作电解质,构成原电池。
有关物质之间的转化关系如下图:
(注意:
其中有些反应的条件及部分生成物被略去)
请填写下列空白:
(1)反应④为A在某种气体中燃烧,生成单质Y和A的氧化物,其反应方程式为
。
(2)从D溶液制备D的无水晶体的“操作a”为
。
(3)反应②的化学方程式为
。
(4)反应⑤的化学方程式为
。
(5)原电池反应①中正极的电极反应式为
7.下图是部分短周期元素的单质及其化合物的转化关系图(有关反应的条件及生成的H2O已略去),已知:
(a)A、B、C、D是非金属单质,其中B、C、D在常温常压下是气体。
(b)反应①②是化工生产中的重要反应。
(c)化合物E是形成酸雨的污染物之一,化合物K是常用的氮肥。
(d)化合物L具有漂白性,可由Cl2与NaOH溶液反应而制得。
(e)化合物J由两种元素组成,其相对分子质量为32。
请按要求填空:
⑴反应③的化学方程式______________。
⑵C的电子式______________;
H的化学式______________。
⑶L的溶液与化合物E反应的离子方程式______________。
⑷化合物J的化学式______________。
8.U、V、W、X、Y、Z是原子序数依次增大的六种常见元素。
Y的单质在W2中燃烧的产物可使品红溶液褪色。
Z和W元素形成的化合物Z3W4具有磁性。
U的单质在W2中燃烧可生成UW和UW2两种气体。
X的单质是一种金属,该金属在UW2中剧烈燃烧生成黑、白两种固体。
请回答下列问题:
⑴.V的单质分子的结构式为_______________;
XW的电子式为____________;
Z元素在周期表中的位置是_____________。
⑵.U元素形成的同素异形体的晶体类型可能是(填序号)__________。
①原子晶体②离子晶体③分子晶体④金属晶体
⑶.U、V、W形成的10电子氢化物中,U、V的氢化物沸点较低的是(写化学式)_________;
V、W的氢化物分子结合H+能力较强的是(写化学式)______,用一个离子方程式加以证明___________________。
⑷.YW2气体通人BaCl2和HNO3的混合溶液,生成白色沉淀和无色气体VW,有关反应的离子方程式为______________,由此可知VW和YW2还原性较强的是(写化学式)__________________。
9.A、B两种固体,都由甲、乙两种元素组成。
在A、B中,甲、乙两种元素的原子个数比分别为1:
1和1:
2,高温煅烧A、B时,产物都是C(固体)和D(气体)。
由D可制得E(酸)。
E和另一种酸组成的混合酸跟甲苯反应可生成三硝基甲苯。
C与E的稀溶液反应得到溶液F,往F溶液中加入氢氧化钠溶液,有红褐色沉淀生成,该沉淀经灼烧后转变成C。
往F溶液中加入甲元素的单质得到溶液G。
试根据以上信息填写下列空白:
(1)A的化学式(分子式)是;
(2)B煅烧生成C和D的化学方程式是;
甲元素的单质与F溶液反应的离子方程式是;
(3)往G溶液中加入NaOH溶液发生的现象是;
10.A、B、C、D、E、F六种中学常见的物质,皆由短周期元素组成,有转化关系:
(1)若A、C、E皆为氧化物,且常温下A为无色液体,E为有毒气。
B、D、F皆为非金属单质,且D为气体。
则A的结构式为,1molC中含有个共价键。
(2)若A、C、E皆为氢化物,三者皆为极性分子,其中C的相对分子质量最小;
D、E、F皆为氧化物,其中D、F为有毒气体。
则
①A、C、E沸点由高到低的顺序为(填化学式)。
②A跟D常温下反应可生成一种单质,化学方程式为。
11.根据下列框图关系填空,已知反应①、③是我国工业生产中的重要反应,X常温下为无色无味透明液体;
C焰色反应火焰呈黄色,J为红褐色沉淀;
D、E常温下为气体,且E能使品红溶液褪色;
A固体中仅含两种元素,其中金属元素的质量分数约为46.7%。
+X
+D,高温
Δ
B固体
A固体
C
D
E
F
G
H
I
J
①
②
③
④
(1)G的化学式为;
(2)固体A中所包含的化学键与固体B类似,则A的电子式为;
(3)反应②的离子方程式:
;
(4)反应④的离子方程式:
(5)已知每生成16gE,放出106.5kJ热量,则反应①的热化学方程式为:
。
12.A-H及X均为中学化学常见物质,X是一种金属单质,A、B是非金属单质且A在常温下为气体。
它们在一定条件下有如下转化关系(图中条件均已略去)。
A
X
B
H(红褐色沉淀)+……
NaClO溶液
⑤
(1)写出C物质的化学式 ;
(2)在上述①-⑤反应中肯定不属于氧化还原反应的是 (填编号);
(3)指出元素X在元素周期表中的位置:
第 周期,第 族;
(4)请写出反应④和⑤的离子方程式:
④ ,
⑤ ;
(5)用离子方程式表示在D溶液中加入NaClO溶液产生红褐色沉淀的原因:
答案
1、
(1)NaOH
(2)①2Na2O2+2CO2====2Na2CO3+O2②2Mg+CO22MgO+C
(3)3MgCO3·