初升高化学衔接班第2讲Word格式.docx
《初升高化学衔接班第2讲Word格式.docx》由会员分享,可在线阅读,更多相关《初升高化学衔接班第2讲Word格式.docx(33页珍藏版)》请在冰豆网上搜索。
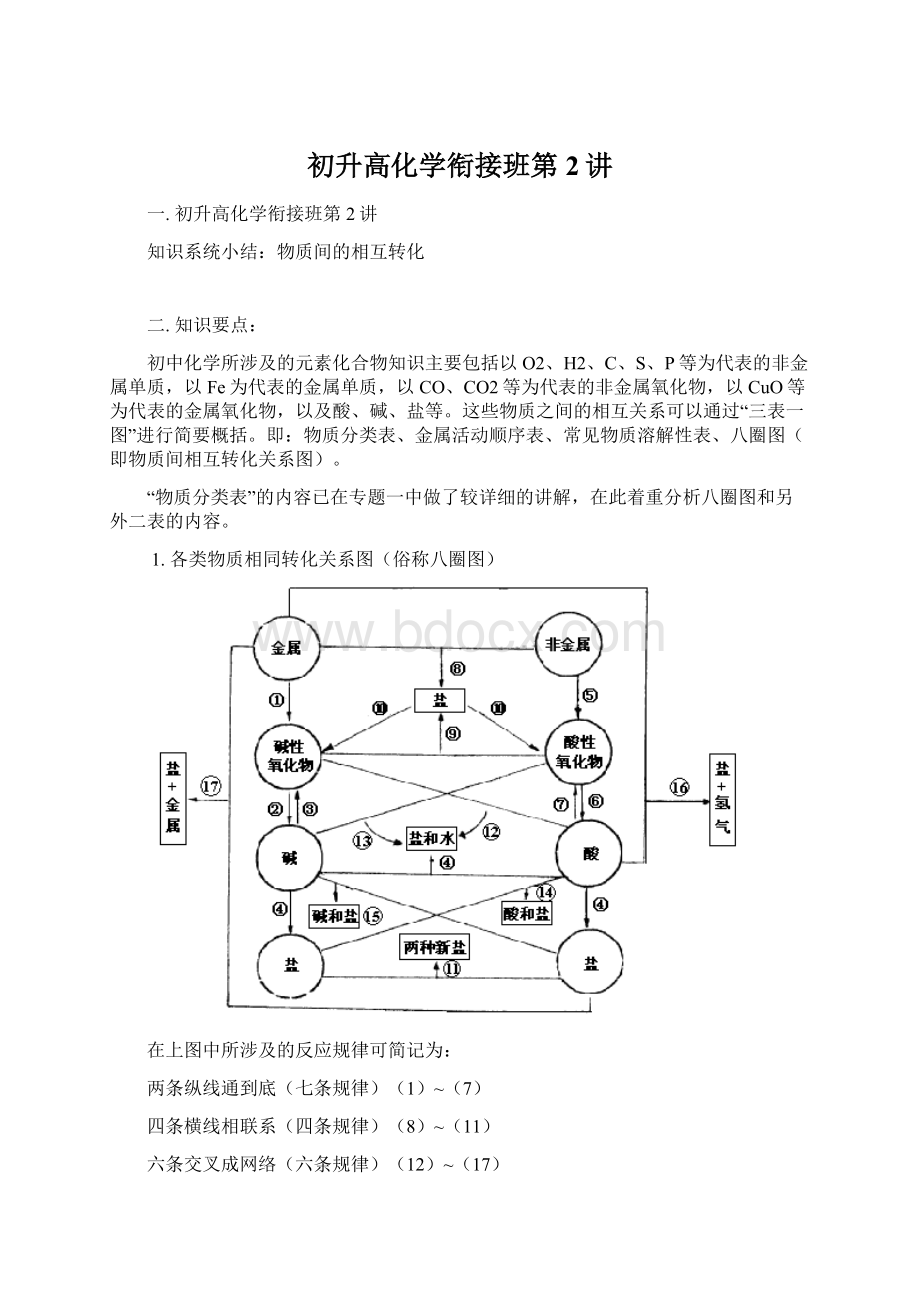
非金属氧化物(酸性氧化物)
(6)酸性氧化物(易溶)+水
酸(易溶)
(7)酸(易挥发/难溶)
酸氧+水(易挥发/难溶)
从纵向来看,金属
碱性氧化物
碱
盐,其中金属元素相同。
非金属
酸性氧化物
酸(含氧酸)
盐,其中非金属元素相同。
横向:
(8)金属+非金属
(无氧酸)盐
(9)碱氧+酸氧
(含氧酸)盐
(10)含氧酸盐
碱氧+酸氧
(11)盐+盐
两种新盐
交叉:
(12)酸+碱氧
盐+水
(13)碱+酸氧
(14)酸+盐
新酸+新盐
(15)碱+盐
新碱+新盐
(16)金属+酸
盐+
(17)金属+盐
新盐+新金属
以上十七条规律的应用:
(1)可知某物质的性质。
(2)可知某物质的制法。
如:
(4)、(8)、(9)、(11)~(17)为盐的十种制法。
(3)已知各类物质间的相互关系。
说明:
<
1>
以上各规律为各物质间相互转化的一般规律,具体到某些物质有些规律要具体分析,未必均适用。
制取
的方法与制取
的方法各有几种?
(思考)
答:
:
①
②
③
④
⑤
⑥
⑦
因
为无氧酸盐,故规律(9)、(13)不适用。
为难溶碱,故规律(15)不适用。
∴只有如上7种制法。
因Cu为H后金属,
为难溶碱、CuO不能直接与SO3反应生成CuSO4,Ag2SO4为微溶物,不符合与CuCl2发生复分解反应的条件,也不能与Cu发生置换反应等原因,∴CuSO4只有上述三种制取方法(初中范围内,方法③也不常见)
2>
此外,在物质的制取中还有一些常见的规律,如:
对于盐+酸
新盐+新酸,有如下规律:
①强酸
弱酸
②稳定的(不易分解的)酸
不稳定的(另分解的)酸。
③高沸点(不易挥发的)酸
低沸点(易挥发的)酸。
④可溶性酸
难溶性酸。
3>
从反应规律与反应类型的关系来看。
属于化合反应的有:
规律
(1)、
(2)、(5)、(6)、(8)、(9)。
属于分解反应的有:
规律(3)、(7)、(10)。
属于置换反应的有:
规律(16)、(17)。
属于复分解反应的有:
规律(4)、(11)、(12)、(14)、(15)。
规律(13)不属于任何一种基本反应类型。
初中阶段不属于任何一种基本反应类型的反应包括:
酸氧+碱
盐+水
2.金属活动顺序表及其使用范围:
(1)金属活动顺序:
(2)在金属活动性顺序里,位于氢以前的较活泼金属,能与盐酸或稀硫酸发生置换反应,置换出酸中的氢,氢后的金属则不能。
较活泼的金属能将不活泼金属从它的盐溶液里置换出来。
(3)很活泼的金属与某些盐溶液反应时,先与水反应生成碱,然后碱再与盐溶液发生复分解反应,无金属生成。
铁钉与
溶液反应,可在铁钉表面覆盖一层红色物质(Cu),溶液逐渐由蓝色变为浅绿色(
)
反应方程式为:
若将新切好的金属钠(钠单质化学性质非常活泼,易与水、空气反应,通常保存于煤油中,其表面有氧化膜。
用时需用小刀切去其表面的氧化膜,随切随用)放入
溶液中,则不会得到红色的Cu,溶液也不会由蓝色的
直接变为澄清的无色的
,事实上,反应现象为:
钠在液面上熔为光亮的银色小球,四处游动,并同时伴随着“嘶嘶”的响声,反应完全后生成蓝色絮状沉淀。
若钠的颗粒较大,而反应容器口较小的话,还可见到在液面上发生燃烧现象,生成物中有黑色物质。
解析:
这是因为Na为很活泼的金属,它可与水发生反应,生成
和
。
若做Na与
反应的实验,可以收集所得的气体,点燃产生爆鸣声可证明为
,向反应后的溶液中加入1~2滴酚酞,溶液变为红色,证明生成物为碱。
生成的
再与
反应,则产物为蓝色絮状沉淀
容器口较小时观察到的燃烧现象是由于Na与
反应时放出大量的热,而又未能及时散失,达到
的着火点使之燃烧,又进一步放热,使部分
分解,因此产物中会有黑色物质(
)出现。
化学方程式:
(
,
结论:
金属活动顺序表表示金属单质的原子在水溶液中失去电子变为阳离子的能力,其位置越靠前,表明该金属的原子在溶液中失电子的能力越强。
而其对应的阳离子在水溶液中得电子的能力越弱。
金属活动性越强,金属越易失电子进入溶液。
金属活动性越弱,金属阳离子越易得到电子而从溶液中析出。
(4)浓硫酸及浓、稀硝酸与金属反应不生成氢气,即不发生置换反应。
(5)铁与非氧化性的酸或盐溶液发生置换反应时,生成亚铁盐,即铁为+2价。
(6)金属活动性顺序只适用于金属和酸、金属和盐发生的置换反应,不能用于复分解反应,也不宜用金属活动性顺序去说明非水溶液中的某些反应,如:
3.酸、碱、盐的溶解性规律
(1)酸:
无机化合物中,除硅酸(
)不溶于水,大多数常见的酸易溶于水。
(2)碱:
一水合氨(
)、
易溶;
微溶;
其余碱不溶于水。
(3)盐:
铵盐、钾盐、钠盐、硝酸盐易溶;
盐酸盐中
(氯化亚汞)不溶,其余溶;
硫酸盐中
不溶,
、
微溶,其余都溶;
碳酸盐中,
溶,
微溶,其余不溶;
磷酸盐、硫化物中除
溶外,其余不溶。
(4)酸中
为强酸,
为中强酸,
为弱酸。
(5)可溶性碱除
(弱碱)外均为强碱,不溶性碱为弱碱。
了解酸、碱、盐的溶解性的应用之一是判断某些复分解反应能否发生。
4.复分解反应的发生条件
(1)复分解反应需在溶液里才能发生,在固态时无自由移动的离子时不发生反应。
还要看生成物是否满足下列条件之一:
①产生沉淀②放出气体③生成难电离的水
(2)复分解反应常发生在下列几条反应规律中:
①酸+碱
盐+水(有强酸或强碱,至少一种物质可溶,若碱不溶于水但能溶于酸)
②酸+碱性氧化物
盐+水(碱氧可不溶于水,但要溶于酸,酸为强酸)
③酸+盐
新酸+新盐(盐可不溶于水,但要溶于酸,酸为强酸)
④碱+盐
新碱+新盐(反应物的碱和盐均要溶于水)
⑤盐+盐
两种新盐(反应物均要溶于水)
【典型例题】
[例1]科学实验发现,有一类酸溶液的酸根离子(可用
表示)与
的化学性质类似,请用化学方程式表示该类酸溶液的通性。
(1);
(2);
(3);
(4);
(5);
题中所给予的信息是,酸根
与
性质相似,即
的性质相似,
的通性与
的通性相似,由此可以得出答案:
(1)
(2)
(3)
(4)
(5)
[例2]有三种金属M、N、R,其氧化物中只有N的氧化物溶于水,且水溶液pH值大于7,已知R能从
溶液中置换出
,R不溶于盐酸,M能在
中剧烈燃烧,火星四射,生成黑色固体物质。
则M、N、R在金属活动顺序表中的正确位置是()
A.M、N、H、RB.R、M、H、N
C.R、H、M、ND.N、M、H、R
解析:
本题考查根据实际反应推导金属活动性顺序,关键是先确定一个标准,其他的与它相比较。
排在前面的金属能把排在后面的金属从它的盐溶液里置换出来,而不管它是在氢前还是在氢后,但要注意金属与盐反应时,盐应为可溶性盐。
根据题意溶于水且水溶液pH>7的碱性氧化物只有
,这些金属的活动性都很强。
又据题干信息可知,
,M是铁,故M、N、R的金属活动性顺序应为N、M、H、R。
答案:
D
[例3]某化工厂有甲、乙两个车间,它们排放的工业废水澄清透明,共有
六种离子。
(1)甲车间的废水中含有三种离子,明显呈碱性,则甲车间废水中不可能存在的阳离子是。
(2)乙车间的废水中含有另外三种离子,其中阴离子是。
(3)如果加足量的铁粉,把甲车间和乙车间的废水按适当的比例混合,可以使废水中的某些离子转化为两种沉淀,经过滤后的废水主要含(填化学式)可用来浇灌农田。
此题联系生产实际考查综合能力。
根据两个车间排放的工业废水澄清透明,可知废水中无沉淀物存在,每个车间废水中的离子间不会发生反应(能共存),由甲车间的废水含三种离子且呈碱性,说明甲车间的废水中含有
,则无
,甲车间废水中不可能存在的阳离子是
,则只能是
,乙车间废水中含有另外三种离子只能是
;
如向乙的废水中加足量铁粉,可回收其中的
如果将甲车间和乙车间的废水按适当的比例混合,可使废水中的
转化为
两种沉淀,经过滤后废水中主要含有
(属复合肥),其溶液可浇灌农田。
[例4]某工厂中含有少量氧化铜和锌粉的废渣与废盐酸混合形成污水,若向污水中加入足量的铁粉,则处理后的水中一定含有的金属离子是()
A.
、
B.
C.
D.只有
理解题中各物质加入的先后顺序及量之间的关系是解此题的关键。
含有少量氧化铜和锌粉的废渣在未加入铁粉前先与废盐酸作用:
,未反应完的废盐酸与加入的铁粉继续反应直至废盐酸消耗尽:
,另外,铁粉还要与溶液中的
反应:
,至
反应完,铁粉仍有剩余(∵铁粉足量),此时溶液中含有的金属阳离子只有
与未参与反应的
B
[例5]在某无色透明溶液中,下列离子能大量共存的是()
B.
D.
此题为离子共存问题的考察。
溶液中大量共存的离子必须相互不起反应,另外还要注意题目中的隐含条件“无色”,说明虽能共存但有色的离子也不符合要求。
A中
,反应生成
B中
为蓝色;
D中
为紫色,且
反应生成
C
[例6]某溶液中可能有下列阴离子:
(1)当溶液中存在大量
时,溶液中不能大量存在的离子是。
(2)当溶液中存在大量
(3)当溶液中存在大量和离子时,上述阴离子都不能存在。
此题仍为离子共存问题,解题关键是要了解哪些离子不能共存,即符合复分解