人教版九年级中考化学计算试题汇编Word格式文档下载.docx
《人教版九年级中考化学计算试题汇编Word格式文档下载.docx》由会员分享,可在线阅读,更多相关《人教版九年级中考化学计算试题汇编Word格式文档下载.docx(18页珍藏版)》请在冰豆网上搜索。
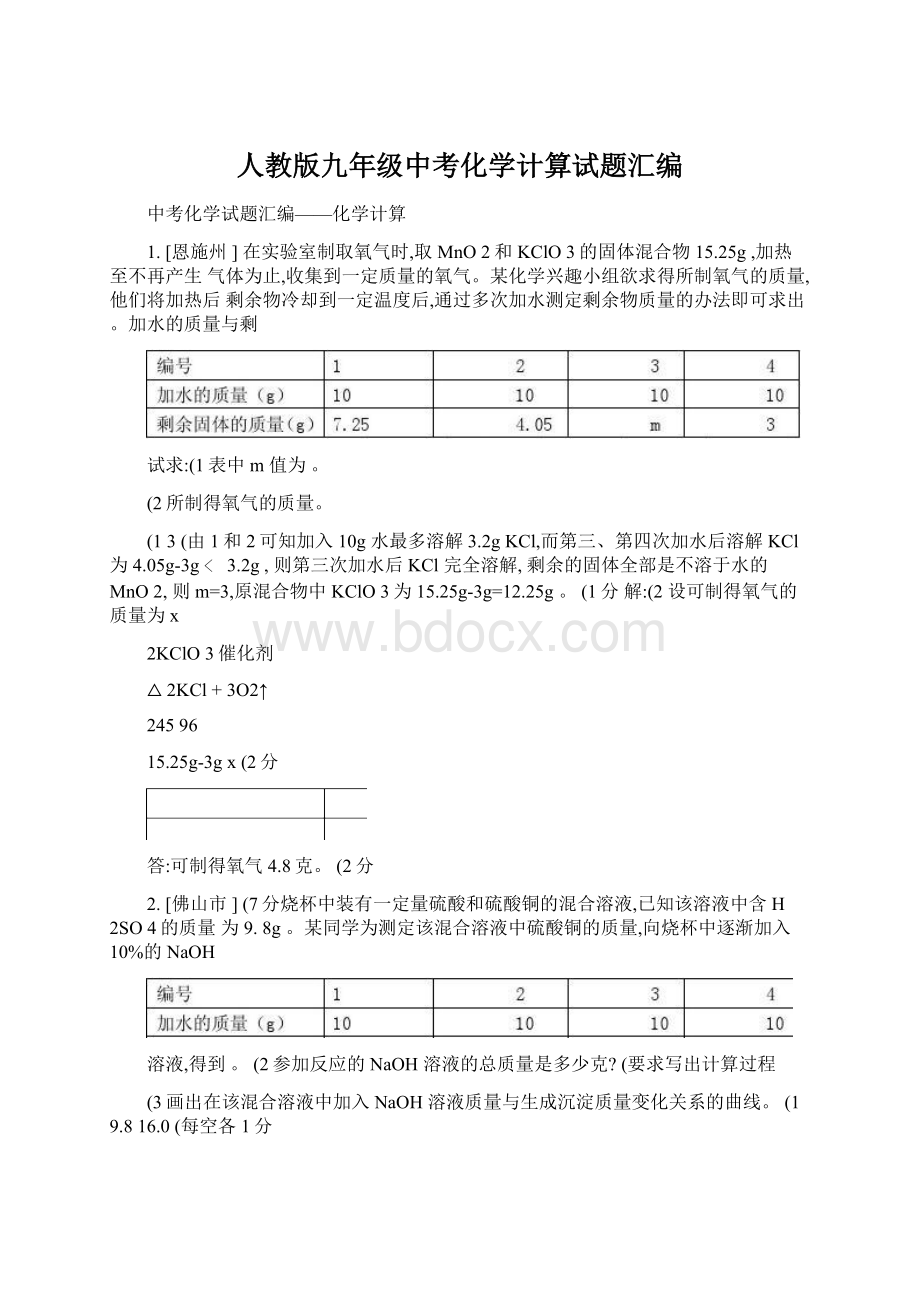
2.[佛山市](7分烧杯中装有一定量硫酸和硫酸铜的混合溶液,已知该溶液中含H2SO4的质量为9.8g。
某同学为测定该混合溶液中硫酸铜的质量,向烧杯中逐渐加入10%的NaOH
溶液,得到。
(2参加反应的NaOH溶液的总质量是多少克?
(要求写出计算过程
(3画出在该混合溶液中加入NaOH溶液质量与生成沉淀质量变化关系的曲线。
(19.816.0(每空各1分
(2(设未知数及作答1分,建立关系式2分,计算结果1分,共4分解:
设与硫酸反应的NaOH的质量为x,与CuSO4反应的NaOH的质量为y。
H2SO4+2NaOH=Na2SO4+2H2OCuSO4+2NaOH=Cu(OH2↓+Na2SO498
8080989.8gxy9.8g
x=8g
y=8g
故参加反应的NaOH溶液的质量共为=160g
整个过程中参加反应的NaOH溶液的总质量是160克。
(3(抓住起点、折点及曲线走势给分,共1分
3.[广东省](7分同学们从山上采集到一种石灰石,他们取80克该样品进行煅烧实验(所含杂质
(1当石灰石完全反应后,生成CO2的质量为g。
(2求该石灰石中CaCO3的质量分数,写出计算过程。
(3请在下面坐标图中,画出煅烧时生成气体的质量(m随时间(t变化的曲线。
分(122g(2(2解:
设样品中含CaCO3的质量为x
989.8g80x=80y
989.8g=
8g+8g
10%
高温
CaCO3CaO+CO2↑(1分
10044
x22g
x100=g2244x=44
22100g
=50g(1分石灰石中CaCO3的质量分数=(50g÷
80g×
100%=62.5%(1分
(3曲线3分。
其中to—t5(气体从0~22g曲线段正确1分;
从t5以后曲线段正确1分。
4.[安徽省](6分称取铜、锌混合物粉末10.0g置于烧杯中,慢慢加入稀硫酸使其充分反应,
直至固体质量不再减少为止,此时用去49.0g稀硫酸。
剩余固体3.5g。
⑴该混合物粉末中铜的质量分数为多少?
⑵所用的稀硫酸溶质的质量分数是多少?
⑴铜的质址分数=
3.5g
10.0g
×
100%=35.0%(2分⑵设所用稀硫酸溶质的质量分数为x
Zn+H2SO4=ZnSO4+H2↑659810.0g-3.5g49g·
x
6598=10.0g-3.5g49g·
xx=20.0%答:
略。
5.[常州市](5分为测定某碳素钢样品中铁的质量分数,现取一定质量的样品粉未于质量为51.8克的烧杯中,然后逐步加入一定质量分数的稀硫酸,当加入80g稀硫酸时反应恰好完全,加入稀硫酸的质量与烧杯及烧杯内物质的总质量的关系如右图。
试通过计完成下列填空:
(不能整除时,结果保留一位小数(1该实验取用的样品质量为:
_▲_;
(2样品中铁的质量分数为:
_▲_;
(3小王不慎在反应结束后,向烧杯中多加了20g
稀硫酸,此时,溶液中亚铁离子在溶液
总质量中的质量分数为:
▲,若在上图中补绘此过程中稀硫酸的质量与烧杯及烧杯内物质的总质量的关系图,所得线段的终点位于线段AB延长线的_▲_(填:
上方、下方或线上。
(117g(1分
(298.8%(2分
(314.4%(1分上方(1分
6.[鄂州市]用“候氏制碱法”制得的纯碱中常含有少量的氯化钠。
为测定某纯碱样品中碳酸钠的质量分数,小雯同学称取该样品5.6g加入到盛有100g足量稀盐酸的烧杯中,完全反应后称得烧杯中的溶液质量为103.4g。
求该纯碱样品中碳酸钠的质量分数。
(反应的化学方程式为:
Na2CO3+2HCl==2NaCl+CO2↑+H2O解:
生成二氧化碳的质量为
100g+5.6g-103.4g=2.2g┄┄┄┄┄┄┄┄┄┄┄┄┄┄┄┄┄┄┄(1分设样品中碳酸钠的质量为x
Na2CO3+2HCl==2NaCl+CO2+H2O10644
x2.2g┄┄┄┄┄┄┄┄┄┄┄(1分
┄┄┄┄┄┄┄┄┄┄┄┄┄┄┄┄┄┄┄(1分
x=5.3g┄┄┄┄┄┄┄┄┄┄┄┄┄┄┄┄┄┄┄┄┄┄┄(1分
则该纯碱样品中碳酸钠的质量分数为
100%=94.6%┄┄┄┄┄┄┄┄┄┄┄┄┄┄┄┄┄(2分
所求样品中碳酸钠的质量分数为94.6%
7.[贵港市]酸和碱能发生中和反应,它在日常生活和工农业生产中有广泛的应用。
小强同学在做中和反应实验时,向盛有40g10%的氢氧化钠溶液的烧杯中逐滴加入稀盐酸,当恰好完全反应时,共滴加了36.5g稀盐酸。
(1配置40g10%的氢氧化钠溶液需要水_________mL。
(ρ水=1.0g/mL(2求:
所加稀盐酸的溶质质量分数和反应后所得溶液中溶质的质量。
(写出计算过程(136
(2设稀盐酸中溶质的质量为x,反应生成的NaCl的质量为y
2O4036.558.540g×
10%xy
yx5.5836.510%40g40==⨯解之得x=3.65g,y=5.85g所以,所加稀盐酸的溶质质量分数为:
36.5g
g65.3×
100%=10%
44
=x2.2g5.3g
5.6g
所加稀盐酸的溶质质量分数为10%;
反应后所得溶液中溶质的质量为5.85g。
8.[哈尔滨](5分在实验室里,大刚同学用氯酸钾和二氧化锰混合加热制取一定量的氧气后.剩余47.4g的固体。
小强同学继续加热这些固体至完全反应后又制得了一些氧气.同时得到37.8g的固体,小强将其充分溶解于170.2g水中,搅拌后过滤,得一定质量的滤液.并将过滤后所得固体洗涤、干燥,回收得到8g黑色固体纯净物。
请回答下列问题:
(1小强所做的实验中发生反应的化学方程式为.(2小强所做的实验中制得氧气的质量为:
(3在小强的实验中,列出求解氯酸钾质量(x的比例式:
(4上述实验所得滤液中溶质的质量分数为:
(5大刚和小强在实验中消耗氯酸钾的质量比为。
9.[海南省]黄铜是铜和锌的合金,在20g黄铜样品中加入足量稀盐酸使其完全反应,生成氢气0.2g,求样品中铜的质量。
[解答]解:
设生成0.2g氢气,需锌的质量为XZn+2HCl==ZnCl2+H2↑652X0.2g65/X==2/0.2gX==6.5g
铜的质量==20g-6.5g==13.5g答:
铜的质量为13.5g
10.[河北省]将50gCaCl2溶液混合后,恰好完全反应。
过滤得到115g溶液。
请计算:
(1反应后生成CaCO3沉淀的质量为。
(2参加反应的Na2CO3的质量。
(3过滤后所得溶液中溶质的质量分数。
(结果精确到0.1%(15g
解(2设参加反应的Na2CO3的质量为x,生成NaCl的质量为y。
NaClCaCOCaClCONa23232+↓=+
106100117x5gy
gx5100106=ggx3.5100
5106=⨯=yg5117100=ggy85.5100
5117=⨯=(3过滤后所得溶液中溶质的质量分数为%1.5%10011585.5=⨯g
g答:
参加反应的Na2CO3的质量为5.3g,过滤后所得溶液中溶质的质量分数为5.1%。
11.[河南省]若73g质量分数为20%的盐酸与127g氢氧化钠溶液恰好完全中和,试计算反应后所得溶液中溶质的质量分数。
12.[黄冈市]用“侯氏制碱法”制得的纯碱常含有少量的氯化钠。
将10g含有氯化钠的纯碱
溶解于102.32g稀盐酸中,恰好完全反应,收集到3.52g的气体(假设生成的气体全部逸出。
求:
反应后得到的不饱和溶液中溶质的质量分数。
解:
设该纯碱样品中碳酸钠的质量为x,生成的氯化钠的质量为y,则(0.5分
Na2CO3+2HCl=2NaCl+H2O+CO2↑(1分10611744
xy
3.52g
x=8.48g(1分y=9.36g(1分
(1分
反应后得到的不饱和溶液中溶质的质量分数为10%(0.5分
13.[黄石市]称取1.0g熟石灰样品,加适量水使之充分溶解,搅拌过滤后,往滤液中滴
入酚酞试液,同时加入溶质质量分数为10%的盐酸至溶液刚好变为无色,消耗盐酸溶液
7.3g。
求样品中Ca(OH2的质量分数(写出计算过程。
设样品中含Ca(OH2的质量为x克
Ca(OH2+2HCl=CaCl2+2H2O…………………………………………(l分7413
xl0%×
7.3g
x74=7.3g
1073…………………………………………(l分x=0.74g…………………………………………(l分
则样品中Ca(OH2的质量分数为Ca(OH2%=g
g174.0×
100%=74%………(1分答:
样品中Ca(OH2质量分数为74%。
4.425.1
15.[连云港](7分某班一次社会实践活动是到连云港碱厂参观,该厂主要产品之一是小苏
打(碳酸氢钠。
参观结束,同学们带回一些化
验室里废弃的小苏打样品,来测定其中碳酸氢
钠的质量分数(假设该样品中只含有氯化钠一种杂质。
取样品9.3g逐滴加入稀盐酸,生成
CO2气体的质量与滴加稀盐酸的质量关系如右
图所示,求:
(计算结果用百分数表示,保留到
小数点后一位数字(1样品中碳酸氢钠的质量分数。
(2恰好完全反应时,所得溶液中溶质的质量分数。
设样品中碳酸氢钠的质量为x,生成氯化钠的质量为y
NaHCO3+HClNaCl+CO2↑+H2O(1分
8458.544
xy4.4g
==x=8.4g(1分
==y=5.85g(1分
(1样品中碳酸氢钠的质量分数为:
╳100%=90.3%(2