四川省成都市龙泉驿区第一中学高一重点班分班考试化学试题Word文档格式.docx
《四川省成都市龙泉驿区第一中学高一重点班分班考试化学试题Word文档格式.docx》由会员分享,可在线阅读,更多相关《四川省成都市龙泉驿区第一中学高一重点班分班考试化学试题Word文档格式.docx(29页珍藏版)》请在冰豆网上搜索。
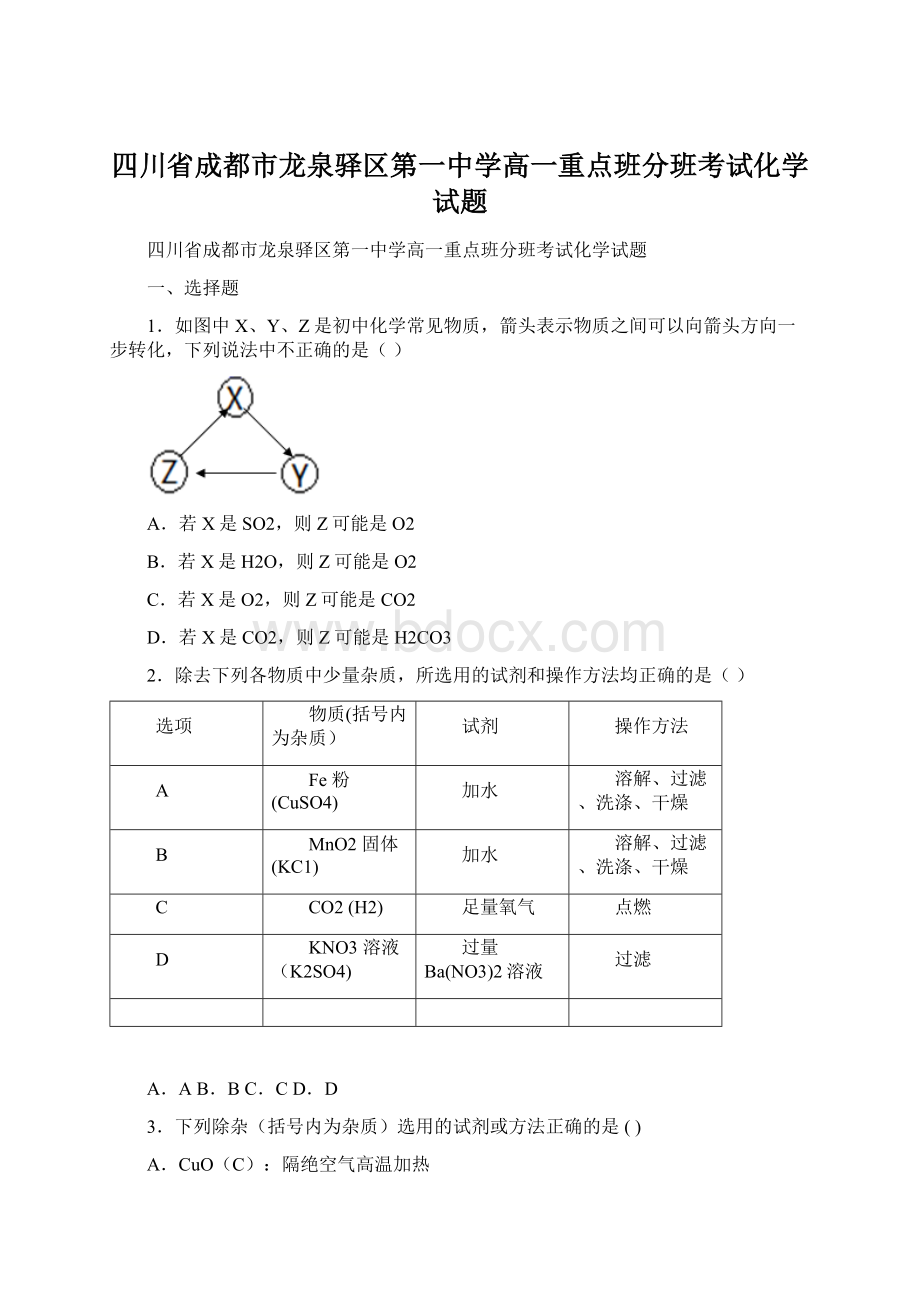
D
KNO3溶液(K2SO4)
过量Ba(NO3)2溶液
过滤
A.AB.BC.CD.D
3.下列除杂(括号内为杂质)选用的试剂或方法正确的是()
A.CuO(C):
隔绝空气高温加热
B.Na2SO4溶液(NaOH):
加适量稀盐酸
C.CO2(HCl):
将气体通入足量的氢氧化钠溶液
D.CaCl2溶液(HCl):
加入过量碳酸钙,充分反应后过滤
4.下列四个图像中,能正确反映对应关系的是
A.一定温度下,向一定量水中加入KNO3固体
B.加热一定量的高锰酸钾固体
C.向一定量的硫酸铜溶液中加入铁粉
D.向一定量的MnO2中加入H2O2溶液
5.下列曲线能正确表达对应的反应或过程的是
A.向一定量的盐酸中逐滴加水稀释
B.某温度下将一定量接近饱和的KNO3溶液恒温蒸发水分
C.金属与一定量的稀硫酸反应,由图像可知,金属N比金属M活泼
D.将a、b、c三种物质的饱和溶液分别由t1℃升温至t2℃时,所得溶液中溶质质量分数大小关系是:
a>b>c
6.甲、乙两种物质的溶解度曲线如图所示,下列说法正确的是()
A.
时,甲物质的饱和溶液溶质质量分数为50%
B.乙物质的溶解度小于甲物质的溶解度
C.
时,乙的饱和溶液降温至
,乙溶液变为不饱和溶液
D.当甲中含有少量乙时,可以用降温结晶提纯甲
7.取一定质量的CaCO3高温煅烧一段时间后冷却,测得剩余固体为12.8g,向剩余固体中加入200g稀盐酸,恰好完全反应,得到208.4g不饱和溶液。
则加热前碳酸钙的质量为
A.15gB.18gC.20gD.30g
8.下列制备物质的设计中,理论上正确,操作上可行。
经济上合理的是
B.
D.
9.下列物质的鉴别、除杂的试验中所用的试剂或方法正确的是( )
实验目的
所用试剂或方法
鉴别CO和CO2
闻气味
鉴别稀硫酸和稀盐酸
加氯化钡溶液
除去生石灰中杂质石灰石
除去氧化铜中碳粉
加稀硫酸
10.将6g碳放在盛有12g氧气的密闭容器中燃烧,两者恰好完全反应,此时密闭容器中的物质是
A.COB.CO2C.CO、CO2D.无法确定
11.下列说法正确的是
A.将草木灰(含K2CO3)与氯化铵混合施用能增加肥效
B.用Ba(NO3)2除去ZnCl2溶液中的ZnSO4杂质
C.只用一种试剂即可鉴别NaCl、NH4NO3、(NH4)2SO4、Na2SO4四种无色溶液
D.不用其它试剂无法鉴别Na2CO3、K2SO4、BaCl2、HCl四种无色溶液
12.在相同的温度和压强下,相同体积的气体具有相同的分子数,反之亦然。
取20℃和101kPa下相同体积的CH4和O2混合,在一定条件下充分反应,恢复到初始温度和压强。
下列说法正确的是()
A.参加反应的CH4和O2的体积比为1:
1
B.生成的CO2分子个数为原来气体分子数的三分之一
C.反应后气体的体积为原来的二分之一
D.反应后的气体中C、O原子的个数比为1:
2
13.除去下列物质中混有的少量杂质(括号内为杂质),所用方法正确的是()
A.CaCO3固体(CaO固体)—高温煅烧
B.N2气体(O2气体)——通过灼热的铜网
C.CO2气体(CO气体)——在氧气中点燃
D.KCl溶液(CaCl2溶液)——加碳酸钠溶液至恰好完全反应,过滤
14.将盛有等质量、等溶质质量分数的稀硫酸的两只烧杯,放在托盘天平(灵敏度较高)左右两盘上,调节至平衡,再向两只烧杯中分别放入质量相等的铁和锌,待反应停止后(不考虑反应中水分挥发,不考虑空气成分参加反应),请判断,下列说法合理的是
A.若天平失去平衡,指针一定偏向放锌的一边
B.若天平仍保持平衡,烧杯中的铁一定没有剩余
C.反应后两只烧杯中溶液的质量都比反应前的溶液质量减轻了
D.放铁的一边产生的氢气一定比放锌的一边产生的氢气多
15.向一定质量AgNO3和Cu(NO3)2的混合溶液中加入Zn,溶液质量与加入Zn的质量关系如图所示。
下列说法正确的是
A.取a点溶液,滴加稀盐酸,无白色沉淀
B.c点溶液中溶质为Zn(NO3)2
C.若取b~c段固体,滴加稀盐酸,有气泡产生
D.取d点的固体有2种
16.在一定质量的甲溶液中逐渐加入乙至过量,反应过程中溶液的总质量与加入乙的质量关系,能用下图曲线表示的是
序号
甲
乙
①
H2SO4溶液
NaOH溶液
②
HCl溶液
大理石
③
BaCl2溶液
Na2SO4溶液
④
锌粒
A.①②B.②④C.②③④D.①②④
17.如图所示,其中甲、乙、丙、丁、戊分别是铁、盐酸、氢氧化钙、二氧化碳、碳酸钠中的一种。
图中相连的两圆表示相应物质能发生反应,已知乙是铁。
下列说法错误的是
A.五种物质中,只有铁是单质
B.丙是氢氧化钙
C.戊是二氧化碳、甲是碳酸钠
D.甲、丙、丁之间的反应属于复分解反应
18.下列四个图象能正确反映实验变化关系的有()
19.下列有关物质的提纯、除杂和鉴别所用的试剂或方法错误的是()
所加物质或方法
提纯硫酸钠中的硝酸钠
溶解、加适量的硝酸钡溶液,过滤,洗涤,干燥
B
除去氧化铜中的碳粉
在足量的空气中灼烧
除去CO2中少量的HCl
将混合气体通入饱和碳酸氢钠溶液、再通入浓硫酸
D
鉴别NaCl固体和NaOH固体
加水溶解
20.下列各组对比实验,能达到实验目的的是:
实验方案
实验①
实验②
探究碘在汽油和植物油中的溶解性
探究温度对反应剧烈程度的影响
探究催化剂对反应快慢的影响
探究CO2的化学性质
21.现有铁、氧化铁、稀盐酸、氢氧化钙溶液、碳酸钠溶液五种物质,存在如图所示的反应和转化关系。
图中“—”表示两端物质间可发生化学反应,“→”表示物质间存在相应的转化关系。
下列判断合理的是
A.X、Y、M两两间都可以发生复分解反应
B.X一定是碳酸钠溶液
C.Y可能是稀盐酸
D.N转化为铁的反应属于置换反应
22.下列实验能达到目的的是
分离溶液中的NaCl和CuSO4
检验蜡烛燃烧生成的水
检验CO32-的存在
测溶液pH
23.常温下,在饱和石灰水中加少量生石灰,溶液中的相关量随时间变化描述正确的是
24.把一定量氧化铜和0.8g氧化镁的混合物投入到溶质质量分数为9.8%的稀硫酸中,待固体完全溶解后,再往溶液里加入溶质质量分数为8%的NaOH溶液,生成沉淀质量与加入溶液质量关系如图所示。
下列说法中正确的是
A.稀硫酸的质量为120g
B.a的取值范围为0<a<60
C.当a值为60时,b值为4.8g
D.混合物的质量可能为7.0g
25.除去下列各组物质中的杂质,所用试剂和方法均正确的是
物质
杂质
除杂所用的试剂和方法
CaO
CaCO3
加入适量的稀盐酸,蒸发
H2
HCl
依次通过NaOH溶液、浓硫酸
Ca(OH)2
先加入过量的Na2CO3溶液,再过滤
KCl溶液
CuCl2
加入氢氧化钠溶液至不再产生沉淀,过滤
二、流程题
26.纯碱是一种重要的有机化工原料,主要用于平板玻璃、玻璃制品和陶瓷釉的生产。
还广泛用于生活洗涤、酸类中和以及食品加工等。
(一)侯德榜是我国著名科学家,1933年出版《纯碱制造》一书,创立了中国自己的制碱工艺。
其纯碱制造原理如图所示:
(1)NH3和CO2通入饱和食盐水的顺序是___________(填字母序号)。
A先通NH3,后通CO2B先通CO2,后通NH3
(2)NaHCO3在水中溶解度相对比较小,以沉淀形式析出,图中“操作”的名称是___________,该操作中使用的玻璃仪器有烧杯、漏斗和___________。
(二)为了充分利用副产品NH4Cl,利用NH4Cl生产NH3和HCl。
(1)方法一:
直接加热分解NH4Cl。
但是这种方法获得NH3和HCl的产率往往很低,原因是___________(用化学反应方程式表示)。
(2)方法二:
采用MgO循环分解NH4Cl。
加热,在300℃以下获得NH3;
继续加热至350℃~600℃获得HCl气体。
利用下列装置(加热及加持装置略)可测量NH3和HCl的产率。
①低于300℃时,干燥管盛装的干燥剂是___________。
NH3吸收完全后,更换干燥剂和吸收装置中的吸收液。
②产生NH3的化学反应方程式是___________。
③在350℃~600℃,如图虚线框内应选择的安全瓶是___________。
④侯氏制碱法在滤去碳酸氢钠的母液中通氨气并加入细小食盐颗粒,冷却析出副产品,通氨气的作用是:
①___________;
②使NaHCO3转化为Na2CO3,提高析出的NH4Cl纯度。
27.某钢铁厂高炉炼铁的主要原料是焦炭,赤铁矿石(主要含Fe2O3)、空气等,主要反应过程如下(省略部分反应物、生成物和反应条件):
请回答:
(1)反应②的化学方程式___________________________________。
(2)反应③的化学方程式___________________________________。
(3)向硝酸银和硝酸铜的混合溶液中,加入一定量的铁粉,反应停止后过滤,得到滤渣和滤液。
向滤渣中滴加稀盐酸,无气泡产生,则滤渣中一定含有_______(填化学式),滤液中一定含有的溶质是___________(填化学式)。
(4)钢铁厂使用含氧化铁80%的赤铁矿炼铁,若每日铁产量为112t,则钢铁厂每日消耗铁矿石_________t。
28.某学习小组欲从高锰酸钾制氧气的剩余物中回收副产物,设计了如下图所示的实验方案:
(资料卡片)
①KMnO4在中性溶液中比较稳定,碱性环境中加热KMnO4溶液会有部分KMnO4和H2O反应,生成MnO2;
②锰酸钾溶于水为墨绿色,不稳定,在水溶液中能全部转化为KMnO4、MnO2和KOH,反应的化学方程式如下:
3K2MnO4+2H2O═2KMnO4+MnO2↓+4KOH
(实验方案)
(1)将剩余物加入水中,观察到的现象是:
①部分固体溶解;
②有少量不溶物出现;
③_____。
(2)回收物甲是_____(