初中化学知识点专练 21 溶液C卷.docx
《初中化学知识点专练 21 溶液C卷.docx》由会员分享,可在线阅读,更多相关《初中化学知识点专练 21 溶液C卷.docx(10页珍藏版)》请在冰豆网上搜索。
初中化学知识点专练21溶液C卷
2020年初中化学知识点专练21溶液C卷
一、填空题(共12题;共59分)
1.(5分)化学就在我们身边,它与我们的生产、生活息息相关。
现有干冰、熟石灰、钛合金金刚石四种物质,请选择适当的物质填空。
①可用于人工降雨的是________;
②可用于制造人造骨的是________;
③可用于改良酸性土壤的是________;
④可用于切割玻璃的是________。
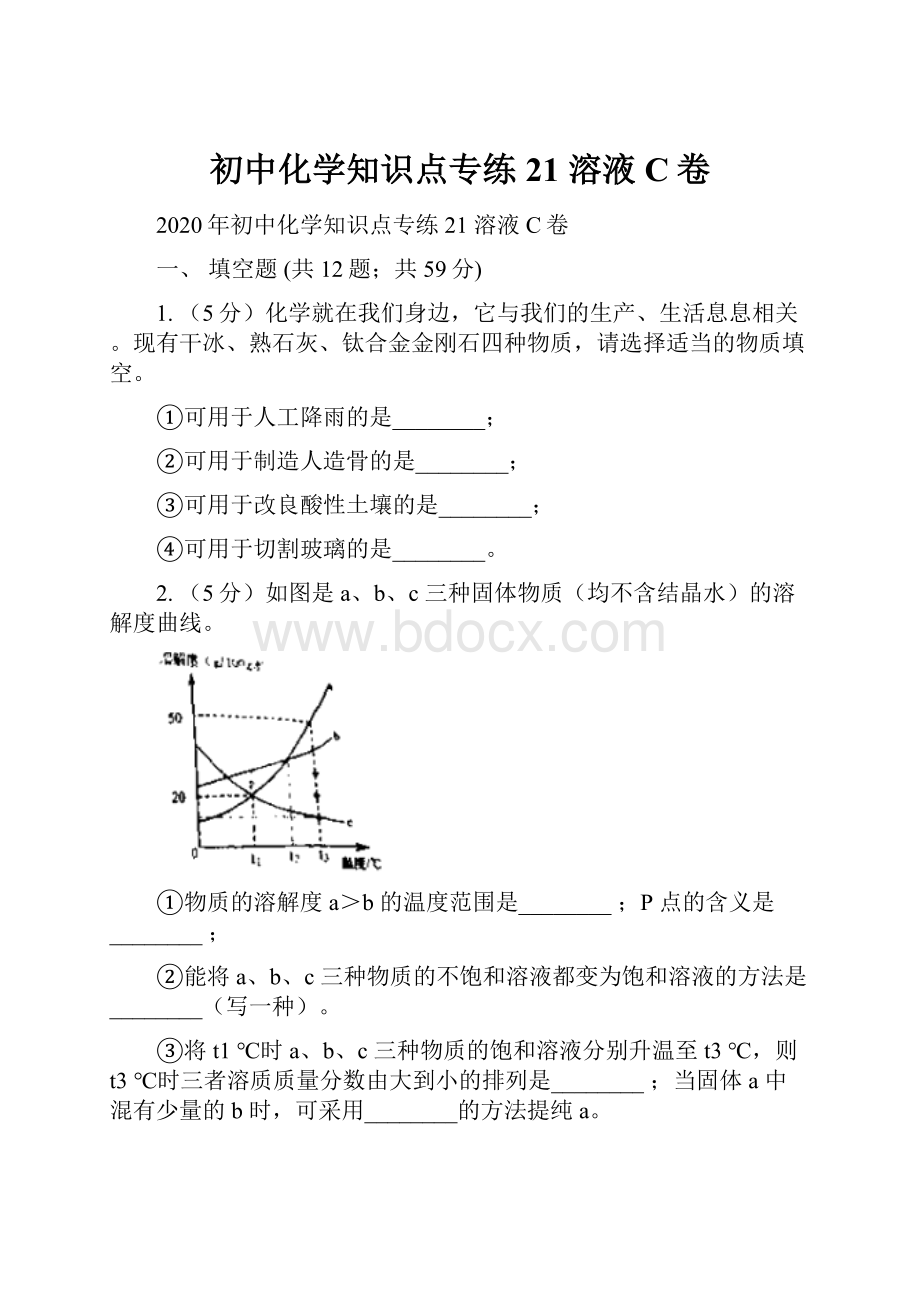
2.(5分)如图是a、b、c三种固体物质(均不含结晶水)的溶解度曲线。
①物质的溶解度a>b的温度范围是________;P点的含义是________;
②能将a、b、c三种物质的不饱和溶液都变为饱和溶液的方法是________(写一种)。
③将t1℃时a、b、c三种物质的饱和溶液分别升温至t3℃,则t3℃时三者溶质质量分数由大到小的排列是________;当固体a中混有少量的b时,可采用________的方法提纯a。
④t3℃时将35ga物质加入到有60g水的烧杯中充分溶解,所得溶液的质量为________g,所得溶液的质量分数为________,如果要改变该溶液中溶质的质量分数,采取的方法有________。
3.(3分)如图是硝酸钾溶解度曲线.
(1)硝酸钾溶液中的溶质是________.
(2)从右图曲线可以得到的信息是_________(写一条即可).
(3)小明在20℃时进行了如下实验,得到相应的溶液①~⑤,下列说法正确的是________.
A.④中溶质的质量分数最大 B.②、⑤中溶质的质量分数相等
C.①、③、④中没有固体存在 D.②、④、⑤的溶液为饱和溶液
4.(5分)根据给出的KNO3和NaCl两种物质的溶解度表,回答下列问题。
温度(℃)
0
20
40
60
80
100
溶解度(g)
KNO3
13.3
31.6
63.9
110
169
246
NaCl
35.7
36.0
36.6
37.3
38.4
39.8
(1)20℃时,KNO3和NaCl中________的溶解度较大;
(2)KNO3和NaCl中,更适合用“冷却热饱和溶液”的方法从溶液中获得较多晶体的是:
________;
(3)60℃时,饱和KNO3溶液中溶质和溶剂的质量比为________。
5.(5分)
(1)如图所示,氯化铵和硝酸钾溶解度曲线。
根据相关信息完成下列问题:
①t2℃时,硝酸钾的溶解度________氯化铵的溶解度(填“<”或“=”)
②________℃时,氯化铵饱和溶液与硝酸钾饱和溶液的溶质质量分数相等;
③t2℃时,100g水中加入60g氯化铵,充分搅拌,得到的氯化铵溶液的质量为________g,该溶液的溶质质量分数为________(只列出算式,不计算结果)。
④硝酸钾中混有少量的氯化铵,想要得到纯净的硝酸钾的方法是________ 。
(2)M是硝酸钾或氯化铵中的一种。
用物质M进行了如图所示实验。
①物质M是________ (填“硝酸钾”或“氯化铵”);
②将t2℃时A烧杯中的不饱和的M溶液变成饱和溶液,下列方法中一定能达到目的的有________(填字母序号)。
a.升温b.降温c.加溶质Md.加水e.恒温蒸发水f.与t2℃时M的饱和溶液混合
6.(5分)(2015•庆阳)如图是甲、乙两种固体物质的溶解度曲线.
(1)在温度为 ________℃时,甲、乙两种物质的溶解度相等.
(2)甲、乙两物质中,通过降温的方法能将接近饱和溶液变为饱和溶液的是 ________.
(3)t2℃时,将35g甲物质投入到50g水中,充分溶解后可得到甲溶液 ________g.
(4)将t2℃甲、乙两物质的饱和溶液分别降温到t1℃,溶液中溶质质量分数大小关系为甲 ________乙(填“>”、“<”或“=”).
7.(3分)NaCl、KNO3物质的溶解度曲线如图
①a点表示的意义是20℃时,在________中最多溶解硝酸钾31.6克。
②60℃时,50克水中加入________克硝酸钾恰好形成饱和溶液,再往该溶液中加入115克水后,硝酸钾溶液的溶质质量分数是________。
③提纯混合溶液中的硝酸钾,进行如下实验。
操作III为下图中的________(填序号),溶液M中所含溶质为________。
④20℃时,将等质量的NaCl、KNO3固体分别加入到盛有100g水的烧杯中,充分搅拌后现象如图1,加热到60℃时现象如图2(不考虑水分蒸发)。
根据NaCl、KNO3物质的溶解度曲线回答:
甲烧杯中的加入固体是________(填“KNO3”或“NaCl”)。
对乙烧杯中溶液的分析,正确的是________(选填编号)
Ⅰ.从20℃升温到60℃过程中,溶质质量没有改变
Ⅱ.20℃时,其中溶质与溶剂的质量比为31.6:
100
Ⅲ.将溶液从20℃降温,一定会析出晶体
Ⅳ.60℃时,乙烧杯中溶液一定是不饱和溶液
8.(5分)将t2℃时将一定量的甲物质加入100g水中,完全溶解,再降温至t1℃,析出10g甲,则t2℃加入甲的质量为________g;将t2℃时乙的饱和溶液浓度变大应采取的方法有________。
9.(6分)学习化学能使我们更好地认识生活中的有关现象,更合理地解决实际问题.
(1)铝和铜常用于制造电线,是用到了铝和铜的________性.
(2)衣服上沾上了较多的油污时,可用汽油洗去的原因是________.
(3)防止铁锅生锈的方法是(写一条)________.
(4)25m3的石油气在加压的情况下可装入容积0.024m3的钢瓶中,原因是________.
10.(9分)如表是氯化钠和碳酸钠在不同温度时的溶解度,根据此表回答:
温度/℃
10
20
30
40
溶解度/g
氯化钠
35.8
36.0
36.3
36.6
碳酸钠
12.2
21.8
39.7
53.2
①由表中数据可知,溶解度随温度变化较大的物质是________,氯化钠与碳酸钠溶解度相等的温度范围是________至________℃.
②10℃时,分别配制表中两种物质的饱和溶液,其中溶质质量分数较大的物质是________;20℃时,100g水最多能溶解________gNaCl;
③向烧杯中加100g水和50.0g碳酸钠配成40℃的溶液,再冷却到20℃,烧杯中析出固体为________g(不考虑结晶水);若在碳酸钠溶液中混有少量的氯化钠,则分离的方法可采用________.
11.(3分)水和溶液在生命活动和生产、生活中起着十分重要的作用。
(1)电解水实验揭示了水的组成。
右图实验中得到氢气的试管是________(填“1”或“2”);电解水的微观示意图如下,请在方框中补全相应微粒的图示________ 。
(2)农业生产常用溶质的质量分数为10%~20%的NaCl溶液来选种。
现将600g25%的NaCl溶液稀释为15%的NaCl溶液,需要加水的质量为________g。
(3)根据下表回答问题。
温度/℃
0
20
40
60
80
100
溶解度
/g
NaCl
35.7
36.0
36.6
37.3
38.4
39.8
NH4Cl
29.4
37.2
45.8
55.2
65.6
77.3
①40℃时,向两个分别盛有40gNaCl和NH4Cl的烧杯中,各加入100g的水,充分溶解后,为饱和溶液的是________溶液。
②采用一种操作方法,将上述烧杯中的剩余固体全部溶解,变为不饱和溶液。
下列说法错误的是________(填字母序号)。
A.溶质的质量不变
B.溶液质量一定增大
C.可升高温度或增加溶剂
D.溶液中溶质的质量分数一定减小
12.(5分)为了测定粗盐(混有少量的泥沙及可溶性杂质)中氯化钠的纯度,进行如下操作:
①a.计算产率,b.过滤,c.溶解,d.蒸发,e.称量粗盐,f.称量精盐。
实验步骤的正确顺序是:
________、a(填编号)。
②称量时正确的操作次序是________(填字母序号)。
a.校正,b.去皮,c.放称量纸,d.放食盐,e.读数
③过滤时用到的玻璃仪器有玻璃棒、烧杯、________,其中玻璃棒的作用是________。
实验过程中发现过滤两次滤液仍然浑浊,可能的原因是(写一点)________。
④最后得到的精盐属于________(填“混合物”或“纯净物”)。
组别
1
2
3
4
产率
75%
65%
88%
72%
教师评价
偏低
偏低
偏高
偏低
⑤已知:
产率=
×100%。
各小组的产率及评价如下,对造成产率偏高或偏低的原因分析,正确的是________。
A.第1组:
烧杯里的食盐未溶解完就开始过滤
B.第2组:
没有蒸发干,精盐中仍然有水分
C.第3组:
滤液浑浊就开始蒸发
D.第4组:
过滤时滤液高于滤纸的边缘
参考答案
一、填空题(共12题;共59分)
1-1、
2-1、
3-1、
3-2、
3-3、
4-1、
4-2、
4-3、
5-1、
5-2、
6-1、
7-1、
8-1、
9-1、
9-2、
9-3、
9-4、
10-1、
11-1、
11-2、
11-3、
12-1、