人教版学年九年级第一学期期末考试化学试题I卷.docx
《人教版学年九年级第一学期期末考试化学试题I卷.docx》由会员分享,可在线阅读,更多相关《人教版学年九年级第一学期期末考试化学试题I卷.docx(11页珍藏版)》请在冰豆网上搜索。
人教版学年九年级第一学期期末考试化学试题I卷
人教版2019-2020学年九年级第一学期期末考试化学试题(I)卷
姓名:
________班级:
________成绩:
________
一、单选题
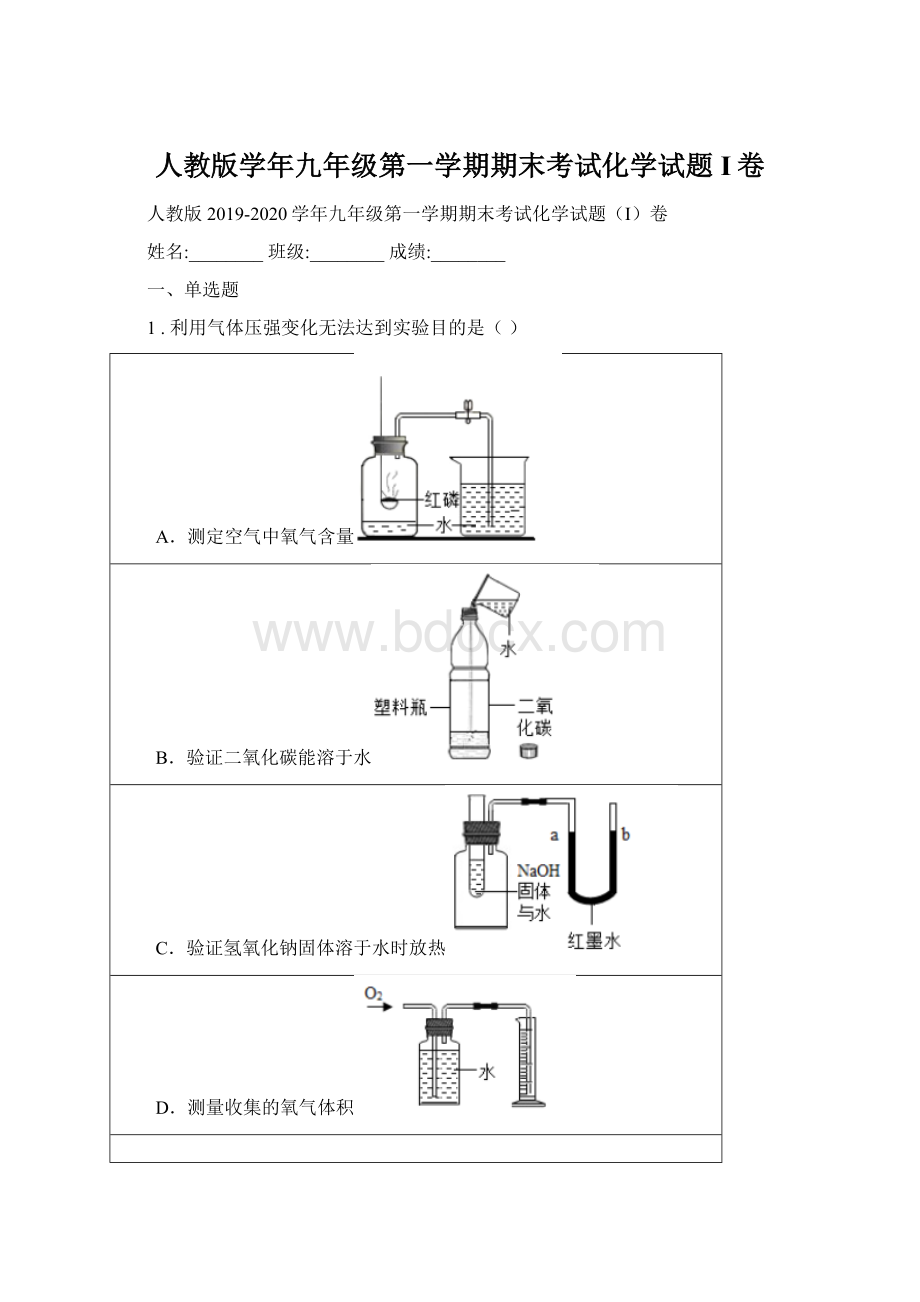
1.利用气体压强变化无法达到实验目的是()
A.测定空气中氧气含量
B.验证二氧化碳能溶于水
C.验证氢氧化钠固体溶于水时放热
D.测量收集的氧气体积
2.下列关于饱和溶液的说法,正确的是 ()
A.饱和溶液降温一定析出晶体
B.不饱和溶液降温不一定能得到饱和溶液
C.溶液加入溶质质量分数必然一定增大
D.恒温蒸发少量溶剂一定能得到饱和溶液
3.下列反应的化学方程式不正确的是
A.用胃舒平(主要成分是AI(OH)3)治疗胃酸过多症:
2Al(OH)3+3H2SO4=Al2(SO4)3+6H2O
B.用熟石灰处理硫酸厂排放的污水:
Ca(OH)2+H2SO4═CaSO4+2H2O
C.用烧碱溶液处理炼铜厂用黄铜矿(CuFeS2)、辉铜矿(Cu2S)炼铜排出的废气中的二氧化硫:
SO2+2NaOH═NaSO3+H2O
D.新使用的铝桶或铝壶,浸水部分变黑:
2Al+Fe2(SO4)3═Al2(SO4)3+2Fe
4.取2%的NaOH溶液20g和2%的HCl溶液20g,使其充分反应,所得到的溶液能使紫色石蕊试液显
A.红色
B.蓝色
C.无色
D.紫色
5.分离、除杂、提纯和检验是化学实验的重要环节。
下面实验设计能够达到目的的是()
A.A
B.B
C.C
D.D
6.下列有关实验现象的描述中,正确的是
A.加热试管内的碱式碳酸铜,绿色粉末逐渐变黑,试管口有小水滴
B.细铁丝在氧气中燃烧,火星四射,生成红棕色固体
C.镁条在空气中燃烧,产生黑烟,生成黑色粉末
D.向少量氧化铜中加入稀硫酸,有气泡产生,黑色粉末逐渐消失,溶液变蓝
7.下列物质中,不能使紫色石蕊溶液变色的是
A.稀盐酸
B.食盐水
C.石灰水
D.白醋
8.结合下图判断,下列说法正确的是
A.硝酸钾的溶解度为45.8g
B.硝酸钾的溶解度大于氯化钠的溶解度
C.升高温度可将硝酸钾的不饱和溶液变为饱和溶液
D.两条曲线的交点所对应溶液的溶质质量分数相等
9.若分别将100g甲、乙的饱和溶液从t2℃降温到t1℃,对所得溶液的叙述正确的是()
A.甲、乙都是饱和溶液
B.溶质质量分数:
甲=乙
C.溶液质量:
甲>乙
D.所含溶剂质量:
甲<乙
10.将CO、CO2、H2、N2的混合气体依次通过灼热的氧化铜、氢氧化钠溶液、浓硫酸,最后剩余的气体是()
A.N2和CO
B.H2和N2
C.CO2和N2
D.只有N2
11.下列关于溶液颜色的判断不正确的是()
A.氯化亚铁溶液是黄色的
B.高锰酸钾溶液是紫红色的
C.硫酸铜溶液是蓝色的
D.葡萄糖水是无色的
12.胃液中含有胃酸,其主要成分是
A.盐酸
B.硫酸
C.硝酸
D.醋酸
13.下列离子在pH=1的溶液中能大量存在的是
A.CO32—
B.HCO3—
C.OH—
D.Cl—
14.30℃时,向两支试管中加入等质量的甲和乙,分别加入10g水,使其充分溶解,观察到如下图1所示的实验现象。
下列说法中,正确的是
A.图2中的a表示甲的溶解度
B.要使甲物质完全溶解可以采取升温的办法
C.30℃时甲的饱和溶液中溶质的质量分数小于乙
D.将乙溶液降温到10℃,乙溶液的质量分数一定减小
15.下列各组物质分别加入到足量的水中,能共存且得到无色透明溶液的是()
A.KNO3、NaCl、HCl
B.FeCl3、Na2SO4、KCl
C.Na2CO3、H2SO4、NaCl
D.MgCl2、KCl、NaOH
二、填空题
16.在实验室里可用以下两种方法配制质量分数为10%的NaOH溶液
(1)方法一中配制100g10%的NaOH溶液,需要NaOH固体___________g。
(2)方法二中用量筒量取25%的NaOH溶液时仰视读数,其他操作均正确,所配溶液中溶质的质量分数___________10%(选填“大于”、“小于”或“等于”);
(3)方法一中的“溶解”和方法二中的“混匀”,都要用到的仪器是___________。
17.回答下列实验中的有关问题。
A
B
C
(1)A中正极产生气体的检验方法是_____。
(2)B中通过比较①②塑料瓶变瘪的不同,可得出的结论是_____。
(3)C中可观察到的现象是_____,反应的化学方程式是_____。
三、简答题
18.20℃时,将等质量的甲、乙两种固体(不含结晶水),分别加入到盛有100g水的烧杯中,充分搅拌后现象如图1所示,加热到50℃时现象如图2所示,甲、乙两种物质的溶解度曲线如图3所示。
请回答下列问题:
(1)图2中乙溶液一定是______溶液(填“饱和”或“不饱和”)。
(2)图3中表示乙的溶解度曲线的是______(填“M”或“N”):
图2中乙溶液降温至30℃______析出晶体(填“会”或“不会”)。
(3)50℃时甲的饱和溶液中溶质质量分数为______(计算结果精确到0.1%)。
19.根据如表回答问题
温度(℃)
20
40
50
60
80
溶解度
(g/100g水)
NaCl
36.0
36.6
37.0
37.3
38.4
NH4Cl
37.2
45.8
50.4
55.2
65.6
KNO3
31.6
63.9
85.5
110
169
(1)50℃时,100g水中最多溶解NaCl______g
(2)A是80℃含有120g水的KNO3溶液,经过如下操作,得到102gKNO3固体。
①A溶液为________(选填“饱和”或“不饱和”)溶液
②对以下过程的分析,正确的是_________(选填编号)
a.A到B的过程中,溶质质量没有改变 b.B中溶质与溶剂的质量比为169:
100
c.A溶液的质量等于222g d.开始析出KNO3固体的温度在60℃至80℃之间
四、推断题
20.A、B、C、D、E是初中所学的常见物质。
B、C、D常温下为气体,且B、C组成元素相同,A、E是黑色粉末。
它们转化关系如下(部分物质及反应条件省略):
(1)A的化学式为_______________;C的化学式为____________________;
(2)写出A+E反应的化学方程式__________;B→C的反应属于__________类型;
(3)列举一例B在生活中的用途__________________。
五、科学探究题
21.如图所示,小娟同学在进行酸碱中和反应的实验时,向烧杯中氢氧化钠溶液滴加稀盐酸一会儿后,发现忘记了滴加指示剂。
为了确定盐酸与氢氧化钠是否恰好完全反应,小娟从烧杯中取少量反应后的溶液于一支试管中,并向试管中滴加几滴无色酚酞试液,振荡,观察到酚酞试液不变色。
于是她得出“两种物质已恰好完全中和”的结论。
(1)你认为她得出的结论是否正确_____;理由是__________。
(2)学习小组的同学们欲探究“NaOH和HCl是否恰好完全反应”,他们设计了如下实验方案,请你和他们一起完成:
实验方法
可能观察到的现象
结论
方案一
用玻璃棒蘸取反应后的溶液滴在pH试纸上,并与标准比色卡对比
pH试纸的颜色与标准比色卡上pH为7处的颜色一致(浅黄色)
_____
方案二
取反应后的水少量溶液于试管中,加入几颗锌粒
_____
盐酸已完全反应
再取反应后的少量溶液于另一支试管中,滴加_____溶液
_____
氢氧化钠已完全反应
六、计算题
22.如下图为几种固体的溶解度曲线,回答下列问题:
(1)CuSO4的溶解度约为20g时,其对应的温度是_______℃;若想使该饱和溶液转化为不饱和溶液,可采取的方法是______(写出一种即可),用此方法后,溶液的质量分数____(填“有”或“没有”)发生变化。
(2)80℃时,140gNaNO3溶于100g水形成的溶液 是_______溶液(填“饱和”或“不饱和”)。
(3)20℃时,NH4NO3溶液的溶质质量分数最大为___________(计算结果保留到0.1%)。
(4)若KNO3溶液中混有少量的NaCl杂质,可以采取______方法获得较纯净的KNO3固体。
(5)60℃时分别将等质量的KNO3、NaCl、CuSO4的 饱和溶液各500g恒温蒸发掉100g水,析出晶体
最多的是____。
(6)60℃时,10gNaCl和90gKNO3完全溶解于100g蒸馏水中,冷却到30℃后,_________(“有”或“没有”)NaCl析出,有______________gKNO3结晶析出。
23.如图所示,用干燥的20g的烧杯做铁粉和稀硫酸反应的实验,假设稀硫酸反应完全且生成气体全部逸出。
请计算。
(1)生成H2的质量为___________g。
(2)稀硫酸中溶质质量分数为_______?
参考答案
一、单选题
1、
2、
3、
4、
5、
6、
7、
8、
9、
10、
11、
12、
13、
14、
15、
二、填空题
1、
2、
三、简答题
1、
2、
四、推断题
1、
五、科学探究题
1、
六、计算题
1、
2、