浙教版九年级科学上册第一章酸碱盐集训.docx
《浙教版九年级科学上册第一章酸碱盐集训.docx》由会员分享,可在线阅读,更多相关《浙教版九年级科学上册第一章酸碱盐集训.docx(13页珍藏版)》请在冰豆网上搜索。
浙教版九年级科学上册第一章酸碱盐集训
浙教版九年级上册第一章酸碱盐集训
姓名:
________班级:
________成绩:
________
一、选择题
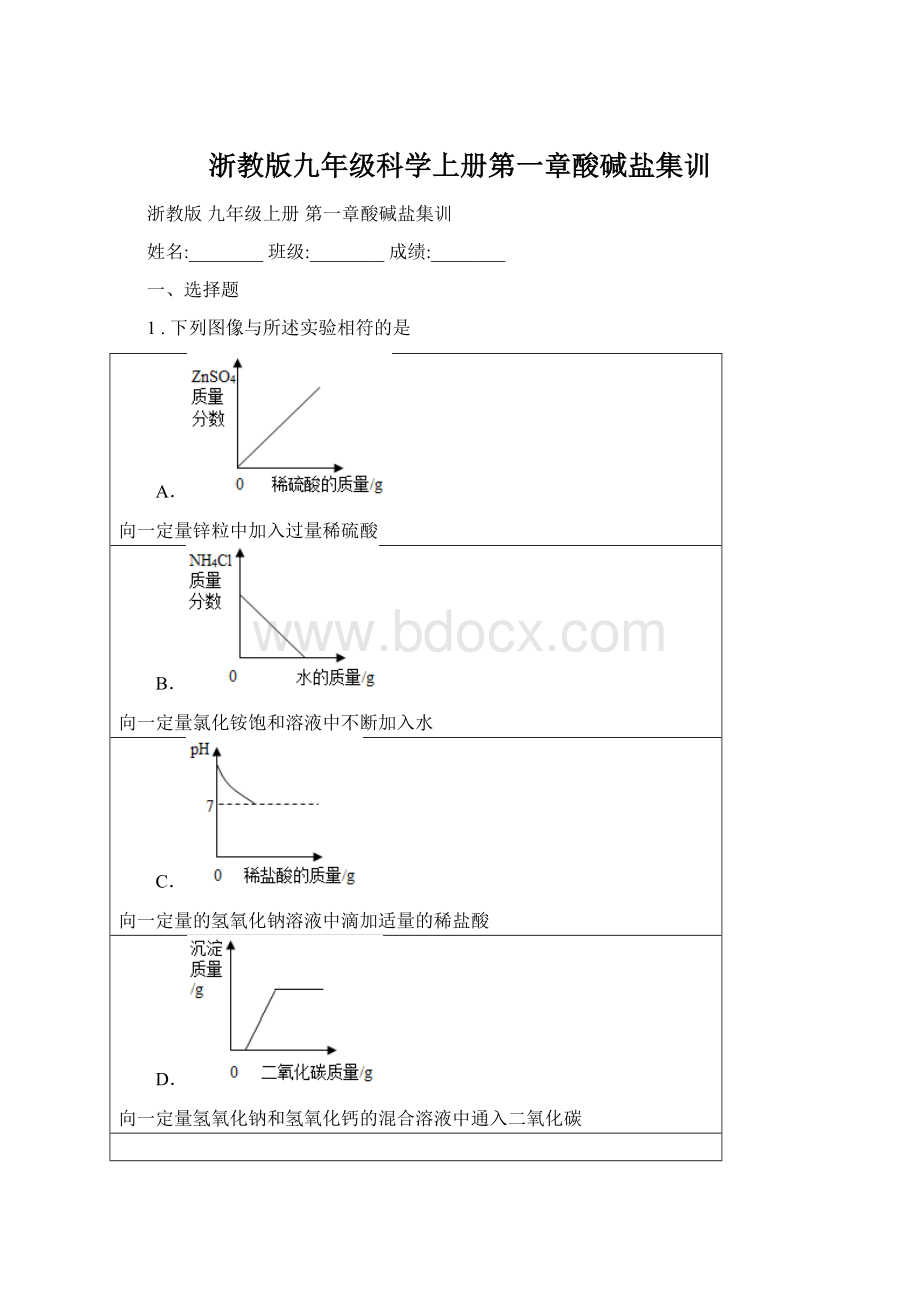
1.下列图像与所述实验相符的是
A.
向一定量锌粒中加入过量稀硫酸
B.
向一定量氯化铵饱和溶液中不断加入水
C.
向一定量的氢氧化钠溶液中滴加适量的稀盐酸
D.
向一定量氢氧化钠和氢氧化钙的混合溶液中通入二氧化碳
2.在反应2A+3B===2C+4D中,若A、B、C、D的质量比为8∶12∶11∶9,则A、B、C、D的相对分子质量之比为()
A.8∶12∶11∶9
B.16∶36∶22∶36
C.16∶16∶22∶9
D.2∶3∶2∶4
3.为了中和溶质质量分数一定的氢氧化钠溶液,要消耗一定量的盐酸,如改用与盐酸质量分数相同的等质量的硝酸,则反应后的溶液的pH()
A.等于7
B.大于7
C.小于7
D.等于0
4.类推是学习中常用的思维方法,现有以下类推结果,其中错误的是()
①碱的水溶液通常呈碱性,所以碱性溶液一定是碱的溶液
②氧化物都含有氧元素,所以含氧元素的化合物不一定是氧化物
③酸碱发生反应生成盐和水,所以生成水的反应一定是酸碱反应
A.只有①
B.①②
C.①③
D.①②③
5.分类是科学研究的重要方法,下列物质对应的类别不正确的是()
选项
A
B
C
D
物质
H2O2
O3
CH3COOH
Cu(OH)2
类别
氧化物
化合物
酸
碱
A.A
B.B
C.C
D.D
6.下列说法正确的是()
①浓盐酸会在空气中形成白烟 ②液态氯化氢就是盐酸 ③盐酸遇石蕊变红④浓盐酸受热易分解
A.①
B.②和③
C.③和④
D.都不对
7.下列说法正确的是
A.测硫酸溶液pH时,用玻璃棒蘸取溶液滴在湿润的pH试纸上,会使测得pH值偏小
B.浓硫酸露置于空气中,溶质的质量分数变小
C.烧碱的“潮解”和碳酸钠晶体的“风化”均属化学变化
D.稀释浓硫酸时,将水沿烧杯壁慢慢注入浓硫酸中,并用玻璃棒不断搅拌
8.向200gAgNO3溶液中加入m克Fe和Cu的混合粉末,搅拌,充分反应后过滤、洗涤、于燥得32.4g固体。
向滤液中滴加NaCl溶液,产生白色沉淀。
下列说法正确的是()
A.滤液的质量是167.6g
B.混合粉末的质量范围是8.4<m<9.6
C.固体中加入稀盐酸可能没有气体生成
D.原AgNO3溶液的溶质质量分数是25.5%
9.通过测定,我们可以得知:
植物
葡萄汁
苹果汁
牛奶
鸡蛋清
pH
3.5~4.5
2.9~3.3
6.3~6.6
7.6~8.0
下列说法正确的是()
A.胃酸过多的人应该多吃苹果;
B.苹果汁的酸性比葡萄汁弱;
C.牛奶和鸡蛋清都是碱性食物;
D.葡萄汁能使紫色石蕊试液变红。
10.下列除杂(括号内的是杂质)所选试剂合理的是()
A.Cu(Zn) 稀盐酸
B.CO2气体(HCl)氢氧化钠溶液
C.CuO(Cu)浓硫酸
D.Na2SO4溶液(Na2CO3) 氯化钡溶液
11.利用括号中的物质除去杂质.其中能达到除杂目的的是()
A.CO2气体中混有CO气体(通入O2点燃)
B.Cu中混有CuO(加入足量的稀盐酸,过滤,洗涤,干燥)
C.氯化钡溶液中混有盐酸(通入过量的氢氧化钡溶液)
D.CaCO3中混有CaCl2(适量稀盐酸)
12.初中化学的很多反应可以表示为:
甲+乙=丙+丁,其中甲、乙、丙、丁既可能是单质也可能是化合物。
下列说法中,正确的是()
A.若甲、乙、丙、丁均是化合物,则该反应一定是复分解反应
B.若甲、乙、丙分别是酸、碱、盐,则丁一定是水
C.若甲是一氧化碳,乙是金属氧化物,则丙一定是二氧化碳
D.若甲是锌,丙是氢气,则乙一定是稀硫酸
13.定义科学概念,可以使科学知识由无序变得有序,使科学如识形成体系。
下列科学概念定义正确的是()
A.生成盐和水的反应叫做中和反应
B.单位时间内完成的功叫做功率
C.生活在一定区域内的同种生物个体的总和叫做种群
D.原子的质量与碳原子质量的比值为该原子的相对原子质量
14.向盛有HCl和CuCl2混合溶液中逐滴加入NaOH溶液至过量,下列4个图像能正确反应烧杯内的某些物理量变化趋势的是()
A.①③
B.①②③
C.②④
D.①②④
15.小明在家里整理厨房时,发现三种可用于科学小实验的物质:
食盐、白醋、白糖。
下面是他设计的利用这些物质所进行的家庭小实验,能成功的是
①检验洗衣粉中是否含SO42-
②做植物细胞失水的实验
③探究鸡蛋壳是否含有碳酸钙
④比较食盐和白糖在相同温度下的溶解能力
A.①②
B.①③
C.②④
D.③④
二、填空题
16.某化学兴趣小组学习酸、碱、盐的性质后,做了如下实验(已知:
BaCl2溶液呈中性,Na2CO3溶液呈碱性,BaCl2+Na2CO3=BaCO3↓+2NaCl).
(1)甲同学将酚酞试液滴入Ba(OH)2溶液中,观察到溶液变红,得出结论:
Ba(OH)2溶液呈___(填“酸性”、“碱性”或“中性”);
(2)乙同学将过量的稀盐酸加入到甲同学所得溶液中,观察到红色褪去,此时所得溶液中含有的溶质有____________________________(用化学式表示,酸碱指示剂除外,下同);
(3)丙同学将Na2CO3溶液与乙同学所得溶液混合,静置后发现:
上层为无色透明的溶液,底部有白色沉淀.则上层溶液中一定含有的溶质是___,可能含有的溶质是___.
17.实验室有一瓶碳酸钙和氯化钙粉末组成的均匀混合物,小科用相同溶质质量分数的稀盐酸和该混合物反应(所得溶液均为不饱和溶液),四组实验数据记录如下表。
请分析计算:
实验组别
一
二
三
四
稀盐酸质量/g
100.0
100.0
100.0
100.0
混合物质量/g
3.0
6.0
9.0
12.0
所得溶液质量/g
101.9
103.8
105.0
a
剩余固体质量/g
0
0
m
n
(1)混合物中能和稀盐酸反应的物质是_____
(2)反应后,稀盐酸还有剩余的是第_____组。
(3)表中a的值为_____。
(4)求混合物中碳酸钙和氯化钙质量之比_____(通过计算说明)。
18.向含AgNO3、Cu(NO3)2、Mg(NO3)2混合液中,加入一定量的锌粒,充分反应后过滤,向滤液中加稀盐酸,没有白色沉淀产生.则滤渣中一定有 ,可能有 。
19.归纳总结是学习化学的重要方法,下面是某同学对有关知识的总结,请你填写空格:
(1)逻辑关系:
物质类属间存在着如下关系,其中酸和盐属于____________关系。
(2)转化关系:
下图表示几种化合物能通过一步反应转化为含镁化合物M。
上图中物质M属于_______(选填“单质”、“氧化物”、“酸”、“碱”或“盐”);
从①—③表示的化学反应中任选一个,写出化学方程式 。
20.小明以化合价为纵坐标,以物质类别为横坐标绘制了如图所示的坐标轴,图中字母代表含硫元素的常见物质。
(1)图中单质a在氧气中燃烧生成的产物是________(填上图字母)
(2)图中d、e、f三种物质都含有的元素除了硫元素外,还有________元素。
(3)若在空气中久置的氢氧化钠溶液中滴加过量d溶液,充分反应后试管中溶液的溶质是________(填化学式)。
21.化学用语是最简明、信息丰富、国际通用的语言,请用化学用语填空:
(1)n个铁离子__________;
(2)碳酸铵__________;
(3)氧化镁中镁元素的化合价为+2价______。
三、探究题
22.(2017·山东菏泽)实验室有一瓶标签残缺并且瓶盖没有完全密封的无色溶液(如图甲所示),科学小组的同学经过询问老师后只知道是NaCl、NaOH、Na2CO3、NaHCO3溶液中的一种,为确认原瓶中是何种溶质并判断其是否变质,科学小组的同学进行了如下的探究活动:
(进行猜想)猜想Ⅰ:
原溶液的溶质是NaCl。
猜想Ⅱ:
原溶液的溶质是NaOH。
猜想Ⅲ:
原溶液的溶质是Na2CO3。
猜想Ⅳ:
原溶液的溶质是NaHCO3。
(查阅资料)常温下,有关物质的相关信息如下表:
物质
NaCl
NaOH
Na2CO3
NaHCO3
常温下的溶解度/g
36
109
21.5
9.6
常温下稀溶液的pH
7
13
11
9
从物质的相关信息可知,原溶液的溶质一定不是NaHCO3,因为________。
(进行实验)
(1)取少量样品,测得溶液的pH大于7,则原溶液的溶质肯定不是________。
(2)同学们另取样品又进行了如图乙所示实验,实验过程如下:
①写出生成白色沉淀A的反应的化学方程式:
_____。
②通过实验可以判断样品无色溶液中含有的溶质有_____。
(获得结论)实验完成后,最终得到的结论:
原瓶中的溶质是____,且已变质。
23.CaO和NaOH固体的混合物,俗名“碱石灰”,实验室常用作干燥剂。
碱石灰在空气中久置会吸收空气中的水和二氧化碳而变质。
某实验小组为确定一瓶久置的碱石灰样品的成分,设计了如图所示实验流程。
请你参与探究过程:
(1)为了使样品充分溶解,操作一定还要用到的玻璃仪器是_________________;操作二的名称是____。
(2)固体A中一定含有_______________________________。
(3)溶液B成分的探究。
(查阅资料)
①Ca(OH)2、Na2CO3溶于水无明显的温度变化;
②Na2CO3溶液呈碱性,能使酚酞试液变红;
③CaCl2溶液呈中性。
(猜想)溶液B中溶质可能为:
①NaOH;②Na2CO3;③NaOH和Na2CO3;④Ca(OH)2和__________
(设计方案并进行实验)甲、乙同学分别设计如下方案并进行探究:
甲同学:
取少量溶液B于试管中,滴加足量的稀盐酸,产生大量气泡,则溶液B中的溶质是Na2CO3。
乙同学:
取少量溶液B于试管中,滴加几滴酚酞试液,溶液变成红色,则溶液B中的溶质一定含有NaOH。
(反思与评价)丙同学认真分析上述二位同学的实验,认为他们的结论均有不足之处,并且做出了正确的判断。
他认为B溶液中一定含有Na2CO3,可能含有NaOH。
为进一步确认溶液B中是否含NaOH,做了如下实验。
实验步骤①中发生的化学反应方程式是____________________________________,其实验目的是__________________________________________________________。
(4)实验过程中,同学们发现向样品中加水时还放出大量的热。
综合以上探究,下列对样品成分分析正确的是____(填序号)。
A.一定有NaOH
B.一定有Na2CO3
C.一定有CaO
D.至少有NaOH、CaO中的一种
24.某次实验中,某同学在3毫升氯化铁溶液中滴入几滴氢氧化钙溶液后,没有观察到红褐色沉淀。
什么原因导致没有沉淀出现呢?
他进行了进一步的探究。
建立猜想:
猜想1:
可能是氯化铁溶液呈酸性。
猜想2:
可能是氢氧化钙溶液变质,导致溶液没有碱性。
(1)请你再提出一个合理猜想:
_____。
(2)该同学想利用实验室的相关药品来验证猜想2,请你帮他完成实验设计:
并描述预期的实验现象。
_____
(3)经过相关实验验证,发现氢氧化钙溶液没有变质。
且猜想1正确。
由此得出结论:
氢氧化钙先与酸性的氯化铁溶液中和反应,所以没有沉淀生成。
据此,在该同学的实验中,你认为如何操作可以得到预期的实验现象:
有红褐色沉淀生成:
_____(写出一种方法即可)。
四、简答题
25.配制一定溶质质量分数的氯化钠溶液”是初中化学的基础实验之一。
请回答下列问题:
(1)现欲配制一瓶75g溶质质量分数为10%的氯化钠溶液,需氯化钠的质量________g。
(2)请用图中的序号表示配制溶液的正确操作顺序________。
(3)认真观察,图中某步骤错误,写出该步骤的正确操作为________。
若不进行改正,其他操作步骤正确,则所配制溶液的溶质的质量分数________(填“大于”、“小于”或“等于”)10%。
(4)实验室若用15%的氯化钠溶液加水稀释成5%的氯化钠溶液,问需要15%的氯化钠溶液________克才可配得120克5%的氯化钠溶液。
26.向200g一定质量分数的CuSO4溶液中先后逐滴滴加100gBa(OH)2溶液后再加入一定量的HCl溶液,反应过程中加入溶液的质量与产生沉淀质量的关系如图所示。
请回答相关问题:
(1)O~a溶液导电性逐渐____(填“增强”或“减弱”)。
(2)通过计算确定m的值。
_____
(3)d点溶液的溶质成分有____(用化学式表示)。
(4)能否计算出Ba(OH)2溶液的溶质质量分数?
若能,请写出计算过程;若不能,请说明理由。
_____
27.市场上出售的牙膏种类繁多,每种牙膏中都添加有细粉末状的摩擦剂,它能配合牙刷一起摩擦牙齿的表面,起到增强清洁牙齿的效果。
下表给出了三种牙膏中的摩擦剂。
牙膏
A
B
C
摩擦剂
氢氧化铝
碳酸钙
二氧化硅
(1)可选作摩擦剂的物质必须 (填“易溶于水”或“难溶于水”)。
(2)碳酸钙可用石灰石制备,小新设计了两种制备碳酸钙的实验方案。
你认为哪一种实验方案更合理,并说明理由 。
(3)小新为了测定B牙膏中碳酸钙的含量。
称取B牙膏100克放入烧杯中,缓慢加入稀盐酸至不再有气泡产生(假设除碳酸钙外,牙膏中的其他物质不与盐酸反应),共用去稀盐酸200克。
反应完毕后,称得烧杯内剩余物质的质量为278克。
①在测定中,反应生成的二氧化碳质量为 克。
②请计算牙膏中碳酸钙的质量分数。
28.在制作“叶脉书签”中,需用到10%的氢氧化钠溶液。
现配制80g质量分数为10%的氢氧化钠溶液。
(l)若用氢氧化钠固体配制,需称量氢氧化钠的质量为________g。
(2)用氢氧化钠固体配制10%的氢氧化钠溶液过程中需要用到的仪器除了托盘天平、药匙、量筒、烧杯、胶头滴管、试剂瓶外,还需要的一个玻璃仪器是________。
(3)本实验中,下列操作正确的是________(可多选)。
A.称量氢氧化钠固体时,右盘放砝码
B.在托盘天平的左右托盘上垫滤纸称量氢氧化钠固体
C.天平平衡后的称量过程中,若指针略偏左,则可向右调节游码
D.将准确称量的氢氧化钠固体放入装有水的量筒中溶解
E.氢氧化钠固体易潮解,称量过程尽量要缩短时间
参考答案
一、选择题
1、
2、
3、
4、
5、
6、
7、
8、
9、
10、
11、
12、
13、
14、
15、
二、填空题
1、
2、
3、
4、
5、
6、
三、探究题
1、
2、
3、
四、简答题
1、
2、
3、
4、