高考化学真题分项解析专题16《化学实验设计与探.docx
《高考化学真题分项解析专题16《化学实验设计与探.docx》由会员分享,可在线阅读,更多相关《高考化学真题分项解析专题16《化学实验设计与探.docx(23页珍藏版)》请在冰豆网上搜索。
高考化学真题分项解析专题16《化学实验设计与探
专题16:
化学实验设计与探究
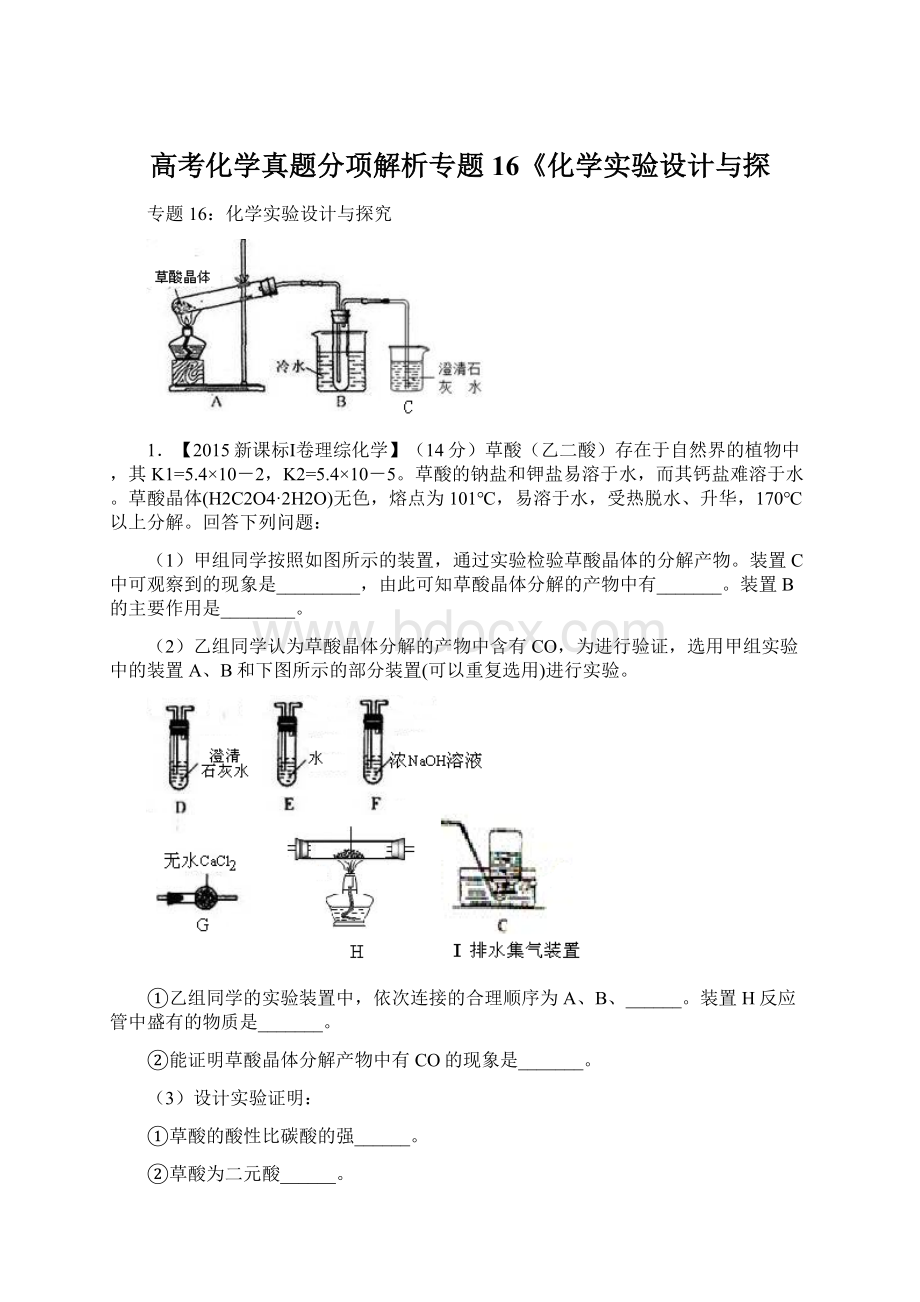
1.【2015新课标Ⅰ卷理综化学】(14分)草酸(乙二酸)存在于自然界的植物中,其K1=5.4×10-2,K2=5.4×10-5。
草酸的钠盐和钾盐易溶于水,而其钙盐难溶于水。
草酸晶体(H2C2O4·2H2O)无色,熔点为101℃,易溶于水,受热脱水、升华,170℃以上分解。
回答下列问题:
(1)甲组同学按照如图所示的装置,通过实验检验草酸晶体的分解产物。
装置C中可观察到的现象是_________,由此可知草酸晶体分解的产物中有_______。
装置B的主要作用是________。
(2)乙组同学认为草酸晶体分解的产物中含有CO,为进行验证,选用甲组实验中的装置A、B和下图所示的部分装置(可以重复选用)进行实验。
①乙组同学的实验装置中,依次连接的合理顺序为A、B、______。
装置H反应管中盛有的物质是_______。
②能证明草酸晶体分解产物中有CO的现象是_______。
(3)设计实验证明:
①草酸的酸性比碳酸的强______。
②草酸为二元酸______。
【答案】
(1)有气泡逸出,澄清石灰水变浑浊;CO2;冷凝(水蒸气、草酸等),避免草酸进入装置C反应生成沉淀,干扰CO2的检验。
(2)①F、D、G、H、D、I;CuO(氧化铜);
②H中的粉末有黑色变为红色,其后的D中的石灰水变浑浊;
(3)①向盛有少量NaHCO3溶液的试管中滴加草酸溶液,有气泡产生。
②用氢氧化钠标准溶液滴定草酸溶液,消耗氢氧化钠的物质的量是草酸的两倍
【考点定位】CO、CO2的性质;化学实验基本知识;化学实验知识的简单应用。
难度为较难等级
△
【名师点晴】相信每个考生看到这道高考题的第一感都是:
题目情景绝对的新颖!
这个实验是我没有做过的!
其实破题的关键是要分析出草酸分解的产物,那个反应(H2C2O4·2H2O===CO2↑+CO↑+3H2O)高中化学里并不常见,我们要学会从题文中捕捉信息来猜想关键产物(CO2来自澄清石灰水的联想,CO来自第二小问),进而用氧化还原反应原理(化合价升降)来验证。
知道发生装置中产生的气体是CO2、CO、H2O(g)、少量草酸蒸气(由“受热脱水、升华”这句联想),后续的实验分析和设计大家基本就会了,一道刚刚谋面的新题就变成你的常规题了。
可以看出:
对你所研究体系的成分进行仔细分析,是好多难题的突破良方。
2.【2015新课标Ⅱ卷理综化学】(15分)二氧化氯(ClO2,黄绿色易溶于水的气体)是高效、低毒的消毒剂,回答下列问題:
(1)工业上可用KC1O3与Na2SO3在H2SO4存在下制得ClO2,该反应氧化剂与还原剂物质的量之比为。
(2)实验室用NH4Cl、盐酸、NaClO2(亚氯酸钠)为原料,通过以下过程制备ClO2:
①电解时发生反应的化学方程式为。
②溶液X中大量存在的阴离子有__________。
③除去ClO2中的NH3可选用的试剂是(填标号)。
a.水b.碱石灰C.浓硫酸d.饱和食盐水
(3)用下图装置可以测定混合气中ClO2的含量:
Ⅰ.在锥形瓶中加入足量的碘化钾,用50mL水溶解后,再加入3mL稀硫酸:
Ⅱ.在玻璃液封装置中加入水,使液面没过玻璃液封管的管口;
Ⅲ.将一定量的混合气体通入锥形瓶中吸收;
Ⅳ.将玻璃液封装置中的水倒入锥形瓶中:
Ⅴ.用0.1000mol·L-1硫代硫酸钠标准溶液滴定锥形瓶中的溶液
(I2+2S2O32-=2I-+S4O62-),指示剂显示终点时共用去20.00mL硫
代硫酸钠溶液。
在此过程中:
①锥形瓶内ClO2与碘化钾反应的离子方程式为。
②玻璃液封装置的作用是。
③V中加入的指示剂通常为,滴定至终点的现象是。
④测得混合气中ClO2的质量为g。
(4)用ClO2处理过的饮用水会含有一定最的亚氯酸盐。
若要除去超标的亚氯酸盐,下列物质最适宜的是_______(填标号)。
a.明矾b.碘化钾c.盐酸d.硫酸亚铁
【答案】
(1)2:
1
(2)①NH4Cl+2HCl
3H2↑+NCl3②Cl—、OH—③c
(3)①2ClO2+10I-+8H+=2Cl-+5I2+4H2O②吸收残余的二氧化氯气体(避免碘的逸出)
③淀粉溶液;溶液由蓝色变为无色,且半分钟内溶液颜色不再改变④0.02700(4)d
【考点定位】本题考查阅读题目获取信息能力、氧化还原反应滴定及应用、电解原理、对工艺流程及装置理解分析等,难度中等,要求学生要有扎实的实验基础知识和灵活应用信息解决问题的能力,注意基础知识的全面掌握。
【名师点晴】本题从知识上考查了重要物质的化学性质、化学实验基本操作、实验现象的判断与分析、化学探究实验方案的设计与评价、化学方程式的书写、氧化还原反应原理等知识。
考查了学生对基础知识的记忆、理解和运用,运用所学知识分析具体问题的能力。
也涉及到运用所学知识分析问题、解决问题的能力,同时把元素化合物、基本化学原理和化学实验联系在一起,充分体现了学生对基础知识的掌握和分析问题、解决问题的思维能力,凸显了理科综合考试中的综合性与实用性的特点。
【注】本题分类与专题4、16
3.【2015浙江理综化学】(15分)某学习小组按如下实验流程探究海带中碘含量的测定和碘的制取。
实验
(一)碘含量的测定
取0.0100mol·Lˉ1的AgNO3标准溶液装入滴定管,取100.00mL海带浸取原液至滴定池,用电势滴定法测定碘含量。
测得的电动势(E)反映溶液中c(Iˉ)的变化,部分数据如下表:
V(AgNO3)/mL
15.00
19.00
19.80
19.98
20.00
20.02
21.00
23.00
25.00
E/mV
-225
-200
-150
-100
50.0
175
275
300
325
实验
(二)碘的制取
另制海带浸取原液,甲、乙两种实验方案如下:
已知:
3I2+6NaOH=5NaI+NaIO3+3H2O。
请回答:
(1)实验
(一)中的仪器名称:
仪器A,仪器B。
(2)
根据表中数据绘制滴定曲线:
②该次滴定终点时用去AgNO3溶液的体积为mL,计算得海带中碘的百分含量为%。
(3)
分液漏斗使用前须检漏,检漏方法为。
②步骤X中,萃取后分液漏斗内观察到的现象是。
③下列有关步骤Y的说法,正确的是。
A.应控制NaOH溶液的浓度和体积
B.将碘转化成离子进入水层
C.主要是除去海带浸取原液中的有机杂质
D.NaOH溶液可以由乙醇代替
④实验
(二)中操作Z的名称是。
(4)方案甲中采用蒸馏不合理,理由是。
【答案】
(1)坩埚500mL容量瓶
(2)
20.00mL0.635%(3)①向分液漏斗中加入少量水,检查旋塞处是否漏水;将漏斗倒转过来,检查玻璃塞是否漏水②液体分上下两层,下层呈紫红色③AB④过滤(4)主要由于碘易升华,会导致碘的损失
【解析】
(1)A、B两种仪器的名称分别为坩埚、500mL容量瓶(须注明容量瓶的容量)。
(2)①根据表中数据描出各点,然后连成光滑的曲线即可。
②从图像可知,有20.00mL附近滴定曲线发生突变,可判断滴定终点时用去AgNO3溶液的体积为20.00mL;根据关系式Ag+~I-可计算求得海带中碘的百分含量=
。
(3)①分液漏斗的检漏方法为:
向分液漏斗中加入少量水,检查旋塞处是否漏水;将漏斗倒转过来,检查玻璃塞是否漏水。
②步骤X中,加入CCl4的作用是萃取碘水中的I2,萃取后I2溶解在CCl4中而呈紫色,由于CCl4的密度比水大,沉在下层,所以观察到的实验现象是:
液体分上下两层,下层呈紫红色。
③步骤Y加入NaOH的目的是把I2转化为离子(I-和IO3-)进入水层而与CCl4分离,并非浸取有机杂质,也不能用乙醇代替,但NaOH的用量要控制,用量过多会使后续酸化操作步骤消耗硫酸过多,故选AB。
④Z步骤为过滤操作。
(4)I2的CCl4溶液采用蒸馏的方法虽然可以把CCl4蒸馏出去,但同时碘易升华,导致碘的损失。
【考点定位】本题主要是考查定量实验、实验设计与评价、实验流程分析与应用,涉及仪器识别、仪器选择与使用、物质的分离与提纯实验操作等
4.【2015重庆理综化学】(15分)ClO2与Cl2的氧化性相近,在自来水消毒和果蔬保鲜等方面应用广泛。
某兴趣小组通过题9图1装置(夹持装置略)对其制备、吸收、释放和应用进行了研究。
(1)仪器D的名称是。
安装F中导管时,应选用题9图2中的。
(2)打开B的活塞,A中发生反应:
2NaClO3+4HCl=2ClO2↑+Cl2↑+2NaCl+2H2O。
为使ClO2在D中被稳定剂充分吸收,滴加稀盐酸的速度宜(填“快”或“慢”)。
(3)关闭B的活塞,ClO2在D中被稳定剂完全吸收生成NaClO2,此时F中溶液的颜色不变,则装置C的作用是。
(4)已知在酸性条件下NaClO2可发生反应生成NaCl并释放出ClO2,该反应的离子方程式为,在ClO2释放实验中,打开E的活塞,D中发生反应,则装置F的作用是。
(5)已吸收ClO2气体的稳定剂Ⅰ和稳定剂Ⅱ,加酸后释放ClO2的浓度随时间的变化如题9图3所示。
若将其用于水果保鲜,你认为效果较好的稳定剂是,原因是。
【答案】9.(15分)
(1)锥形瓶b
(2)慢(3)吸收Cl2
(4)4H++5ClO2-=Cl-+4ClO2↑+2H2O验证是否有ClO2生成
(5)稳定剂Ⅱ,稳定剂Ⅱ可以缓慢释放ClO2,能较长时间维持保鲜所需的浓度
【解析】
(1)根据仪器特征,仪器D的名称是锥形瓶;根据操作分析,F装置应是Cl2和KI反应,所以应该长管进气,短管出气,选b。
(2)为使ClO2在D中被稳定剂充分吸收,滴加稀盐酸的速度要慢。
(3)F装置中能发生Cl2+2KI=2KCl+I2,碘遇淀粉变蓝,所以F中溶液的颜色若不变,则装置C的作用是吸收Cl2。
(4)在酸性条件下NaClO2可发生反应生成NaCl并释放出ClO2,再根据化合价升降相等和电荷守恒以及原子守恒配平,该反应的离子方程式为4H++5ClO2-=Cl-+4ClO2↑+2H2O;在ClO2释放实验中,打开E的活塞,D中发生反应,则装置F的作用是验证是否有ClO2生成.
(5)根据图3可知,稳定剂Ⅱ可以缓慢释放ClO2,能较长时间维持保鲜所需的浓度,所以稳定剂Ⅱ好。
5.【2015四川理综化学】(13分)(NH4)2SO4是常见的化肥和化工原料,受热易分解。
某兴趣小组拟探究其分解产物。
[查阅资料](NH4)2SO4在260℃和400℃时分解产物不同。
[实验探究]该小组拟选用下图所示装置进行实验(夹持和加热装置略)
实验1:
连接装置A-B-C-D,检查气密性,按图示加入试剂(装置B盛0.5000mol/L盐酸70.00mL)。
通入N2排尽空气后,于260℃加热装置A一段时间,停止加热,冷却,停止通入N2。
品红溶液不褪色,取下装置B,加入指示剂,用0.2000mol/LNaOH溶液滴定剩余盐酸,终点时消耗NaOH溶液25.00mL。
经检验滴定后的溶液中无SO42-。
(1)仪器X的名称是________________。
(2)滴定前,下列操作的正确顺序是_________(填字母编号)。
a.盛装0.2000mol/LNaOH溶液b.用0.2000mol/LNaOH溶液润洗
c.读数、记录d.查漏、清洗e.排尽滴定管尖嘴的气泡并调整液面
(3)装置B内溶液吸收气体的物质的量是________