元素周期表中各元素名称及性质.docx
《元素周期表中各元素名称及性质.docx》由会员分享,可在线阅读,更多相关《元素周期表中各元素名称及性质.docx(107页珍藏版)》请在冰豆网上搜索。
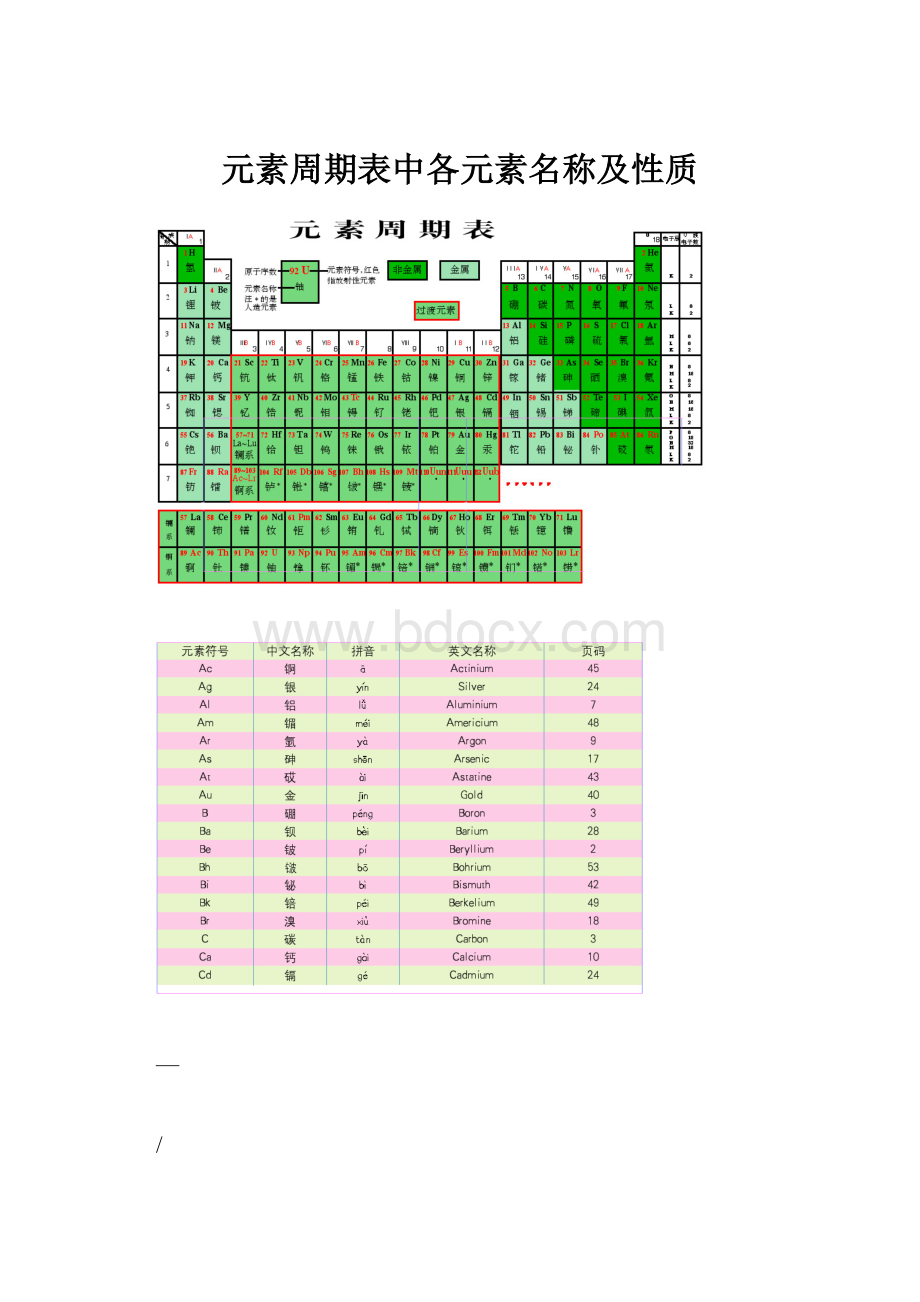
元素周期表中各元素名称及性质
—
/
[
*
、
…
氢(H)
[
主要性质和用途
熔点为℃,沸点为℃,密度为0.08988g/L(10℃)。
无色无臭气体,不溶于水,能在空气中燃烧,与空气形成爆炸混合物。
工业上用于制造氨、环已烷、甲醇等。
发现
1766年由卡文迪许()在英国判明。
氦(He)
;
主要性质和用途
熔点为℃(加压),沸点为-℃,密度为5 g/L(0℃)。
无色无臭气体。
化学性质不活泼。
用于深海潜水、气象气球和低温研究仪器。
发现
1895年由拉姆塞(Sir)在英国、克利夫等(和在瑞典各自独立分离出。
锂(Li)
。
主要性质和用途
熔点为℃,沸点为1347℃,密度为g/cm3(20℃)。
软的银白色金属,跟氧气和水缓慢反应。
用于合金、润滑油、电池、玻璃、医药和核弹。
发现
1817年由阿尔费德森(.Arfvedson)在瑞典发现。
铍(Be)
主要性质和用途
~
熔点为1278±5℃,沸点为2970℃(加压下),密度为g/cm3(20℃)。
较软的银白色金属,在空气和水中稳定,即使在红热时也不反应。
用于与铜和镍制合金,其导电性和导热性极好。
发 现
1798年由沃克兰()发现
硼(B)
主要性质和用途
*
熔点为2300℃,沸点为3658℃,密度为g/cm3(β-菱形)(20℃)。
具有几种同素异形体,无定形的硼为暗色粉末,跟氧气、水、酸和碱都不起反应,跟大多数金属形成金属硼化物。
用于制硼硅酸盐玻璃、漂白和防火。
发 现
1808年由戴维(SirHumphreyDavy)在英国、盖-吕萨克()和泰纳)在法国发现。
碳(C)
主要性质和用途
熔点约为3550℃(金刚石),沸点约为4827℃(升华),密度为g/cm3(金刚石)、g/cm3(石墨)(20℃)。
用于首饰(金刚石)、炼钢(焦炭)、印刷(炭黑)和精制糖(活性炭)等。
;
发 现
在自然界中以石墨(和金刚石)存在。
古代已知有木炭和烟炱。
氮(N)
主要性质和用途
熔点为℃,沸点为℃,密度为g/L(0℃)。
无色无臭气体。
在室温下一般不活泼。
用于制硝酸、化肥、炸药、塑料和染料等。
发 现
!
1772年由卢瑟福()在苏格兰发现。
氧(O)
主要性质和用途
熔点为℃,沸点为℃,密度为g/L(0℃)。
无色无臭气体。
非常活泼,与除稀有气体以外的所有元素形成氧化物,在水中有一定的溶解性。
用于炼钢、金属切割和化学工业。
发 现
1773年由舍勒()在瑞典、1774年由普利斯特里()在英国,拉瓦锡)在法国各自独立发现。
【
氟(F)
主要性质和用途
熔点为℃,沸点为℃,密度为g/L(0℃)。
淡黄色气体,是最活泼的非金属元素。
用于制氟化试剂以及金属冶炼中的助熔剂等。
发 现
1886年由莫瓦桑()在法国制得。
*
钠(Na)
主要性质和用途
熔点为℃,沸点为℃,密度为9g/L(0℃)。
无色无臭气体。
化学性质不活泼。
用于装饰灯(霓红灯广告牌)。
发 现
1898年由拉姆塞(SirWilliamRamsay)和特拉弗斯()在英国发现。
|
钠(Na)
主要性质和用途
熔点为℃,沸点为℃,密度为g/cm3(20℃)。
软的银白色金属,切割时迅速被氧化,跟水剧烈反应。
用于原子反应堆的热交换器中。
发 现
1807年由戴维(SirHamphryDavy)在英国分离出。
{
镁(Mg)
主要性质和用途
熔点为℃,沸点为1090℃,密度为g/cm3(20℃)。
较软的银白色金属,在空气中燃烧,跟热水反应。
用于制合金以及保护其他金属的牺牲阴极。
发 现
1808年由戴维(SirHamphryDavy)在英国制得。
铝(Al)
#
主要性质和用途
熔点为℃,沸点为2467℃,密度为g/cm3(20℃)。
银白色金属,由于表面形成氧化层而保护其不与空气和水起反应。
溶于热的浓盐酸和氢氧化钠溶液。
作为金属和合金在飞机、建筑业、容器、铝箔等方面有许多用途。
发 现
1825年由厄斯泰德(HansChristianDersted)在丹麦发现。
硅(Si)
(
主要性质和用途
熔点为1410℃,沸点为2355℃,密度为g/cm3(20℃)。
超纯半导体晶体是蓝灰色,用碳还原砂子得到的无定形硅为黑色。
不跟氧气、水、酸(HF除外)反应,但溶于热碱。
用于制半导体、合金和聚合物。
发 现
1823年由贝采里乌斯()在瑞典制得。
磷(P)
主要性质和用途
熔点为℃(白磷),410℃(红磷,加压),沸点为280℃,密度为g/cm3,g/cm3(红磷)。
白磷软而易燃,红磷呈粉末状,通常不易燃。
都不跟水或稀酸反应,但跟碱反应生成磷化氢气体。
用于制化肥、杀虫剂、清洁剂以及金属处理等。
&
发 现
1669年由布兰特(HennigBrandt)在德国制得白磷。
硫(S)
主要性质和用途
熔点为℃(α),沸点为℃,密度为g/cm3(α)(20℃)。
有几种同素异形体,其中正交晶型的S8是最稳定的。
对空气和水稳定,但加热时会燃烧;跟氧化性的酸反应。
是重要的工业化学品。
发 现
古代已发现天然硫。
|
氯(Cl)
主要性质和用途
熔点为℃,沸点为℃,密度为g/cm3(0℃)。
黄绿色具有强烈刺激性气味的气体。
用于制漂白剂、有机氯溶剂和聚合物(PVC)。
发 现
1774年由舍勒()在瑞典制得,1810年由戴维(SirHamphryDavy)在英国确认。
氩(Ar)
-
主要性质和用途
熔点为℃,沸点为℃,密度为g/cm3(0℃)。
无色无臭气体。
在灯泡和高温冶金中用作惰性气氛。
发 现
1894年由雷利(LordRayleigh)和拉姆塞(SirWilliamRamsay)在英国发现。
钾(K)
《
主要性质和用途
熔点为℃,沸点为774℃,密度为g/cm3(20℃)。
软的白色金属,切割时有银白色光泽,但同时迅速被氧化,跟水剧烈反应。
用于制化肥、化学品和玻璃等。
发 现
1807年由戴维(SirHamphryDavy)在英国发现。
钙(Ca)
主要性质和用途
熔点为839℃,沸点为1484℃,密度为g/cm3(20℃)。
较软的银白色金属,跟氧和水反应。
用于制合金、生产锆、钍、铀和稀土金属。
生石灰用于冶金、水处理、化学工业和建筑等。
'
发 现
1808年由戴维(SirHamphryDavy)在英国分离出。
钪(Sc)
主要性质和用途
熔点为1541℃,沸点为2831℃,密度为g/cm3(0℃)。
软的银白色金属,在空气中失去光泽并且容易燃烧,跟水反应生成氢气,跟酸反应形成盐。
很少应用。
发 现
1879年由尼尔森()在瑞典发现。
-
钛(Ti)
主要性质和用途
熔点为1660℃,沸点为3287℃,密度为g/cm3(20℃)。
硬而有光泽的银白色金属。
因氧化物膜而抗腐蚀,但金属粉末在空气中燃烧,不跟酸和碱反应。
主要用制轻合金、用于化工厂,钛白粉用于涂料。
发 现
1791年由格雷戈尔()在英国发现。
钒(V)
!
主要性质和用途
熔点为1887℃,沸点为3377℃,密度为g/cm3(20℃)。
闪亮的银白色金属,纯净时软。
因氧化物膜而抗腐蚀,能与浓酸作用,但不跟熔融的碱反应。
主要用于制造合金和制钢。
发 现
1830年由塞夫斯特伦()在瑞典发现。
铬(Cr)
,
主要性质和用途
熔点为1857±20℃,沸点为2672℃,密度为g/cm3(20℃)。
硬的蓝白色金属。
溶于盐酸和硫酸,但因形成保护层而不溶于硝酸、磷酸或高氯酸,在空气中抗氧化。
主要用于合金、镀铬和金属陶瓷。
发 现
1797年由沃克兰在法国发现。
锰(Mn)
主要性质和用途
熔点为1244℃,沸点为1962℃,密度为(α)g/cm3(20℃)。
硬而脆的银白色金属。
含杂质时活泼,在氧气中燃烧,在空气中发生表面氧化,跟水反应,溶于稀酸中。
用于钢铁生产、陶瓷、肥料添加剂、动物饲料补充剂等。
》
发 现
1774年由甘恩()在瑞典分离出。
铁(Fe)
主要性质和用途
熔点为1535℃,沸点为2750℃,密度为g/cm3(20℃)。
银白色有光泽的金属,纯时较软。
在潮湿空气中生锈,溶于酸中,在冷的浓硫酸、硝酸中钝化。
主要用于钢铁。
发 现
古代文明已知。
:
钴(Co)
主要性质和用途
熔点为1495℃,沸点为2870℃,密度为g/cm3(20℃)。
坚硬的银色发蓝、有光泽的金属,具有铁磁性。
在空气中稳定,跟稀酸缓慢反应。
60Co是有用的放射性同位素。
用于磁性合金、陶瓷、催化剂和涂料中。
发 现
1735年由布兰特()在瑞典发现。
镍(Ni)
。
主要性质和用途
熔点为1453℃,沸点为2732℃,密度为g/cm3(25℃)。
银白色、有光泽、有延展性和韧性的金属。
抗腐蚀,溶于酸中(浓硝酸除外),不跟碱反应。
发 现
1751年由克郎斯塔特()在瑞典发现。
铜(Cu)
—
主要性质和用途
熔点为1084℃,沸点为2567℃,密度为g/cm3(20℃)。
红色、有光泽、有延展性和韧性的金属,具有高的导电性和导热性。
难跟空气和水反应,但会缓慢地被侵蚀而生成铜绿。
用于制造合金、电线、电器、钱币等。
发 现
古代文明已知。
锌(Zn)
主要性质和用途
熔点为℃,沸点为907℃,密度为g/cm3(20℃)。
略带浅蓝色的白色金属,铸锌较脆。
在空气中失去光泽,跟酸和碱反应。
用于镀锌铁皮、合金、电池等,氧化锌用在橡胶中,可以用作聚合物稳定剂。
、
发 现
1500年前在中国和印度已知。
镓(Ga)
主要性质和用途
熔点为℃,沸点为2403℃,密度为g/cm3(20℃)。
软的银白色金属。
在空气和水中稳定,溶于酸和碱中。
在所有元素中具有最长的液态范围。
用磷、砷和锑掺杂具有半导体性质。
用于发光二极管和微波装置。
发 现
1875年由布瓦博德朗Boisbaudran)在法国发现。
*
锗(Ge)
主要性质和用途
熔点为℃,沸点为2830℃,密度为g/cm3(20℃)。
超纯锗是银白色、脆的类金属元素。
在空气和水中稳定,不跟酸(硝酸除外)和碱反应。
用于半导体、合金和红外装置用的特种玻璃。
发 现
1886年由文克勒()在德国发现。
砷(As)
#
主要性质和用途
熔点为817℃(加压下),沸点为616℃(升华),密度为 g/cm3(α),g/cm3(β)(20℃)。
准金属元素,有几种同素异形体。
其中灰α-砷软而脆,无光泽,具有金属性,在氧气中燃烧,在水、酸和碱中不活泼,但能跟热酸和熔融的氢氧化钠反应。
用于合金、半导体、杀虫剂、木材防腐剂和玻璃等。
发 现
1250年由马格耐斯()发现。
硒(Se)
}
主要性质和用途
熔点为217℃(加压下),沸点为℃,密度为g/cm3(灰)(20℃)。
从银白色金属同素异形体或红色无定形粉末获得,不太稳定。
在空气中燃烧,不跟水反应,溶于浓硝酸和碱中。
用于光电池、复印和半导体中。
发 现
1817年由贝采里乌斯()在瑞典发现。
溴(Br)
主要性质和用途
熔点为℃,沸点为℃,密度为g/cm3(20℃)。
深红色、稠密的、具有强刺激性气味的液体。
具有强烈的氧化性,腐蚀性。
其化合物用于燃料添加剂、杀虫剂、阻燃剂和照相等。
—
发 现
1825年由罗威()在德国、1826年由巴拉尔()在法国分别发现。
氪(Kr)
主要性质和用途
熔点为℃,沸点为℃,密度为g/L(0℃)。
无色无臭气体,从液态空气中获得。
化学上对氟以外的所有物质都呈惰性。
86Kr原子光谱中有一条桔红谱线,被用作长度的基本标准:
1m等于该谱线波长的1650倍。
发 现
1898年由拉姆塞和特拉弗斯()在英国发现。
&
铷(Rb)
主要性质和用途
熔点为℃,沸点为688℃,密度为g/cm3(20℃)。
很软的金属,切割时有银白色光泽。
在空气中燃烧,跟水激烈反应。
除科研外很少使用。
发 现
1861年由本生()和基尔霍夫()在德国发现。
【
锶(Sr)
!
主要性质和用途
熔点为769℃(加压下),沸点为1384℃,密度为g/cm3(20℃)。
较软的银白色金属,由铝高温还原制得。
在空气中可燃烧,可与水反应。
用于电视机和录像机的特种玻璃,也用于烟火和照明弹等发出红的色彩。
发 现
1790年克劳福德()在苏格兰发现;1808年戴维()在英国分离出来。
钇(Y)
!
主要性质和用途
熔点为1438℃,沸点为3338℃,密度为g/cm3(20℃)。
软的银白色金属,因形成氧化膜而在空气中稳定,易燃,跟水反应生成氢气。
用作钇磷光体使电视屏幕产生红色彩,还用于X线滤波器、超导体和超合金。
发 现
1794年由加多林()在芬兰发现。
锆(Zr)
主要性质和用途
[
熔点为1852℃,沸点为4377℃,密度为g/cm3(20℃)。
硬而有光泽的银白色金属,因氧化物膜而高度抗腐蚀,但可在空气中燃烧,不跟酸(HF除外)和碱反应。
金属用于合金、彩釉和核反应堆,氧化物用于铸造坩埚、砖、陶瓷和研磨料。
发 现
1789年由.克拉普罗特()在德国发现。
铌(Nb)
主要性质和用途
熔点为2741℃,沸点为4742℃,密度为g/cm3(20℃)。
闪亮的银白色金属,纯净时软。
因氧化膜的保护作用而抗腐蚀,与热的浓酸作用,但不跟熔融的碱反应。
用在不锈钢中。
发 现
】
1801年由哈契特()在英国发现。
钼(Mo)
主要性质和用途
熔点为2617℃,沸点为4612℃,密度为g/cm3(20℃)。
有光泽,银色,纯净时较软,通常获得的是灰白色粉末。
用于合金、电极和催化剂。
发 现
1782年由埃尔姆()在瑞典发现。
锝(Tc)
·
主要性质和用途
熔点为2172℃,沸点为4877℃,密度为g/cm3(估计)(20℃)。
放射性金属,自然界中不存在。
该金属呈银白色,但通常获得的是灰色粉末。
抗氧化,在潮湿的空气中缓慢失去光泽,在氧气中燃烧,溶于硝酸和硫酸。
发 现
1937年由佩里埃()和塞格瑞()在意大利发现。
钌(Ru)
\
主要性质和用途
熔点为2310℃,沸点为3900℃,密度为g/cm3(20℃)。
有光泽的银白色铂族金属。
在空气、水和酸中稳定,但溶于熔融的碱。
用于硬化铂和钯,以及用作催化剂。
发 现
1844年由克劳斯()在俄国发现。
铑(Rh)
主要性质和用途
)
熔点为1966℃,沸点为3727℃,密度为g/cm3(20℃)。
有光泽的银白色、坚硬的铂族金属,稀有。
在空气中稳定至602℃。
对所有酸惰性,跟熔融碱反应。
用作催化剂。
发 现
1803年由武拉斯顿()在英国发现。
钯(Pd)
主要性质和用途
熔点为1552℃,沸点为3140℃,密度为g/cm3(20℃)。
有光泽的银白色金属,具有延展性和韧性。
抗腐蚀,溶于氧化性酸和熔融碱,易吸附氢气。
主要用作催化剂。
发 现
-
1803年由武拉斯顿()在英国发现。
银(Ag)
主要性质和用途
熔点为℃,沸点为2212℃,密度为g/cm3(20℃)。
具有特征银色光泽的金属,软,可延展。
对于水和氧气稳定,但在空气中会受到硫化合物的作用而生成黑色硫化物层,溶于硫酸和硝酸。
用于照相、银器、珠宝、电工和玻璃镜。
发 现
古代文明已知。
*
镉(Cd)
主要性质和用途
熔点为℃,沸点为765℃,密度为g/cm3(20℃)。
银白色金属。
在空气中失去光泽,溶于酸,不溶于碱。
用于可充电电池、合金、颜料。
发 现
1817年由斯特罗迈耶()在德国发现。
铟(In)
·
主要性质和用途
熔点为℃,沸点为2080℃,密度为g/cm3(20℃)。
软的银白色金属。
在空气和水中稳定,溶于酸。
用在安全装置的低熔点合金中,InAs和InSb作为半导体用于晶体管和热敏电阻等。
发 现
1863年由赖希(F.Reich)和里希特(H.Richter)在德国发现。
锡(Sn)
(
主要性质和用途
熔点为℃,沸点为2270℃,密度为g/cm3(α)、g/cm3(β)(20℃)。
软而柔韧的银白色金属。
在氧化物膜的保护下不跟氧反应,也不跟水反应,但溶于酸和碱中。
用于焊锡、合金、镀锡、聚合物添加剂和防腐涂料。
发 现
远古文明已知。
锑(Sb)
主要性质和用途
~
熔点为℃,沸点为1635℃,密度为g/cm3(20℃)。
准金属元素,有多种同素异形体,金属明亮、银白色、硬而脆。
在干燥空气中稳定,不跟稀酸和碱反应。
用于提高其他金属的硬度,也用于蓄电池和轴承。
发 现
古代文明已知。
碲(Te)
主要性质和用途
熔点为℃,沸点为℃,密度为g/cm3(20℃)。
碲块呈银白色,看上去像金属,但通常得到的是暗灰色粉末。
在空气或氧气中燃烧,不跟水和盐酸反应,但溶于硝酸中。
用于合金以改善加工性能,还用于化学品、催化剂等。
发 现
!
1783年由缪勒(FranzJosephMuller)在罗马尼亚发现。
碘(I)
主要性质和用途
熔点为℃,沸点为℃,密度为g/cm3(20℃)。
黑色光亮的非金属固体,易升华。
用于消毒、药品、食品补充剂、染料、催化剂和照相等。
发 现
1811年由库特瓦()在法国发现。
氙(Xe)
;
主要性质和用途
熔点为℃,沸点为℃,密度为g/cm3(0℃)。
无色无臭气体,从液态空气中获得。
化学上除跟氟反应生成氟化氙外,对大多数其他化学物质都呈惰性。
除研究工作外很少应用。
发 现
1898年由拉姆塞(SirWilliamRamsay)和特拉弗斯()在英国发现。
铯(Cs)
¥
主要性质和用途
熔点为℃,沸点为℃,密度为g/cm3(20℃)。
软的、闪光的金色金属,跟氧迅速反应,遇水发生爆炸。
用作催化促进剂,也用于特种玻璃和放射性检测装备。
发 现
1860年由本生()和基尔霍夫()在德国发现。
钡(Ba)
主要性质和用途
¥
熔点为729℃,沸点为1637℃,密度为g/cm3(20℃)。
较软的银白色金属,由铝加热还原BaO制得。
跟空气和水反应。
主要以硫酸钡的形式被用于钻探石油和天然气,少量用于涂料、玻璃等。
发 现
1808年由戴维(SirHumphreyDavy)在英国发现。
镧(La)
主要性质和用途
熔点为921℃,沸点为3457℃,密度为g/cm3(25℃)。
银白色金属,质软,在空气中很快失去光泽。
易燃烧,与水反应放出氢气。
用于制造光学玻璃和打火石等;La3+被用作研究Ca2+的生物示踪物。
发 现
。
1839年由莫桑德尔(C.)在瑞典发现。
铈(Ce)
主要性质和用途
熔点为799℃,沸点为3426℃,密度为g/cm3(α)(25℃)。
灰色活泼的金属,是镧系金属中自然丰度最高的一种,性质活泼。
在空气中失去光泽,加热时燃烧,与水迅速反应,溶于酸。
用于制造玻璃、打火石、陶瓷和合金等。
发 现
1803年由贝采里乌斯()等在瑞典发现。
镨(Pr)
>
主要性质和用途
熔点为931℃,沸点为3512℃,密度为g/cm3(20℃)。
银白色金属,质软,有延展性。
与氧气反应缓慢,与水反应迅速。
用于制作永久磁铁的合金、打火石、焊接用保护镜片等。
发 现
1885年由威斯巴赫()在奥地利分离出。
钷(Pm)
~
主要性质和用途
熔点为1021℃,沸点为3068℃,密度为g/cm3(20℃)。
银白色金属,在空气中失去光泽。
与冷水反应缓慢,与热水反应迅速。
用于制作永久磁铁的合金、打火石、釉料和玻璃等。
发 现
1885年由威斯巴赫(Welsbach)在奥地利分离出。
钷(Pm)
主要性质和用途
【
熔点为1168℃,沸点约为3000℃,密度为g/cm3(25℃)。
放射性金属。
用于制造特殊用途的微型电池。
发 现
1945年由马林斯基()、格伦登宁()和科里尔()在美国制备出。
钐(Sm)
主要性质和用途
熔点为1077℃,沸点为1791℃,密度为g/cm3(20℃)。
银白色稀土金属。
在干燥空气中比较稳定,在潮湿空气中会形成氧化物层。
用于永久磁铁、有机反应剂、特种玻璃、催化剂、陶瓷和电子学。
发 现
)
1879年由布瓦博德朗()在法国发现。
铕(Eu)
主要性质和用途
熔点为822℃,沸点为1597℃,密度为g/cm3(20℃)。
银白色稀土金属,质软,是稀土金属中最活泼的一种。
与氧气和水反应迅速。
应用很少,有时用在薄膜超导合金中。
发 现
1896年由德马尔赛()在法国发现。
】
钆(Gd)
主要性质和用途
熔点为1313℃,沸点为3266℃,密度为g/cm3(20℃)。
银白色稀土金属。
与氧气和水反应缓慢,溶于酸。
用于磁铁、耐火材料、中子射线照像、合金等;与铁结合用作光磁记录材料。
发 现
1880年由马里纳克(Marignac)在瑞士发现。
钬(Ho)
主要性质和用途
熔点为1356℃,沸点为3123℃,密度为g/cm3(20℃)。
银白色稀土金属。
在空气中缓慢氧化,能与冷水反应。
用于激光器和固态装置等。
发 现
1843年由莫桑德尔(C.)在瑞典发现。
镝(Dy)
/
主要性质和用途
熔点为1412℃,沸点为2562℃,密度为g/cm3(20℃)。
银白色稀土金属。
坚硬,性质活泼。
易被氧气氧化,与水反应迅速,溶于酸。
用于制作磁铁的合金。
发 现
1886年由布瓦博德朗()在法国发现。
钬(Ho)
主要性质和用途
熔点为1474℃,沸点为2695℃,密度为g/cm3(25℃)。
银白色稀土金属,跟氧和水缓慢反应,溶于酸。
用于高磁场的磁通量集中器。
]
发 现
1879年由克利夫()在瑞典发现。
铒(Er)
主要性质和用途
熔点为1529