高考理科综合化学试题统计与分析.docx
《高考理科综合化学试题统计与分析.docx》由会员分享,可在线阅读,更多相关《高考理科综合化学试题统计与分析.docx(12页珍藏版)》请在冰豆网上搜索。
高考理科综合化学试题统计与分析
2016年高考理科综合(化学)试题统计与分析
26题
以氮的氧化物与氨气反应生成氮气为背景,考查了氨气制备实验的原理、实验装置的选择连接、氨气与二氧化氮反应实验的操作步骤、实验现象和原因。
比较全面地考查了学生实验能力和文字表达能力。
本题满分14分,平均分6.4分。
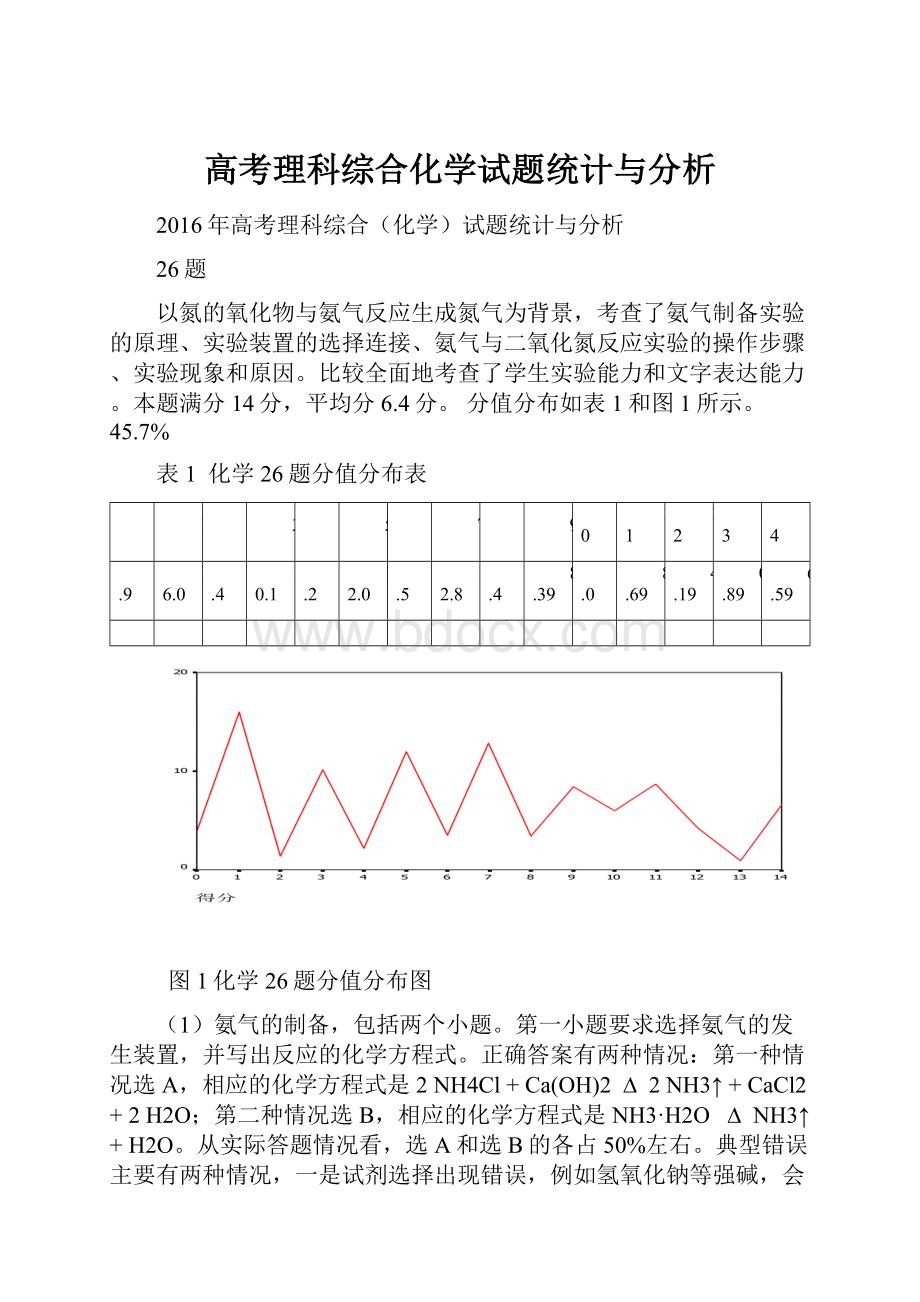
分值分布如表1和图1所示。
45.7%
表1化学26题分值分布表
0
1
2
3
4
5
6
7
8
9
10
11
12
13
14
3.9
16.0
1.4
10.1
2.2
12.0
3.5
12.8
3.4
8.39
6.0
8.69
4.19
0.89
6.59
图1化学26题分值分布图
(1)氨气的制备,包括两个小题。
第一小题要求选择氨气的发生装置,并写出反应的化学方程式。
正确答案有两种情况:
第一种情况选A,相应的化学方程式是2NH4Cl+Ca(OH)2∆2NH3↑+CaCl2+2H2O;第二种情况选B,相应的化学方程式是NH3·H2O∆NH3↑+H2O。
从实际答题情况看,选A和选B的各占50%左右。
典型错误主要有两种情况,一是试剂选择出现错误,例如氢氧化钠等强碱,会造成试管损坏。
另一种情况是化学式或方程式写错,比如把氨水写成NH4OH,NH4Cl∆NH3↑+HCl↑。
第二小题要求按气流方向,用小写字母写出收集一瓶干燥氨气的装置连接顺序,正确答案是“dcfei”,如果写成“dcfedci”、“adcfei”、“bdcfei”、“adcfedci”、“bdcfedci”也可得分。
此题正答率较低,只有17%。
典型错误一是干燥管连反,有27%的考生写成“cdfei”,二是收集装置连反,有15%的考生写成“dcefi”,可能没有考虑氨气的密度比空气小,也可能是“长进短出”造成的负迁移。
三是有15%的考生丢掉尾气吸收装置,写成“dcef”或者“dcfe”。
(2)氨气与二氧化氮的反应。
给出氨气与二氧化氮反应的实验装置和操作步骤,要求回答实验现象并解释原因。
一共包括4个小问题、第一问要求写出Y管中的实验现象,正确答案是红棕色气体慢慢变浅;第二问要求写出反应的化学方程式,正确答案是8NH3+6NO2催化剂7N2+12H2O。
这两问都比较简单,有50%的考生能正确回答。
第三问要求写出打开K2后的实验现象,正确答案是Z中NaOH溶液产生倒吸现象,这个问题不难,有50%的考生能答出“倒吸”。
“第四问要求写出原因,正确答案是反应后气体分子数减少,Y管中压强小于外压。
这个问题也不难,有68%的考生都能正确作答。
27题
以铬元素各种离子的性质和转化为背景。
考查了Cr3+的化学性质、CrO42-与Cr2O72-的转化反应的离子方程式、溶液的酸碱性对CrO42-平衡转化率的影响以及转化反应平衡常数的计算、温度、转化率与焓变的关系、根据Ksp计算离子浓度等知识点。
本题满分15分,平均分7.86。
分值分布如表2和图2所示。
52.4%
表2化学27题分值分布表
0
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
2.29
4.4
4.9
6.5
6.59
6.3
5.6
7.69
8.29
6.4
12.6
5.2
12.39
4.0
4.9
2.2
图2化学27题分值分布图
(1)要求学生根据题意,写出向Cr2(SO4)3溶液中逐滴加入NaOH溶液直至过量,可观察到的实验现象,正确答案是蓝紫色溶液变浅;生产蓝灰色沉淀;沉淀溶解形成绿色溶液。
此题正答率只有12%,得2分的居多。
一方面是因为与Al3+进行类比,只写出生成沉淀和沉淀溶解两点,而忽略了蓝紫色溶液变浅。
另一方面是只写始态和终态,忽略中间过程的实验现象,如写成蓝紫色溶液变成绿色溶液。
(2)包括三个小问题。
第一问要求用离子方程式表示Na2CrO4的转化反应,正确答案是:
2CrO42-+2H+
Cr2O72-+H2O,如果写成2CrO42-+H2O
Cr2O72-+2OH-也可得分。
此题难度不大,正答率70%。
典型错误是方程式不配平,化学式书写错误,最典型的就是把Cr2O72-写成CrO72-。
第二问要求根据图示写出溶液酸性增大时,CrO42-平衡转化率变化情况,正确答案是增大,正答率75%。
根据A点数据,计算该转化反应的平衡常数,正确答案要与所书写的离子方程式相对应,分别是1.0×1014、1.0×10-14。
第三问要求回答升高温度时,溶液中CrO42-的平衡转化率减小,则该反应的△H(焓变)变化情况,正确答案是小于零。
此题正答率74%。
(3)要求根据溶液溶度积常数Ksp计算Ag+和CrO42-,正确答案分别是2.0×10-5(正答率60%),5.0×10-3(正答率40%)。
(4)要求写出用NaHSO4将废液中Cr2O72-还原生成Cr3+的离子方程式,正确答案是Cr2O72-+3HSO3-+5H+
2Cr3++3SO42-+4H2O,正答率27%。
28题
以NaClO2生产工艺为背景,考查学生化合价判断、陌生氧化还原反应方程式的书写、除杂的原理和方法、氧化还原反应中氧化剂和还原剂、氧化产物和还原产物等基本概念以及“有效氯含量”计算等。
满分14分,平均分5.42分。
难度较大。
分值分布如表3和图3所示。
38.7%
表3化学28题分值分布表
0
1
2
3
4
5
6
7
8
9
10
11
12
13
14
4.3
1.5
10.3
9.5
15.7
12.89
12.7
11.5
5.69
7.8
2.5
2.29
2.0
0.3
1
图3化学28题分值分布
(1)要求写出NaClO2中Cl的化合价,正确答案是+3。
此题难度很小,正答率90%。
但依然有学生写成+1或+5。
原因可能是学生没有见过NaClO2这种物质,感觉很陌生。
而对NaClO和NaClO3很熟悉。
这两种物质中Cl的化合价分别是+1或+5,是知识负迁移造成的结果。
(2)要求写出“反应”步骤中生成ClO2的化学方程式,正确答案是2NaClO3+SO2+H2SO4=2ClO2+2NaHSO4。
约有40%的考生写成2NaClO3+SO2=2ClO2+Na2SO4。
错误原因主要是考生没有充分理解题干信息,题干中明确写出生成NaHSO4,但学生没有注意到。
(3)要求回答要除去粗盐水中的Mg2+和Ca2+,需要加入的试剂,正确答案是NaOH溶液(正答率73%)和Na2CO3溶液(正答率60%),这两空分子式正确无“溶液”两字的给分;汉字书写正确的给分;“NaOH”答烧碱、火碱或苛性钠的,“Na2CO3”答纯碱或苏打的均给分;顺序错误的不给分。
第三空要求回答“电解”中阴极反应的主要产物,正确答案是ClO2-(或NaClO2),如果答成“亚氯酸根”、“亚氯酸根离子”、“亚氯酸钠”或“亚氯酸盐”的也给分。
此题错误较多,60%的学生写成H2,原因是单纯按照教材氯碱工业的产物去写,不会根据题意灵活运用。
(4)考查尾气吸收反应中,氧化剂与还原剂的物质的量之比,正确答案是2:
1,此题正答率是40%,氧化产物是O2,正答率是30%。
典型错误是学生答成NaClO2,原因可能是在日常教学中,H2O2是典型的氧化剂,学生认为H2O2把ClO2氧化,还原剂ClO2对应的氧化产物是NaClO2。
(5)考查NaClO2的有效氯含量,结果要求保留两位有效数字,正确答案是1.57.此题难度较大,正答率只有5%,原因一是对有效氯含量的理解有问题。
二是计算能力较差。
36题
以软锰矿(主要成分为MnO2)为原料生产KMnO4的工艺路线为背景,考查了元素化合物知识以及化学反应原理的运用。
本题满分15分,平均分3.64分。
分值分布如表4和图4所示。
24.2%
表4化学36题分值分布表
0
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
26.89
0.4
11.9
2.89
24.39
12
4.5
7.1
1.4
4.8
0.2
2.29
0.1
0.89
0
0.3
图4化学36题分值分布
(1)要求写出将软锰矿粉碎的作用,正确答案是增大反应物接触面积,加快反应速率,提高原料利用率,正答率87%。
(2)要求写出平炉中发生反应的化学方程式,正确答案是2MnO2+O2+4KOH
2K2MnO4+2H2O,学生基本不会写,正答率只有13%。
(3)要求写出平炉中需要加压的目的,正确答案是提高氧气压强,加快反应速率,增加软锰矿转化率。
此题正答率87%。
(4)利用两种方法将锰酸钾转化为高锰酸钾。
第
小问用二氧化碳歧化法,要求写出除了高锰酸钾和二氧化锰之外的反应产物,正确答案是KHCO3,此题正答率很低,只有6%。
典型错误是写成K2CO3,原因是没有注意到题干中明确给出反应是在中性或弱酸性的条件下发生的。
第
小问利用电解法,要求写出电解槽中阳极发生的电极反应,正确答案是MnO42--e-=MnO4-,阳极逸出的气体是H2,此题正答率很低,第一空20%,第二空50%。
典型错误主要有MnO42--e-=MnO2-,2H2O-4e-=4H++O2。
第
小问要求比较电解法和歧化法中K2MnO4的利用率之比,正确答案是3:
2,此题正答率13%,典型错误主要有1:
2或者3:
1等。
(5)要求计算样品纯度,只列出计算式即可。
正确答案的变式很多,这里不再一一列举。
此题正答率只有4%,绝大部分同学都没做。
37题
以半导体元素锗为背景,综合考查了物质结构与性质的相关知识。
本题满分15分,平均分9.45。
分值分布如表5和图5所示。
63%
表5化学37题分值分布表
0
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
1.2
1.79
2.89
3.2
3.79
4.3
5.2
6.3
7.59
8.9
9.09
10.89
9.09
12.3
4.09
9.3
图5化学37题分值分布
(1)要求写出基态Ge原子的核外电子排布式,正确答案是[Ar]3d104s24p2,此题答案唯一,正答率73.3%。
典型错误主要有4s24p23d43d104s23p24s23d104p2。
(2)要求从原子结构角度分析为何Ge与C是同族元素,C原子间可以形成双键和叁键,但Ge原子间难以形成双键和叁键的原因。
正确答案是Ge原子半径大,原子间形成的δ单键较长,P-P轨道肩并肩重叠很少或几乎不能重叠,难以形成Π键。
此题属于文字叙述题,难度较大,正答率27.6%。
主要原因是学生不知道解答的方向和思路。
例如有7.5%的学生从碳的角度回答,对于Ge的结构和性质只字不提。
典型错误主要有:
最外层只有两个未成对电子;Ge的金属性强于碳的金属性,碳的还原性强于Ge;Ge的相对分子质量大于C,与其他原子之间形成价键使电子对向Ge偏移,导致不能形成稳定的双键,三键;Ge的电负性小于C原子,对电子的吸引能力弱;Ge的键能大;Ge为金属,C为非金属易形成共价键;C原子半径小,键能大,双键、三键稳定,不易断裂。
(3)要求分析锗卤化物的熔点和沸点变化的规律和原因。
变化规律非常简单,熔沸点依次增高,原因是分子结构相似,分子量依次增大,分子间相互作用力逐渐增强,正答率60.9%。
典型错误主要是原因说不对:
卤离子的还原性越强,锗卤化物的键能越大,从而使其的熔点和沸点越大;键长越小,键能增加,金属性增强;随着卤素离子原子序数增加,卤化物的熔沸点均升高。
(4)给出带状纳米Zn2GeO4的化学式,要求按照由大到小的顺序回答Zn、Ge、O的电负性顺序,正确答案是O、Ge、Zn。
此题很简单,正答率81.6%。
(5)要求写出Ge单晶中Ge原子的杂化方式,正确答案是SP3,微粒之间存在的作用力是共价键(或非极性共价键或非极性键)。
正答率56.3%,典型错误主要是范德华力;金属键;分子间作用力;氢键。
(6)第
小问要求写出D原子的坐标参数,正确答案是(
;
;
);正答率:
51.6%。
典型错误:
(
0,
);(
;
;
);(
;
;
)。
第
小问要求计算晶胞密度(列出计算式即可),正确答案是
,正答率是41%。
典型错误主要有
。
38题
以秸秆的综合利用为背景,给出姐秸秆为原料合成聚酯类高分子化合物的路线,主要考查了糖类物质的性质、有机合成反应的类型、官能团名称、同分异构体的书写、根据核磁共振氢谱判断结构简式以及合成路线的设计等。
本题满分15分,平均分6.02分。
分值分布如表6和图6所示。
40.1%
表6化学38题分值分布表
0
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
5.4
6.09
5.6
7.1
9.89
12.1
11.59
10.19
8.19
6.8
6
3.59
3.29
2.2
0.89
1.2
图6化学38题分值分布
(1)要求选择有关糖类物质的正确说法,正确答案是cd,此题正答率32.5%,典型错误主要有bd、bc、bcd、CD。
(2)要求回答B生成C的反应类型,正确答案是取代反应(或酯化反应),正答率73.1%,典型错误:
脂化反应、加成反应。
(3)要求写出D中官能团的名称,正确答案是酯基、碳碳双键,反应类型是消去反应,正答率55.2%。
典型错误主要有脂基;酯键;碳碳两键;双键;还原反应;催化氧化。
(4)第一问要求写出F的化学名称,正确答案是己二酸,正答率:
45%。
典型错误主要有1,4-丁二酸、1,4-己二酸、1-6-己二酸、1,4-二羧基丁烷、1,6-乙二酸。
第二问要求写出由F生成G的化学方程式,正确答案是nHOOC(CH2)4COOH+nHOCH2CH2CH2CH2OH
+(2n-1)H2O;正答率:
13.3%,典型错误主要有:
(5)要求写出W的同分异构体数目,正确答案是12种;正答率:
24%写9种的较多。
核磁共振氢谱为三组峰的结构简式为
,正答率37.5%。
典型错误是
。
(6)要求参照给出的合成路线,设计制备对苯二甲酸的合成路线。
正确答案是
,正答率:
13.3%。
典型错误主要有: